文档内容
zxxk.com
身边的化学物质--空气课后练习
题一: 下列关于空气的说法正确的是( )
A. 空气的主要成分是氮气和氧气
B. 空气中氮气体积分数约为21%
C. 空气中PM2.5含量高说明空气质量好
D. 洁净的空气是纯净物
题二: 2006年7月1日,青藏铁路正式通车,许多旅客乘车穿越青藏高原时,会发生高原反应,感
到呼吸困难,这是因为高原地区空气里( )
A. 氧气体积分数大大低于21%
B. 氮气体积分数大大超过78%
C. 氧气体积分数仍约为21%,但空气稀薄
D. CO 气体含量大大增多
2
题三: 下列关于空气的说法不正确的是( )
A. 洁净的空气是纯净物
B. 空气是一种重要的资源
C. 空气质量对于人类的生存至关重要
D. 植物的光合作用是空气中氧气的主要来源
题四: 下列关于空气的说法,正确的是( )
A. 空气质量报告中所列的空气质量级别越小,空气质量越好
B. CO、SO 、NO 属于空气污染物
2 2 2
C. 工业上用分离液态空气的方法制取氧气是分解反应
D. 按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1%
[来源:学科网]
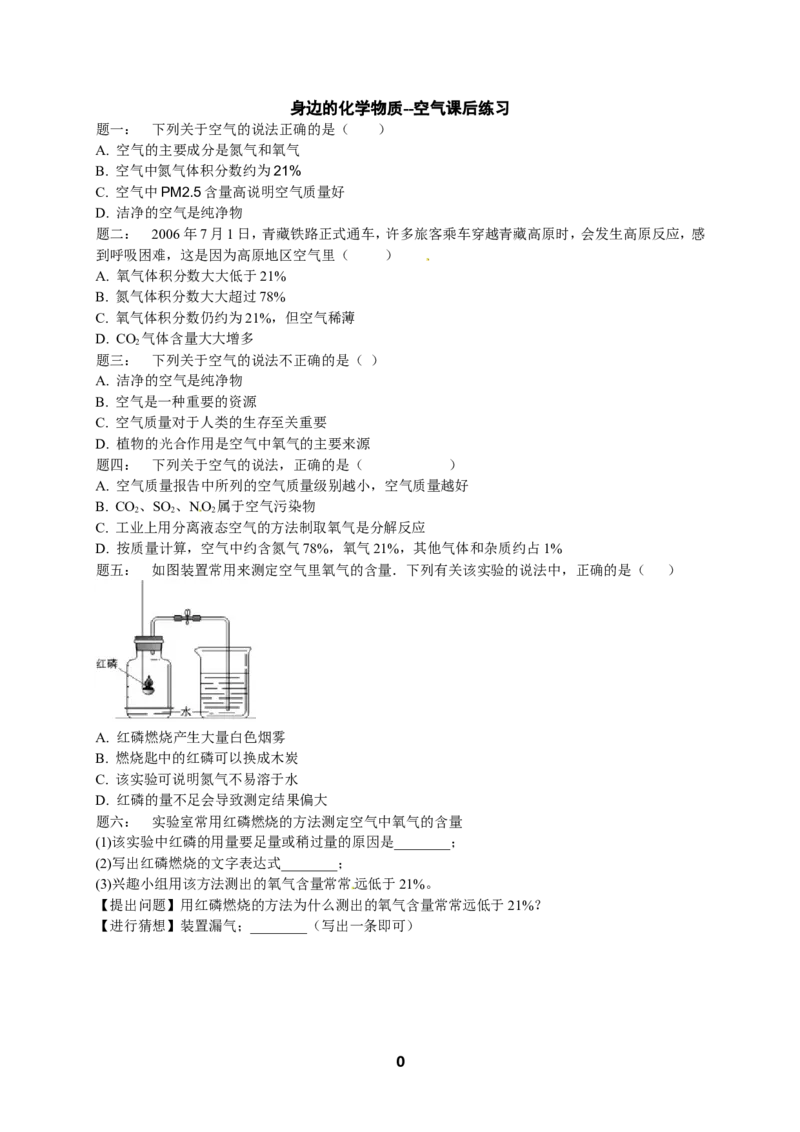
题五: 如图装置常用来测定空气里氧气的含量.下列有关该实验的说法中,正确的是( )
A. 红磷燃烧产生大量白色烟雾
B. 燃烧匙中的红磷可以换成木炭
C. 该实验可说明氮气不易溶于水
D. 红磷的量不足会导致测定结果偏大
题六: 实验室常用红磷燃烧的方法测定空气中氧气的含量
(1)该实验中红磷的用量要足量或稍过量的原因是________;
(2)写出红磷燃烧的文字表达式________;
(3)兴趣小组用该方法测出的氧气含量常常远低于21%。
【提出问题】用红磷燃烧的方法为什么测出的氧气含量常常远低于21%?
【进行猜想】装置漏气;________(写出一条即可)
0zxxk.com
题七: 以下是俄国化学家罗蒙诺索夫曾开展的实验:
①先用天平称取质量为m 的金属锡粉。
1
②将这些锡粉放在密闭容器里进行完全燃烧,生成了白色固体物质,称量容器的总质量为m。
2
③打开容器,听到了空气进入容器发出的“咝咝的声响”,称量所得白色物质的质量为m。
3
④把白色物质放回原容器里(容器中空气的组成恢复到初始状态),重新称量容器的总质量为m。
4
(1)根据所学知识判断,锡的燃烧是_____变化。
(2)罗蒙诺索夫分析数据后发现,生成白色物质的质量m=_______,于是提出了“参加反应的物质的
3
总质量,等于反应后产物的总质量”的观点。
题八: 通过本期学习,我们已经知道,加热高锰酸钾(KMnO )制取氧气时,还会有锰酸钾
4
(KMnO )和二氧化锰(MnO )两种固体生成.现将18g高锰酸钾加热一段时间后冷却,称得其剩余
2 4 2
固体质量为16.4g。(假若无高锰酸钾逸散到空气中)
(1)写出加热高锰酸钾的化学反应方程式_________。
(2)依据质量守恒定律可知生成氧气的质量为_______。
(3)剩余固体中含高锰酸钾的质量为多少g?(写出详细的计算过程)
题九: 19世纪末,物理学家瑞利在研究中发现,从分离空气得到的氮气的密度与从含氮物质中制
得的氮气的密度有0.0064kg/m3的差异,凭科学家敏锐的智慧,他没有放过这一微小的差异,在化学家
拉姆塞的协作下,经过十几年的努力,终于在1894年发现了空气中的氩。下列说法错误的是_______。
A. 分离空气得到氮气是化学变化
B. 从含氮物质中制得氮气是化学变化
C. 稀有气体在空气中的含量较少
D. 氩是一种无色无味的气体
题十: 小资料:1775年法国化学家拉瓦锡在定量研究空气组成时,发现从空气中分离得到N 的密
2
度与分离含氮物质得到N 的密度之间总有一个微小的差异,但这并没引起他的注意.一百多年后,英
2
国科学家雷利对这0.0064g/cm3的差异进行了分析,几经努力,他终于发现在空气中还存在着一种懒
惰的气体--氩气,从而发现了惰性气体家族。
[来源:学§科§网Z§X§X§K][来源:学|科|网Z|X|X|K]
(1)下面是科学家雷利在实验探究中的几个重要步骤,请补充完整:问题与猜想→______→分析与结
论→_______;
(2)某同学在探究空气成分中氧气的含量时,模拟了科学家的探究过程。他设计了如下实验:在由两
个注射器组成的密闭容器内留有25mL空气,给装有细铜丝的玻璃管加热(如图)。请你与之合作。继
续完成该实验的探究。
[来源:学科网]
1zxxk.com
身边的化学物质--空气
课后练习参考答案
题一: A
解析:A. 空气的主要成分是氮气和氧气,故A正确;B. 氮气占空气的体积分数约78%,氧气约为
21%,故B错;C. PM2.5 属于可吸入颗粒,可吸入颗粒是空气污染物监测的项目之一,含量越高说明
空气质量越差,故C错;D. 洁净的空气中含有氧气、氮气、二氧化碳等物质,属于混合物,故D错;故
选A。
题二: C
解析:空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸
气和杂质:0.03%;由于空气的成分一般是固定不变的许多旅客乘车穿越青藏高原时,会发生高原反
应,感到呼吸困难,这是因为高原地区空气比较稀薄,空气中各成分的含量不变,由于空气稀薄氧气
的含量相对来说就少了。故选C。
题三: A
解析:A. 空气中含有氧气与氮气等多种气体,再洁净也是混合物,故此选项正确;B. 空气是一种重
要的自然资源,对人类至关重要,故此选项错误;C. 空气中的多种气体成分都是与人类至关重要的,
是人赖以生存的资源之一,故此选项错误;D. 植物光合作用会消耗二氧化碳生成氧气,是自然界气
体循环的主要方式,故此选项错误;故选:A。
题四: A
解析:A. 空气质量报告中所列的空气质量级别越小,空气质量越好;故A说法正确;B. SO 、NO 属
2 2
于空气污染物,二氧化碳属于空气的成分;故B说法错误;C. 氧气的工业制法,它是利用氧气和氮气
的沸点不同,来分离出氧气,是物理方法;故C说法错误;D. 空气的成分及各成分的体积分数分别是:
氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%,是体积而不是质量。故D说法错误;故选A。
题五: C
解析:A. 红磷燃烧产生大量的白烟,而不是白色烟雾,故选项说法错误。B. 燃烧匙中的红磷不能换
成木炭,因为木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去
氧气,而增加了新的气体,不能用来测定空气中氧气含量,故选项说法错误。C. 冷却至室温后,打开
弹簧夹,加入集气瓶的水约占其容积的1/5,水不再继续进入,可说明氮气不易溶于水,故选项说法正
确。D. 红磷的量不足,不能将装置内的氧气完全消耗掉,会导致测定结果偏小,故选项说法错误。故
选:C。
题六: (1)将瓶内氧气耗尽(2)磷+氧气 五氧化二磷(3)红磷的量不够 (或未冷却到室温就
打开弹簧夹)
解析:(1)该实验中红磷应过量,目的是耗尽氧气。故填:将瓶内氧气耗尽;(2)磷与氧气在点燃的条
件下反应生成五氧化二磷;故填:磷+氧气 五氧化二磷;(3)进行此实验时,必须保证装置的气
密性良好,红磷足量,瓶子冷却后再打开弹簧夹,否则会导致结果不准确。红磷量不足,则不能将集气
瓶内空气中的氧气完全消耗掉,导致所测值偏小;同样如果装置密闭性不好,瓶外的空气进入集气瓶
内,导致进入水的体积减小,导致测得值偏小;如果未冷却至室温就打开止水夹,会使进入水的体积
偏小,导致测得值偏小。故填:红磷的量不够(或未冷却到室温就打开弹簧夹)。
题七: (1)化学;(2)m-m+m
4 2 1
解析:(1)锡粉放在密闭容器里进行完全燃烧,生成了白色固体物质,有新物质生成,锡的燃烧是化学
变化;(2)将这些锡粉放在密闭容器里进行完全燃烧,生成了白色固体物质,称量容器的总质量为
m。把白色物质放回原容器里(容器中白色的组成恢复到初始状态),重新称量容器的总质量为m,则
2 4
2zxxk.com
参加反应的气体的质量为m-m,生成白色物质的质量m=m-m+m。
4 2 3 4 2 1
题八: (1)2KMnO KMnO + MnO + O↑;(2)1.6g;(3)设参加反应的KMnO 质量为x,
4 2 4 2 2 4
2KMnO KMnO + MnO + O↑
4 2 4 2 2
316 32
x 1.6g
解得:x=15.8g
剩余的高锰酸钾的质量为:18g-15.8g=2.2g
解析:(1)高锰酸钾受热分解后生成锰酸钾、二氧化锰和氧气。化学反应方程式是:
2KMnO KMnO + MnO + O↑;(2)由质量守恒定律可知生成氧气的质量为=18g-16.4g=1.6g;
4 2 4 2 2
(3)设参加反应的KMnO 质量为x,
4
2KMnO KMnO + MnO + O↑
4 2 4 2 2
316 32
[来源:学科网ZXXK]
x 1.6g
解得:x=15.8g
剩余的高锰酸钾的质量为:18g-15.8g=2.2g。
题九: A
详解:分离空气得到氮气是物理变化,因此A说法错误;从含氮物质中制得氮气,因此有新物质生成,
是化学变化,因此B说法正确;稀有气体在空气中的含量较少,只占空气体积的0.94%,因此C说法
正确;氩是一种无色无味的气体,因此D说法正确,因此答案为A。
题十: (1)方案与实验、反思与评价(2)实验及现象:给玻璃管加热,交替缓慢推动两注射器,使铜
丝完全变为黑色,停止加热。玻璃管冷却至室温,将气体全部推入一支注射器。观察到活塞停至注射
器约20mL处。分析:加热时,空气中的氧气与铜发生反应,使玻璃管内的压强减小,所以减小的体积
即为空气中O 的体积;结论:空气并不是一种成分单一的气体,其中O 含量约占总体积的1/5。反思
2 2
与评价:在给玻璃管加热过程中,应同时交替缓慢推动两注射器,使反应更充分快速,铜丝的量要足。
解析:(1)实验探究中的重要步骤,主要有:问题与猜想→方案与实验→分析与结论→反思与评价。
(2)由于铜丝在加热的条件下与氧气,充分反应后,根据消耗的氧气的体积可知空气中氧气的体积分
数。所以,继续的实验探究为:实验及现象:给玻璃管加热,交替缓慢推动两注射器,使铜丝完全变为
黑色,停止加热。玻璃管冷却至室温,将气体全部推入一支注射器。观察到活塞停至注射器约20mL处。
分析:加热时,空气中的氧气与铜发生反应,使玻璃管内的压强减小,所以减小的体积即为空气中O
2
的体积;结
论:空气并不是一种成分单一的气体,其中O 含量约占总体积的1/5。反思与评价:在给玻璃管加热过
2
程中,应同时交替缓慢推动两注射器,使反应更充分快速,铜丝的量要足。因此答案为:(1)方案与实
验、反思与评价(2)实验及现象:给玻璃管加热,交替缓慢推动两注射器,使铜丝完全变为黑色,停止
加热。玻璃管冷却至室温,将气体全部推入一支注射器。观察到活塞停至注射器约20mL处。分析:加
3zxxk.com
热时,空气中的氧气与铜发生反应,使玻璃管内的压强减小,所以减小的体积即为空气中O 的体积;
2
结论:空气并不是一种成分单一的气体,其中O 含量约占总体积的1/5。反思与评价:在给玻璃管加热
2
过程中,应同时交替缓慢推动两注射器,使反应更充分快速,铜丝的量要足。
4