文档内容
zxxk.com
身边的化学物质--酸、碱经典精讲课后练习
题一: 氢氧化钠的俗名是( )
A.烧碱 B.小苏打 C.生石灰 D.纯碱
题二: 下列物质的性质中,属于化学性质的是( )
A.干冰易升华 B.浓盐酸易挥发
C.氢气可燃烧 D.氢氧化钠固体易潮解
题三: 下列是人体几种体液的正常pH范围,其中呈酸性的是( )
A.胰液7.5~8.0 B.胆汁7.1 ~7.3
C.血浆7.35~7.45 D.胃液0.9 ~1.5
题四: 下列物质加入水中,所得溶液pH可能为10的是( )
A.生石灰 B.醋酸 C.水杨酸 D.食盐
题五: 甲酸(HCOOH)是一种无色、有刺激性气味的液体,有较强的腐蚀性。
(1)若证明甲酸具有酸性,可选用的指示剂是 。
(2)甲酸与盐酸化学性质相似,能与碳酸钠反应,产生 气体。
(3)利用浓硫酸的脱水性,将甲酸和浓硫酸混合加热。甲酸脱水后会转变成 。
题六: 硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应: ;
②与碳酸钠溶液反应: ;
③与氯化钡溶液反应: ;
上述反应中,属于酸的共同性质的是 (填编号)。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)。
①除金属表面的锈 ②制造氯化锌 ③除去氯化钠中的氢氧化钠
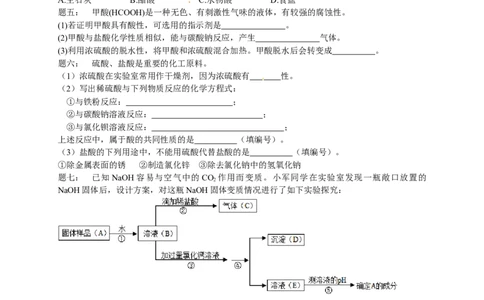
题七: 已知NaOH容易与空气中的CO 作用而变质。小军同学在实验室发现一瓶敞口放置的
2
NaOH固体后,设计方案,对这瓶NaOH固体变质情况进行了如下实验探究:
回答下列问题:
⑴上述实验操作的名称分别是:操作① ,操作④ 。
⑵根据上述实验,可以确定该固体 变质(选填“已”或“未”)
⑶步骤③中加过量氯化钙溶液的目的是 。
⑷若测得E的pH=7,则A的成分 ,若测得E的PH>7,则A的成分 。
题八: 实验室有一瓶久置的氢氧化钙粉末,某学习小组对这瓶氢氧化钙粉末的成分进行操究。
[提出问题]这瓶氢氧化钙粉末是否变质?
[猜想一]小丽同学认为这瓶氢氧化钙粉末已经变质。
[实验验证]请你设计实验证明小丽同学的观点,简要写出实验步骤及现象:
。
第 0 页zxxk.com
[结论一]这瓶氢氧化钙粉末已经变质。
[猜想二]小明同学认为“结论一”不全面,这瓶氢氧化钙粉末可能部分变质。
[实验验证]小明同学设计实验进行验证,请你将他的实验报告补充完整。
实验步骤 实验现象 结论
这瓶氢氧化钙粉末部分变质。
[思维拓展]由以上实验可知,清洗盛放石灰水的试剂瓶壁上的白色固体时可用 ,
请写出有关反应的化学方程式 。
题九: 化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧
化钠溶液的反应进行了探究,请你参与并填写以下空白。
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应。
第一组同学设计了实验方案一:
实验步骤 实验现象 结论
先用 H试纸测定稀盐酸的 H,再逐渐滴加氢氧化 H逐渐变大, 稀盐酸与氢氧化
P P P
钠溶液能发生反
钠溶液,并不断振荡,同时测定混合液的
P
H。 最后
P
H≥7
应
①请你分析上述方案中为什么强调只有测得的 H≥7才能证明反应发生了?
P
[来源:学科网ZXXK]
。
②写出稀盐酸与氢氧化钠溶液反应的化学方程式 。
(2)设计实验,探究稀盐酸与氢氧化钠溶液的反应是否放热
提供的实验仪器与药品:10%的盐酸、10%的氢氧化钠溶液、烧杯、温度计、玻璃棒、胶头滴管。
实验步骤 实验现象 结论 (3)探究
稀盐酸与氢氧化钠
稀盐酸与
溶液反应放热
氢氧化钠
溶液是否
恰好完全反应请你完成实验方案设计:
第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后,为探究稀盐酸与氢氧化钠溶液是否恰好完
全反应,设计了实验方案二:
实验步骤 实验现象 结论
取少量上述反应后的溶液于试 若 氢氧化钠溶液过量
管中,滴加硫酸铜溶液。
若没有明显现象 稀盐酸与氢氧化钠溶液恰好完
全反应
此时有同学提出方案二不能证明稀盐酸与氢氧化钠溶液恰好完全反应,其原因是
。为此,还需要选择 (填一种试剂),再进行实验即可。
第 1 页zxxk.com
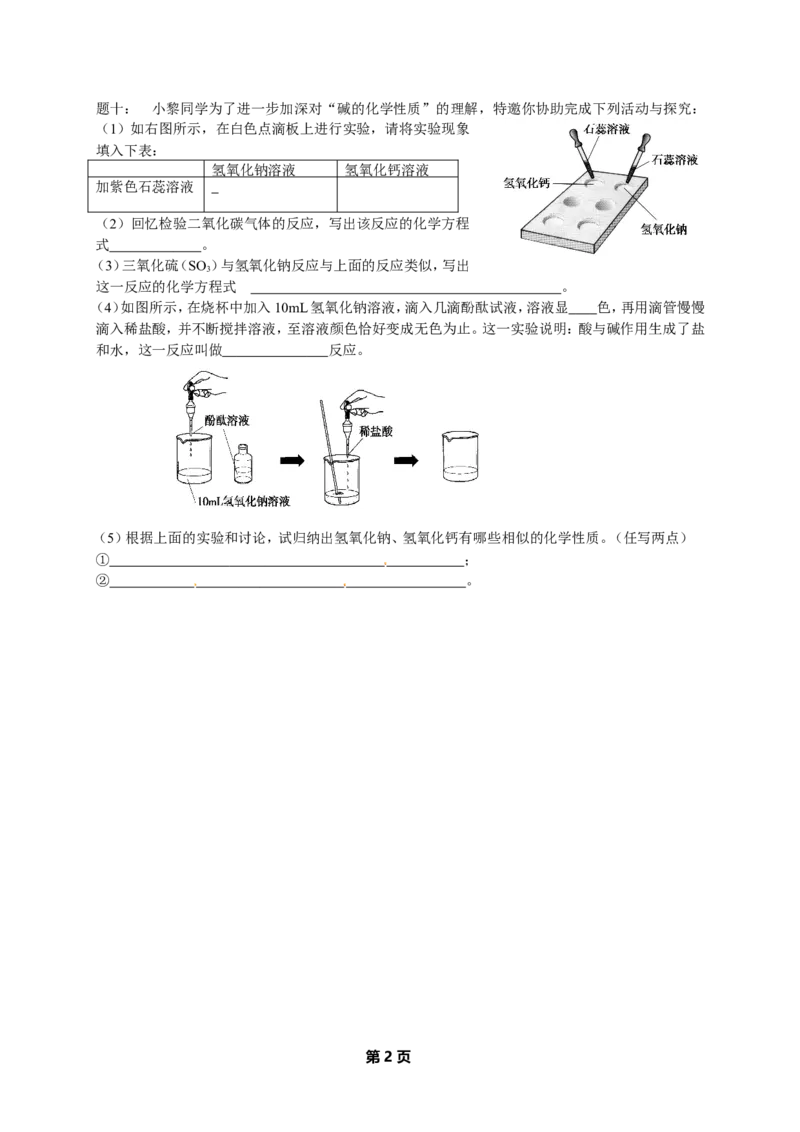
题十: 小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
(1)如右图所示,在白色点滴板上进行实验,请将实验现象
填入下表:
氢氧化钠溶液 氢氧化钙溶液
加紫色石蕊溶液
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程
式 。
(3)三氧化硫(SO )与氢氧化钠反应与上面的反应类似,写出
3
这一反应的化学方程式 。
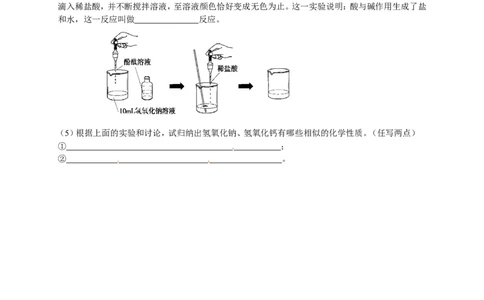
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显 色,再用滴管慢慢
滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐
和水,这一反应叫做 反应。
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点)
① ;
[来源:学科网]
② 。
[来源:学#科#网Z#X#X#K]
第 2 页zxxk.com
身边的化学物质--酸、碱经典精讲
[来源:Z*xx*k.Com]
课后练习参考答案
题一: A
解析:本题考查物质的俗名,属容易题。氢氧化钠的俗名是烧碱,小苏打的化学名称是碳酸氢钠,生石
灰是氧化钙,纯碱是碳酸钠,故选A。
题二: C
解析:解题的关键是明确物理性质与化学性质的根本区别为:是否需要通过化学变化表现出来。干冰
易升华、浓盐酸易挥发、氢氧化钠固体易潮解都不需通过化学变化就能表现出来,属于物理性质;氢
气可燃烧是通过氢气燃烧这一化学变化表现出来的,属于化学性质。
题三: D
解析:pH大于7的溶液显碱性,pH等于7的溶液呈中性,pH小于7的溶液呈酸性。胰液、胆汁、血浆
的pH大于7,都呈碱性;胃液的pH小于7,呈酸性。本题应选D。
题四: A
解析:pH大于7的溶液显碱性、pH等于7的溶液呈中性、pH小于7的溶液呈酸性。水呈中性,其
pH=7,向水中加入某种物质后,使水溶液的pH=10,则所加物质形成的溶液一定显碱性(pH>7)。生
石灰是氧化钙,溶于水后生成的氢氧化钙溶液显碱性,其pH有可能为10;醋酸、水杨酸均显酸性,其
溶液的pH均小于7;食盐的水溶液呈中性,其溶液的pH=7。本题应选A。
题五: (1)紫色石蕊溶液 (2)二氧化碳 (3)一氧化碳和水(或一氧化碳)
解析:本题考查酸的性质。紫色石蕊试液遇酸、碱性不同的溶液能够显示不同的颜色,因此可用紫色
石蕊试液证明甲酸是否具有酸性;碳酸钠等碳酸盐均能与酸溶液发生反应生成二氧化碳气体;分析甲
酸(HCOOH)的分子结构,可以推断出甲酸与浓硫酸反应脱水后会生成CO气体。
题六: ⑴ 吸水性
⑵①Fe + H SO =FeSO + H ↑ ②NaCO + H SO =Na SO + H O + CO ↑
2 4 4 2 2 3 2 4 2 4 2 2
③HSO + BaCl =BaSO ↓+ 2HCl;
2 4 2 4
⑶ ②③
解析:(1)浓硫酸具有吸水性,所以实验室常用作干燥剂;(2)铁与硫酸反应生成硫酸亚铁和氢气,硫
酸与碳酸钠反应生成硫酸钠、水和二氧化碳,氯化钡与硫酸反应生成硫硫酸反应是因为铁将酸中的氢
元素置换出来,碳酸钠与硫酸反应是因为酸钡沉淀和氯化氢,根据反应物生成物及书写化学方程式的
原则写出化学方程式;铁与碳酸根离子与氢离子结合成了二氧化碳和水,这两条都属于酸的共同性质,
而硫酸与氯化钡反应是因为硫酸根离子与钡离子结合成硫酸钡沉淀,不属于酸的共同性质;(3)盐酸
与硫酸都能除金属表面的锈,故盐酸可用硫酸代替;盐酸制造氯化锌是盐酸中的阴离子氯离子与锌离
子结合成氯化锌,不能用硫酸代替;除去氯化钠中的氢氧化钠,盐酸与氢氧化钠反应生成氯化钠,硫
酸与氢氧化钠反应生成新杂质硫酸钠,故不能用硫酸代替盐酸。
题七: ⑴①溶解 ④过滤 ⑵已 ⑶使碳酸钠(或碳酸根离子)沉淀完全 ⑷碳酸钠钠;氢氧化钠和碳
酸钠
解析:固体溶解于水得到溶液,不溶性的固体和液体分离需采用过滤的方法;NaOH变质是氢氧化钠
与空气中的二氧化碳发生了化学反应(2NaOH+CO =Na CO+H O),NaCO 与稀盐酸能够反应产生
2 2 3 2 2 3
二氧化碳气体,图中显示,向样品溶于水得到的溶液中加入稀盐酸后产生气体(反应②),说明该氢氧
化钠固体样品已经变质;由于氢氧化钠和碳酸钠都具有碱性,故需将 NaCO 转化为呈中性的盐后
2 3
(CaCl +Na CO=CaCO ↓+2NaCl),才能检验是否含有氢氧化钠;若测得E的pH=7,则说明氢氧化钠
2 2 3 3
已全部变质,其成分为碳酸钠;若测得E的pH>7,说明该氢氧化钠固体样品中仍有未变质的氢氧化
钠,即氢氧化钠部分变质,其成分为氢氧化钠和碳酸钠。
题八: 取少量粉末于试管中,向试管中加入适量的稀盐酸,有气泡产生;
实验步骤 实验现象 结论
取少量粉末于试管中,加水 无色酚酞变红色 这瓶氢氧化钙粉末部分变质。
第 3 页zxxk.com
溶解,静置,向试管中滴加 (或有白色沉淀产生)
无色酚酞试液(或取少量粉
末于试管中,加水溶解,静
置,取上层清液,加入适量
的碳酸溶液)
稀盐酸;CaCO +2HCl=CaCl +H O+CO↑
3 2 2 2
解析:氢氧化钙易与空气中的二氧化碳发生化学反应而变质,变质的氢氧化钙中会含有碳酸钙,检验
碳酸钙的最佳方法是向样品中滴加稀盐酸,看是否产生使澄清石灰水变浑浊的二氧化碳气体;若要
证明氢氧化钙是否部分变质,应在向样品中滴加稀盐酸之前,先用酚酞试液检验样品放入水中后形成
的上层清液是否显碱性或向上层清液中滴加碳酸钠溶液,看是否有白色沉淀产生,以检验样品中是否
含有未变质的氢氧化钙;由于碳酸钙能与稀盐酸反应而被溶解,因此试剂瓶壁上的碳酸钙可用稀盐酸
除去。
题九: ⑴①排除因氢氧化钠溶液的加入,稀释盐酸而引起 H变大(或只有 H≥7才能说明盐酸已
P P
经反应掉了)② NaOH+HCl=NaCl+H O
2
⑵如下表所示。
⑶生成 实验步骤 实验现象 蓝色沉
取一定量10%的氢氧化钠溶液于烧杯,插入温度计测温 温度计示数上升
淀;若 盐酸过
度;加入适量10%的盐酸,用玻璃棒搅拌,再测温度。 (或温度升高)
量,加 入硫酸
铜溶液时也无明显现象(或盐酸可能有剩余);紫色石蕊试液(或锌粒、碳酸钠、氧化铜、氢氧化铜、pH
试纸等)
解析:⑴稀盐酸的pH<7,若向其中加入一种不能与之发生反应的溶液,其pH会因溶液被稀释而升
高,但只能无限趋近于7而不能大于7,因此,若测得溶液的 H≥7,表明稀盐酸与加入的氢氧化钠溶
P
液发生了化学反应,二者反应的化学方程式为:NaOH+HCl=NaCl+H O;⑶用温度计测量反应前后溶
2
液温度的变化,即可判断出该反应是否放热;由复分解反应发生的条件可以判断出:NaCl、 HCl均不
与CuSO 发生反应,而NaOH能与CuSO 发生反应并生成蓝色絮状沉淀,反应的化学方程式为
4 4
CuSO +2NaOH=Cu(OH) ↓+Na SO ;因此,向反应后的溶液中加入CuSO 溶液,根据是否产生蓝色沉
4 2 2 4 4
淀可判断NaOH是否过量;若无蓝色沉淀产生,可向反应后的溶液中加入紫色石蕊试液(或锌粒、碳
酸盐、不溶性的金属氧化物和不溶性的碱等物质),以验证溶液中是否有HCl剩余,则可进一步判断
稀盐酸和氢氧化钠是否恰好完全反应。
题十: (1)溶液变蓝;溶液变蓝;(2)CO+Ca(OH) =CaCO↓+H O;
2 2 3 2
(3)SO +2NaOH=Na SO +H O;红;(4)中和;(5)都能使指示剂变色;都能和某些非金属氧化物反应
3 2 4 2
(或都能跟酸反应,其他合理答案均可)
解析:⑴碱会使紫色石蕊变蓝色,氢氧化钠和氢氧化钙溶液中具有相同的氢氧根离子,都能使紫色石
蕊试液变蓝色;⑵CO 是酸性氧化物与碱反应生成盐和水,实验室检验CO 的存在,常用和澄清石灰
2 2
水反应生成CaCO 沉淀来检验;⑶SO 和NaOH反应生成硫酸钠和水;⑷酚酞与碱变红色,与酸不变
3 3
色,氢氧化钠是碱,所以与酚酞溶液变红,酸和碱反应生成盐和水的反应叫中和反应;⑸根据以上实
验可总结出其化学性质。
第 4 页