文档内容
雅礼教育集团 2025 年上期期中考试
高一化学试卷
命题人:李剑锋 审题人:王念慈
时量:75分钟 满分:100分
可能用到的相对原子质量:H~1 C~12 O~16 Mg~24
一、单选题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求)
1.科学技术的持续发展离不开每一位能工巧匠、科学大家的不懈努力,下列说法错误的是
A.我国是世界上发明陶瓷、冶金、火药、造纸、酿酒等较早的国家,在长期的生活和生产实
践中,积累了大量有关物质及其变化的实用知识和技能
B.抗战时期,我国科学家侯德榜先生通过数百次对原有的制碱法——氨碱法改进试验,发明
了侯氏制碱法,大大提高了原料利用率,缩短生产流程,减少对环境污染。
C.意大利科学家阿伏加德罗经过不懈努力,编制了一张现代元素周期表,使化学的研究变得
有规律可循
D.我国科学家第一次用化学方法合成了具有生物活性的蛋白质——结晶牛胰岛素
2.中国中医药博大精深,《疡医大全·卷二十九》记载“皂矾(又名绿矾,成份FeSO 7HO)”
4 2
具有外用治疗癣痒功效。按物质组成分类,FeSO 7HO属于
4 2
A.碱 B.盐 C.酸 D.混合物
3.下列关于分散系的说法中,不正确的是
A.分散系的稳定性:溶液>胶体>浊液
B.分散质粒子的直径大小:溶液<胶体<浊液
C.利用丁达尔效应可以区分溶液与胶体
D.向氢氧化钠溶液中边滴加饱和FeCl 溶液边振荡制备Fe(OH) 胶体
3 3
4.下列对应离子方程式书写正确的是
A.Fe(OH) 溶于稀硫酸:H+ + OH-===HO
3 2
B.Fe粉投入CuSO 溶液:2Fe + 3Cu2+ ===3Cu + 2Fe3+
4
C.NaHCO 溶液和NaOH溶液混合:HCO - + OH-===CO↑ + H O
3 3 2 2
D.向漂白粉溶液中通入少量CO:Ca2+ + 2ClO- + CO + H O ===CaCO↓+ 2HClO
2 2 2 3
5.下列图示中,操作规范的是
A. 配制
B.洗涤盛有氯化 D.长期存放NaCO 标
CuSO C.蒸发NaCl溶液 2 3
4 钠废液的试管 准溶液
溶液
A.A B.B C.C D.D
6.氮化铝(AlN)被广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过如下反应制取:
Al O+N+3C 2AlN+3CO。下列叙述正确的是
2 3 2A.AlN中N元素的化合价为-3价
B.Al O 发生氧化反应
2 3
C.反应中N 做还原剂,被氧化
2
D.反应中有电子的转移,是因为有元素的化合价发生变化
7.工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Ni、Si等元素)制备MnSO ,工艺流
4
程如图:
下列说法正确的是
A.已知“滤渣1”中含有S,“溶浸”中生成S的反应中氧化剂与还原剂的物质的量之比为
1:2
B.“氧化”中添加适量的MnO 的作用是将 氧化 为以保证铁元素全部进入“滤渣2”
2
C.为提高生产效率,“调pH”工序应该在较高温度下进行
D.沉锰的离子反应为:Mn2+ + HCO -= MnCO ↓ + H+
3 3
8.室温下,通过下列实验探究新制饱和氯水的性质。
实验1:用pH计测量新制饱和氯水的pH,测得pH约为2.2;
实验2:向淀粉KI溶液中滴加过量氯水,溶液先变蓝,后褪色;
实验3:向FeCl 溶液中滴加适量氯水,溶液颜色变成棕黄色;
2
实验4:向氯水中加入少量碳酸钙粉末,产生无色气体。
下列说法正确的是
A.用强光照射实验1中的溶液,溶液的pH增大
B.实验2可以证明HClO有强氧化性
C.实验3反应后溶液中大量存在的离子有:ClO-、Fe3+、Cl-、H+
D.实验4产生的气体是CO,反应后的溶液漂白能力增强
2
9.下列“推理或结论”与“实验操作及现象”相符的一组是
选项 实验操作及现象 推理或结论
取少量NaO 粉末放在脱脂棉上,再将1滴水滴到
A 2 2 NaO 与水的反应是放热反应
NaO 上,脱脂棉燃烧 2 2
2 2
B 向碳酸钠溶液中逐滴滴加盐酸 立即产生大量气泡
C 将NaO 投入到紫色石蕊溶液中 溶液先变红,后褪色
2 2
用洁净的铂丝蘸取某溶液样品,在酒精灯外焰上灼
D 溶液中含有 ,不含
烧,透过蓝色钴玻璃观察到火焰为紫色
A.A B.B C.C D.D
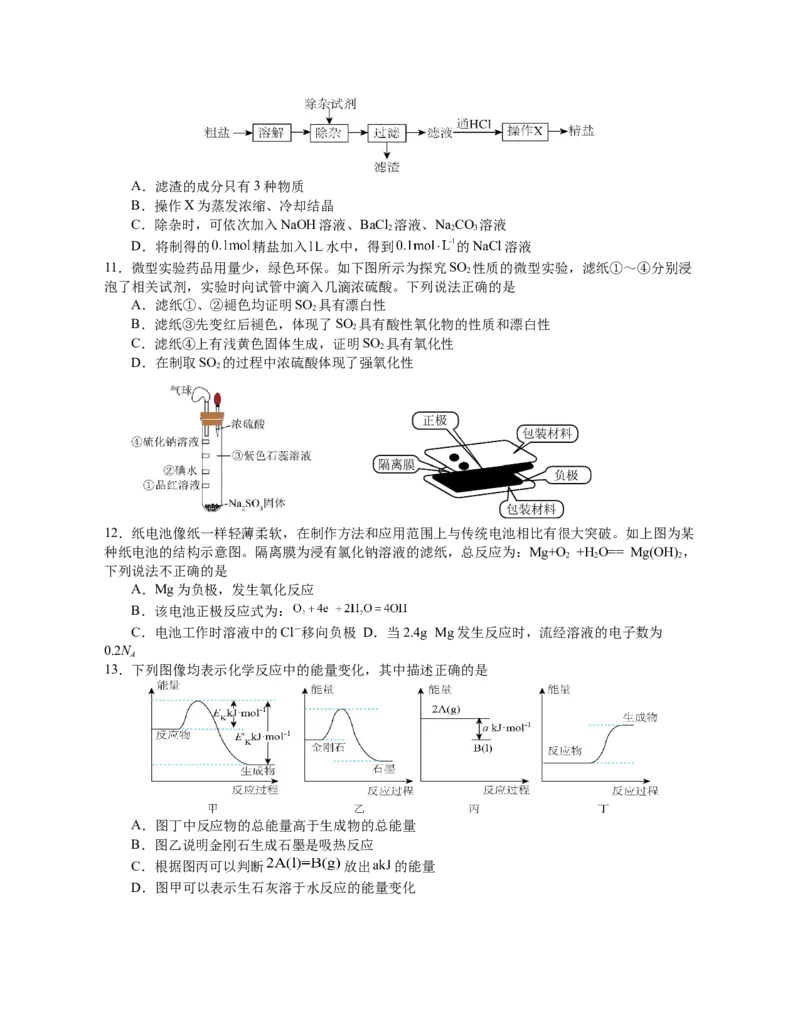
10.粗盐中含有Ca2+、Mg2+、SO 2-杂质,通过如图所示的流程制备精盐,并配制一定浓度的
4
溶液。下列说法正确的是A.滤渣的成分只有3种物质
B.操作X为蒸发浓缩、冷却结晶
C.除杂时,可依次加入NaOH溶液、BaCl 溶液、NaCO 溶液
2 2 3
D.将制得的 精盐加入 水中,得到 的NaCl溶液
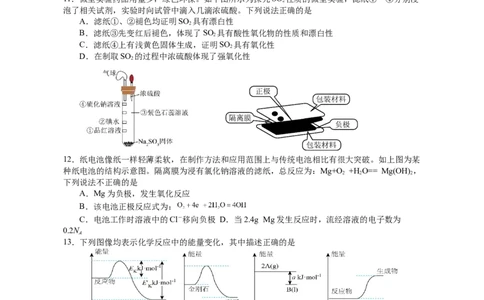
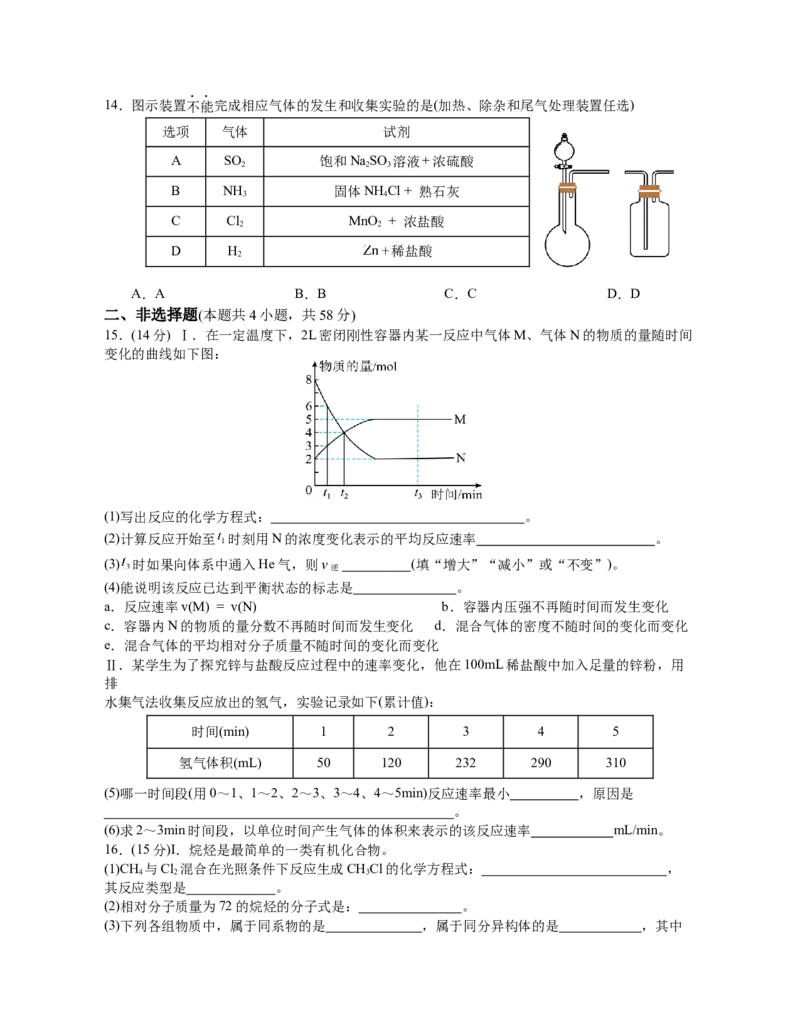
11.微型实验药品用量少,绿色环保。如下图所示为探究SO 性质的微型实验,滤纸①~④分别浸
2
泡了相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法正确的是
A.滤纸①、②褪色均证明SO 具有漂白性
2
B.滤纸③先变红后褪色,体现了SO 具有酸性氧化物的性质和漂白性
2
C.滤纸④上有浅黄色固体生成,证明SO 具有氧化性
2
D.在制取SO 的过程中浓硫酸体现了强氧化性
2
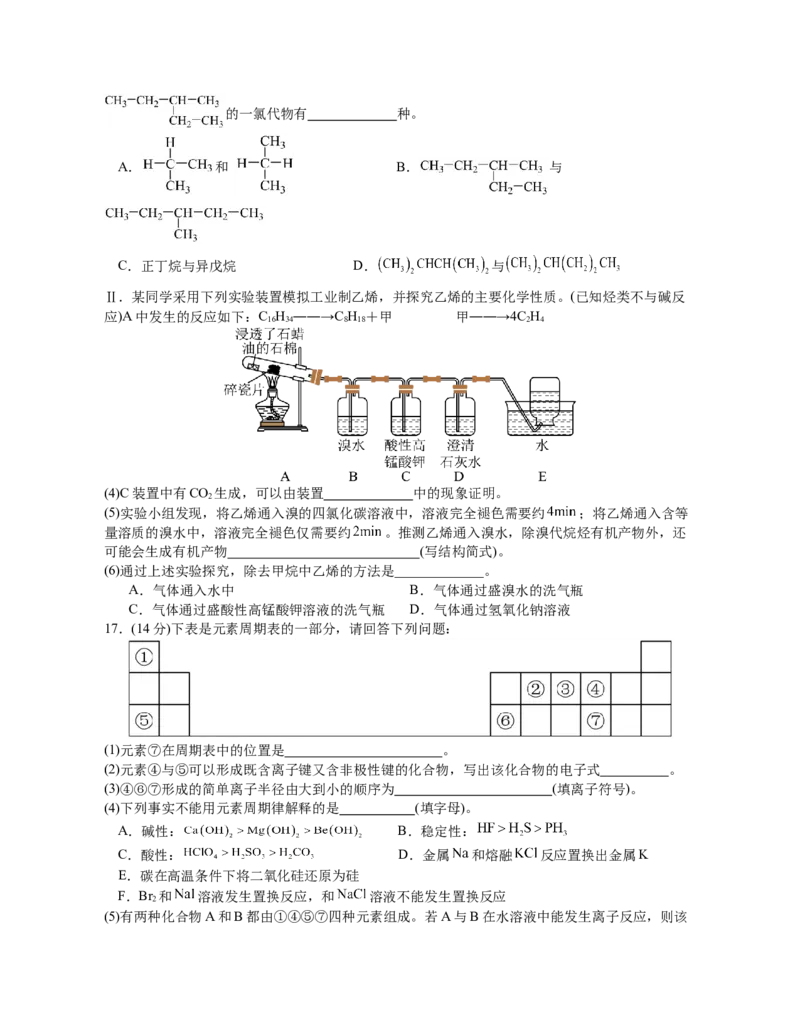
12.纸电池像纸一样轻薄柔软,在制作方法和应用范围上与传统电池相比有很大突破。如上图为某
种纸电池的结构示意图。隔离膜为浸有氯化钠溶液的滤纸,总反应为:Mg+O +H O== Mg(OH) ,
2 2 2
下列说法不正确的是
A.Mg为负极,发生氧化反应
B.该电池正极反应式为:
C.电池工作时溶液中的Cl-移向负极 D.当2.4g Mg发生反应时,流经溶液的电子数为
0.2N
A
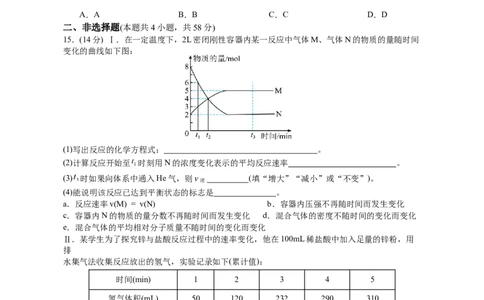
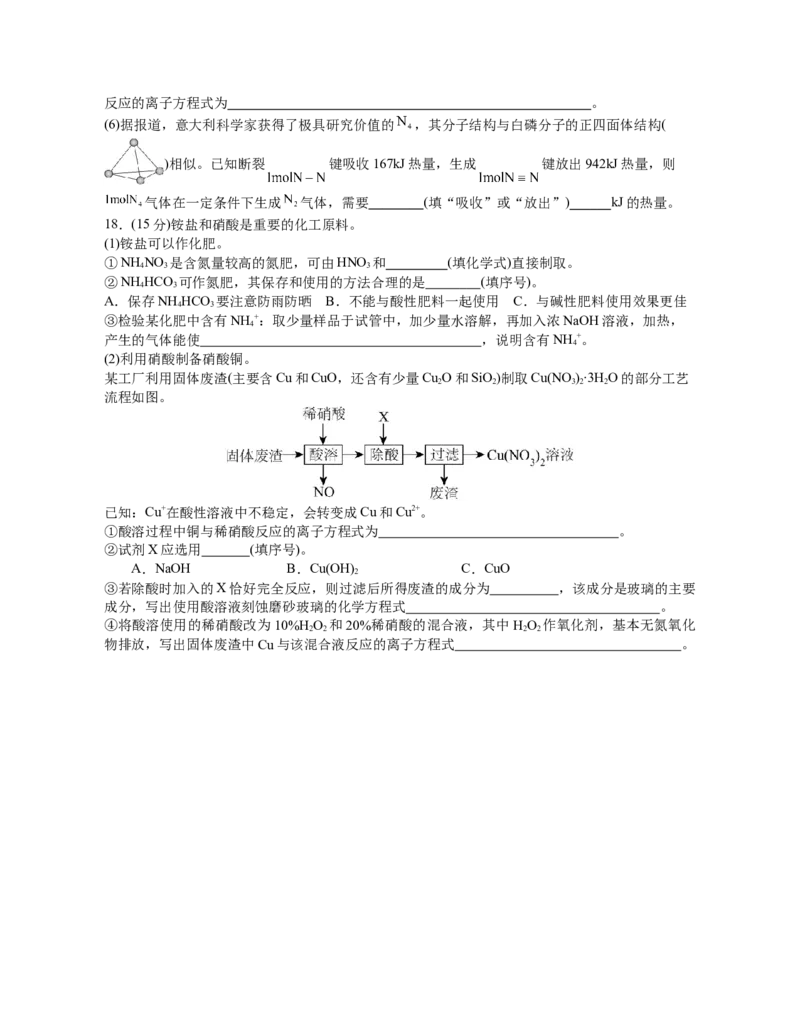
13.下列图像均表示化学反应中的能量变化,其中描述正确的是
A.图丁中反应物的总能量高于生成物的总能量
B.图乙说明金刚石生成石墨是吸热反应
C.根据图丙可以判断 放出 的能量
D.图甲可以表示生石灰溶于水反应的能量变化14.图示装置不能完成相应气体的发生和收集实验的是(加热、除杂和尾气处理装置任选)
选项 气体 试剂
A SO 饱和NaSO 溶液 浓硫酸
2 2 3
B NH 固体NH Cl + 熟石灰
3 4
C Cl MnO + 浓盐酸
2 2
D H 稀盐酸
2
A.A B.B C.C D.D
二、非选择题(本题共4小题,共58分)
15.(14分) Ⅰ.在一定温度下,2L密闭刚性容器内某一反应中气体M、气体N的物质的量随时间
变化的曲线如下图:
(1)写出反应的化学方程式: 。
(2)计算反应开始至 时刻用N的浓度变化表示的平均反应速率 。
(3) 时如果向体系中通入He气,则v (填“增大”“减小”或“不变”)。
逆
(4)能说明该反应已达到平衡状态的标志是 。
a.反应速率v(M) = v(N) b.容器内压强不再随时间而发生变化
c.容器内N的物质的量分数不再随时间而发生变化 d.混合气体的密度不随时间的变化而变化
e.混合气体的平均相对分子质量不随时间的变化而变化
Ⅱ.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用
排
水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) 1 2 3 4 5
氢气体积(mL) 50 120 232 290 310
(5)哪一时间段(用0~1、1~2、2~3、3~4、4~5min)反应速率最小 ,原因是
。
(6)求2~3min时间段,以单位时间产生气体的体积来表示的该反应速率 mL/min。
16.(15分)Ⅰ.烷烃是最简单的一类有机化合物。
(1)CH 与Cl 混合在光照条件下反应生成CHCl的化学方程式: ,
4 2 3
其反应类型是 。
(2)相对分子质量为72的烷烃的分子式是: 。
(3)下列各组物质中,属于同系物的是 ,属于同分异构体的是 ,其中的一氯代物有 种。
A. 和 B. 与
C.正丁烷与异戊烷 D. 与
Ⅱ.某同学采用下列实验装置模拟工业制乙烯,并探究乙烯的主要化学性质。(已知烃类不与碱反
应)A中发生的反应如下:C H ――→C H +甲 甲――→4C H
16 34 8 18 2 4
(4)C装置中有CO 生成,可以由装置 中的现象证明。
2
(5)实验小组发现,将乙烯通入溴的四氯化碳溶液中,溶液完全褪色需要约 ;将乙烯通入含等
量溶质的溴水中,溶液完全褪色仅需要约 。推测乙烯通入溴水,除溴代烷烃有机产物外,还
可能会生成有机产物 (写结构简式)。
(6)通过上述实验探究,除去甲烷中乙烯的方法是_____________。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
17.(14分)下表是元素周期表的一部分,请回答下列问题:
(1)元素⑦在周期表中的位置是 。
(2)元素④与⑤可以形成既含离子键又含非极性键的化合物,写出该化合物的电子式 。
(3)④⑥⑦形成的简单离子半径由大到小的顺序为 (填离子符号)。
(4)下列事实不能用元素周期律解释的是 (填字母)。
A.碱性: B.稳定性:
C.酸性: D.金属 和熔融 反应置换出金属K
E.碳在高温条件下将二氧化硅还原为硅
F.Br 和 溶液发生置换反应,和 溶液不能发生置换反应
2
(5)有两种化合物A和B都由①④⑤⑦四种元素组成。若A与B在水溶液中能发生离子反应,则该反应的离子方程式为 。
(6)据报道,意大利科学家获得了极具研究价值的 ,其分子结构与白磷分子的正四面体结构(
)相似。已知断裂 键吸收167kJ热量,生成 键放出942kJ热量,则
气体在一定条件下生成 气体,需要 (填“吸收”或“放出”) kJ的热量。
18.(15分)铵盐和硝酸是重要的化工原料。
(1)铵盐可以作化肥。
①NH NO 是含氮量较高的氮肥,可由HNO 和 (填化学式)直接制取。
4 3 3
②NH HCO 可作氮肥,其保存和使用的方法合理的是 (填序号)。
4 3
A.保存NH HCO 要注意防雨防晒 B.不能与酸性肥料一起使用 C.与碱性肥料使用效果更佳
4 3
③检验某化肥中含有NH +:取少量样品于试管中,加少量水溶解,再加入浓NaOH溶液,加热,
4
产生的气体能使 ,说明含有NH +。
4
(2)利用硝酸制备硝酸铜。
某工厂利用固体废渣(主要含Cu和CuO,还含有少量Cu O和SiO)制取Cu(NO )∙3H O的部分工艺
2 2 3 2 2
流程如图。
已知:Cu+在酸性溶液中不稳定,会转变成Cu和Cu2+。
①酸溶过程中铜与稀硝酸反应的离子方程式为 。
②试剂X应选用 (填序号)。
A.NaOH B.Cu(OH) C.CuO
2
③若除酸时加入的X恰好完全反应,则过滤后所得废渣的成分为 ,该成分是玻璃的主要
成分,写出使用酸溶液刻蚀磨砂玻璃的化学方程式 。
④将酸溶使用的稀硝酸改为10%H O 和20%稀硝酸的混合液,其中HO 作氧化剂,基本无氮氧化
2 2 2 2
物排放,写出固体废渣中Cu与该混合液反应的离子方程式 。