文档内容
zxxk.com
身边的化学物质--二氧化碳课后练习
题一: 下列实验方法一定能达到实验目的是( )
选 实验目的 实验方法
项
A 鉴别KCl和NH NO 取样与熟石灰混合研磨,闻气味
[来源:学,科,网 4 3
Z,X,X,K]
B 鉴别H 和CH 分别点燃,在火焰上方罩一干冷
2 4
烧杯
C 鉴别石灰水和NaOH溶 加入适量的稀盐酸
液
D 检验一瓶气体是否为 将燃着的木条伸入瓶中
CO
2
题二: (双选)下列鉴别物质的方法中,切实可行的是( )
A. 用酚酞溶液鉴别NaCl溶液和盐酸
B. 用燃着的木条鉴别CO 和CO
2
C. 用石蕊溶液鉴别稀盐酸和稀硫酸
D. 用水鉴别NaOH和CaCO 固体
3
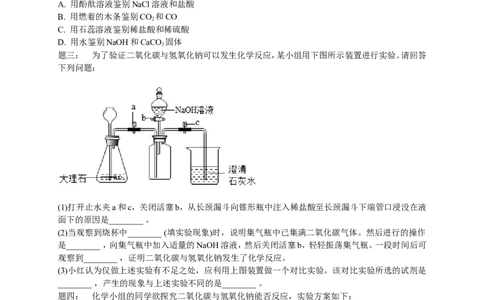
题三: 为了验证二氧化碳与氢氧化钠可以发生化学反应,某小组用下图所示装置进行实验。请回答
下列问题:
(1)打开止水夹a和c,关闭活塞b,从长颈漏斗向锥形瓶中注入稀盐酸至长颈漏斗下端管口浸没在液
面下的原因是________ 。
(2)当观察到烧杯中________ (填实验现象)时,说明集气瓶中已集满二氧化碳气体。然后进行的操作
是________ ,向集气瓶中加入适量的NaOH溶液,然后关闭活塞b,轻轻振荡集气瓶。一段时间后可
观察到________ ,证明二氧化碳与氢氧化钠发生了化学反应。
(3)小红认为仅做上述实验有不足之处,应利用上图装置做一个对比实验。该对比实验所选的试剂是
________ ,产生的现象与上述实验不同的是________ 。
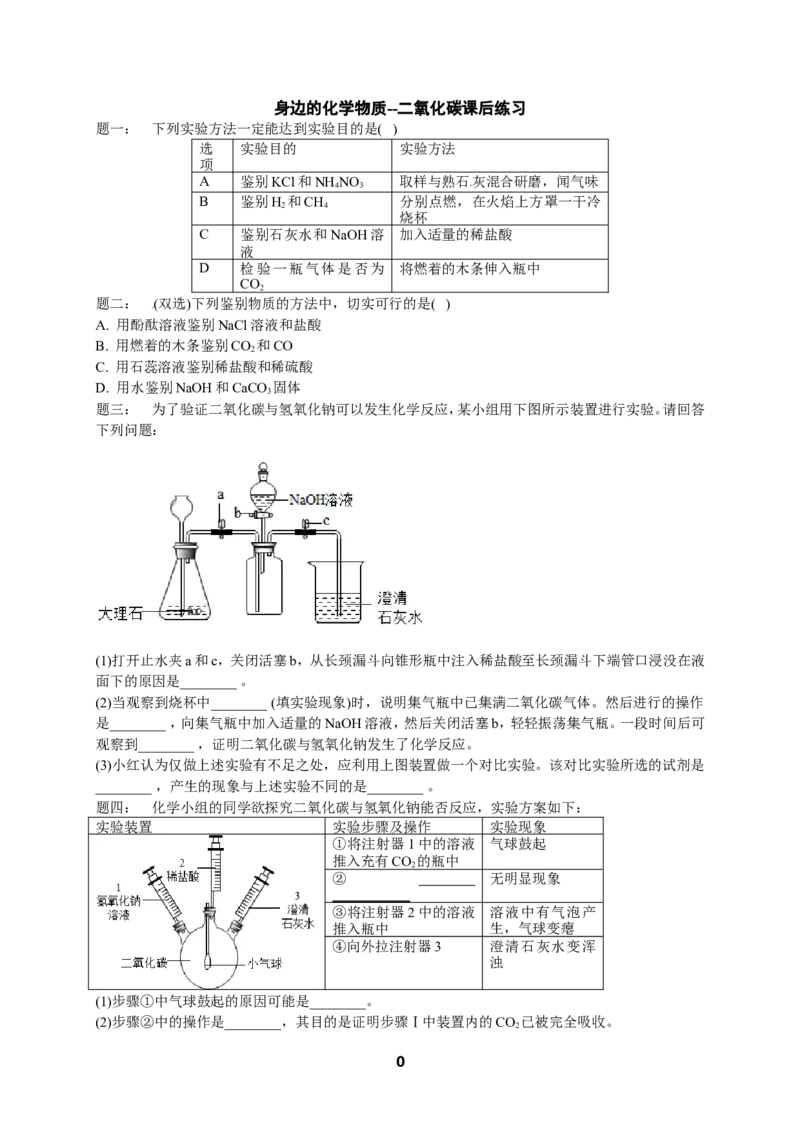
题四: 化学小组的同学欲探究二氧化碳与氢氧化钠能否反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液 气球鼓起
推入充有CO 的瓶中
2
② 无明显现象
___________
③将注射器2中的溶液 溶液中有气泡产
推入瓶中 生,气球变瘪
④向外拉注射器3 澄清石灰水变浑
浊
(1)步骤①中气球鼓起的原因可能是________。
(2)步骤②中的操作是________,其目的是证明步骤Ⅰ中装置内的CO 已被完全吸收。
2
0zxxk.com
(3)步骤④中发生反应的化学方程式为________。
(4)本实验的结论是________。
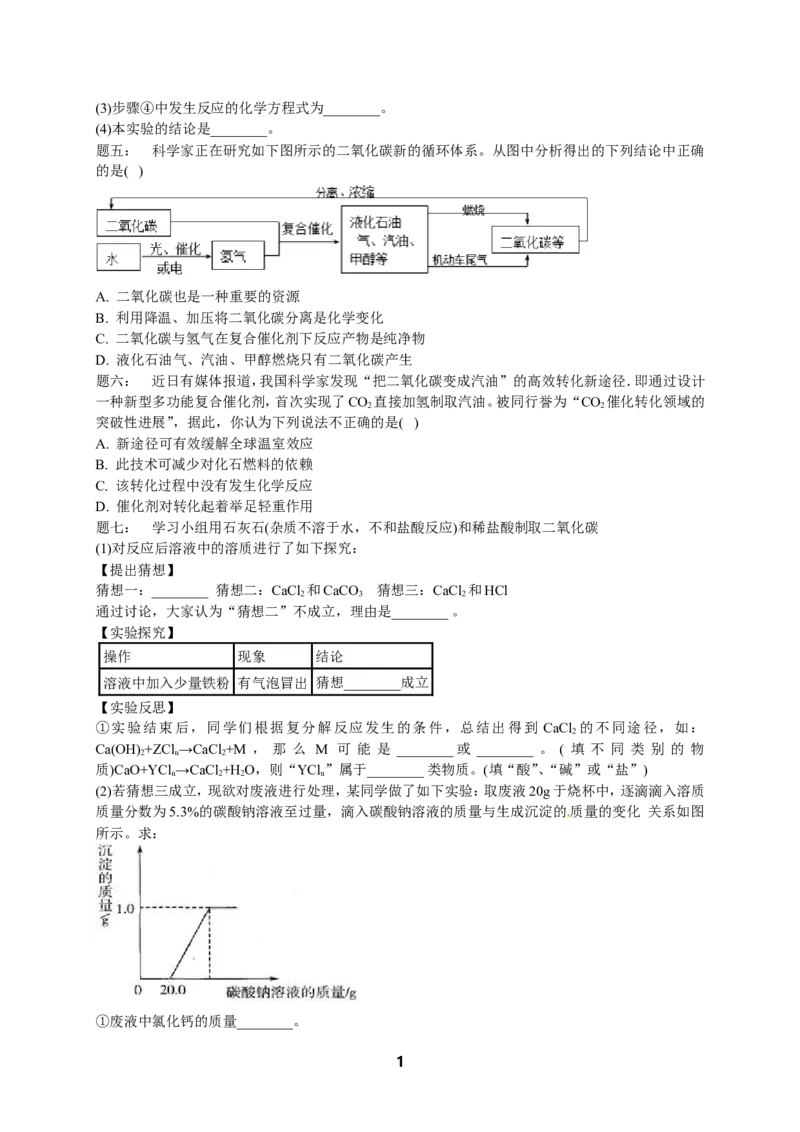
题五: 科学家正在研究如下图所示的二氧化碳新的循环体系。从图中分析得出的下列结论中正确
的是( )
A. 二氧化碳也是一种重要的资源
B. 利用降温、加压将二氧化碳分离是化学变化
C. 二氧化碳与氢气在复合催化剂下反应产物是纯净物
D. 液化石油气、汽油、甲醇燃烧只有二氧化碳产生
题六: 近日有媒体报道,我国科学家发现“把二氧化碳变成汽油”的高效转化新途径.即通过设计
一种新型多功能复合催化剂,首次实现了CO 直接加氢制取汽油。被同行誉为“CO 催化转化领域的
2 2
突破性进展”,据此,你认为下列说法不正确的是( )
A. 新途径可有效缓解全球温室效应
B. 此技术可减少对化石燃料的依赖
C. 该转化过程中没有发生化学反应
D. 催化剂对转化起着举足轻重作用
题七: 学习小组用石灰石(杂质不溶于水,不和盐酸反应)和稀盐酸制取二氧化碳
(1)对反应后溶液中的溶质进行了如下探究:
【提出猜想】
猜想一:________ 猜想二:CaCl 和CaCO 猜想三:CaCl 和HCl
2 3 2
通过讨论,大家认为“猜想二”不成立,理由是________ 。
【实验探究】
操作 现象 结论
溶液中加入少量铁粉 有气泡冒出 猜想________成立
【实验反思】
①实验结束后,同学们根据复分解反应发生的条件,总结出得到 CaCl 的不同途径,如:
2
Ca(OH)+ZCl →CaCl +M , 那 么 M 可 能 是 ________ 或 ________ 。 ( 填 不 同 类 别 的 物
2 n 2
质)CaO+YCl →CaCl +H O,则“YCl ”属于________ 类物质。(填“酸”、“碱”或“盐”)
n 2 2 n
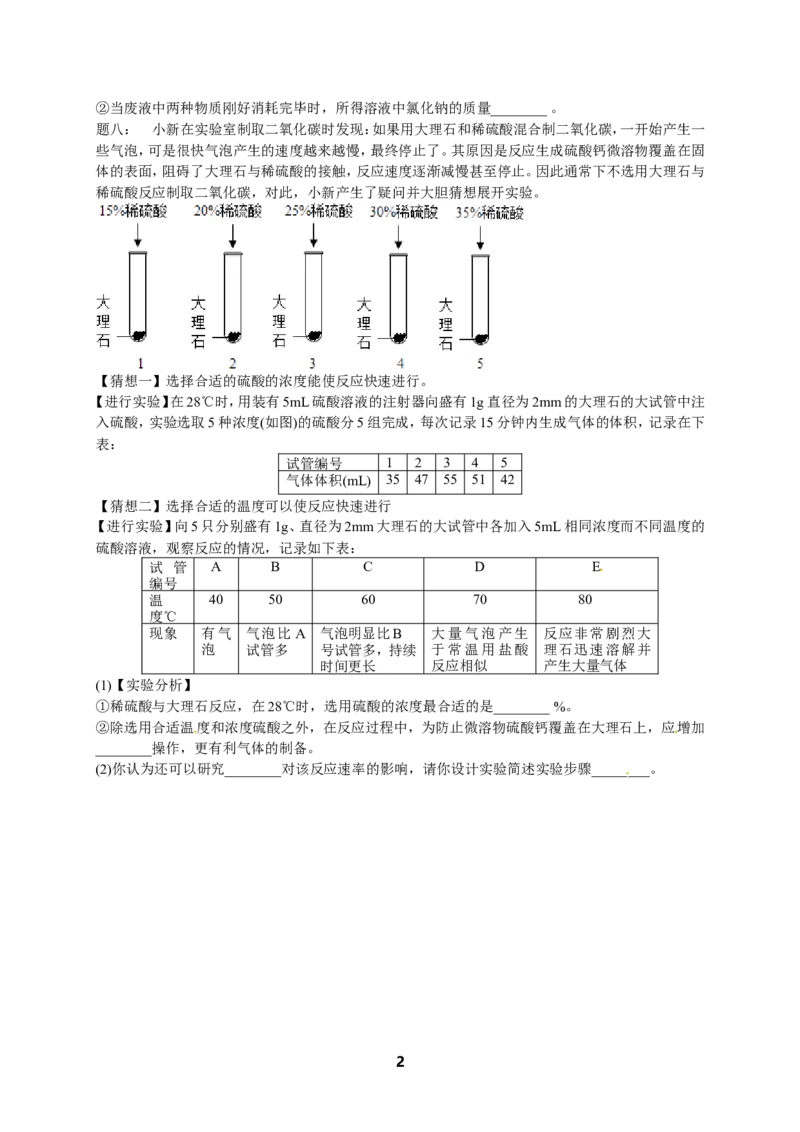
(2)若猜想三成立,现欲对废液进行处理,某同学做了如下实验:取废液20g于烧杯中,逐滴滴入溶质
质量分数为5.3%的碳酸钠溶液至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化 关系如图
所示。求:
①废液中氯化钙的质量________。
1zxxk.com
②当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量________ 。
题八: 小新在实验室制取二氧化碳时发现:如果用大理石和稀硫酸混合制二氧化碳,一开始产生一
些气泡,可是很快气泡产生的速度越来越慢,最终停止了。其原因是反应生成硫酸钙微溶物覆盖在固
体的表面,阻碍了大理石与稀硫酸的接触,反应速度逐渐减慢甚至停止。因此通常下不选用大理石与
稀硫酸反应制取二氧化碳,对此,小新产生了疑问并大胆猜想展开实验。
【猜想一】选择合适的硫酸的浓度能使反应快速进行。
【进行实验】在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm的大理石的大试管中注
入硫酸,实验选取5种浓度(如图)的硫酸分5组完成,每次记录15分钟内生成气体的体积,记录在下
表:
试管编号 1 2 3 4 5
气体体积(mL) 35 47 55 51 42
[网来Z源XX:学K]科
【猜想二】选择合适的温度可以使反应快速进行
【进行实验】向5只分别盛有1g、直径为2mm大理石的大试管中各加入5mL相同浓度而不同温度的
硫酸溶液,观察反应的情况,记录如下表:
试 管 A B C D E
编号
温 40 50 60 70 80
[来源:学科网ZXXK]
度℃
现象 有气 气泡比 A 气泡明显比B 大量气泡产生 反应非常剧烈大
泡 试管多 号试管多,持续 于常温用盐酸 理石迅速溶解并
时间更长 反应相似 产生大量气体
[来源:Z_xx_k.Com]
(1)【实验分析】
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适的是________ %。
②除选用合适温度和浓度硫酸之外,在反应过程中,为防止微溶物硫酸钙覆盖在大理石上,应增加
________操作,更有利气体的制备。
(2)你认为还可以研究________对该反应速率的影响,请你设计实验简述实验步骤________。
2zxxk.com
身边的化学物质--二氧化碳课后练习参考答案
题一:A
解析:A、NH NO 与熟石灰混合研磨,放出有刺激性气味的气体,KCl不能,可以鉴别,故选项实验方
4 3
法能达到实验目的。 B、H 和CH 燃烧均会产生水蒸气,分别点燃,在火焰上方罩一干冷烧杯,均会
2 4
生成水蒸气,不能鉴别,故选项实验方法不能达到实验目的。C、石灰水和NaOH溶液均能与稀盐酸反
应,分别生成氯化钙和水、氯化钠和水,均无明显变化,不能鉴别,故选项实验方法不能达到实验目的。
D、检验一瓶气体是否为CO , 应使用澄清的石灰水,不能使用燃着的木条,故选项实验方法不能达
2
到实验目的。故选:A。
题二:BD
解析:A、氯化钠溶液呈中性,盐酸呈酸性,酚酞在酸性和中性溶液中为无色,现象相同,无法鉴别,故
A错误; B、二氧化碳不支持燃烧,能使燃着的木条熄灭,一氧化碳能燃烧,现象不同,可以鉴别,故
B正确;C、盐酸和硫酸都呈酸性,石蕊试液在酸性溶液中为红色,现象相同,无法鉴别,故C错误;D、
氢氧化钠易溶于水,而碳酸钙不溶于水,现象不同,可以鉴别,故D正确;故选BD。
题三:(1)防止生成的气体从长颈漏斗中逸出;(2)溶液出现浑浊 ;关闭止水夹a,打开活塞b;烧杯中
的混浊液体从导管倒吸入集气瓶中;(3)水;从烧杯中倒吸入集气瓶中的液体较少
解析:(1)如果长颈漏斗下端管口没有浸没在液面以下,则生成的气体会从长颈漏斗中逸出。(2)由于集
气瓶采用的是向上排空气法收集二氧化碳,故当集气瓶中已集满二氧化碳气体后,气体会从导气管进
入烧杯中的石灰水中去,则可根据烧杯中澄清石灰水变浑浊,证明集气瓶中已集满二氧化碳气体;向
集气瓶中加入适量的NaOH溶液,需打开活塞b;因为本实验是通过集气瓶内的压强改变来证明二氧
化碳与氢氧化钠的反应,故需同时关闭止水夹a;由于集气瓶中二氧化碳与氢氧化钠反应,集气瓶中
的气压会减小,则大气压会将烧杯中的浊液,压入集气瓶中。(3)由于CO 不仅能溶于水,而且能与水
2
反应,故也会造成集气瓶内压强减小,所以不能得出CO 与NaOH溶液发生反应的结论;为了更严谨,
2
应将氢氧化钠溶液换成水,进行对比实验,可观察到二氧化碳与水反应时,水从烧杯中倒吸进入集气
瓶中的液体要少的多,从而证明CO 与NaOH溶液发生了反应。
2
题四:(1)NaOH溶液吸收CO 装置内压强变小,气球鼓起;(2)向外拉注射器3(或充分振荡);
2
(3)Ca(OH)+CO ═HO+CaCO ↓;(4)CO 能和NaOH反应
2 2 2 3 2
解析:(1)NaOH溶液吸收CO 装置内压强变小,在外界大气压的作用下气球鼓起;(2)向外拉注射器
2
3(或充分振荡),如果无任何现象,证明步骤1中装置内的CO 已被完全吸收;(3)二氧化碳与氢氧化钙
2
反应生成碳酸钙沉淀和水,碳酸钙后面标上沉淀符号,所以化学方程式是:Ca(OH)+CO =
2 2
HO+CaCO ↓;(4)本实验就是为了证明二氧化碳能与氢氧化钠发生化学反应。故答案为:(1)NaOH溶
2 3
液 吸 收 CO 装 置 内 压 强 变 小 , 气 球 鼓 起 ; (2) 向 外 拉 注 射 器 3( 或 充 分 振 荡 ) ;
2
(3)Ca(OH)+CO ═HO+CaCO ↓(4)CO 能和NaOH反应。
2 2 2 3 2
题五:A
解析:A. 二氧化碳也是一种重要的资源,正确;B. 利用降温、加压将二氧化碳分离的过程中没有新
物质生成,属于物理变化,错误;C. 二氧化碳与氢气在复合催化剂下反应产物是混合物,错误;D. 液
化石油气、汽油、甲醇等物质燃烧有二氧化碳和水产生,
错误;故选A。
题六:C
解析:A. 我国科学家发现“把二氧化碳变成汽油”的高效转化新途径,通过设计一种新型多功能复
合催化剂,首次实现了CO 直接加氢制取汽油,可有效缓解全球温室效应,故选项说法正确。B. 由题
2
意,实现了CO 直接加氢制取汽油,此技术可减少对化石燃料的依赖,故选项说法正确。C. 实现了
2
CO 直接加氢制取汽油,有新物质生成,属于化学变化,故选项说法错误。D. 通过设计一种新型多功
2
能复合催化剂,首次实现了CO 直接加氢制取汽油,催化剂对转化起着举足轻重作用,故选项说法正
2
确。故选:C。
3zxxk.com
题七:CaCl ;CaCO 不溶于水;猜想三成立;Cu(OH) ;HO;酸;1.11g;2.34g
2 3 2 2
解析:⑴【提出猜想】根据题意可知,石灰石(杂质不溶于水,不和盐酸反应)和稀盐酸反应生成氯化钙、
水和二氧化碳气体(逸出),故反应后溶液中的溶质中一定含有生成的氯化钙,若二者恰好完全反应,
则只生成氯化钙;若盐酸过量,则可能还含有盐酸;结合题意可知,猜想一为CaCl ;由于探究的是反
2
应后溶液中的溶质,而CaCO 不溶于水,不可能为溶质,故“猜想二”不成立。【实验探究】根据反应
3
现象“溶液中加入少量铁粉,有气泡冒出”可知,该溶液中含有酸,故猜想三成立。【实验反思】:根
据复分解反应发生的条件,结合氢氧化钙的化学性质分析可知,若要Ca(OH) +ZCl →CaCl +M的反
2 n 2
应能成立,则M要么是Z(OH) 沉淀,要么是水,故该反应可能是碱和盐的反应,生成新碱(沉淀)和新
2
盐,因此M可能是Cu(OH) 、Fe(OH) 、Mg(OH) 、Zn(OH) 、Al(OH) 、Fe(OH) 等难溶性碱,则Z可能是
2 2 2 2 3 3
CuCl 、FeCl 、MgCl 、ZnCl、AlCl 、FeCl 中的一种;也有可能是酸和碱的反应,生成盐和水,故Z可能
2 2 2 2 3 3
是盐酸。根据金属氧化物与酸反应能生成盐和水,结合CaO+YCl →CaCl +H O,可知YCl 属于酸。
n 2 2 n
(2)①由图中数据可知,开始加入碳酸钠溶液,并没有沉淀生成,说明是碳酸钠溶液先与盐酸反应,而
CaCl 尚未反应;当碳酸钠溶液滴加至20g时,碳酸钠与盐酸恰好完全反应;继续滴加碳酸钠溶液,碳
2
酸钠才与氯化钙反应,生成碳酸钙沉淀和氯化钠;且二者恰好完全反应时,生成碳酸钙沉淀1g。
设废液中氯化钙的质量为x
CaCl +NaCO=CaCO ↓+2NaCl
2 2 3 3
111 100
x 1g
解得x=1.11g
答:废液中氯化钙的质量为1.11g。
②由于废液中的两种物质都能与碳酸钠溶液反应,都能生成氯化钠,故当废液中两种物质刚好消耗完
毕时,所得溶液中的氯化钠的质量等于两个反应生成的氯化钠的质量和。
设与氯化钙反应生成的氯化钠的质量为y
CaCl +NaCO=CaCO ↓+2NaCl
2 2 3 3
100 117
1g y
解得,y = 1.17g
设与盐酸反应生成的氯化钠的质量为z
NaCO+2HCl=2NaCl+HO+CO↑
2 3 2 2
106 117
20g×5.3% z
解得,z = 1.17g
所以,氯化钠的总质量 = 1.17 g + 1.17 g = 2.34 g
答:当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量为2.34 g。
题八:(1)25;摇动试管;(2)碳酸钙固体颗粒大小;取1 g块状大理石与5 mL 25%稀硫酸,有少量气
泡;取1g粉末状大理石与5 mL 25%稀硫酸,迅速产生较多气泡
4zxxk.com
解析:(1)①观察实验一图表,3号试管收集的气体最多,此时管中硫酸浓度是25%。浓度大于或小于
此浓度值生成的气体体积都少。②为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法除去覆盖在
大理石上的硫酸钙。(2)碳酸钙固体颗粒大小也会影响反应的速率,也可作为研究课题;设计实验步骤
如下:
取1 g块状大理石与5 mL 25%稀硫酸,有少量气泡;取1g粉末状大理石与5mL25%稀硫酸,迅速产
生较多气泡。故答案为:(1)①25;②摇动试管。(2)碳酸钙固体颗粒大小;取1 g块状大理石与5 mL
25%稀硫酸,有少量气泡;取1 g粉末状大理石与5 mL 25%稀硫酸,迅速产生较多气泡。
5