文档内容
第三章 章末测试
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
一、单选题(每题4分,共14题,56分)
1.(2020·全国高一单元测试)下列中国制造的产品主体用料不是金属材料的是
世界最大射电望远镜 中国第一艘国产航母 中国大飞机C919 世界最长的港珠澳大桥
A.钢索 B.钢材 C.铝合金 D.硅酸盐
2.(2020·全国课时练习)金属和合金是生活中常用的材料。下列说法正确的是
A.不锈钢是铁合金,只含金属元素
B.镧镍(La-Ni)合金能大量吸收H 形成金属氢化物,可作储氢材料
2
C.目前世界上使用量最大的合金是铝合金
D.常温下,铁粉可以和水发生置换反应得到氢气
3.(2020·全国课时练习)下列有关铝及其化合物的说法错误的是( )
A.铁易生锈,而铝在空气中较稳定,所以铁比铝活泼
B.可用铝壶烧水,不可用其长期存放食醋、碱水
C.氧化铝是—种较好的耐火材料,但不可用氧化铝坩埚熔化
D. 能跟强酸、强碱溶液反应生成盐和水,所以它是两性氧化物
4.(2020·上海市南洋模范中学月考)用FeCl 溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉。对加
3
入铁粉充分反应后的溶液分析合理的是
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出5.(2020·全国课时练习)在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡,将两球分别浸
没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是( )
A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
B.铝球表面有气泡产生,溶液澄清
C.反应后去掉两烧杯,杠杆仍平衡
D.铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边上升
6.(2020·洮南市第一中学月考)13.6gFe和Fe O 的混合物,加入150mL足量的稀硫酸,在标准状况下收
2 3
集到1.12LH ,向反应后的溶液中滴加KSCN溶液不变红。为中和过量的HSO ,并使Fe元素全部转化为
2 2 4
Fe(OH) 沉淀,恰好消耗了200mL 3mol/L的NaOH溶液,则该稀HSO 的物质的量浓度为( )
2 2 4
A.2.25mol/L B.2mol/L C.3mol/L D.0.6mol/L
7.(2020·全国高一单元测试)下列有关铁及其化合物的说法正确的是( )
A.铁的氧化物有 、 、 ,它们都是黑色的固体
B. 、 的混合物可能是灰绿色
C.鉴别 中混有的 ,可先加入氯水,再加入 溶液
D.生铁含碳量低于钢
8.(2020·全国高一单元测试)某无色稀溶液与铝作用放出H,则下列离子在该溶液中可能大量共存的是
2
( )
A. 、Cu2+、 、 B.K+、Na +、Cl-、Mg2+
C.Na+、K+、 、 D.K+、Ca2+、 、
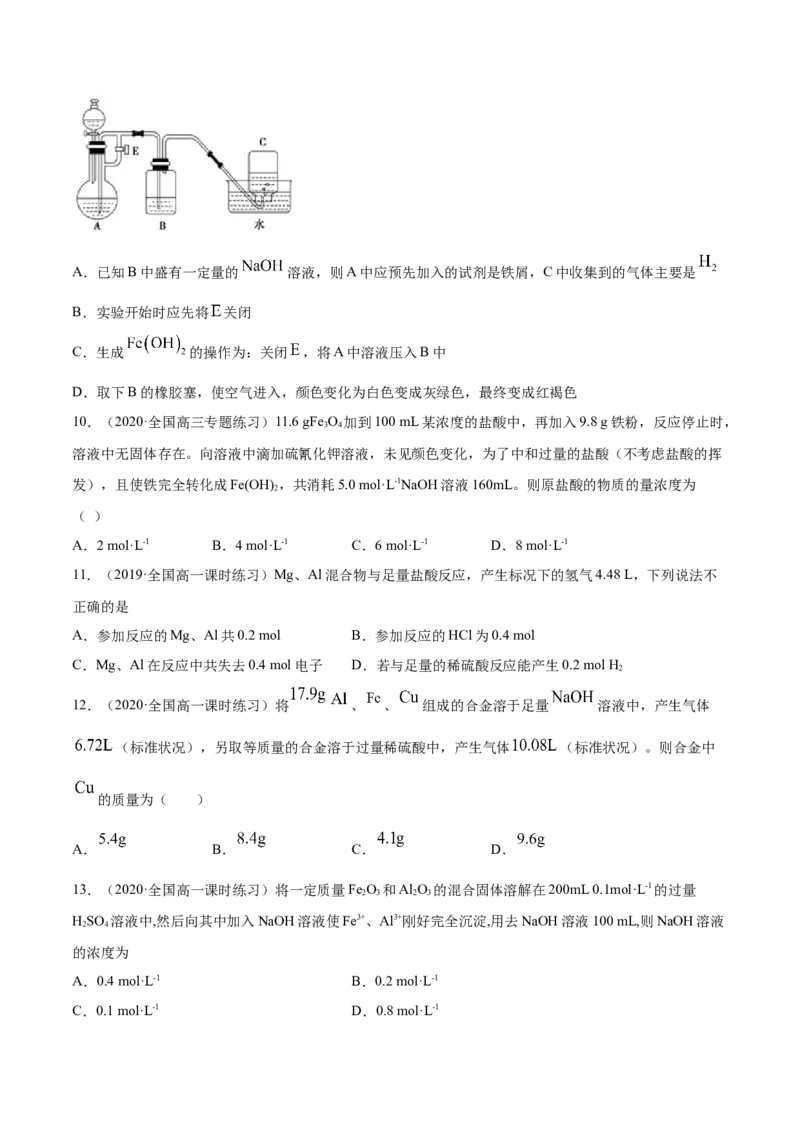
9.(2019·全国高一课时练习)如图所示装置可用来制取 和观察 在空气中被氧化时的
颜色变化。实验提供的试剂:铁屑、 的硫酸溶液、 溶液。下列说法错误的是( )A.已知B中盛有一定量的 溶液,则A中应预先加入的试剂是铁屑,C中收集到的气体主要是
B.实验开始时应先将 关闭
C.生成 的操作为:关闭 ,将A中溶液压入B中
D.取下B的橡胶塞,使空气进入,颜色变化为白色变成灰绿色,最终变成红褐色
10.(2020·全国高三专题练习)11.6 gFe O 加到100 mL某浓度的盐酸中,再加入9.8 g铁粉,反应停止时,
3 4
溶液中无固体存在。向溶液中滴加硫氰化钾溶液,未见颜色变化,为了中和过量的盐酸(不考虑盐酸的挥
发),且使铁完全转化成Fe(OH) ,共消耗5.0 mol·L-1NaOH溶液160mL。则原盐酸的物质的量浓度为
2
( )
A.2 mol·L-1 B.4 mol·L-1 C.6 mol·L-1 D.8 mol·L-1
11.(2019·全国高一课时练习)Mg、Al混合物与足量盐酸反应,产生标况下的氢气4.48 L,下列说法不
正确的是
A.参加反应的Mg、Al共0.2 mol B.参加反应的HCl为0.4 mol
C.Mg、Al在反应中共失去0.4 mol电子 D.若与足量的稀硫酸反应能产生0.2 mol H
2
12.(2020·全国高一课时练习)将 、 、 组成的合金溶于足量 溶液中,产生气体
(标准状况),另取等质量的合金溶于过量稀硫酸中,产生气体 (标准状况)。则合金中
的质量为( )
A. B. C. D.
13.(2020·全国高一课时练习)将一定质量Fe O 和Al O 的混合固体溶解在200mL 0.1mol·L-1的过量
2 3 2 3
HSO 溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100 mL,则NaOH溶液
2 4
的浓度为
A.0.4 mol·L-1 B.0.2 mol·L-1
C.0.1 mol·L-1 D.0.8 mol·L-114.(2020·全国高一课时练习)工业上以铝土矿(主要成分为Al O,含Fe O 杂质)为原料冶炼铝的工艺流
2 3 2 3
程如下:
下列叙述正确的是( )
A.试剂X 可以是氢氧化钠溶液,也可以是盐酸
B.反应①过滤后所得沉淀为氢氧化铁
C.反应②的化学方程式为NaAlO +CO +2H O=Al(OH) ↓+NaHCO
2 2 2 3 3
D.图中所有反应都不是氧化还原反应
第II卷(非选择题)
二、填空题(共44分)
15.(8分)(2020·全国高一单元测试)某同学设计如下实验方案,以分离混合溶液中的AlCl 和FeCl 。
3 2
(1)沉淀A的化学式为________________ 。
(2)写出AlCl 溶液与过量NaOH溶液反应的离子方程式:___________________________。
3
(3)写出沉淀A转化为沉淀B反应的化学方程式:___________________。
(4)写出检验溶液A中是否含有Fe2+时的方法:________________________________。
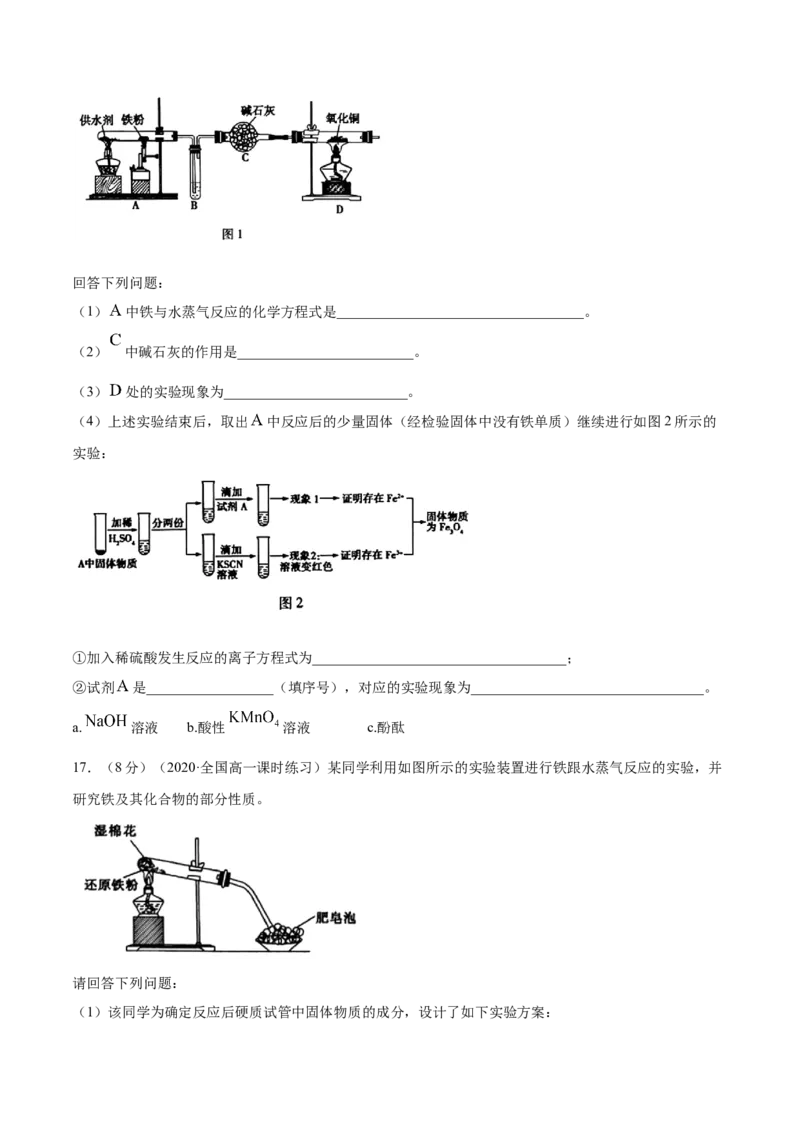
16.(8分)(2020·全国高一课时练习)在 时能产生稳定水蒸气的物质都可以作为铁与水蒸气
反应的供水剂,已知铁与水蒸气的反应在 左右进行。某化学兴趣小组同学采用西红柿(或洋葱)作
为供水剂,设计了如图1所示的装置进行实验,并对铁与水蒸气反应的产物进行检验。回答下列问题:
(1) 中铁与水蒸气反应的化学方程式是___________________________________。
(2) 中碱石灰的作用是_________________________。
(3) 处的实验现象为__________________________。
(4)上述实验结束后,取出 中反应后的少量固体(经检验固体中没有铁单质)继续进行如图2所示的
实验:
①加入稀硫酸发生反应的离子方程式为____________________________________;
②试剂 是__________________(填序号),对应的实验现象为_________________________________。
a. 溶液 b.酸性 溶液 c.酚酞
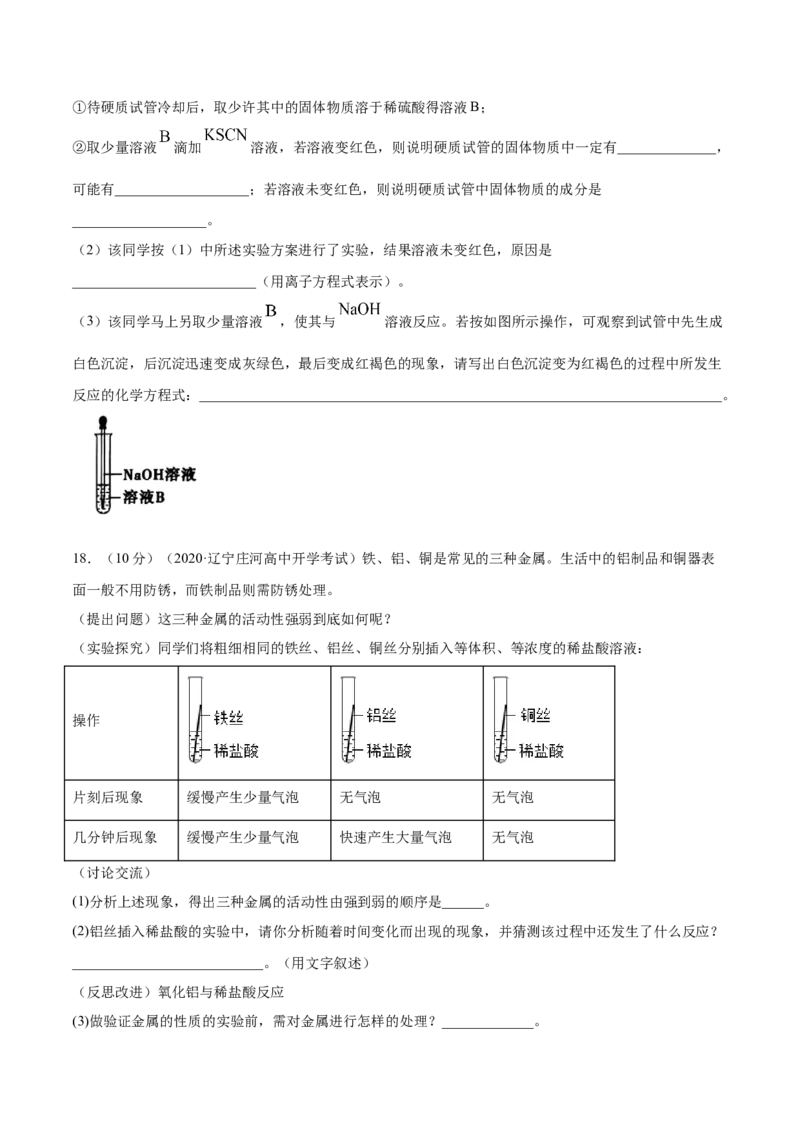
17.(8分)(2020·全国高一课时练习)某同学利用如图所示的实验装置进行铁跟水蒸气反应的实验,并
研究铁及其化合物的部分性质。
请回答下列问题:
(1)该同学为确定反应后硬质试管中固体物质的成分,设计了如下实验方案:①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液 滴加 溶液,若溶液变红色,则说明硬质试管的固体物质中一定有______________,
可能有___________________;若溶液未变红色,则说明硬质试管中固体物质的成分是
___________________。
(2)该同学按(1)中所述实验方案进行了实验,结果溶液未变红色,原因是
__________________________(用离子方程式表示)。
(3)该同学马上另取少量溶液 ,使其与 溶液反应。若按如图所示操作,可观察到试管中先生成
白色沉淀,后沉淀迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变为红褐色的过程中所发生
反应的化学方程式:__________________________________________________________________________。
18.(10分)(2020·辽宁庄河高中开学考试)铁、铝、铜是常见的三种金属。生活中的铝制品和铜器表
面一般不用防锈,而铁制品则需防锈处理。
(提出问题)这三种金属的活动性强弱到底如何呢?
(实验探究)同学们将粗细相同的铁丝、铝丝、铜丝分别插入等体积、等浓度的稀盐酸溶液:
操作
片刻后现象 缓慢产生少量气泡 无气泡 无气泡
几分钟后现象 缓慢产生少量气泡 快速产生大量气泡 无气泡
(讨论交流)
(1)分析上述现象,得出三种金属的活动性由强到弱的顺序是______。
(2)铝丝插入稀盐酸的实验中,请你分析随着时间变化而出现的现象,并猜测该过程中还发生了什么反应?
___________________________。(用文字叙述)
(反思改进)氧化铝与稀盐酸反应
(3)做验证金属的性质的实验前,需对金属进行怎样的处理?_____________。(4)有同学提出“只用一支盛有少量稀盐酸的试管,只需调整金属丝的插入顺序,也能证明三种金属的活动
性顺序”。则金属丝的插入顺序可以为______(填一种顺序即可)。
(拓展迁移)将一定质量的铝粉放入含有硫酸亚铁、硫酸铜的混合溶液中,充分反应后,过滤。向滤出的
固体中滴加稀硫酸,发现有气泡产生。
(5)滤液中一定含有的溶质是______(填化学式)。
(6)该过程中产生气体时,一定发生的反应的化学方程式为______。
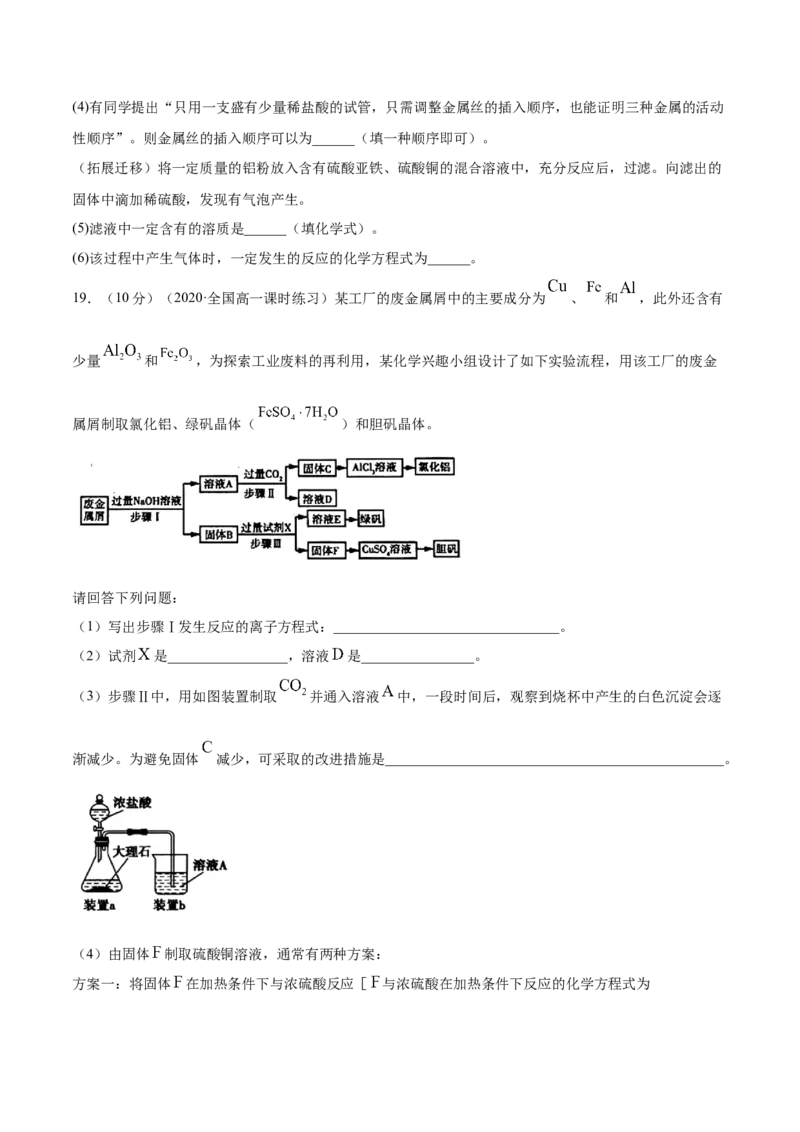
19.(10分)(2020·全国高一课时练习)某工厂的废金属屑中的主要成分为 、 和 ,此外还含有
少量 和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的废金
属屑制取氯化铝、绿矾晶体( )和胆矾晶体。
请回答下列问题:
(1)写出步骤Ⅰ发生反应的离子方程式:________________________________。
(2)试剂 是_________________,溶液 是________________。
(3)步骤Ⅱ中,用如图装置制取 并通入溶液 中,一段时间后,观察到烧杯中产生的白色沉淀会逐
渐减少。为避免固体 减少,可采取的改进措施是________________________________________________。
(4)由固体 制取硫酸铜溶液,通常有两种方案:
方案一:将固体 在加热条件下与浓硫酸反应[ 与浓硫酸在加热条件下反应的化学方程式为];
方案二:将固体 投入热的稀硫酸中,然后通入氧气。
方案一的缺点是_____________________________________________________________________________。