文档内容
第三章章末检测
1.晶体是一类非常重要的材料,在很多领域都有广泛的应用。我国现已能够拉制出直
径为300 mm、重达81 kg的大直径硅单晶,晶体硅材料被大量用于电子产业。下列叙
述正确的是( )
A.形成晶体硅的速率越快越好
B.晶体硅有固定的熔点,研碎后就变成了非晶体
C.可用X射线衍射实验来区分晶体硅和玻璃
D.晶体硅具有自范性,但无各向异性
2.下列物质固态时,一定是分子晶体的是( )
A.酸性氧化物 B.非金属单质 C.碱性氧化物 D.含氧酸
3.三氯化硼的熔点为-107.3℃,沸点为12.5℃,三氯化硼中Cl B C1键角为120°,
它可以水解,水解产物之一是氯化氢。下列关于三氯化硼的叙述中正确的是( )
A.三氯化硼是共价晶体
B.熔融时,三氯化硼能导电
C.三氯化硼是一种极性分子
D.三氯化硼的水解方程式为
4.下列关于晶体的说法一定正确的是( )
A.分子晶体中都存在共价键
B.在镁晶体中,1个 只与2个电子之间存在强烈的相互作用
C. 和SiC熔化时克服的作用力类型相同
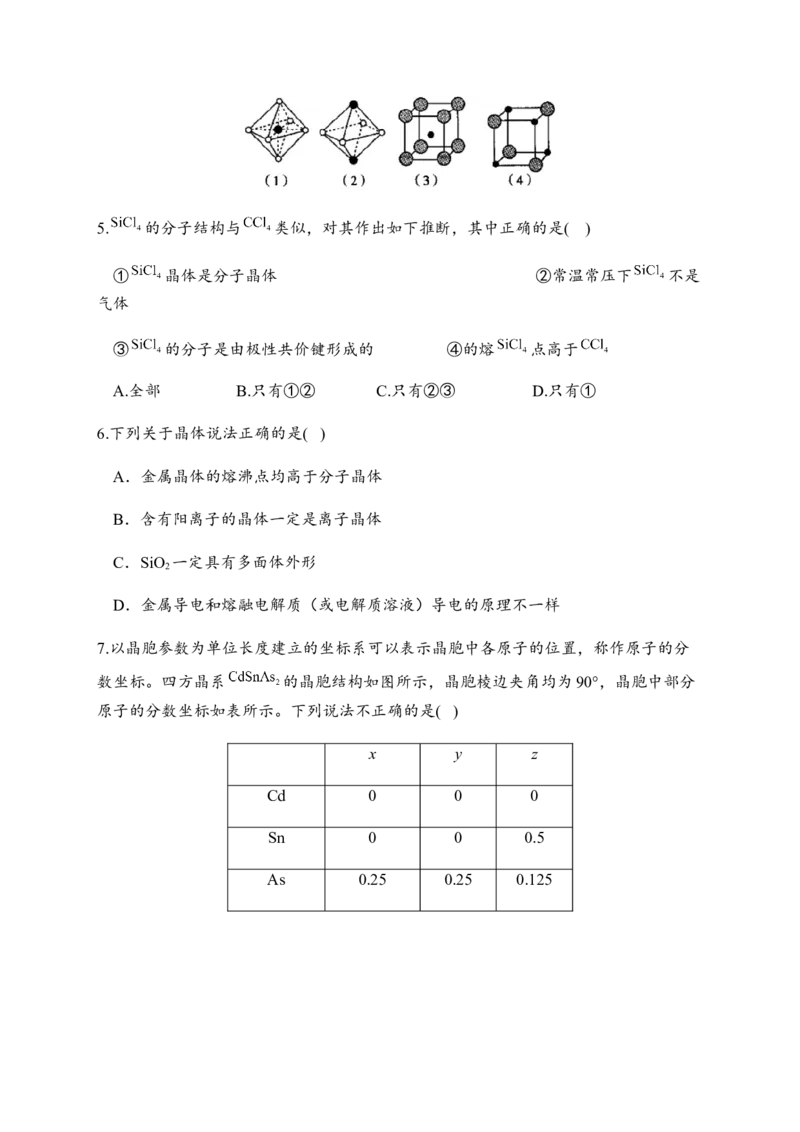
D.如图所示,其中(1)和(4)是从NaCl晶体结构中分割出来的部分结构5. 的分子结构与 类似,对其作出如下推断,其中正确的是( )
① 晶体是分子晶体 ②常温常压下 不是
气体
③ 的分子是由极性共价键形成的 ④的熔 点高于
A.全部 B.只有①② C.只有②③ D.只有①
6.下列关于晶体说法正确的是( )
A.金属晶体的熔沸点均高于分子晶体
B.含有阳离子的晶体一定是离子晶体
C.SiO 一定具有多面体外形
2
D.金属导电和熔融电解质(或电解质溶液)导电的原理不一样
7.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分
数坐标。四方晶系 的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分
原子的分数坐标如表所示。下列说法不正确的是( )
x y z
Cd 0 0 0
Sn 0 0 0.5
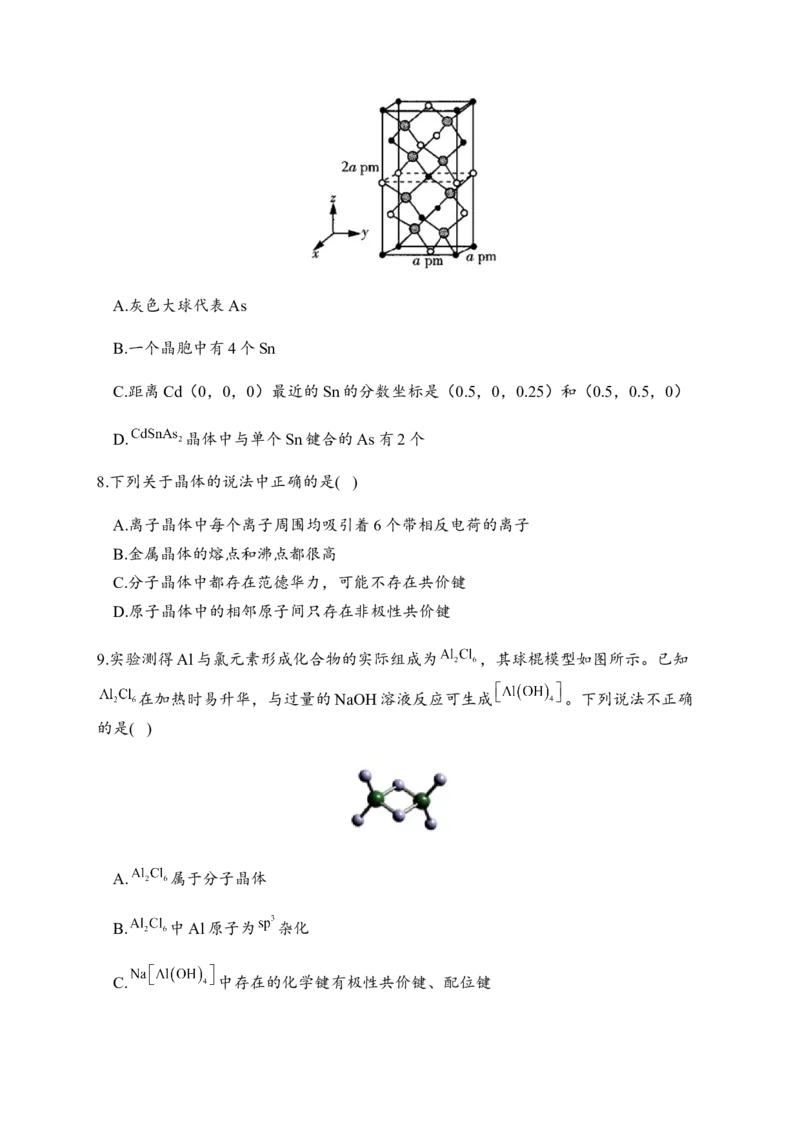
As 0.25 0.25 0.125A.灰色大球代表As
B.一个晶胞中有4个Sn
C.距离Cd(0,0,0)最近的Sn的分数坐标是(0.5,0,0.25)和(0.5,0.5,0)
D. 晶体中与单个Sn键合的As有2个
8.下列关于晶体的说法中正确的是( )
A.离子晶体中每个离子周围均吸引着6个带相反电荷的离子
B.金属晶体的熔点和沸点都很高
C.分子晶体中都存在范德华力,可能不存在共价键
D.原子晶体中的相邻原子间只存在非极性共价键
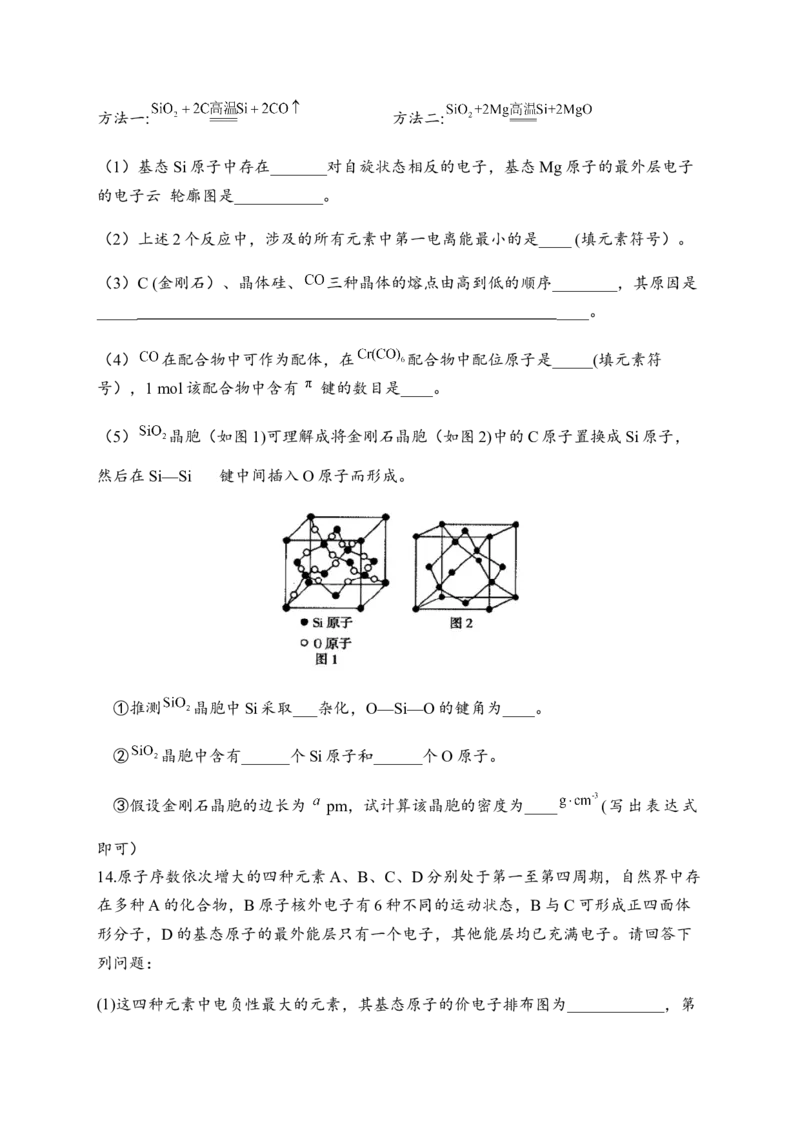
9.实验测得Al与氯元素形成化合物的实际组成为 ,其球棍模型如图所示。已知
在加热时易升华,与过量的NaOH溶液反应可生成 。下列说法不正确
的是( )
A. 属于分子晶体
B. 中Al原子为 杂化
C. 中存在的化学键有极性共价键、配位键D. 属于配合物
10.金属晶体、离子晶体、分子晶体采取密堆积方式的原因是( )
A.构成晶体的微粒均可视为圆球
B.金属键、离子键、范德华力均无饱和性和方向性
C.三种晶体的构成微粒相同
D.三种晶体的构成微粒多少及相互作用相同
11.下列关于超分子和配合物的叙述不正确的是( )
A.利用超分子的分子识别特征,可以分离 和
B.配合物中只含配位键
C. 中 提供空轨道, 中氧原子提供孤对电子,从而形成配位键
D.配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域有广泛应用
12.如图为石英晶体的平面示意图,它实际上是立体的网状结构(可以看作晶体硅中的每
个Si—Si键中插入一个O),其中硅、氧原子个数比是 ,下列有关叙述正确的是(设
代表阿伏加德常数的值)( )
A. = 2:1 B.6 g该晶体中含有0.1 个分子
C. = 1: 2 D.石英晶体中由硅、氧原子构成的最小的环上有8 个
原子
13.碳和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。设
代表阿伏加德罗常数的值。粗硅的制备方法有两种:方法一: 方法二:
(1)基态Si原子中存在_______对自旋状态相反的电子,基态Mg原子的最外层电子
的电子云 轮廓图是___________。
(2)上述2个反应中,涉及的所有元素中第一电离能最小的是____ (填元素符号)。
(3)C (金刚石)、晶体硅、 三种晶体的熔点由高到低的顺序________,其原因是
_____ ____。
(4) 在配合物中可作为配体,在 配合物中配位原子是_____(填元素符
号),1 mol该配合物中含有 键的数目是____。
(5) 晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,
然后在Si—Si 键中间插入O原子而形成。
①推测 晶胞中Si采取___杂化,O—Si—O的键角为____。
② 晶胞中含有______个Si原子和______个O原子。
③假设金刚石晶胞的边长为 pm,试计算该晶胞的密度为____ (写出表达式
即可)
14.原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存
在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体
形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下
列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为____________,第一电离能最小的元素是__________(填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是
___________(填化学式)。
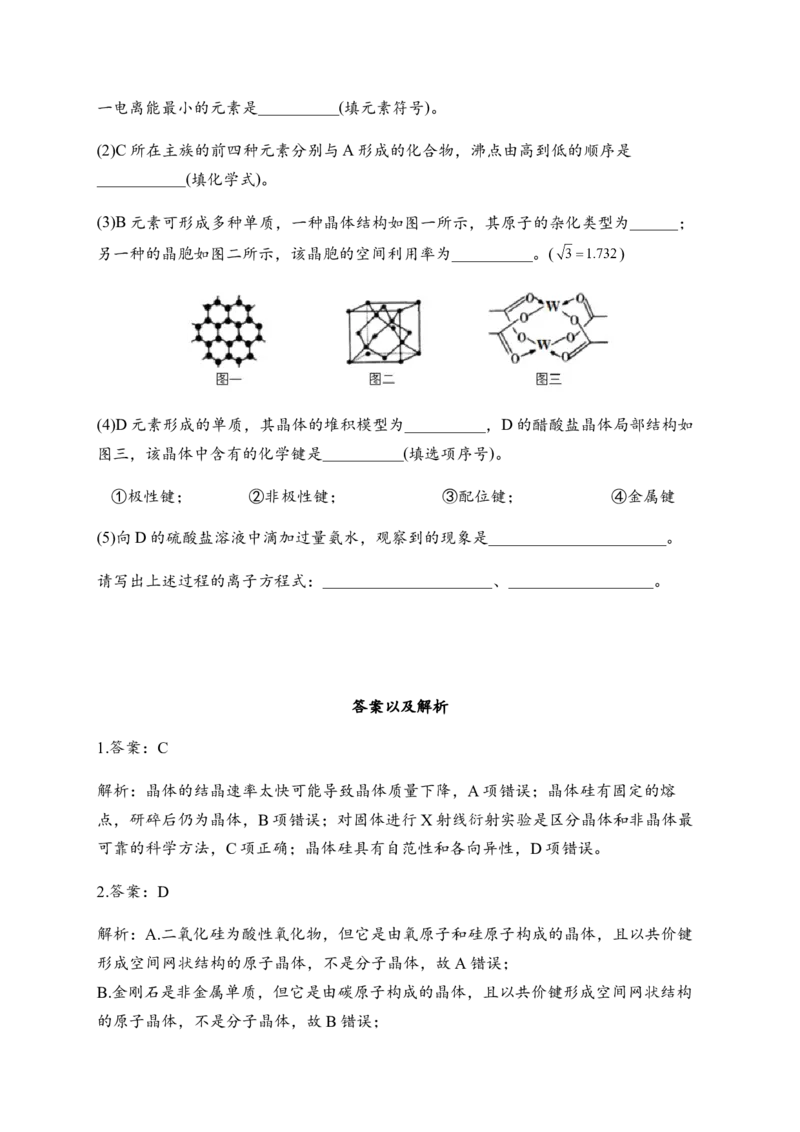
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为______;
另一种的晶胞如图二所示,该晶胞的空间利用率为__________。( )
(4)D元素形成的单质,其晶体的堆积模型为__________,D的醋酸盐晶体局部结构如
图三,该晶体中含有的化学键是__________(填选项序号)。
①极性键; ②非极性键; ③配位键; ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是______________________。
请写出上述过程的离子方程式:_____________________、__________________。
答案以及解析
1.答案:C
解析:晶体的结晶速率太快可能导致晶体质量下降,A项错误;晶体硅有固定的熔
点,研碎后仍为晶体,B项错误;对固体进行X射线衍射实验是区分晶体和非晶体最
可靠的科学方法,C项正确;晶体硅具有自范性和各向异性,D项错误。
2.答案:D
解析:A.二氧化硅为酸性氧化物,但它是由氧原子和硅原子构成的晶体,且以共价键
形成空间网状结构的原子晶体,不是分子晶体,故A错误;
B.金刚石是非金属单质,但它是由碳原子构成的晶体,且以共价键形成空间网状结构
的原子晶体,不是分子晶体,故B错误;C.氧化铜是碱性氧化物,但它是离子化合物,是离子晶体,不是分子晶体,故C错
误;
D.所有的酸都是由分子构成,是分子晶体,如乙酸是由乙酸分子构成,是分子晶体,
故D正确;
3.答案:D
解析: 的熔、沸点较低,为分子晶体,分子晶体熔融时不导电,故A、B项错误;
Cl B Cl键角为120°,则 的空间结构为平面三角形,是一种非极性分子,C项
错误; 水解方程式为 ,D 项正确。
4.答案:D
解析:稀有气体分子是单原子分子,其晶体中没有化学键, A项错误;金属晶体中的
“自由电子”属于整个金属,B项错误; 为离子晶体,熔化时克服离子键,SiC
为共价晶体,熔化时克服共价键,C项错误;NaCl晶体中,每个 周围有6个紧邻的
,毎个 周围有6个紧邻的 ,分析图(1) ~ (4),则从NaCl晶体结构中分割出
来的部分结构是(1)和(4),D项正确。
5.答案:A
解析: 属于分子晶体,常温常压下为液体,含有共价键。① 与 结构相
似,则 是分子晶体,正确; ② 与 结构相似,且 的相对分子质量较
大、 是 液体,则常温常压下 不可能是气体,正确;③ 中Si与 形成共
价键,则 是由极性共价键形成的分子,正确;④分 子晶体的相对分子质量越
大,熔点越高,则 的熔点高于 ,正确。故选A。
6.答案:D
7.答案:D
解析:由四方晶系 晶胞及部分原子的分数坐标可知,黑色小球代表Cd,白色
小球代表Sn,灰色大球代表As,A项正确;晶胞中有4个Sn位于棱上,6个Sn位于
面上,则属于一个晶胞的Sn的个数为4×1/4+6×1/2=4,B项正确;与Cd(0,0,0)
最近的Sn原子为如图所示的a、b两个Sn原子,a位置的Sn的分数坐标为(0.5,0,0.25),b位置的Sn的
分数坐标为(0.5,0.5,0),C项正确; 晶体中,晶胞面上的Sn除与该晶胞
中的2个As键合外,还与相邻晶胞中的2个As键合,晶胞棱上的Sn除与该晶胞中的
1个As键合外,还与相邻晶胞中的3个As键合,故晶体中单个Sn与4个As键合,D
项错误。
8.答案:C
解析:不同离子晶体的结构不同,每个离子周围吸引的带相反电荷的离子的数目不
同,A项错误;金属晶体的熔、沸点不一定高,如汞在常温下为液体,B项错误;分
子晶体中都存在范德华力,但不一定存在共价键,如He、Ne等,C项正确;原子晶体
中可能含有极性共价键,如SiO ,D项错误。
2
9.答案:C
解析:A. 的熔点较低, 在加热时易升华,为共价化合物,是分子晶体,故
A正确;
B. Al原子形成4个σ键,没有孤对电子,杂化轨道数目为4,Al原子杂化方式为 ,
故B正确;
C. 中钠离子和 之间存在离子键,Al离子和O原子之间存在配位
键、O−H原子之间存在极性键,配位键也属于共价键,所以存在的化学键有离子键、
极性共价键、配位键,故C错误;
D. 中铝是缺电子结构,能接受氢氧根离子给与的孤对电子形成配位键,
所以 属于配合物,故D正确;
10.答案:B解析:所谓密堆积结构是指在由无方向性的金属键、离子键和分子间作用力等结合的
晶体中,原子、离子或分子等微粒总是趋向于相互配位数高、能充分利用空间的堆积
密度大的那些结构。
11.答案:C
解析:配离子中的配体在溶液中很难电离,已知含0.1 mol氯化铬的水溶液用过量稀硝
酸银溶液处理时,只得到0.2 mol AgCl沉淀,说明该配合物的外界有2个氯离子,则
其内界只有一个氯离子,故C项正确。
12.答案:C
解析:每个 Si原子占有O原子个数为4 =2,故硅、氧原子个数比为1:2,A项错
误、C项正确;该晶体是共价晶体, 不存在分子,B项错误;在 晶体中,由Si、
O构成的最小环中共有12个原子,D项错误。
13.答案:(1)6;球形 (2)Mg
(3)C(金刚石)>晶体硅>CO;金刚石和晶体硅都是共价晶体且晶体结构相似,C原子半
径小于硅原子半径,所以金刚石中C一C键的键长短,键能大,故金刚石的熔点比晶
体硅的大;CO是分子晶体,熔点比金刚石和晶体硅的都小
(4)C;12 (5)①sp ;109 2828'② 8;16 ③
解析: (1)基态Si原子的核外电子排布式为 ,s轨道全充满电子,故
1s、2s、3s轨道共有3对自旋状态相反的电子,2p 轨道有3对自旋状态相反的电子,
所以基态Si原子中存在6对自旋状态相反的电子。基态Mg原子的核外电子排布式为
,最外层电子占据3s轨道,s电子的电子云轮廓图是球形。
(2)题述2个反应中涉及的元素有C、O、Mg、Si,其中S、O、 Si是非金属元素,较
难失去电子,Mg元素的金属性最强,最易失去电子,所以四种元素中第一电离能最小
的是Mg。
(3) C(金刚石)、 晶体硅都是共价晶体,熔点高,二者的结构相似,但碳原子的半径比
硅原子的小,故C—C键的键长短、键能大,所以C(金刚石)的熔点比晶体硅的高,而CO是分子晶体,熔点低,所以三种晶体的熔点从高到低的顺序为C(金刚石)> 晶体硅
>CO。
(4)配体中给出孤对电子与中心离子形成配位键的原子叫配位原子。CO在 中作
配体,配位原子是C,1 mol CO中含有 键的数目是 2 ,所以1 mol该配合物中含
有 键的数目是12 。
(5)①在 晶体中每个硅原子与周围的4个氧原子的成键情况与金刚石晶体中的碳原
子与周围4个碳原子的成键情况是相同的,所以 晶胞中Si采取 杂化,金刚石是
正四面体结构单元,其键角是109 28',所以 晶胞中O—Si—O的键角也是
109°28'。② 晶胞中含有Si原子的个数为 ,由Si、O原子的个数比
知晶胞中含有O原子数是16。③一个金刚石晶胞中含有8个C原子,所以一个晶胞的
质量为 ,晶胞边长为 pm,所以该晶胞的密度 =
。
14.答案:(1) ;Cu (2) (3)sp2;34%
(4)面心立方最密堆积;①②③
(5)首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液;
、
解析:原子序数依次增大的四种元素A. B. C. D分别处于第一至第四周期,自然界中
存在多种A的化合物,则A为氢元素;B原子核外电子有6种不同的运动状态,即核
外有6个电子,则B为碳元素;D的基态原子的最外能层只有一个电子,其他能层均
已充满电子,D原子外围电子排布为3d104s1,则D为铜元素;结合原子序数可知,C
只能处于第三周期,B与C可形成正四面体型分子,则C为氯元素,
(1)四种元素中电负性最大的是Cl,其基态原子的价电子排布为3s23p5,其基态原子的
价电子排布图为 。(2)HF分子之间形成氢键,使其熔沸点较高,HI、HBr、HCl分子之间只有范德华力,
相对分子质量越大,范德华力越大,沸点越高,即沸点由高到低的顺序是
HF>HI>HBr>HCl,
(4)晶体Cu为面心立方最密堆积,结合图三醋酸铜晶体的局部结构可确定其晶体中含
有极性键、非极性键和配位键,
(5)硫酸铜溶液中加入氨水会产生蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的
透明溶液,有关反应的离子方程式为Cu2++2NH ⋅H O═Cu(OH) ↓+2NH +、
3 2 2 4
Cu(OH) +4NH ⋅H O═[Cu(NH ) ]2++2OH−+4H O。
2 3 2 3 4 2