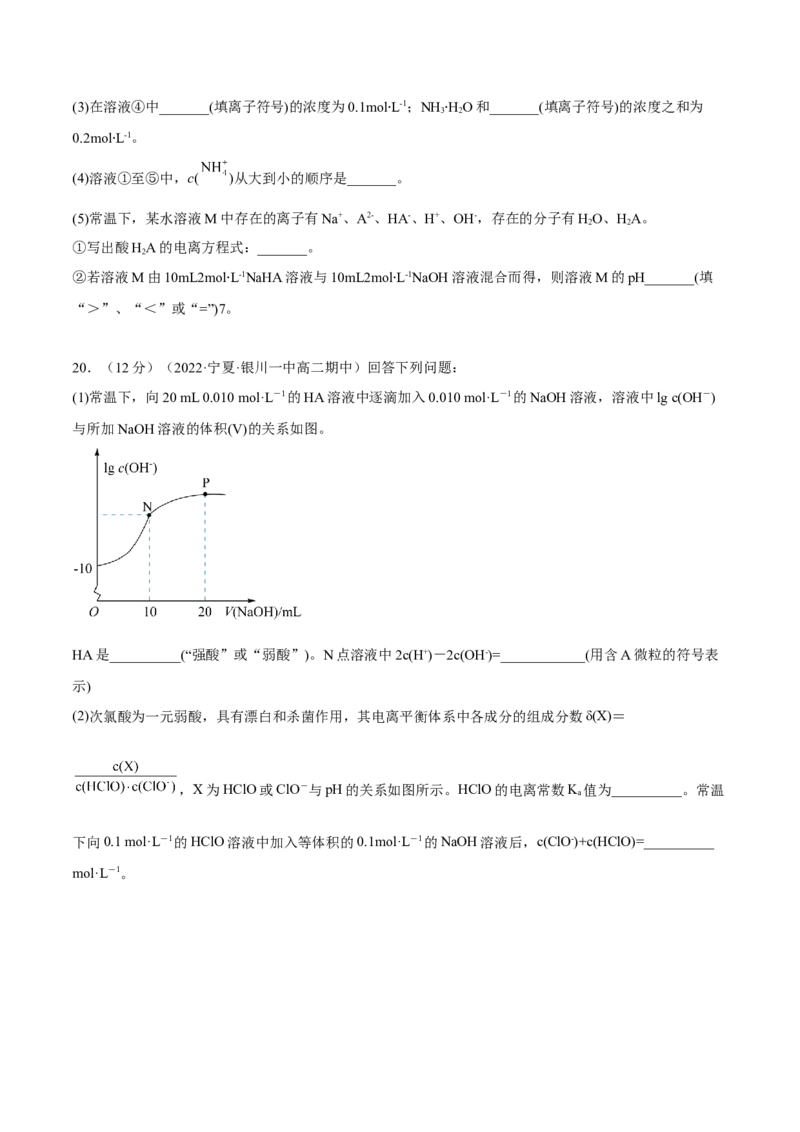文档内容
第三章 章末测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022·宁夏·银川一中高二期中)下列反应中,属于水解反应且使溶液显酸性的是
A. B.
C. D.
2.(2022·山东·济南市章丘区第四中学高二期中)下列物质的分类正确的是
选 电解
混合物 强电解质 弱电解质
项 质
A 明矾
B 碱石灰 烧碱
C 盐酸 液氨
D 空气
3.(2022·上海·复旦附中高二期中)下列说法正确的是
A.洗涤油污常用热的 溶液,这是利用了盐类水解的原理
B.用加热的方法就可以除去 溶液中的
C.配制 溶液时,将 固体溶于稀盐酸中,然后稀释至所需浓度
D.将 溶液和 溶液分别加热蒸干、灼烧后,所得固体为 和
4.(2022·陕西·眉县槐芽中学高二期中)10mL 0.1mol/L的盐酸与过量的锌粉反应,若要减慢反应速率,
又不影响生成H 的量,以下可行的是
2
A.加少量CuSO 固体 B.加KNO 溶液
4 3C.加NaCO 溶液 D.加CHCOONa固体
2 3 3
5.(2022·河南·汝州市第一高级中学高二阶段练习)蚁酸(HCOOH)是一种一元弱酸,下列说法可以证明它
是弱电解质的是
A.蚁酸溶液的pH值=2 B.常温下HCOONa溶液的pH>7
C.蚁酸能与碳酸钠反应放出二氧化碳 D.蚁酸溶液与锌反应比强酸溶液缓
6.(2022·北京·首都师范大学附属中学高二期中)下列反应的发生与“盐类水解平衡”或“难溶电解质的
溶解平衡”无关的是
A.镁条与NH Cl溶液反应生成H
4 2
B.NaHSO 溶液与NaOH溶液反应生成NaSO
4 2 4
C.盐酸与CaCO 反应生成CO
3 2
D.Fe (SO ) 溶液和NaCO 溶液反应生成CO
2 4 3 2 3 2
7.(2022·吉林·长春市第二实验中学高二期中)羟胺( )在水溶液中的电离方程式为
。常温下,向该溶液中加入NaOH固体,下列说法错误的是
A.平衡常数K减小 B. 增大 C.平衡向左移动 D. 增大
8.(2022·山东·济南市章丘区第四中学高二期中)常温下,将浓度为0.1mol/L的HCOOH溶液加水稀释至
0.01mol/L的过程中,下列各量始终保持增大的是
A. B. C. D.
9.(2022·上海·复旦附中高二期中)判断电解质强弱的合理依据是
A.溶液的导电能力 B.水溶性大小
C.一定浓度时的电离程度 D.与酸或碱反应时消耗酸或碱的量10.(2022·上海·复旦附中高二期中)室温下,将等质量的固体 置于等体积的下列液体中,均有
固体剩余,其中剩余固体最少的是
A.在纯水中 B.在 的 溶液中
C.在 的 中 D.在 的 溶液中
11.(2022·上海·复旦附中高二期中)要使 的醋酸溶液中 的值增大,可以采取的
措施是
①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水 ⑤加少量醋酸钠固体
A.①② B.②③④ C.③④⑤ D.②④
12.(2022·河南·鹤壁高中高二阶段练习)向20mL0.01mol/L的醋酸溶液中逐滴加入40mL等浓度的烧碱溶
液,下列说法错误的是
A.当加入10mL的NaOH时,溶液中存在:2c(OH﹣)+c(CH COO﹣)=c(CH COOH)+2c(H+)
3 3
B.当加入20mL的NaOH时,反应放出的热量达到最大值
C.当加入40mL的NaOH时,溶液中存在:c(Na+)>c(OH﹣)>c(CH COO﹣)>c(H+)
3
D.整个滴加过程中,溶液中的水的电离度一直在增大
13.(2022·广东·仲元中学高二期中)物质的量浓度均为0.1mol/L的下列溶液:① ②
③ ④ ⑤ ,按 由小到大的顺序排列正确的是
A.③<②<①<⑤<④ B.②<③<④<⑤<①
C.①<②<③<④<⑤ D.①<③<②<⑤<④
14.(2022·宁夏·银川一中高二期中)下列说法正确的是
A.0.l mol∙L−1CHCOOH加水稀释,溶液中c(OH-)减小
3
B.NaClO溶液中,离子浓度大小关系为:C.向水中加入明矾晶体能促进水的电离,并使溶液中c(H+) > c(OH-)
D.将pH=11的NaOH溶液和pH=13的Ba(OH) 溶液等体积混合,混合液的pH=12
2
15.(2022·河南·汝州市第一高级中学高二阶段练习)下列物质能抑制水的电离且属于弱电解质的是
A.Na B.NH •H O C.SO D.HCl
3 2 2
16.(2022·四川·德阳五中高二期中)在25℃时,用蒸馏水稀释1 的醋酸溶液,随着溶液的稀释,
下列各项中始终保持增大趋势的是
A. B.
C. D.
二、非选择题:共56分。
17.(14分)(2022·广东茂名·高二期中)I.现有以下物质:①NaCl晶体② ③液态醋酸④铜⑤固体
⑥纯蔗糖( )⑦乙醇( )⑧熔化的 ⑨盐酸⑩液氨。请回答下列问题(填相应序
号):
(1)以上物质能导电的是_______;
(2)以上物质属于非电解质的是_______;
(3)以上物质属于强电解质的是_______。
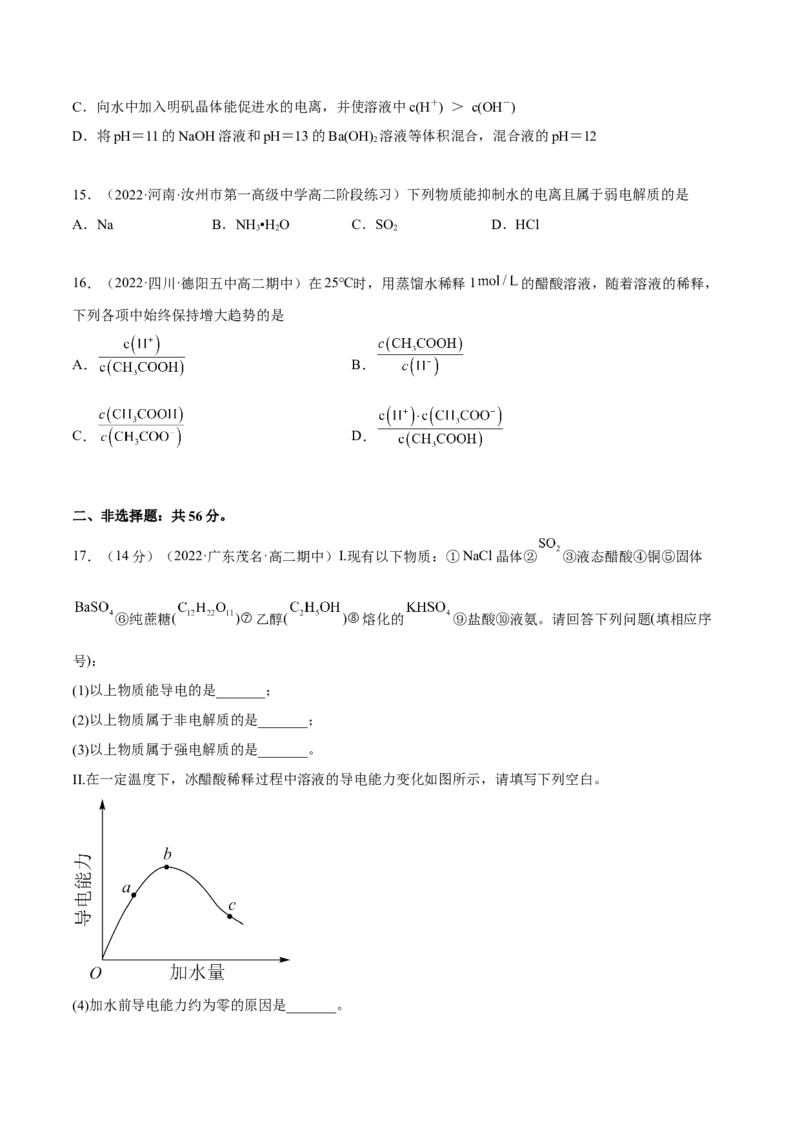
II.在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,请填写下列空白。
(4)加水前导电能力约为零的原因是_______。(5)写出醋酸电离方程式_______。
(6)a、b、c三点对应的溶液中,pH最大的是_______。
(7)若使b点对应的溶液中 增大,可采用的方法是_______(填序号)。
①加入 ②加入NaOH固体 ③加入 固体 ④加入Zn粒
18.(14分)(2022·辽宁·高二期中)I.根据要求回答下列问题:
(1)氨水显碱性的原因(用电离方程式表示):____。
(2)盐碱地(含较多NaCO)产生碱性的原因(用第一步水解离子方程式表示):____。
2 3
II.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 CHCOOH HCO HClO
3 2 3
K =4.3×10-7
a1
电离平衡常数 K =1.8×10-5 K =3.0×10-8
a a
K =5.6×10-11
a2
(3)物质的量浓度均为0.1mol•L-1的下列四种溶液:pH由小到大排列的顺序是____(用字母填写,例如
“a”“<”或“=”)c(HClO);该溶液中所含的4种离子浓度由大到小的顺序为____。
19.(14分)(2022·北京四中高二期中)在室温下,下列五种溶液,请根据要求填写下列空白:
①0.1molL-1NH Cl溶液;②0.1molL-1CHCOONH 溶液;③0.1molL-1NH HSO 溶液;④0.1molL-1
4 3 4 4 4
NH HO∙和0.1molL-1NH Cl混合液∙;⑤0.1molL-1氨水 ∙ ∙
3 2 4
(1)溶∙液①呈______∙_(填“酸”、“碱”或“中”∙ )性,其原因是_______(用离子方程式表示)。
(2)室温下,测得溶液②的pH=7,则说明CHCOO-的水解程度_______(填“>”、“<”或“=”,下同)
3
的水解程度,CHCOO-与 浓度的大小关系是c(CHCOO-)_______c( )。
3 3(3)在溶液④中_______(填离子符号)的浓度为0.1molL-1;NH HO和_______(填离子符号)的浓度之和为
3 2
0.2molL-1。 ∙ ∙
∙
(4)溶液①至⑤中,c( )从大到小的顺序是_______。
(5)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有HO、HA。
2 2
①写出酸HA的电离方程式:_______。
2
②若溶液M由10mL2molL-1NaHA溶液与10mL2molL-1NaOH溶液混合而得,则溶液M的pH_______(填
“>”、“<”或“=”)7。∙ ∙
20.(12分)(2022·宁夏·银川一中高二期中)回答下列问题:
(1)常温下,向20 mL 0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中lg c(OH-)
与所加NaOH溶液的体积(V)的关系如图。
HA是__________(“强酸”或“弱酸”)。N点溶液中2c(H+)-2c(OH-)=____________(用含A微粒的符号表
示)
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ(X)=
,X为HClO或ClO-与pH的关系如图所示。HClO的电离常数K 值为__________。常温
a
下向0.1 mol·L-1的HClO溶液中加入等体积的0.1mol·L-1的NaOH溶液后,c(ClO-)+c(HClO)=__________
mol·L-1。(3)PH相同、等体积的两份溶液A(盐酸)和B(CHCOOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,
3
放出氢气的质量相同,则下列说法正确的是____(填序号)。
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A中有锌剩余 ⑥B中有锌剩余
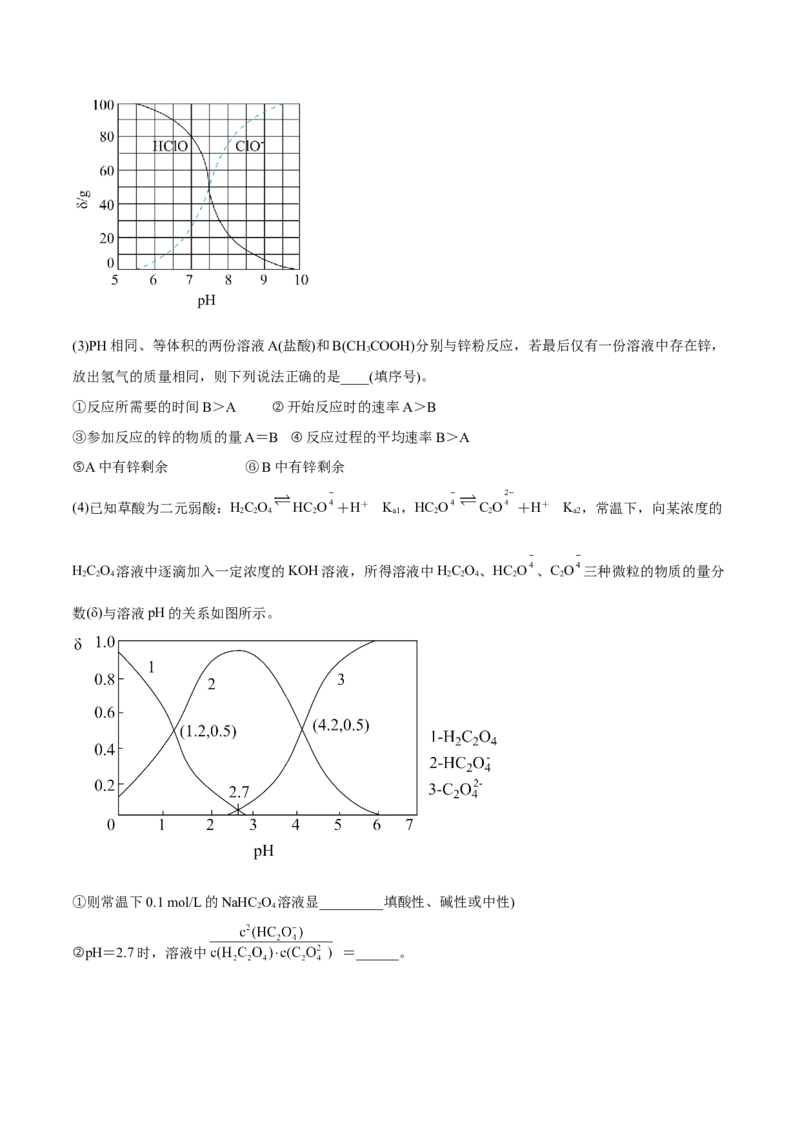
(4)已知草酸为二元弱酸:HC O HC O +H+ K ,HC O C O +H+ K ,常温下,向某浓度的
2 2 4 2 a1 2 2 a2
HC O 溶液中逐滴加入一定浓度的KOH溶液,所得溶液中HC O、HC O 、C O 三种微粒的物质的量分
2 2 4 2 2 4 2 2
数(δ)与溶液pH的关系如图所示。
①则常温下0.1 mol/L的NaHC O 溶液显_________填酸性、碱性或中性)
2 4
②pH=2.7时,溶液中 =______。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育