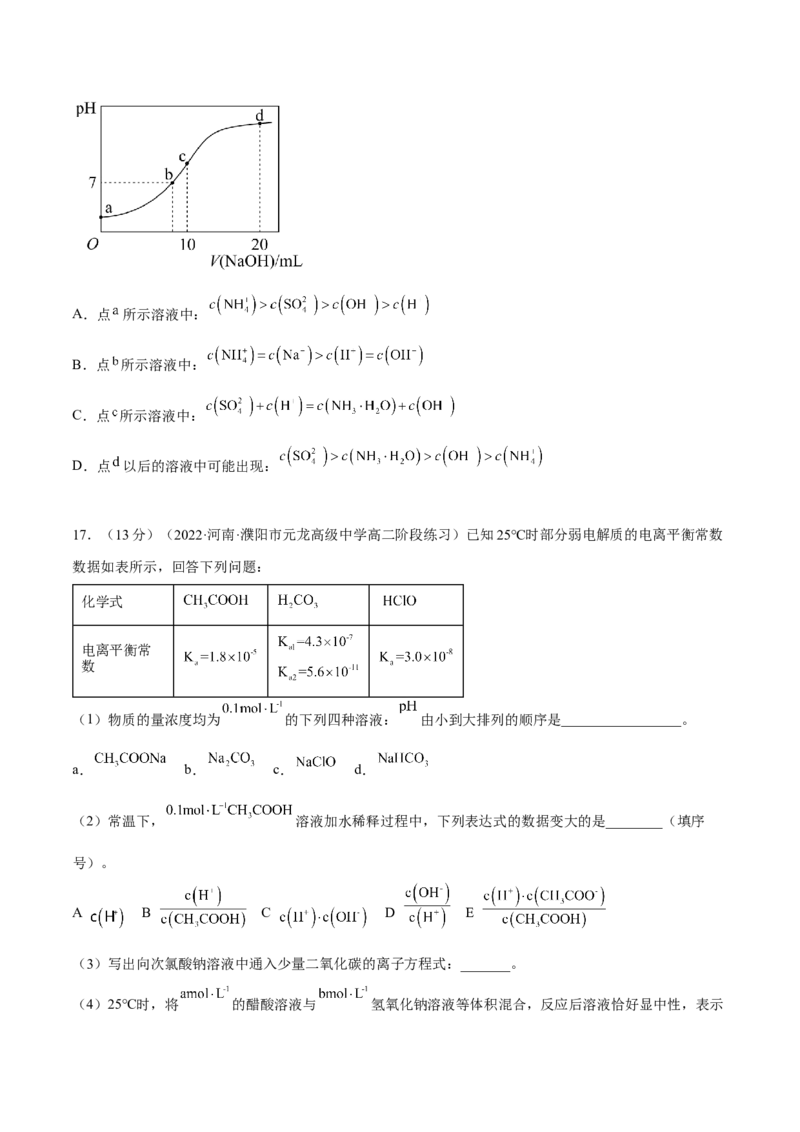文档内容
第三章 章末测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022·天津市第九十五中学益中学校高二期中)常温下,在0.01mol/L氨水中,水的离子积是
A. B. C. D.
2.(2022·广西·浦北中学高二期中)下列措施抑制水的电离的是
A.加热 B.加入NaOH溶液 C.加入CuSO 固体 D.加入NaCO 固体
4 2 3
3.(2022·黑龙江·鸡西市第四中学高二阶段练习)下列仪器使用前不需检查是否漏水的是
A.分液漏斗 B.滴定管 C.容量瓶 D.胶头滴管
4.(2022·吉林·长春市第六中学高二阶段练习)根据表中信息,判断0.10 mol/L的下列各物质的溶液
最大的是
酸 电离常数(常温下)
CHCOOH K=1.8×10-5
3 a
HCO K =4.5×10-7,K =4.7×10-11
2 3 a1 a2
HS K =1.3×10-7,K =1.1×10-11
2 a1 a2
A.CHCOONa B.NaCO C.NaHCO D.NaS
3 2 3 3 2
5.(2022·伊美区第二中学高二开学考试)相同温度下,根据三种酸的电离常数,下列判断正确的是
酸 HX HY HZ
电离常数K/(mol·L-1) 9×10-7 9×10-6 1×10-2
A.三种酸的强弱关系:HX>HY>HZ
B.反应HZ+Y-=HY+Z-能够发生
C.由电离平衡常数可以判断,HZ属于强酸,HX和HY属于弱酸
D.相同温度下,1mol·L-1 HX溶液的电离常数大于0.1mol·L-1 HX溶液的电离常数6.(2022·全国·高二单元测试)用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是
A. B.
C.c(H+)和c(OH-)的乘积 D.OH-的物质的量
7.(2022·黑龙江·佳木斯市第八中学高二期末)常温下,若溶液中由水电离产生的c(OH-)=10-12mol·L-1,满
足此条件的溶液中一定可以大量共存的是
A.Al3+、Na+、NO 、CO B.K+、Na+、Cl-、NO
C.K+、Na+、Cl-、S2- D.K+、NH 、SO 、NO
8.(2021·全国·高二课时练习)室温时,将x mL pH=a 的稀KOH溶液与ymL pH=b的稀硝酸充分反应。
下列关于反应后溶液pH的判断,正确的是
A.若x=y,且a + b = 14,则pH>7 B.若10x = y,且a + b = 13,则pH = 7
C.若ax=by,且a + b = 13,则pH=7 D.若x = 10y,且a + b = 14,则pH>7
9.(2022·河南·濮阳市元龙高级中学高二阶段练习)在相同温度时,100 mL0.01 mol/L醋酸与10 mL0.1
mol/L醋酸相比较,下列数值中,前者大于后者的是
A.溶液中H+的物质的量 B.CHCOOH的电离常数
3
C.中和时所需NaOH的物质的量 D.溶液中CHCOOH的物质的量
3
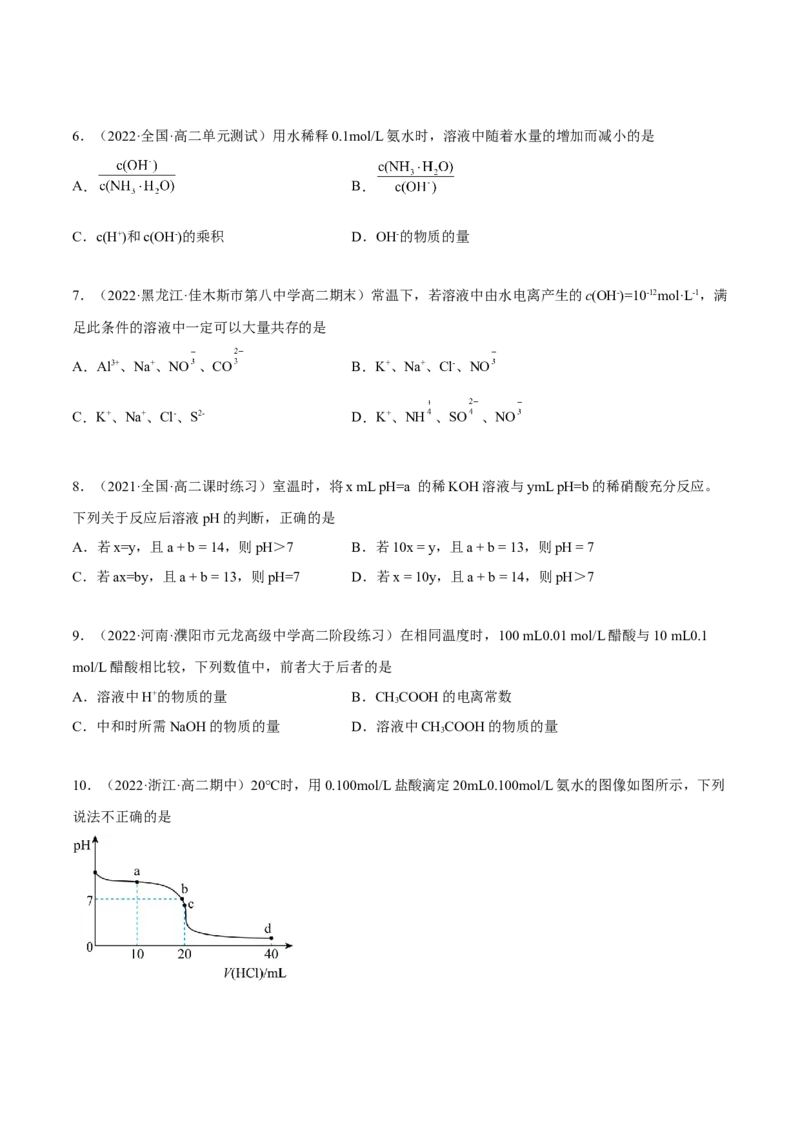
10.(2022·浙江·高二期中)20℃时,用0.100mol/L盐酸滴定20mL0.100mol/L氨水的图像如图所示,下列
说法不正确的是A.a、b、c、d均有c(NH )+c(H+)=c(Cl-)+c(OH-)
B.b点时c(NH )=c(Cl-)=c(H+)=c(OH-)
C.c点表示酸碱恰好完全反应
D.d点时c(Cl-)=2c(NH∙H O)+2c(NH )
3 2
11.(2022·宁夏·银川一中高二期中)下列说法不正确的是
A.某溶液中由水电离出的c(H+)=1×10-amol·L-1,则该溶液的pH=a
B.物质的量浓度均为0.1mol/L的CHCOONa和CHCOOH溶液等体积混合c(CHCOO-)
3 3 3
+c(CH COOH)=0.1mol/L
3
C.常温,等物质的量浓度的醋酸钠溶液和碳酸钠溶液,pH(CH COONa)小于pH(Na CO)
3 2 3
D.稀释醋酸钠溶液溶液的碱性减弱但醋酸钠的水解程度增大.
12.(2022·新疆·乌鲁木齐市第四中学高二期末)下列说法正确的是
A.常温下, 溶液加水稀释后,溶液中 的值增大
B.常温下, 等物质的量浓度的 溶液和HCl溶液中,水的电离程度相同
C.常温下,反应 能自发发生反应,则该反应的
D.常温下,向 的饱和溶液中加入少量BaCl 固体,溶液中 减小
2
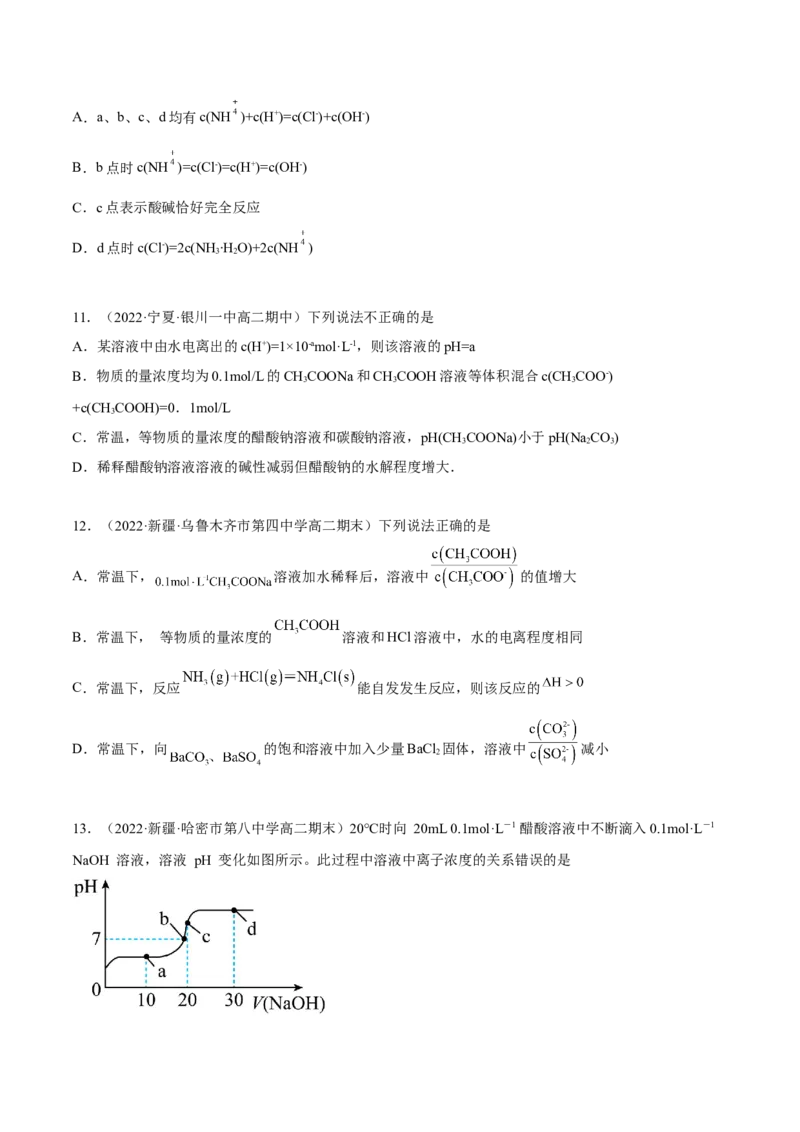
13.(2022·新疆·哈密市第八中学高二期末)20℃时向 20mL 0.1mol·L-1 醋酸溶液中不断滴入0.1mol·L-1
NaOH 溶液,溶液 pH 变化如图所示。此过程中溶液中离子浓度的关系错误的是A.a 点:c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
B.b 点:c(Na+)=c(CHCOO-)>c(H+)=c(OH-)
3
C.c 点:c(H+)=c(CHCOO-)+c(OH-)
3
D.d 点:c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3
14.(2022·天津一中高二阶段练习)关于常温下pH为2的盐酸,下列叙述正确的是
A.将10mL,该溶液稀释至100mL后,
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为
D.该溶液中由水电离出的 (H+)
15.(2022·黑龙江·齐齐哈尔市第八中学校高二开学考试)室温下,下列各组离子在指定溶液中能大量共存
的是
A.pH=2的溶液:Na+、Fe2+、I-、
B.c(NaAlO)=0.1mol·L-1的溶液:K+、OH-、Cl-、
2
C. =0.1mol·L-1的溶液:Na+、K+、 、ClO-
D.c(Fe3+)=0.1mol·L-1的溶液:Al3+、 、 、SCN-
16.(2022·江西·九江一中高二期末)常温下,向 溶液中逐滴加入
的 溶液,溶液的 随 溶液体积的变化如图所示。下列说法正确的是A.点 所示溶液中:
B.点 所示溶液中:
C.点 所示溶液中:
D.点 以后的溶液中可能出现:
17.(13分)(2022·河南·濮阳市元龙高级中学高二阶段练习)已知25℃时部分弱电解质的电离平衡常数
数据如表所示,回答下列问题:
化学式
电离平衡常
数
(1)物质的量浓度均为 的下列四种溶液: 由小到大排列的顺序是_________________。
a. b. c. d.
(2)常温下, 溶液加水稀释过程中,下列表达式的数据变大的是________(填序
号)。
A B C D E
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_______。
(4)25℃时,将 的醋酸溶液与 氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数 _____________(用含a、b的代数式表示)。
(5)标准状况下将 通入 溶液中,用溶液中微粒的浓度符号完成下列等式:
_________________。
18.(15分)(2022·天津一中高二阶段练习)(1)pH相同的下列物质的溶液①(NH )SO ;②NH HSO ;
4 2 4 4 4
③NH NO ,铵根离子浓度由小到大的顺序是__________(填序号)。
4 3
(2)同浓度的下列溶液:①HCl;②NH Cl;③NaCO;④NaHCO ,其中pH由大到小的顺序是
4 2 3 3
______________。
(3)物质的量浓度相同的①盐酸、②硫酸溶液、元③醋酸(CHCOOH)溶液各100mL分别与足量的Zn反应,
3
在相同的条件下,产生H 的体积分别为V、V、V,它们由大到小的顺序是___________。
2 1 2 3
(4)等体积的CHCOOH与NaOH溶液反应后溶液中存在c(Na+)<c(CHCOO-),该溶液呈______性(填“酸”、
3 3
“碱”或“中”),反应前c(NaOH)_____c(CHCOOH)(填“>”“<”或“=”)
3
(5)在化学分析中采用KCrO 为指示剂,以AgNO 标准溶液滴定溶液中Cl-,利用Ag+与 生成砖红色沉
2 4 3
淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为
____mol/L,此时溶液中c(CrO 2-)等于_____mol/L。(已知Ag CrO、AgCl的K 分别为2.0×10-12和2.0×10-
4 2 4 sp
10)。
19.(11分)(2022·甘肃·高台县第一中学高二阶段练习)实验室中有一未知浓度的稀盐酸,某学生为测
定盐酸的浓度在实验室中进行如下实验。
①配制100mL 0.10mol/L NaOH标准溶液。
②取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶
液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编 NaOH溶液的浓度 滴定完成时,NaOH溶液滴入的体积 待测盐酸溶液的体积
号 (mol/L) (mL) (mL)
1 0.10 22.62 20.00
2 0.10 22.72 20.00
3 0.10 22.80 20.00请完成下列问题:
(1)滴定达到终点的现象是_______。
(2)根据上述数据,可计算出该盐酸的浓度约为_______(保留两位有效数字)
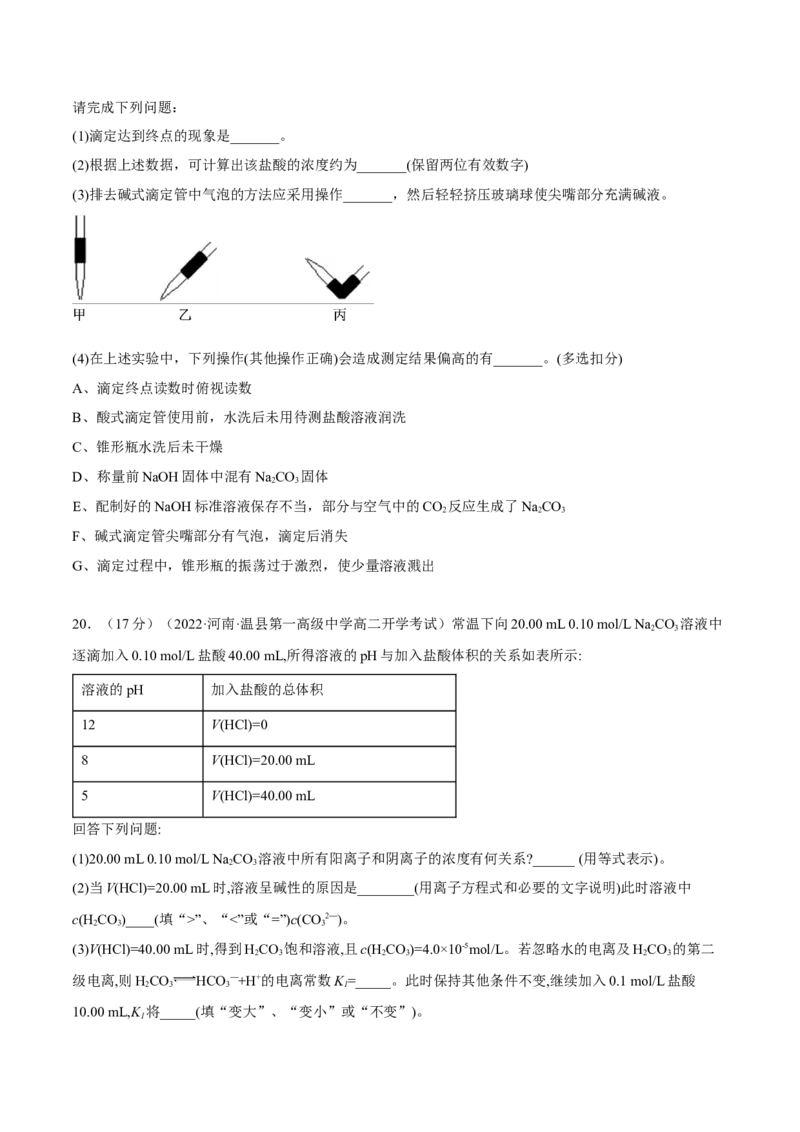
(3)排去碱式滴定管中气泡的方法应采用操作_______,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有NaCO 固体
2 3
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO 反应生成了NaCO
2 2 3
F、碱式滴定管尖嘴部分有气泡,滴定后消失
G、滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
20.(17分)(2022·河南·温县第一高级中学高二开学考试)常温下向20.00 mL 0.10 mol/L Na CO 溶液中
2 3
逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
溶液的pH 加入盐酸的总体积
12 V(HCl)=0
8 V(HCl)=20.00 mL
5 V(HCl)=40.00 mL
回答下列问题:
(1)20.00 mL 0.10 mol/L Na CO 溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
2 3
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________(用离子方程式和必要的文字说明)此时溶液中
c(H CO)____(填“>”、“<”或“=”)c(CO2—)。
2 3 3
(3)V(HCl)=40.00 mL时,得到HCO 饱和溶液,且c(H CO)=4.0×10-5mol/L。若忽略水的电离及HCO 的第二
2 3 2 3 2 3
级电离,则HCO HCO —+H+的电离常数K =_____。此时保持其他条件不变,继续加入0.1 mol/L盐酸
2 3 3 1
10.00 mL,K 将_____(填“变大”、“变小”或“不变”)。
1(4)若向20 mL 0.10 mol/L Na CO 溶液中加入BaCl 粉末3.94×10-7 g时开始产生沉淀BaCO ,则K (Ba CO)=
2 3 2 3 sp 2 3
。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育