文档内容
第三章章末归纳总结
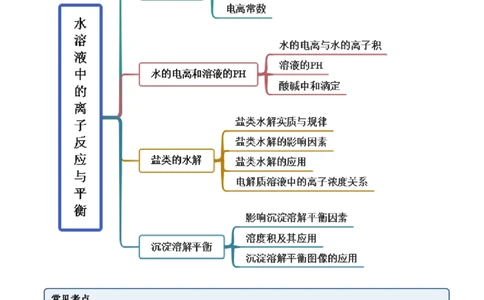
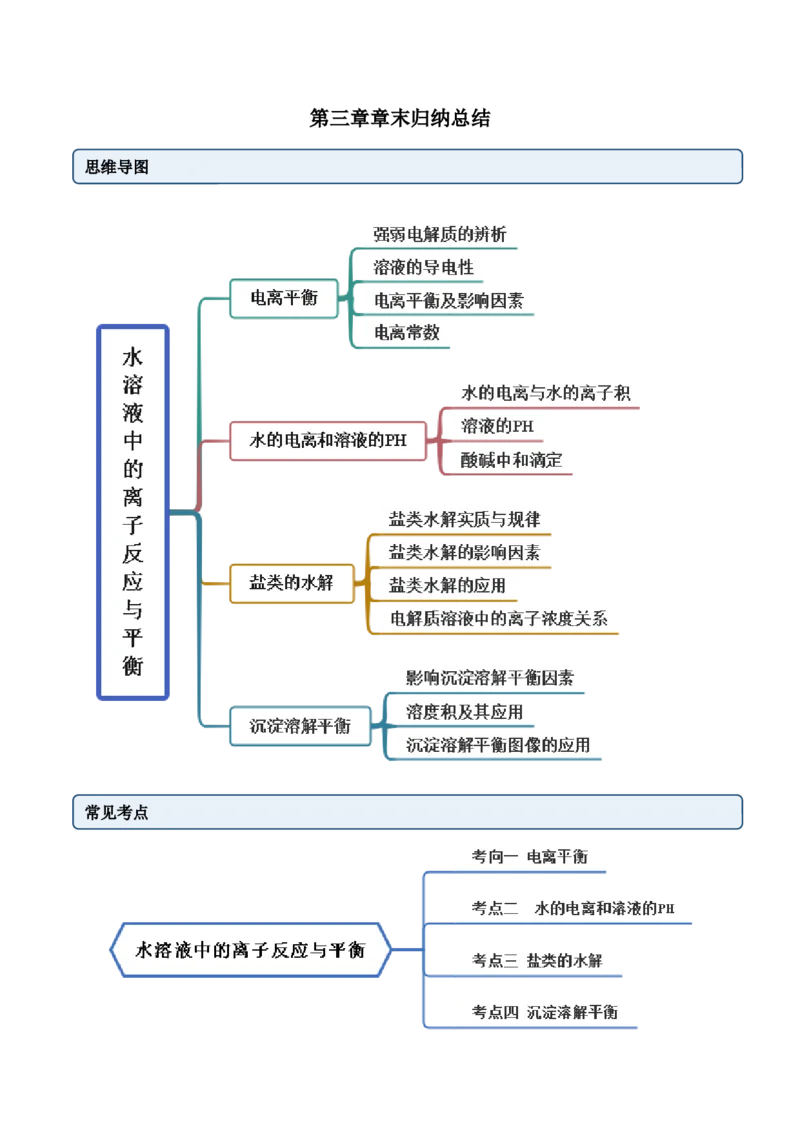
思维导图
常见考点考向一 电离平衡
【例1-1】(2022安康)下列叙述中正确的是 ( )
A.硫酸钡在水中溶解度很小,所以硫酸钡不是电解质
B.NH 的水溶液能导电,但NH 是非电解质
3 3
C.电解质在通电时才能发生电离
D.硫酸不能导电,但硫酸溶液能导电,所以硫酸溶液是电解质
【例1-2】(2022浙江)甲酸(HCOOH)的下列性质中,不能证明它是弱电解质的是( )
A.溶液中HCOOH和 共存
B.0.1mol/L HCOOH溶液的pH大于1
C.10mL 1mol/L HCOOH恰好与10mL 1mol/L NaOH溶液完全反应
D.同浓度的HCOOH溶液的导电性比盐酸溶液的弱
【例1-3】(202广东)一定温度下,将浓度为0.1mol/LHF溶液加水不断稀释,始终保持增大的是
( )
A. B.
C. D.
【一隅三反】
1.(2022广东期中)部分弱酸的电离平衡常数如下表,则下列说法错误的是( )
弱酸 HCOOH HClO
电离平衡常数
(25℃)
A.酸性:
B.同浓度的离子结合的能力由强到弱的顺序为:
C.碳酸钠滴入足量甲酸溶液中的反应为:D.少量 通入NaClO溶液中的反应为:
2(2022湖州)室温时, 某一元酸 在水中的电离度为2.2%,下列叙述错误的是( )
A.升高温度,溶液中的 增大
B.加水稀释过程中, 增大,故 也增大
C.室温时,向该溶液中滴加少量同浓度的 溶液,该酸的电离常数 不变
D.向该 的溶液中,通 气体,溶液中 增大, 的电离平衡逆向移动
3.(2022高二上·通州期中)依据醋酸的性质,请回答下列问题(以下讨论均在常温时)。
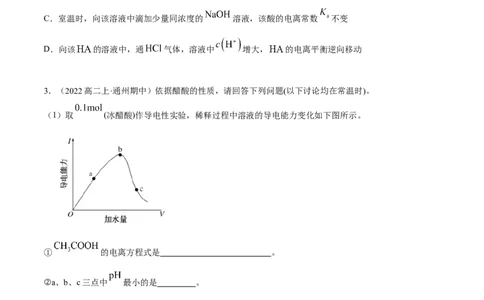
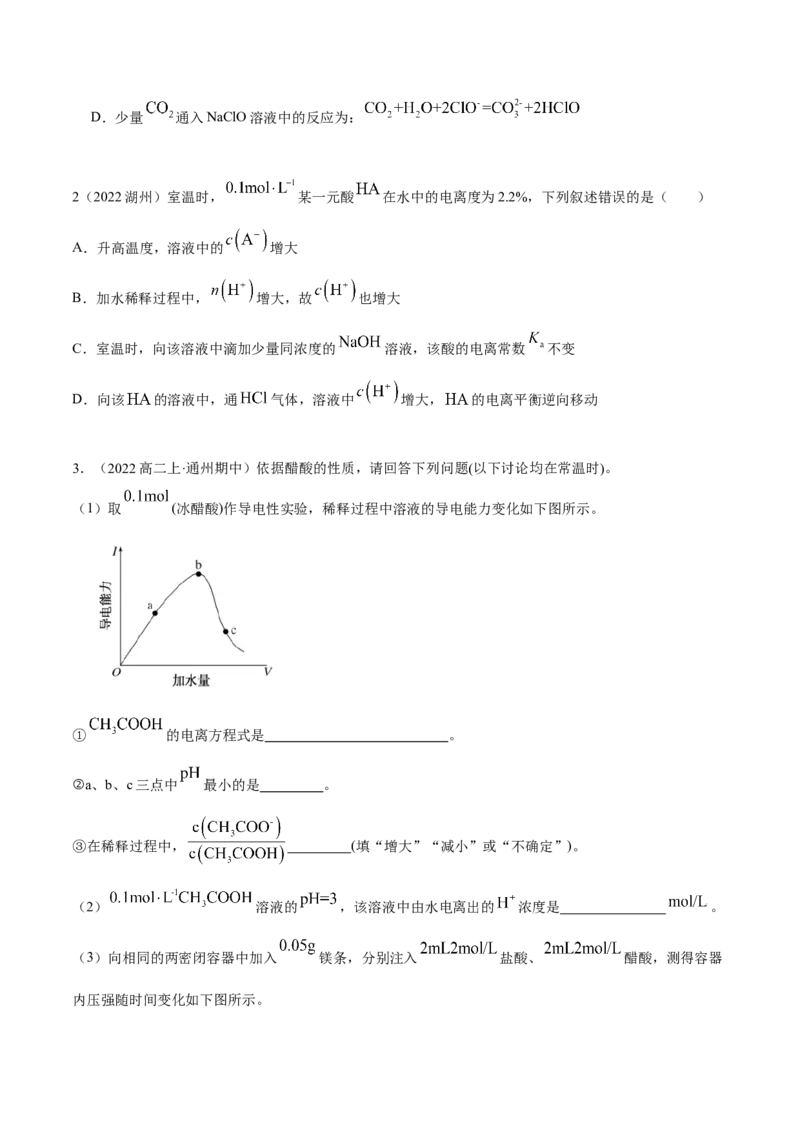
(1)取 (冰醋酸)作导电性实验,稀释过程中溶液的导电能力变化如下图所示。
① 的电离方程式是 。
②a、b、c三点中 最小的是 。
③在稀释过程中, (填“增大”“减小”或“不确定”)。
(2) 溶液的 ,该溶液中由水电离出的 浓度是 。
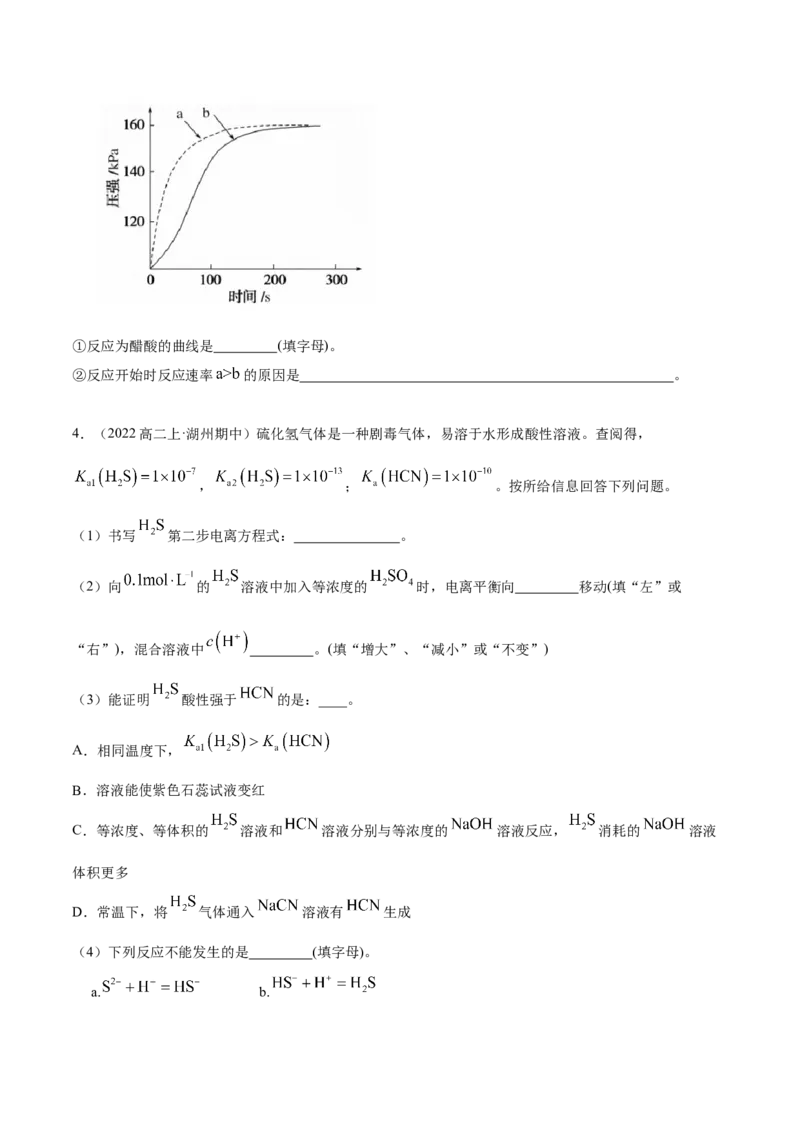
(3)向相同的两密闭容器中加入 镁条,分别注入 盐酸、 醋酸,测得容器
内压强随时间变化如下图所示。①反应为醋酸的曲线是 (填字母)。
②反应开始时反应速率 的原因是 。
4.(2022高二上·湖州期中)硫化氢气体是一种剧毒气体,易溶于水形成酸性溶液。查阅得,
, ; 。按所给信息回答下列问题。
(1)书写 第二步电离方程式: 。
(2)向 的 溶液中加入等浓度的 时,电离平衡向 移动(填“左”或
“右”),混合溶液中 。(填“增大”、“减小”或“不变”)
(3)能证明 酸性强于 的是:____。
A.相同温度下,
B.溶液能使紫色石蕊试液变红
C.等浓度、等体积的 溶液和 溶液分别与等浓度的 溶液反应, 消耗的 溶液
体积更多
D.常温下,将 气体通入 溶液有 生成
(4)下列反应不能发生的是 (填字母)。
a. b.c. d.
考向二 水的电离和溶液的PH
【例2-1】(2022浙江)下列说法正确的是( )
A.常温下,pH=12的NaOH溶液中,
B.常温下,由水电离出的 ,则该溶液一定呈碱性
C.中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同
D.常温下,用水稀释0.1 的醋酸溶液的过程中, 的物质的量增大
【例2-2】.常温下,某溶液中由水电离出的 ,该溶液可能是( )
A. 溶液 B. 溶液 C.氨水 D. 溶液
【例2-3】.(2022高二上·宝应期中)关于水的电离,下列叙述中,正确的是( )
A.升高温度,水的平衡向正反应方向移动,K 增大,c(OH-)增大,pH增大
w
B.向水中加入少量硫酸,水的平衡向逆反应方向移动,K 不变,c(H+)增大
w
C.向水中加入氨水,水的平衡向逆反应方向移动,K 不变,c(OH-)降低
w
D.向水中加入少量固体醋酸钠,平衡向逆反应方向移动,K 不变,c(H+)降低
w
【一隅三反】
1.(2022河南)常温下,某溶液中由水电离出的c(OH-)=1×10-10mol/L,该溶液不可能是( )
A.醋酸 B.氨水 C.盐酸 D.NaCl溶液
2.(2022浙江)常温条件下,下列溶液一定呈酸性的是( )
A.滴加甲基橙指示剂后变为橙色的溶液
B.加入Al产生 的溶液
C.由水电离出的 溶液D.含 的水溶液
3.(2022浙江)下列溶液不一定显中性的是( )
A.pH=6的蒸馏水
B.
C. 的溶液
D.水电离出的氢离子物质的量浓度为 mol/L
4.(2022浙江)室温下,水的电离达到平衡: 。下列叙述错误的是( )
A.向水中加入少量金属Na,平衡正向移动, 增大
B.向水中加入少量 ,平衡逆向移动, 变小
C.向水中加入少量 ,水的电离程度减小, 增大
D.向水中加入少量NaCl固体,溶液呈中性,水的电离平衡不移动
5.(2022河南)酸、碱、盐的水溶液在生产生活及化学实验中有广泛的应用,请同学们运用所学知识解
决下列问题。
(1)某温度T下,0.1mol/L的NaOH溶液中,c(H+)=1.0×10-11mol/L,此时水的离子积常数K =
w
。温度T 25℃(填“大于”“小于”或“等于”),原因是 。由水电
离的c(OH-)= mol/L。
(2)已知水溶液中c(H+)和c(OH-)的关系如图所示:①图中A、B、C、D四点对应的水的离子积常数由大到小的顺序是 。
②若A点到E点,可采用的措施是 (填序号,下同);从A点到C点,可采用的措施是 ;
促进水的电离平衡的措施是 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH
(3)常温下0.1mol/L的HA溶液中,c(H+)=0.001mol/L,写出HA的电离方程式 ,水电离
的c(H+)= mol/L。为使HA溶液中HA和HO的电离平衡正向移动,而水的K 保持不变可
2 w
以采取的措施是 。
6.(2022河南)下列物质中:①CHCOOH②NH ③NH Cl④盐酸⑤NaOH⑥NaHCO 溶液。
3 3 4 3
(1)属于弱电解质的是 (填序号,下同),属于强电解质且其水溶液呈碱性的是 。
(2)在氨水中存在电离平衡:NH •H O NH +OH-。将上述六种物质分别配成0.1mol/L的溶液,向稀
3 2
氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且c(NH )增大的是 (填序号),此
时c(OH-) (填“增大”“减小”或“不变”,下同), = 。
(3)等体积c(H+)相同的盐酸和醋酸分别与0.1mol•L-1的NaOH溶液恰好完全反应,消耗NaOH体积较大的
是 (填化学式),反应过程中醋酸的电离程度 (填“增大”“减小”或“不变”,下
同),n(CHCOO-) ,水的电离程度逐渐 ,水电离的c(H+)= 。
3
(4)已知次氯酸(HClO)的电离平衡常数为K=4.0×10-8,向20mL0.1mol•L-1的HClO溶液中滴加少量硫酸,
a再加水稀释至40mL,此时测得c(H+)=0.05mol•L-1,则溶液中c(ClO-)= mol•L-1。
(5)已知亚硫酸(H SO )的电离平衡常数为K =1.6×10-2,K =1.0×10-7;碳酸(H CO)的电离平衡常数为
2 3 a1 a2 2 3
K =4.0×10-7,K =4.0×10-11。足量的HSO 溶液和NaHCO 溶液发生反应的主要离子方程式为 。
a1 a2 2 3 3
考向三 盐类的水解
【例3-1】.下列方程式中,属于水解反应的是( )
A. B.
C. D.
【例3-2】.下列物质的应用过程中不涉及盐类水解的是( )
A.小苏打用作食品膨松剂
B.硫酸铝钾作净水剂
C.热碱水清洗厨房里的油污
D. 组成 为7.5的缓冲溶液
【例3-3】.(2022温州)下列物质的水溶液因水解而呈碱性的是( )
A.NaOH B.(NH )SO C.NaCl D.NaCO
4 2 4 2 3
【例3-4】(2022安徽)已知 溶液中存在如下平衡: ,下列说
法中正确的是( )
A.加入适量水后平衡向右移动, 增大
B.加热后平衡向左移动, 增大
C.加入 后有气泡产生,一段时间后可得到红褐色沉淀
D.加热蒸干溶液并灼烧可得
【一隅三反】1.(2022桂林)以下应用与盐类水解无关的是( )
A.用热碱去除废铁屑表面油污
B.配制NaS溶液时需将NaS溶于NaOH浓溶液
2 2
C.用硫酸铝溶液和碳酸氢钠溶液混合灭火
D.用FeCl 溶液刻蚀铜制电路板
3
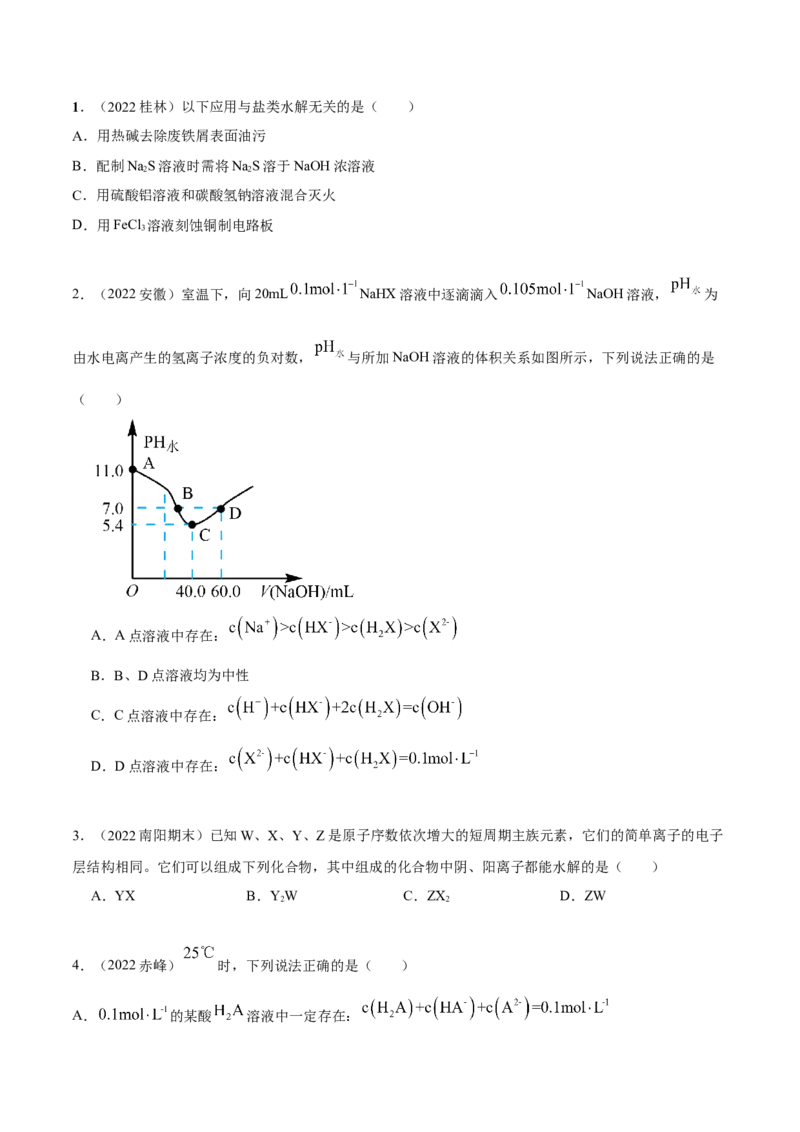
2.(2022安徽)室温下,向20mL NaHX溶液中逐滴滴入 NaOH溶液, 为
由水电离产生的氢离子浓度的负对数, 与所加NaOH溶液的体积关系如图所示,下列说法正确的是
( )
A.A点溶液中存在:
B.B、D点溶液均为中性
C.C点溶液中存在:
D.D点溶液中存在:
3.(2022南阳期末)已知W、X、Y、Z是原子序数依次增大的短周期主族元素,它们的简单离子的电子
层结构相同。它们可以组成下列化合物,其中组成的化合物中阴、阳离子都能水解的是( )
A.YX B.YW C.ZX D.ZW
2 2
4.(2022赤峰) 时,下列说法正确的是( )
A. 的某酸 溶液中一定存在:B. 的氨水溶液稀释10倍后
C. 相同的 溶液、 溶液、 溶液,其浓度大小关系:
D.常温下, 溶液中,由水电离产生的 浓度为
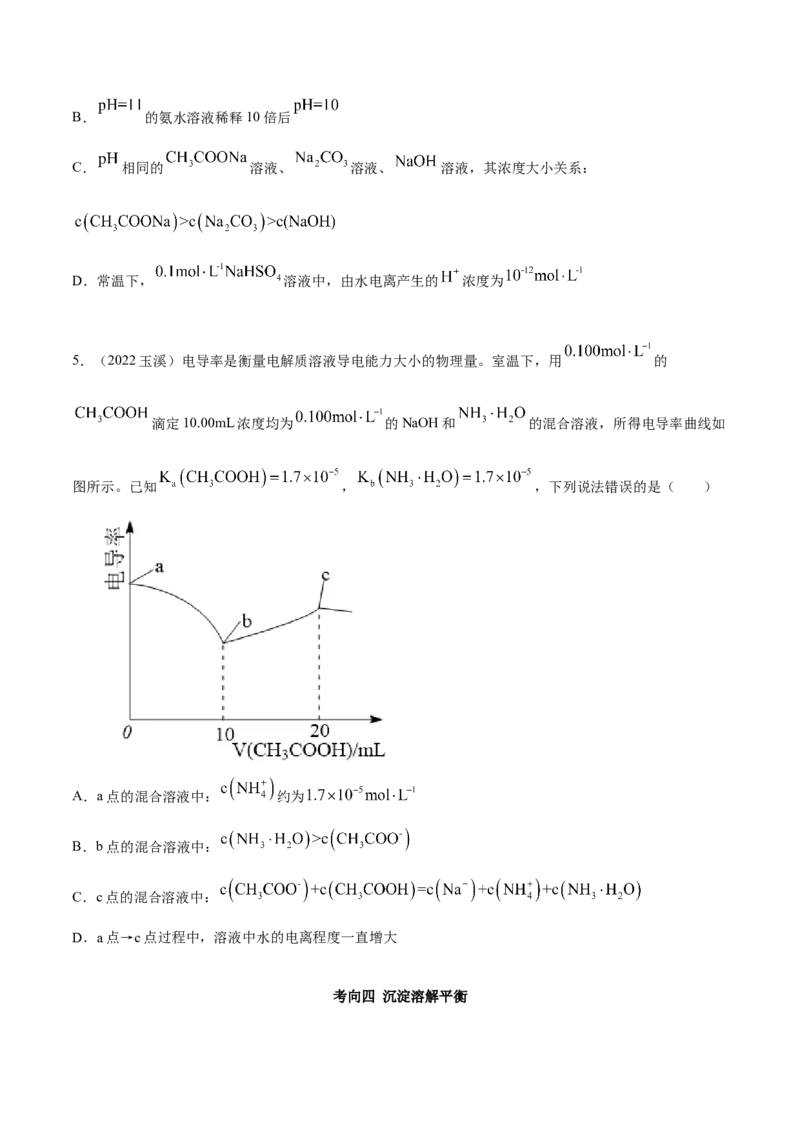
5.(2022玉溪)电导率是衡量电解质溶液导电能力大小的物理量。室温下,用 的
滴定10.00mL浓度均为 的NaOH和 的混合溶液,所得电导率曲线如
图所示。已知 , ,下列说法错误的是( )
A.a点的混合溶液中: 约为
B.b点的混合溶液中:
C.c点的混合溶液中:
D.a点→c点过程中,溶液中水的电离程度一直增大
考向四 沉淀溶解平衡【例4-1】已知:常温下, , , 。在
自然界中,闪锌矿(ZnS)和方铅矿(PbS)遇硫酸铜溶液均能转化成铜蓝(CuS)。下列说法正确的是( )
A.饱和PbS溶液中,
B.相同温度下,在水中的溶解度:ZnS>CuS>PbS
C.向PbS固体中滴加一定量 溶液,反应达到平衡时,溶液中
D.向含浓度相同的 、 、 的混合溶液中逐滴加入 稀溶液, 先沉淀
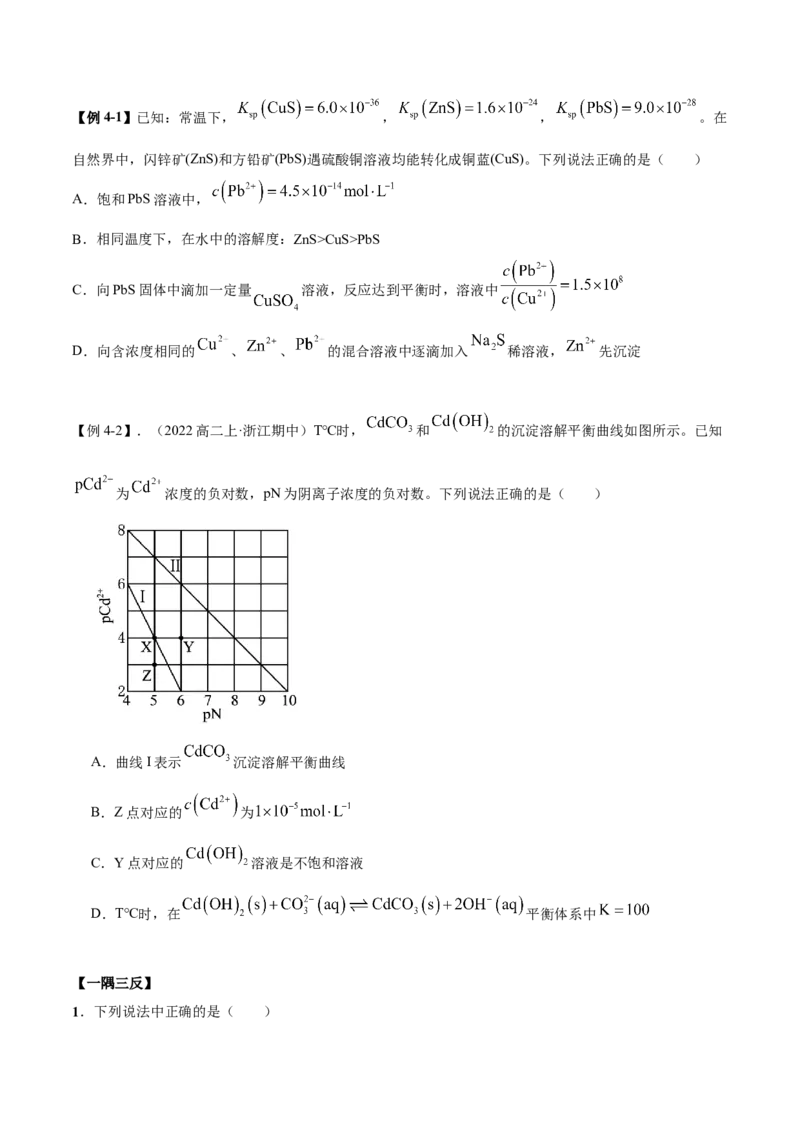
【例4-2】.(2022高二上·浙江期中)T℃时, 和 的沉淀溶解平衡曲线如图所示。已知
为 浓度的负对数,pN为阴离子浓度的负对数。下列说法正确的是( )
A.曲线I表示 沉淀溶解平衡曲线
B.Z点对应的 为
C.Y点对应的 溶液是不饱和溶液
D.T℃时,在 平衡体系中
【一隅三反】
1.下列说法中正确的是( )A.向 悬浊液中加水稀释,平衡右移, 和 增大
B. 在水溶液中存在平衡: ,升温,溶液碱性增强
C.向盛有 溶液的试管中滴加 溶液,再向其中滴加4-5滴
溶液,先观察到白色沉淀,后又产生黄色沉淀,说明
D.将 溶液滴入 和 混合溶液中,先产生
沉淀[ , ]
2.(2022高二上·联合期中)在t℃时 在水中的沉淀溶解平衡曲线如图所示。已知t℃时
。下列推断错误的是( )
A.在t℃时, 的 为
B.向p点的溶液中加入少量 固体,溶液组成沿曲线向n方向移动
C.图中a点代表 的不饱和溶液
D.在t℃时, 的平衡常数3.(2022浙江月考)含 的废水常用 作沉淀剂,原理为
。一定温度下,下列有关该反应的推理正确的是( )
A.该反应达到平衡时,
B.平衡体系中加入少量 后, 变小
C.平衡体系中加入少量 后, 变大
D.该反应平衡常数:
4.(2022河南月考)常温下, 或 的单一饱和溶液体系中,金属阳离子的物质的量浓
度的负对数 与溶液 的变化关系如图所示。已知常温下, ,
下列说法错误的是( )
A.曲线a表示 饱和溶液中的变化关系,且B.向X点对应的饱和溶液中加入少量 固体,可转化为Y点对应的溶液
C.除去 酸性溶液中含有的少量 杂质,可加入适量 ,充分搅拌后过滤
D.当 和 两种沉淀共存时,溶液中倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育