文档内容
初中化学——第十单元 酸和碱 教学设计
课题1常见的酸和碱(1)
襄州区张湾办事处中心学校 魏威
教学目标
1、知识与技能:
(1)认识几种常见的酸,知道酸都具有相似的化学性质。
(2)知道酸的腐蚀性,能熟练取用酸及其溶液。
(3)会用酸碱指示剂检验溶液的酸碱性。
2、过程与方法:
(1)通过浓硫酸的强腐蚀性和浓硫酸的稀释实验,学会浓硫酸的稀释方法,强化实验及生活
中的安全意识。
(2)通过几种常见的酸化学性质的探究比较,能简单的归纳出酸的化学性质。
3、情感态度与价值观:
(1)树立科学的物质观,学会用辩证的观点看待事物,能透过表面现象挖掘事物具有共性的
本质原因。
(2)知道化学作为自然科学的一部分。它本身就起源于人类生产活动,树立学好化学,更要用
好化学的意识。
教学重难点
重点:
1、科学素养的培养和提高。
2、酸化学性质
难点:为什么不同的酸具有相似的化学性质
教学过程
教学 教师活动 学生活动 设计意图
流程
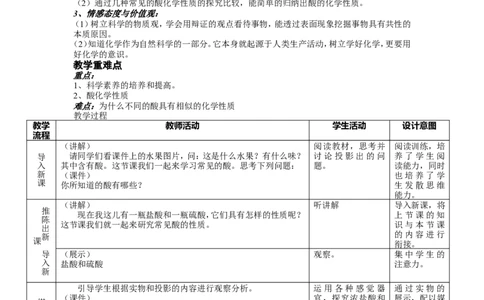
(讲解) 阅读教材,思考并 阅读训练,培
导 请同学们看课件上的水果图片,问:这是什么水果?有什么味? 讨论投影出的问 养了学生阅
入 其中含有酸。这节课我们一起来学习常见的酸。思考下列问题: 题。 读能力,同时
新 (课件) 也培养了学
课 你所知道的酸有哪些? 生发散思维
能力。
推
陈
出
新
(讲解) 听讲解 导入新课,将
现在我这儿有一瓶盐酸和一瓶硫酸,它们具有怎样的性质呢? 上节课的知
这节课我们就一起来研究常见酸的性质。 识与本节课
的内容进行
课
衔接。
导 (展示) 观察。 集中学生的
入 盐酸和硫酸 注意力。
新
媒
体
辅
助
引导学生根据实物和投影的内容进行观察分析。 运用各种感觉器 通过实物的
(课件) 官,探究浓盐酸和 展示,配以媒
浓盐酸 浓硫酸 浓硫酸的物理性 体的辅助,使
颜色、状态 质,并进行对比,完 浓硫酸、浓盐
打开 成表格。 酸的物理性
瓶盖 质清晰地呈
引 现在学生面
气味
导 前。
观 敞口
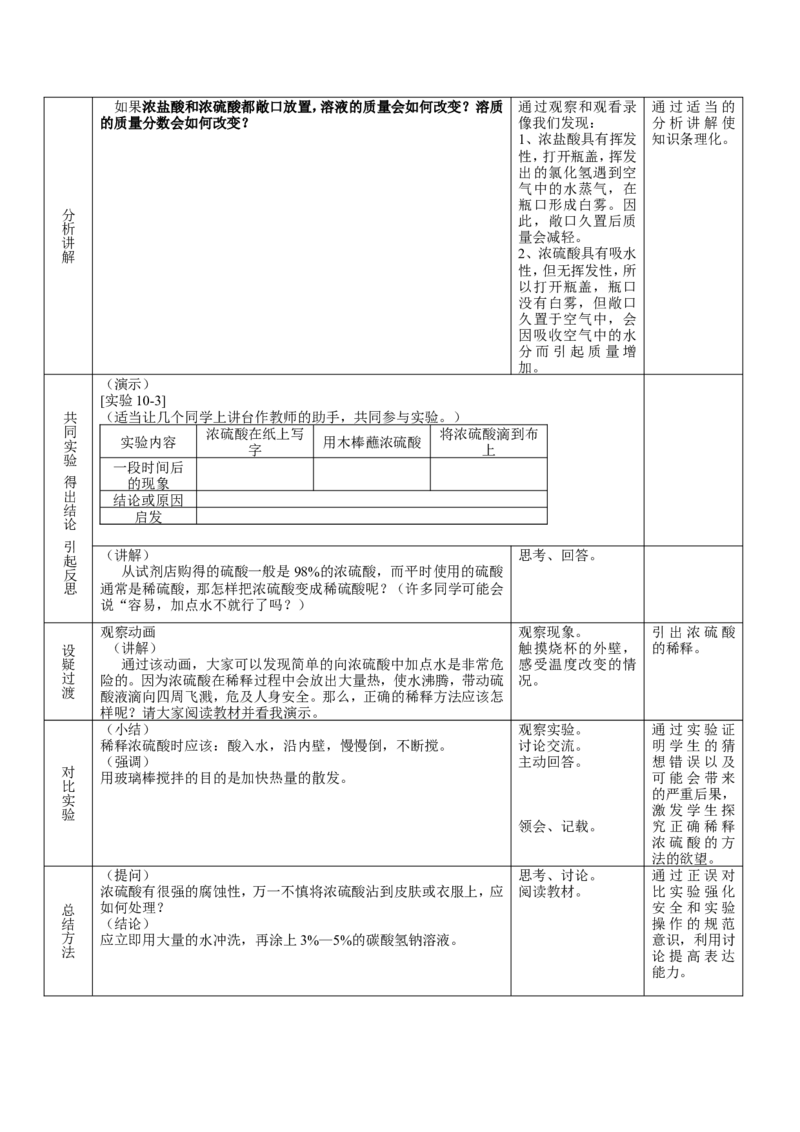
察 久置如果浓盐酸和浓硫酸都敞口放置,溶液的质量会如何改变?溶质 通过观察和观看录 通过适当的
的质量分数会如何改变? 像我们发现: 分析讲解使
1、浓盐酸具有挥发 知识条理化。
性,打开瓶盖,挥发
出的氯化氢遇到空
气中的水蒸气,在
瓶口形成白雾。因
分
此,敞口久置后质
析
量会减轻。
讲
解
2、浓硫酸具有吸水
性,但无挥发性,所
以打开瓶盖,瓶口
没有白雾,但敞口
久置于空气中,会
因吸收空气中的水
分而引起质量增
加。
共
同
实
验
得
出
结
论
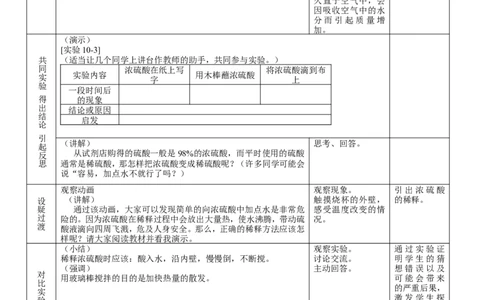
(演示)
[实验10-3]
(适当让几个同学上讲台作教师的助手,共同参与实验。)
浓硫酸在纸上写 将浓硫酸滴到布
实验内容 用木棒蘸浓硫酸
字 上
一段时间后
的现象
结论或原因
启发
引
(讲解) 思考、回答。
起
反 从试剂店购得的硫酸一般是98%的浓硫酸,而平时使用的硫酸
思 通常是稀硫酸,那怎样把浓硫酸变成稀硫酸呢?(许多同学可能会
说“容易,加点水不就行了吗?)
观察动画 观察现象。 引出浓硫酸
设 (讲解) 触摸烧杯的外壁, 的稀释。
疑 通过该动画,大家可以发现简单的向浓硫酸中加点水是非常危 感受温度改变的情
过 险的。因为浓硫酸在稀释过程中会放出大量热,使水沸腾,带动硫 况。
渡 酸液滴向四周飞溅,危及人身安全。那么,正确的稀释方法应该怎
样呢?请大家阅读教材并看我演示。
(小结) 观察实验。 通过实验证
稀释浓硫酸时应该:酸入水,沿内壁,慢慢倒,不断搅。 讨论交流。 明学生的猜
(强调) 主动回答。 想错误以及
对
用玻璃棒搅拌的目的是加快热量的散发。 可能会带来
比
的严重后果,
实
激发学生探
验
领会、记载。 究正确稀释
浓硫酸的方
法的欲望。
(提问) 思考、讨论。 通过正误对
浓硫酸有很强的腐蚀性,万一不慎将浓硫酸沾到皮肤或衣服上,应 阅读教材。 比实验强化
总 如何处理? 安全和实验
结 (结论) 操作的规范
方 应立即用大量的水冲洗,再涂上3%—5%的碳酸氢钠溶液。 意识,利用讨
法 论提高表达
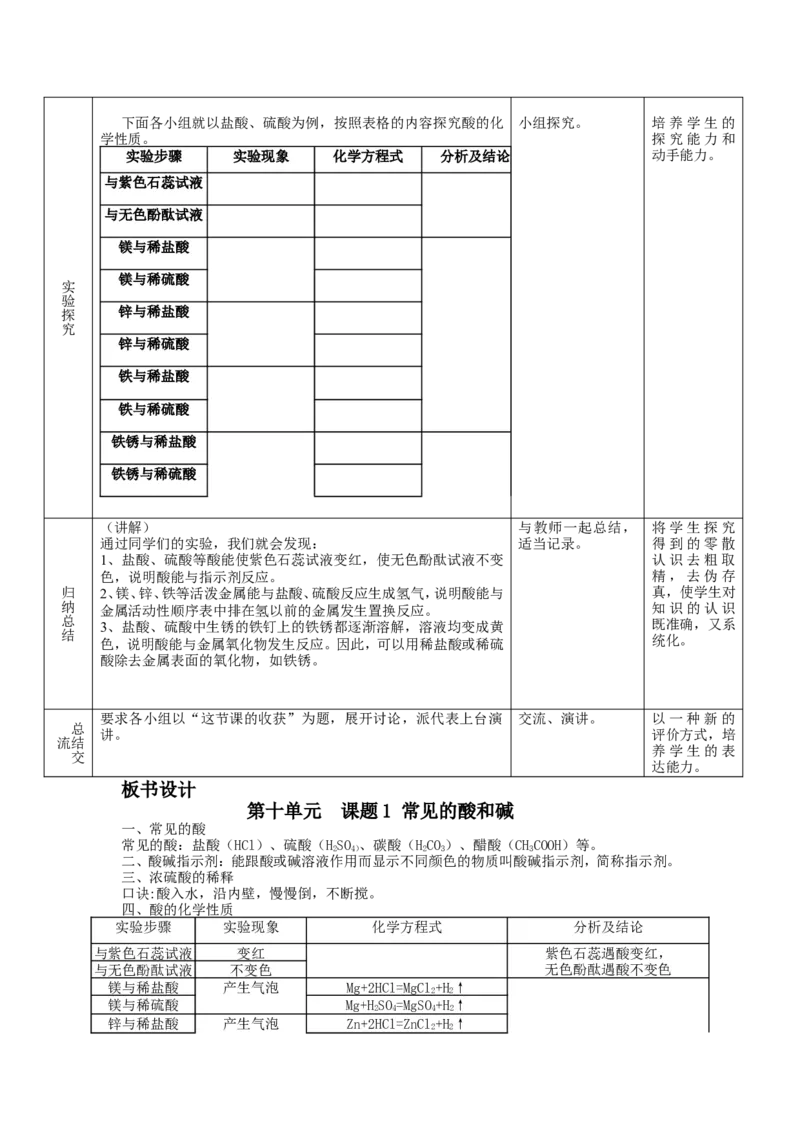
能力。下面各小组就以盐酸、硫酸为例,按照表格的内容探究酸的化 小组探究。 培养学生的
学性质。 探究能力和
实验步骤 实验现象 化学方程式 分析及结论 动手能力。
与紫色石蕊试液
与无色酚酞试液
镁与稀盐酸
镁与稀硫酸
实
验
探 锌与稀盐酸
究
锌与稀硫酸
铁与稀盐酸
铁与稀硫酸
铁锈与稀盐酸
铁锈与稀硫酸
(讲解) 与教师一起总结, 将学生探究
通过同学们的实验,我们就会发现: 适当记录。 得到的零散
1、盐酸、硫酸等酸能使紫色石蕊试液变红,使无色酚酞试液不变 认识去粗取
色,说明酸能与指示剂反应。 精,去伪存
归 2、镁、锌、铁等活泼金属能与盐酸、硫酸反应生成氢气,说明酸能与 真,使学生对
纳 金属活动性顺序表中排在氢以前的金属发生置换反应。 知识的认识
总 3、盐酸、硫酸中生锈的铁钉上的铁锈都逐渐溶解,溶液均变成黄 既准确,又系
结
色,说明酸能与金属氧化物发生反应。因此,可以用稀盐酸或稀硫 统化。
酸除去金属表面的氧化物,如铁锈。
要求各小组以“这节课的收获”为题,展开讨论,派代表上台演 交流、演讲。 以一种新的
总
讲。 评价方式,培
流结
养学生的表
交
达能力。
板书设计
第十单元 课题1 常见的酸和碱
一、常见的酸
常见的酸:盐酸(HCl)、硫酸(HSO 、碳酸(HCO)、醋酸(CHCOOH)等。
2 4) 2 3 3
二、酸碱指示剂:能跟酸或碱溶液作用而显示不同颜色的物质叫酸碱指示剂,简称指示剂。
三、浓硫酸的稀释
口诀:酸入水,沿内壁,慢慢倒,不断搅。
四、酸的化学性质
实验步骤 实验现象 化学方程式 分析及结论
与紫色石蕊试液 变红 紫色石蕊遇酸变红,
与无色酚酞试液 不变色 无色酚酞遇酸不变色
镁与稀盐酸 产生气泡 Mg+2HCl=MgCl+H↑
2 2
镁与稀硫酸 Mg+HSO=MgSO+H↑
2 4 4 2
锌与稀盐酸 产生气泡 Zn+2HCl=ZnCl+H↑
2 2锌与稀硫酸 Zn+HSO=ZnSO+H↑ 酸+金属→盐+氢气
2 4 4 2
铁与稀盐酸 产生气泡 Fe+2HCl=FeCl+H↑
2 2
铁与稀硫酸 溶液变成浅绿 Fe+HSO=FeSO+H↑
2 4 4 2
铁锈与稀盐酸 铁锈消失 FeO+6HCl=2FeCl+3HO
2 3 3 2
铁锈与稀硫酸 溶液变黄 FeO+3HSO=Fe(SO)+3HO
2 3 2 4 2 4 3 2
酸+金属氧化物→盐+水
氧化铜与稀盐酸 黑色粉末消失 CuO+2HCl=CuCl+HO
2 2
溶液变绿
氧化铜与稀硫酸 黑色粉末消失 CuO+ HSO=CuSO+H0
2 4 4 2
溶液变蓝
小结:
1、盐酸、硫酸等酸能使紫色石蕊试液变红,使无色酚酞试液不变色,说明酸能与指示剂反应。
2、镁、锌、铁等活泼金属能与盐酸、硫酸反应生成氢气,说明酸能与金属活动性顺序表中排在
氢以前的金属发生置换反应。
3、盐酸、硫酸中生锈的铁钉上的铁锈都逐渐溶解,溶液均变成黄色,说明酸能与金属氧化物
发生反应。因此,可以用稀盐酸或稀硫酸除去金属表面的氧化物,如铁锈。