文档内容
溶液综合练习重点突破(二)
【例2】A和B两种固体的溶解度曲线如右图所示。下列说法中,正确的是( )
【例1】已知:Na
2
O + H
2
O 2NaOH,向饱和的氢氧化钠溶液中加入一定量 A.通过降温可以将A的饱和溶液变为不饱和溶液
的Na O,充分反应后恢复到原来温度。下列说法中,正确的是( )
2 B.当A和B溶液的溶质质质质量分数相同时时,,温度一定是20℃
A.溶液中溶质质量增多,溶液的质量减少
C.10℃时,10 g水中分别溶解A、B达到饱和,溶解得更多的物质是B
B.溶液中溶质质量增多,溶液的质量增加
D.把把100 gg质质量量分分数数为为10%%的的B溶溶液液从从30℃降降温温到到10℃,,其其质质量量分分数数仍仍为为10%%
C.溶液中水的质量减少,溶质质量分数不变
D.溶液中水的质量减少,溶质质量分数增大
【例3】一定量的NaOH溶液中逐滴加入等质量等质量分数的稀盐酸,下列 【例4】右图是NaOH溶液与稀盐酸恰好完全反应的微观示意图,由此得到
各物质的量与所加入稀盐酸的质量关系不正确的是( ) 的结论不正确的是
A.反应结束时溶液的pH=7 ( )
B.NaOH溶液中存在的粒子是Na+和OH-
C.该反应的实质是H+和OH-结合生成H O分子
2
D.若两者者恰好完全反应应,,所所得得溶液中中溶质质的质质量分数为11.7%,,则则此溶液
中钠离子与水分子的个数比为36:883
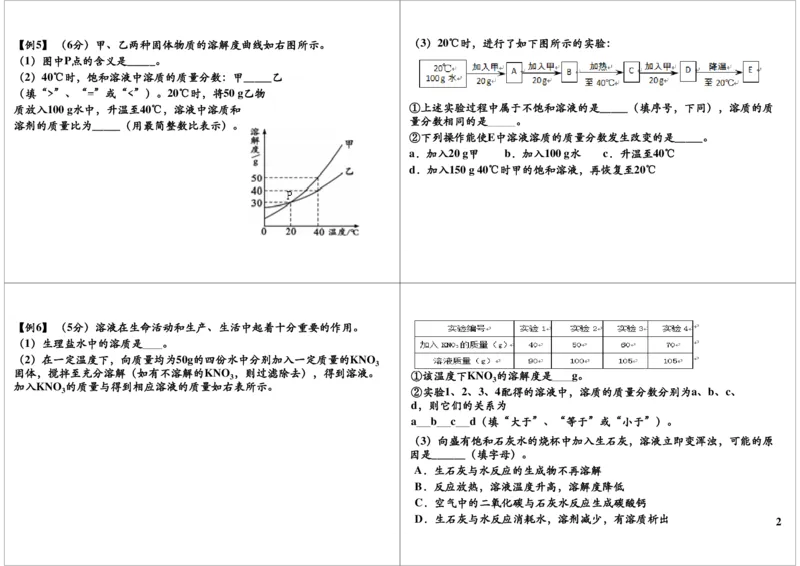
1【例5】(6分)甲、乙两种固体物质的溶解度曲线如右图所示。 (3)20℃时,进行了如下图所示的实验:
((11))图图中中PP点点的的含含义义是是_____。。
(2)40℃时,饱和溶液中溶质的质量分数:甲_____乙
((填填“>>”、、“=”或或“<<”))。。2200℃℃时时,将将5500 gg乙乙物物
质放入100 g水中,升温至40℃,溶液中溶质和 ①上述实验过程中属于不饱和溶液的是_____(填序号,下同),溶质的质
量分数相同的是_____。
溶溶剂剂的的质质量量比比为为_____((用用最最简简整整数数比比表表示示))。
②下列操作能使E中溶液溶质的质量分数发生改变的是_____。
aa..加加入200 gg甲甲 bb..加加入10000 gg水水 cc..升升温温至至400℃℃
d.加入150 g 40℃时甲的饱和溶液,再恢复至20℃
【例6】(5分)溶液在生命活动和生产、生活中起着十分重要的作用。
((11))生生理理盐盐水水中中的的溶溶质质是是 。。
(2)在一定温度下,向质量均为50g的四份水中分别加入一定质量的KNO
3
固固体体,,搅搅拌拌至充分分溶溶解解((如有有不不溶溶解解的的KNO 33 ,,则则过过滤滤除除去)),,得得到到溶溶液液。 ①①该该温温度度下下KKNNOO 33 的的溶溶解解度度是是 gg。。
加入KNO 的质量与得到相应溶液的质量如右表所示。
3 ②实验1、2、3、4配得的溶液中,溶质的质量分数分别为a、b、c、
dd,,则则它它们们的的关关系系为为
a b c d(填“大于”、“等于”或“小于”)。
((33))向向盛盛有有饱饱和和石石灰灰水水的的烧烧杯杯中中加加入入生生石石灰灰,溶溶液液立立即即变变浑浑浊浊,可可能能的的原原
因是______(填字母)。
AA.生生石石灰灰与与水水反反应应的的生生成成物物不不再再溶溶解解
B.反应放热,溶液温度升高,溶解度降低
CC.空空气气中中的的二二氧氧化化碳碳与与石石灰灰水水反反应应生生成成碳碳酸酸钙钙
D.生石灰与水反应消耗水,溶剂减少,有溶质析出 2【例7】(6分)下列数据是氯化钠和氯化铵固体在不同温度时的溶解度。 (4)现有200 g溶质质量分数为10%的氯化钠溶液,若使溶液的溶质质量分
数增加一倍,应该蒸发掉 gg水。
(5)30℃时,向两个分别盛有相同质量的氯化钠和氯化铵的烧杯中,各加
入入110000 gg水水,充充分分溶溶解解后后,恢恢复复至至3300℃℃,其其结结果果如如右右图图所所示示。。有有关关下下列列说说法法
中,正确的是 (填字母序号)。
A.烧烧杯杯②②中中溶溶液液是是不不饱饱和和溶溶液液
(1)医疗上,氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为 B.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
________。。 CC..若若将将烧烧杯杯①①中中的的溶溶液液变变为为不不饱饱和和溶溶液液,,溶溶液液中中溶溶质质质质量量分分数数一定定减减小小
(2)从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高氯 D.将得到的烧杯②中溶液降温至0℃时,溶液中溶质质量分数一定减小
化钠的溶解解度变化 ((填填“大”或“小”))。
(3)20℃时,向100 g水中加入25 g氯化钠,充分溶解后,溶液中溶质质量
分数为________。
3