文档内容
第四章 物质结构 元素周期律
第三节 化学键
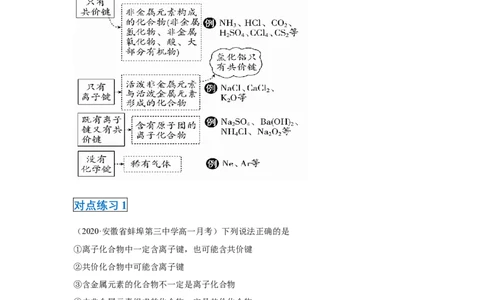
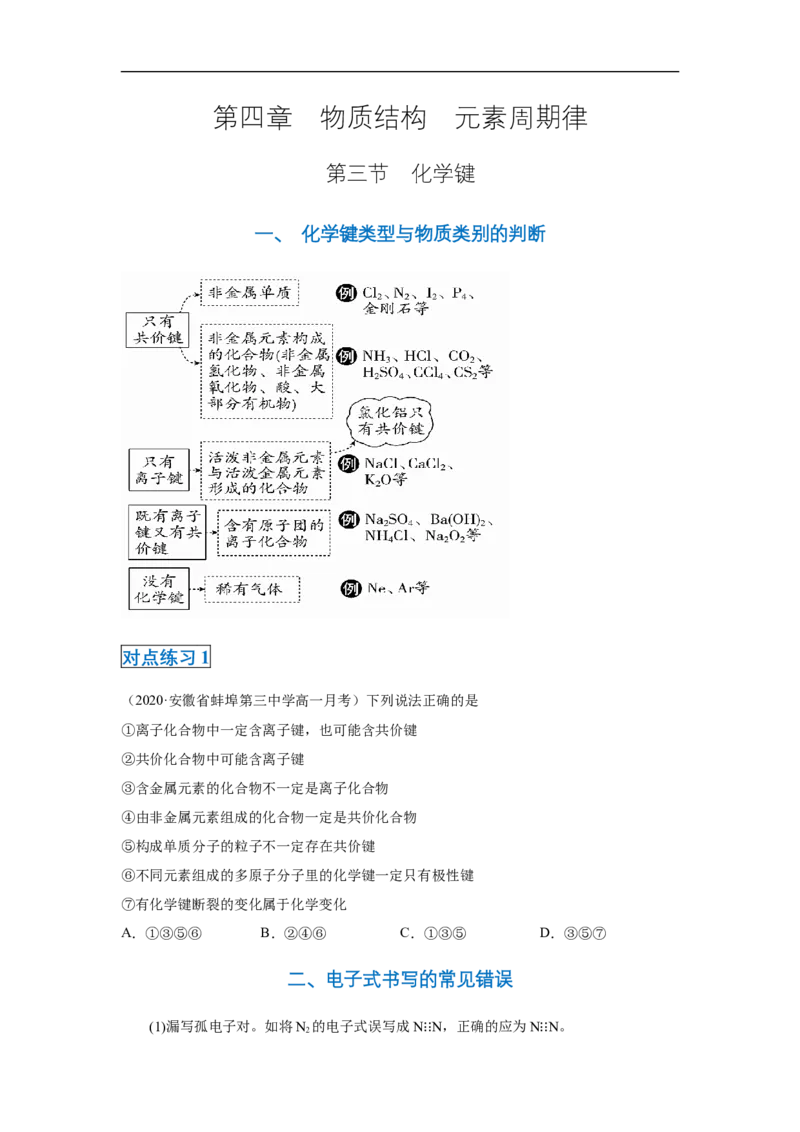
一、 化学键类型与物质类别的判断
对点练习1
(2020·安徽省蚌埠第三中学高一月考)下列说法正确的是
①离子化合物中一定含离子键,也可能含共价键
②共价化合物中可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤构成单质分子的粒子不一定存在共价键
⑥不同元素组成的多原子分子里的化学键一定只有极性键
⑦有化学键断裂的变化属于化学变化
A.①③⑤⑥ B.②④⑥ C.①③⑤ D.③⑤⑦
二、电子式书写的常见错误
(1)漏写孤电子对。如将N 的电子式误写成N N,正确的应为N N。
2
⋮⋮ ⋮⋮(2)混淆电子式与化学式的书写,如将NaS的电子式误写成Na[S]2-。
2
(3)共用电子对数目不清,如将CO 的电子式误写成
2
OCO,正确的应为O·C·O。
· ·
(4)错误使用括号,如将HO的电子式误写成
2
H+[O]2-H+,正确的应为HOH。
(5)原子结构顺序写错,如将HClO的电子式误写成
HClO,正确的应为HOCl。
(6)误将电荷数及电性标成化合价,如将NaO的电子式误写成Na+[O]-2Na+,正确的
2
应为
Na+[O]2-Na+。
对点练习2
(2020·北京东城区·汇文中学高一期中)下列物质的电子式书写正确的是
A. B. C. D.
三、 用电子式表示化合物的形成过程时注意事项
(1)连接号必须使用“―→”,不能用等号。
(2)左边写出原子的电子式并用箭头标出电子转移情况,右边构成离子化合物的每个离
子的电子式都要单独写,不能合并,而且要符合相邻关系。
(3)阳离子的电子式要标离子所带的电荷数,阴离子的电子式要用[ ]表示。
(4)要和化学方程式区别开,形成过程只是表示由原子形成离子的过程,左侧不能写成
物质的化学式。
对点练习3
(2020·全国高一课时练习)下列用电子式表示化合物的形成过程正确的是( )A.
B.
C.
D.
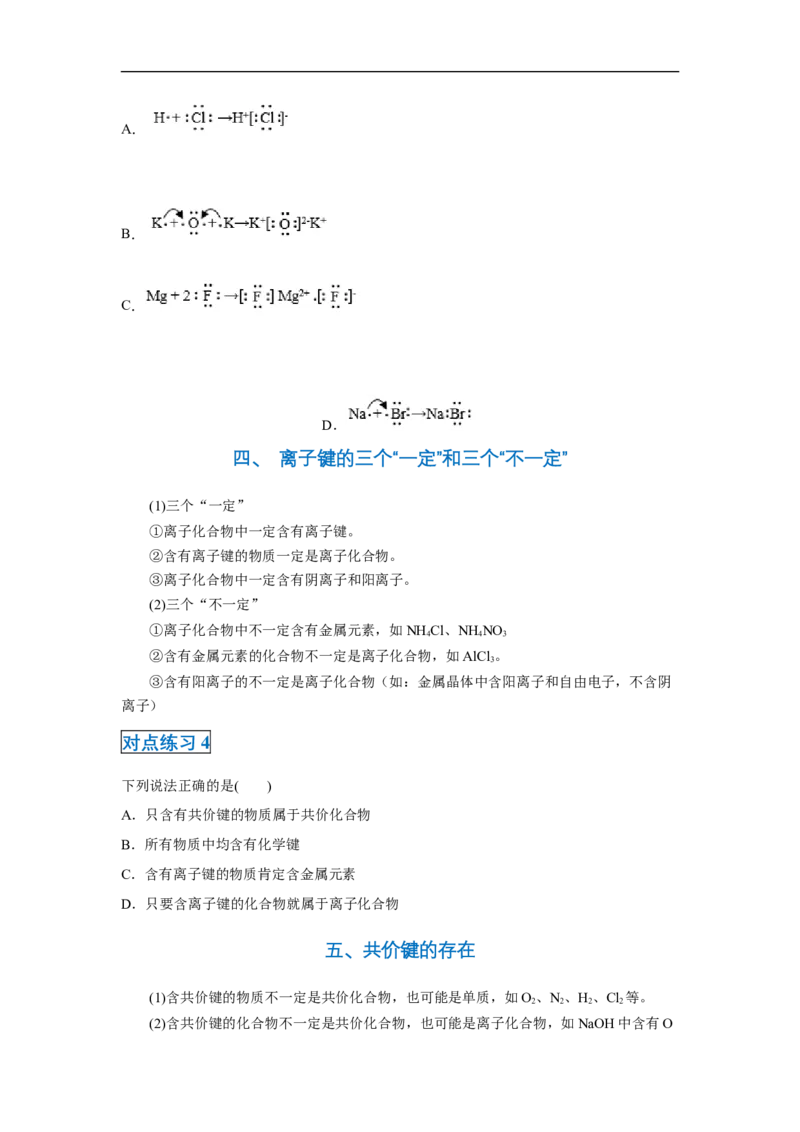
四、 离子键的三个“一定”和三个“不一定”
(1)三个“一定”
①离子化合物中一定含有离子键。
②含有离子键的物质一定是离子化合物。
③离子化合物中一定含有阴离子和阳离子。
(2)三个“不一定”
①离子化合物中不一定含有金属元素,如NH Cl、NH NO
4 4 3
②含有金属元素的化合物不一定是离子化合物,如AlCl 。
3
③含有阳离子的不一定是离子化合物(如:金属晶体中含阳离子和自由电子,不含阴
离子)
对点练习4
下列说法正确的是( )
A.只含有共价键的物质属于共价化合物
B.所有物质中均含有化学键
C.含有离子键的物质肯定含金属元素
D.只要含离子键的化合物就属于离子化合物
五、共价键的存在
(1)含共价键的物质不一定是共价化合物,也可能是单质,如O、N、H、Cl 等。
2 2 2 2
(2)含共价键的化合物不一定是共价化合物,也可能是离子化合物,如NaOH中含有O—H共价键,NaO 中含有O—O共价键,NH Cl中含有N—H共价键,但它们都是离子化
2 2 4
合物。
对点练习5
(2020·云南昆明市·高一学业考试)下列物质中,离子键和共价键都含有的是
A.NaOH B. C. D.
六、离子化合物和共价化合物的判断方法
(1)根据化学键的类型判断
凡含有离子键的化合物,一定是离子化合物;只含有共价键的化合物,是共价化合物。
(2)根据化合物的类型来判断
大多数碱性氧化物、强碱和盐都属于离子化合物;非金属氢化物、非金属氧化物、含
氧酸都属于共价化合物。
(3)根据化合物的性质来判断
熔、沸点较低的化合物(SiO、SiC等除外)是共价化合物。熔化状态下能导电的化合物
2
是离子化合物,如NaCl;熔化状态下不导电的化合物是共价化合物,如HCl。
对点练习6
(2019·上海市杨浦高级中学高一期末)下列物质属于离子化合物的是 ( )
A.NH B.NH HCO C.SiO D.HNO
3 4 3 2 3
本节 跟踪练习
1.(2019·上海市杨浦高级中学高一期末)下列物质属于离子化合物的是 ( )
A.NH B.NH HCO C.SiO D.HNO
3 4 3 2 3
2.(2020·云南昆明市·高一学业考试)下列物质中,离子键和共价键都含有的是
A.NaOH B. C. D.
3.(2020·全国高一课时练习)下列用电子式表示化合物的形成过程正确的是( )
A.B.
C.
D.
4.(2019·上海市杨浦高级中学高一期末)下列物质属于共价化合物的是 ( )
A.KOH B.MgO C.C H D.C
2 6 60
5.(2020·福建台江区·福州四中高三月考)下列说法中正确的是( )
A.N 属于单质,不存在化学键
2
B.KOH中既含有离子键也含有共价键,属于离子化合物
C.MgCl 中既含有离子键,又含有共价键
2
D.NH Cl全部由非金属元素组成,属于共价化合物
4
6.(2020·河南宛城区·南阳中学高二月考)下列说法正确的个数为( )
①化学键断裂,一定发生化学变化
②任何物质中都存在化学键
③氢键是极弱的化学键,分子间作用力不是化学键
④离子键就是阴、阳离子之间的静电吸引力
⑤活泼金属与活泼非金属化合时能形成离子键
⑥共价化合物中,成键原子均满足8电子稳定结构
⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电
⑧由非金属元素形成的化合物中不可能含有离子键
A.1 B.2 C.3 D.4
7.(2020·浙江高一期中)元素符号、反应方程式、结构示意图、电子式、结构式等通常
叫做化学用语。下列有关化学用语的表示方法中不正确的是( )
A.次氯酸的电子式为 B.中子数为16的磷原子为 P
C.CO 分子的结构式为O=C=O D.S2-的结构示意图为
28.(2020·全国高一课时练习)下列化合物的电子式书写正确的是( )
A.Ca2+ B.Na
C. D.K+
9.(2020·全国高一课时练习)下列分子中所有原子都满足最外层为8电子稳定结构的是(
)
A.AlCl B.HO C.SiCl D.PCl
3 2 4 5
10.(2020·河北高碑店市·高碑店一中高一月考)下列说法中不正确的是( )
A.离子化合物中不一定含有金属元素
B.含有金属元素的离子不一定是阳离子
C.分子中不一定存在着共价键
D.由不同原子所形成的纯净物一定是化合物
11.(2020·全国高一课时练习)用电子式表示下列化合物的形成过程:
NaF:_____
CaCl :_____
2
NaS: _____
2
MgO: _____
KO: _____
2
12.(2020·北京东城区·汇文中学高一期中)下表是元素周期表的一部分,请参照元素①
至⑧的位置回答下列问题。
族
Ⅰ Ⅱ Ⅲ Ⅴ
ⅣA ⅥA ⅦA 0
A A A A
周期
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦
(1)元素②的一种原子中,含有8个中子,则该原子的符号是_________。
(2)元素⑥的原子结构示意图是_____________。
(3)由元素③组成的__________(填化学式)和_________(填化学式)互为同素异形体。(4)仅由元素①、④组成的化合物甲,化合物甲的电子式为________ ,该化合物分子中含
有______(填“极性”或“非极性”)共价键。
(5)仅由元素⑤、⑦组成的化合物乙,请用电子式表示化合物乙的形成过程_____________,
该化合物属于___________(填“离子”或“共价”)化合物。
13.(2020·全国高一单元测试)(1)在①NaCl、②NaOH、③NaO、④N、⑤HS、
2 2 2 2
⑥HO 中,只含有离子键的是_____;只含有极性键的是____;只含有非极性键的是___;
2 2
既含有离子键,又含有极性键的是____;既含有离子键,又含有非极性键的是______。
(2)请用电子式表示NaCl的形成过程:______。
(3)N 的结构式为:_____;HO 的结构式为:_____。
2 2 2
(4)写出下列微粒的电子式。
①CO___________;
2
② ___________。
14.(2020·江门市第二中学高二期中)下表是元素周期表的一部分,针对表中的①~⑨种
元素,填写下列空白:
主族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0族
周期
二 ① ② ③
三 ④ ⑤ ⑥ ⑦ ⑧
四 ⑨
(1)在这些元素中,化学性质最不活泼的是___________。(填元素名称)
(2)金属性最强的元素的原子结构示意图为___________。
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式是___________。
(4)元素最高价氧化物是两性氧化物的化合物的化学式是___________;写出它的氧化物与
氢氧化钠反应的离子方程式___________。
(5)表示④与⑥的化合物的电子式___________,该化合物属于___________(填 “共价”或
“离子”)化合物。
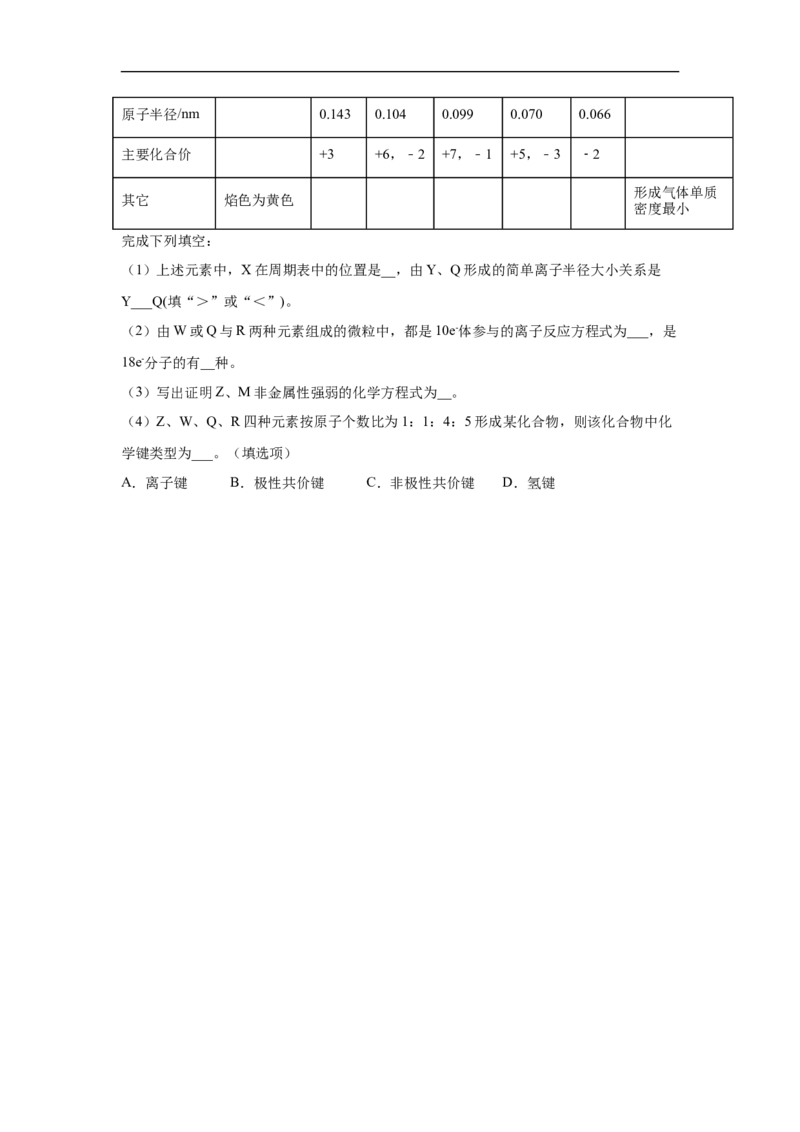
15.(2020·湖南湖南衡阳高新技术产业园区·衡阳市一中高三期中)X、Y、Z、M、W、
Q、R是7种短周期元素,其性质如下:
元素代号 X Y Z M W Q R原子半径/nm 0.143 0.104 0.099 0.070 0.066
主要化合价 +3 +6,﹣2 +7,﹣1 +5,﹣3 ﹣2
形成气体单质
其它 焰色为黄色
密度最小
完成下列填空:
(1)上述元素中,X在周期表中的位置是__,由Y、Q形成的简单离子半径大小关系是
Y___Q(填“>”或“<”)。
(2)由W或Q与R两种元素组成的微粒中,都是10e-体参与的离子反应方程式为___,是
18e-分子的有__种。
(3)写出证明Z、M非金属性强弱的化学方程式为__。
(4)Z、W、Q、R四种元素按原子个数比为1:1:4:5形成某化合物,则该化合物中化
学键类型为___。(填选项)
A.离子键 B.极性共价键 C.非极性共价键 D.氢键