文档内容
乙烯
【学习目标】
1、掌握乙烯的结构特点,会书写乙烯的分子式、结构式、结构简式、电子式
2、认识乙烯能够发生加成反应和氧化反应,熟悉乙烯发生加成反应时的断键和成键情况
3、了解烯烃的概念及烯烃物理性质的递变性和化学性质的相似性
【主干知识梳理】
一、乙烯的结构、物理性质及用途
1、乙烯分子的组成与结构
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C H CH==CH
2 4 2 2
结构特点 乙烯的结构是平面形结构,2个C原子和4个H原子在同一个平面上,键角120°
【微点拨】
①乙烯分子中的碳原子价键没有全部被氢原子“饱和”,为不饱和碳原子
②分子共线、共面问题
类型 结构式 结构特点 共线、共面情况
5个原子最多有3个原子共平面,
正四面体结
构
甲烷型
中的原子不可能共平面
规律:凡是碳原子与其他4个原子形成共价单键时,与碳原子相连的4个原子组成四面体
结构。有机物分子结构中只要出现一个饱和碳原子,则分子中的所有原子不可能共面
所有原子共平面,与碳碳双键直接相
平面形结构
乙烯型
连的4个原子与2个碳原子共平面
规律:有机物分子结构中每出现1个碳碳双键,则整个分子中至少有6个原子共面
分析丙烯(CHCH=CH)原子共面情况
3 2
三个氢原子(①②③)和三个碳原子(④⑤⑥)六原子一定共面。根据三角
情况
形规则(⑤C,⑥C,⑦H构成三角形),⑦H也可能在这个平面上
分析 即:丙烯分子最多7 个原子共平面,至少有6 个原子共平面
2、物理性质:乙烯为无色、稍有气味的气体,密度比空气的略小,难溶于水,易溶于四氯化碳等有机溶剂
3、应用
(1)乙烯是石油化工重要的基本原料,通过一系列反应,乙烯可以合成有机高分子材料、药物等。乙烯产量可以
用来衡量一个国家石油化学工业的发展水平
(2)乙烯还是一种植物生长调节剂,果实催熟剂
【对点训练1】
1、下列分子中的所有原子一定不共面的是( )
A.SO B.HO C.CH==CHCl D.CHCl
2 2 2 3
2、在下列分子中,能够在同一个平面内的原子数最多的是( )
A.甲烷(CH) B.一溴甲烷(CHBr) C.乙烯(CH==CH) D.CH—CH==CH—CH
4 3 2 2 3 3
3、关于乙烯分子结构的描述错误的是( )
A.乙烯的结构简式为CH==CH B.乙烯是最简单的烯烃
2 2
C.乙烯分子中所有原子都在同一平面上 D.乙烯分子中所有原子都在一条直线上
二、乙烯的化学性质:乙烯分子中含有碳碳双键,使乙烯表现出较活泼的化学性质
1、乙烯的氧化反应实验过程 实验现象
(1)点燃纯净的乙烯,观察燃烧时的现象 火焰明亮且伴有黑烟,同时放出大量的热
(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察
酸性高锰酸钾溶液褪色
现象
(1)与氧气的燃烧反应:CH+3O 2CO +2HO (乙烯中的碳碳键、碳氢键全部破坏)
2 4 2 2 2
①实验现象:火焰明亮且伴有黑烟(比甲烷要明亮),同时放出大量的热
②原因:产生黑烟是因为乙烯中碳的质量分数(85.7%)比较大,燃烧不完全产生的碳的小颗粒造成的;火焰明
亮是由于碳微粒受灼热成炽热状态而发光所致
③乙烯具有可燃性,点燃乙烯之前一定要检验乙烯纯度
(2)乙烯可使酸性高锰酸钾溶液褪色
①反应方程式:5CH =CH+12KMnO +18HSO ―→10CO +12MnSO +6KSO +28HO
2 2 4 2 4 2 4 2 4 2
②反应现象:酸性高锰酸钾溶液紫色褪去
③反应机理:碳碳双键易被酸性高锰酸钾溶液氧化,乙烯被氧化为CO,高锰酸钾溶液被还原为无色的Mn2+
2
④应用:高锰酸钾溶液可用于鉴别乙烷和乙烯,但不能用于除去乙烷中的乙烯
2、乙烯的加成反应
实验过程 实验现象
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现
溴的四氯化碳溶液褪色
象
(1)乙烯与溴的四氯化碳溶液(或溴水)反应的化学方程式:CH ==CH +Br ―→CH Br—CH Br (1,2—二溴乙烷)
2 2 2 2 2
①反应的实质:乙烯分子双键中的一个键易于断裂,两个溴原子分别加在两个价键不饱和碳原子上,生成了
1,2—二溴乙烷
②乙烯与溴加成的机理
③加成反应
a.定义:有机物分子里不饱和的碳原子(碳碳双键或碳碳三键)跟其他原子或原子团直接结合生成新的化合
物的反应,叫做加成反应 (有进无出)
b.特点:断一(断双键中的一个键),加二(加两个原子或原子团),只上不下。像“化合反应”
④乙烯与溴水或溴的CCl 溶液反应现象的比较
4
溴水 溴的CCl 溶液
4
反应现象 褪色,褪色后溶液会分层 褪色,褪色后溶液不分层
鉴别乙烯和乙烷,除去乙烷中的乙烯气体,可以将混合气体通过溴水的洗气瓶,
应用
但不能用溴的四氯化碳溶液,因为乙烷能够溶于四氯化碳溶液中
(2)乙烯与其它加成试剂反应:H、卤化氢、HO、卤素单质
2 2
①乙烯在一定条件下与H 加成:CH ==CH +H CH —CH
2 2 2 2 3 3
②乙烯在一定条件下与HCl加成:CH ==CH +HCl CH CH Cl 制取纯净的氯乙烷
2 2 3 2
③乙烯在一定条件下与HO加成:CH ==CH +HO CH CH OH 制取乙醇
2 2 2 2 3 2
④乙烯在一定条件下与Cl 加成:CH ==CH +Cl ―→CH Cl—CH Cl
2 2 2 2 2 2
3、乙烯的加聚反应:乙烯分子自身发生加成反应
(1)乙烯的加聚反应机理CH===CH +CH===CH +CH===CH +……
2 2 2 2 2 2
—CH—CH—+—CH—CH—+—CH—CH—+…… —CH—CH—CH—CH—CH—CH—……
2 2 2 2 2 2 2 2 2 2 2 2
(2)反应的方程式:nCH ==CH
2 2
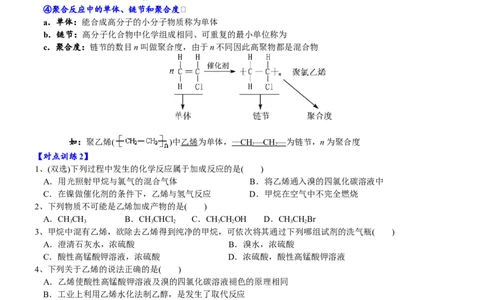
①聚乙烯是一种重要的塑料,如用作食品保鲜膜、水管材料等。生成聚乙烯的这种反应我们称为聚合反应。
由于n的值可能不同,聚合物是混合物
②聚合反应:由相对分子质量小的化合物分子(单体)相互结合成相对分子质量大的聚合物(高分子化合物)的反
应叫聚合反应。由不饱和的相对分子质量小的单体分子以加成反应的形式结合成相对分子质量大的高分子
化合物的反应叫做加成聚合反应,简称加聚反应
③生活中用来包装食品的塑料袋是聚乙烯,如果将乙烯分子中的一个氢原子用氯原子代替,聚合后成为聚氯
乙烯,它就不能用来包装食品了,因为有毒。塑料在高温或长期光照情况下,容易老化,变脆。反应如下:
nCHCl=CH
2
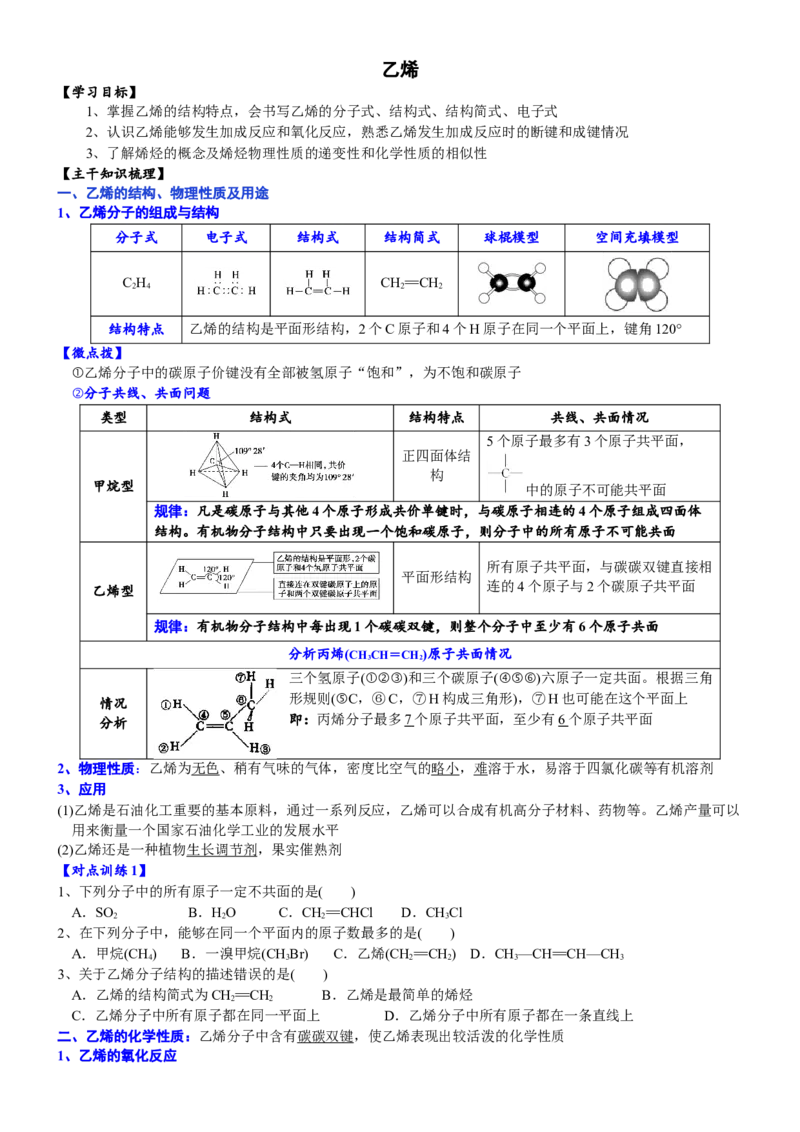
④聚合反应中的单体、链节和聚合度
a.单体:能合成高分子的小分子物质称为单体
b.链节:高分子化合物中化学组成相同、可重复的最小单位称为
c.聚合度:链节的数目n叫做聚合度,由于n不同因此高聚物都是混合物
如:聚乙烯( )中乙烯为单体, — CH —CH—为链节,n为聚合度
2 2
【对点训练2】
1、(双选)下列过程中发生的化学反应属于加成反应的是( )
A.用光照射甲烷与氯气的混合气体 B.将乙烯通入溴的四氯化碳溶液中
C.在镍做催化剂的条件下,乙烯与氢气反应 D.甲烷在空气中不完全燃烧
2、下列物质不可能是乙烯加成产物的是( )
A.CHCH B.CHCHCl C.CHCHOH D.CHCHBr
3 3 3 2 3 2 3 2
3、甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓硫酸 B.溴水,浓硫酸
C.酸性高锰酸钾溶液,浓硫酸 D.浓硫酸,酸性高锰酸钾溶液
4、下列关于乙烯的说法正确的是( )
A.乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色的原理相同
B.工业上利用乙烯水化法制乙醇,是发生了取代反应
C.水果运输中为延长果实成熟期,常在车厢里放置浸泡过酸性KMnO 溶液的硅藻土
4
D.乙烯在空气中燃烧,火焰明亮并带有浓烟、
5、下列反应不属于加成反应的是( )
A.CH==CH+HCl――→CHCHCl B.2CHCH+7O――→4CO+6HO
2 2 3 2 3 3 2 2 2
C. +H――→ D.CH==CH+Br ―→CHBrCHBr
2 2 2 2 2 2
三、烯烃
1、定义:只含有碳和氢两种元素,且碳原子之间有一个或若各干双键的有机物
2、分类
(1)单烯烃:分子中含有一个碳碳双键
(2)多烯烃: 分子中含有两个及以上碳碳双键(3)二烯烃:分子中含有二个碳碳双键。二烯烃又可分为累积二烯烃、孤立二烯烃和共轭二烯烃;累积二烯烃的
结构特点是双键连在一起;共轭二烯烃的结构特点是单、双键交替排列;孤立二烯烃的结构特点是在二个双
键之间相隔二个或二个以上的单键
3、单烯烃:通常所说的烯烃均指单烯烃,简称烯烃。烯烃分子结构与乙烯相似,都有一个C==C,所以烯烃的
通式表示为C H (n≥2),碳氢原子个数比为1∶2
n 2n
4、物理性质 (类似于烷烃)
(1)状态:一般情况下,2~4个碳原子烯烃(烃)为气态,5~16个碳原子为液态,16个碳原子以上为固态
(2)溶解性:烯烃不溶于水,易溶于有机溶剂
(3)熔沸点:随着碳原子数增多,熔沸点增高;分子式相同的烯烃,支链越多,熔沸点越低
(4)密度:随着碳原子数的递增,密度逐渐增加;烯烃的相对密度都小于水的密度
5、烯烃的化学性质:烯烃的结构特征是:C==C,它决定了烯烃的主要化学性质,性质类似于乙烯
(1)氧化反应
①与氧气的燃烧反应:C H +O nCO +nHO
n 2n 2 2 2
②能使酸性KMnO 溶液褪色:将烯烃通入酸性高锰酸钾溶液中会使溶液的颜色变浅直至消失
4
(2)加成反应:(以丙烯为例)
①与溴水加成:CH ==CHCH +Br ―→CH BrCHBrCH (1,2 一二溴丙烷)
2 3 2 2 3
②与H 加成:CH ==CHCH +H CH CH CH (丙烷)
2 2 3 2 3 2 3
③与HCl加成:CH ==CHCH +HCl CH CHClCH (主要)或CH CH CH Cl(次要)
2 3 3 3 3 2 2
马氏规则:凡是不对称结构的烯烃和酸(HX)加成时,酸的负基(X—)主要加到含氢原子较少的双键碳原子上,称
为马尔科夫尼科夫规则,也就是马氏规则 (氢加氢多,卤加氢少)
(3)加聚反应:
①丙烯加聚生成聚丙烯:
②2—丁烯加聚生成聚2—丁烯:
6、二烯烃的化学性质:由于含有双键,二烯烃跟烯烃性质相似,也能发生加成反应、氧化反应和加聚反应
(1)1,3—丁二烯(CH =CHCH=CH )的加成反应
2 2
①CH =CHCH=CH 中有两个双键,与足量溴水反应时,两个双键全部被加成
2 2
CH =CHCH=CH 与溴水1:2加成:CH =CHCH=CH +2Br ―→CH BrCHBrCHBrCH Br
2 2 2 2 2 2 2
②CH =CHCH=CH 中有两个双键,若CH =CHCH=CH 与溴水1:1反应时
2 2 2 2
a.1,2一加成:若两个双键中的一个比较活泼的键断裂,溴原子连接在1、2两个碳原子上
b.1,4一加成:两个双键一起断裂,同时又生成一个新的双键,溴原子连接在1、4两个碳原子上
【1,2-加成和1,4-加成机理】
CH =CH-CH=CH + Br
2 2 21 2 3 4 1 , 2 —加
1 2 3 4
成
Br Br
-80℃ Br Br
1 2 3
4
1 2 3 1 , 4 —加 1 2 3
4 成 4
60℃
Br Br Br Br
【微点拨】一般的,在温度较高的条件下发生1,4-加成,在温度较低的条件下发生1,2-加成)
(2)1,3—丁二烯烃的加聚反应:
(3)天然橡胶的合成:
【对点训练3】
1、由乙烯的结构和性质推测丙烯(CH==CH—CH )的结构或性质正确的是( )
2 3
A.不能使酸性高锰酸钾溶液褪色 B.不能发生加聚反应
C.能使溴的四氯化碳溶液褪色 D.与HCl在一定条件下能加成并只得到一种产物
2、柠檬烯具有良好的镇咳、祛痰、抑菌作用,其结构如图所示。下列关于柠檬烯的说法正确的是( )
A.1 mol柠檬烯只能与1 mol H 反应 B.能发生取代反应和加成反应
2
C.属于乙烯的同系物 D.不能使酸性高锰酸钾溶液褪色
3、不可能是丙烯(CH==CHCH )的加成产物的是( )
2 3
A.CHCHCH B.CHCHCHCl
3 2 3 3 2 2
C.CHCHCHOH D.CHCHCHBr
3 2 2 3 2 2
4、列关于烷烃和烯烃的说法中不正确的是( )
A.它们所含元素的种类相同,但通式不同
B.烷烃分子中所有碳原子不可能在同一平面内,烯烃所有碳原子肯定在同一平面内
C.烯烃分子中的碳原子数≥2,烷烃分子中的碳原子数≥1
D.含碳原子数相同的烯烃和烷烃不互为同分异构体
5、1 mol丙烯与Cl 发生加成反应,得到的产物再与Cl 发生取代反应,两个过程最多消耗Cl 的物质的量为(
2 2 2
)
A.2 mol B.4 mol C.7 mol D.8 mol
6、2-甲基-1,3-丁二烯和等物质的量的溴发生加成反应,其加成产物中二溴代烃有( )
A.一种 B.二种 C.三种 D.四种
7、一种形状像蝴蝶的烯烃分子结构如图所示,有关该分子的说法不正确的是( )
A.该烯烃的分子式为C H B.该分子所有碳原子在同一平面
5 4
C.1 mol该有机物最多可与2 mol Br 发生加成反应 D.可使酸性KMnO 溶液褪色
2 4
四、烷烃与烯烃的比较
烃
烷烃 烯烃
比较项目
概念 碳原子之间全部以单键结合 含有碳碳双键
代表物 CH C H
4 2 4结构简式 CH CH==CH
4 2 2
球棍模型
通式 C H C H (n≥2)
n 2n+2 n 2n
燃烧现象 燃烧火焰较明亮 燃烧火焰明亮,带黑烟
溴水或Br
2 不褪色 褪色
的CCl 溶液
4
通入酸性
不褪色 褪色
KMnO 溶液
4
【对点训练4】
1、下列关于乙烯的叙述中,正确的是( )
A.乙烯的化学性质比乙烷活泼
B.甲烷和乙烯在一定条件下都可以与氯气反应,且反应类型相同
C.乙烯分子中所有原子不可能在同一平面上
D.乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应和取代反应
2、对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )
①二者燃烧时现象完全相同 ②点燃前都应验纯
③甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮,并有大量黑烟生成 ④二者燃烧时都有黑烟生成
A.①② B.③④ C.①④ D.②③
3、既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法是( )
A.与足量溴反应 B.通入足量溴水中
C.在一定条件下通入氢气 D.分别进行燃烧
4、区别CH 和C H 的方法最好是( )
4 2 4
A.比较它们在水中的溶解度大小 B.嗅闻它们的气味
C.通入溴水中观察溶液颜色的变化 D.点燃它们后,观察火焰
5、下列关于乙烯和乙烷的说法中错误的是( )
A.乙烯是不饱和烃,乙烷是饱和烃
B.乙烯分子中的两个碳原子在同一条直线上,乙烷分子中的两个碳原子也在同一条直线上
C.乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键键能的两倍,因此乙烯比乙烷稳定
D.乙烯分子为平面结构,乙烷分子为立体结构
【课后作业】
1、长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
2、为了防止番茄在长途运输过程中发生腐烂,常常运输尚未完全成熟的果实,运到目的地后再用一种植物生长调
节剂将其催熟。这种植物生长调节剂是下列物质中的( )
A.乙烷 B.苯 C.乙烯 D.酒精
3、下列过程中发生了加成反应的是( )
A.C H 使酸性高锰酸钾溶液褪色 B.C H 使溴的CCl 溶液褪色
2 4 2 4 4
C.C H 燃烧生成二氧化碳和水 D.CH 和Cl 的混合气体在光照条件下逐渐褪色
2 4 4 2
4、下列分子中的各原子均在同一平面上的是( )
A.C H B.CHCl C.CHCH==CH D.CH—CH
2 4 3 3 2 3 3
5、下列关于乙烯的结构与性质的叙述,错误的是( )
A.乙烯分子中6个原子都在同一平面内 B.乙烯与酸性KMnO 溶液发生加成反应能使其褪色
4C.乙烯分子没有同分异构体 D.乙烯分子的一氯代物只有一种结构
6、下列说法中,错误的是( )
A.无论乙烯与Br 的加成,还是乙烯使酸性KMnO 溶液褪色,都与分子内含有碳碳双键有关
2 4
B.用溴的四氯化碳溶液或酸性KMnO 溶液都可以鉴别乙烯和乙烷
4
C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
7、(双选)下列过程中发生了加成反应的是( )
A.C H 使酸性高锰酸钾溶液褪色 B.C H 使溴的CCl 溶液褪色
2 4 2 4 4
C.C H 与H 在一定条件下反应 D.CH 和Cl 的混合气体在光照条件下逐渐褪色
2 4 2 4 2
8、制取一氯乙烷最好采用的方法是( )
A.乙烷和氯气反应 B.乙烯和氯气反应
C.乙烯和氯化氢反应 D.乙烯和氢气反应后再和氯气反应
9、下列说法中错误的是( )
A.无论乙烯的加成,还是乙烯使酸性KMnO 溶液褪色,都与分子内含有碳碳双键有关
4
B.无论使用溴的四氯化碳溶液或酸性KMnO 溶液都可以鉴别乙烯和乙烷
4
C.相同质量的乙烯和甲烷完全燃烧后,产生的水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
10、1 mol 乙烯与Cl 完全加成,再与Cl 发生最大程度的取代,两个过程共需Cl( )
2 2 2
A.3 mol B.4 mol C.5 mol D.6 mol
11、将15 g CH 和C H 的混合气体通入盛有足量溴水的容器中,溴水的质量增加了 7 g,则混合气体中CH 和
4 2 4 4
C H 的体积之比为( )
2 4
A.1:2 B.2:1 C.3:2 D.2:3
12、把m mol C H 跟n mol H 混合于密闭容器中,在一定条件下发生反应,生成p mol C H(p<m),若将反应后
2 4 2 2 6
的混合气体点燃,完全燃烧生成CO 和HO时,需要O 的物质的量为( )
2 2 2
A.(3m+n)mol B.(3m+n/2)mol C.(3m+3p+n/2)mol D.(3m+n/2-3p)mol
13、如下图是某种有机物分子的球棍模型图。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同
的短周期元素的原子。对该有机物的叙述不正确的是( )
A.该有机物可能的分子式为C HCl B.该有机物的分子中一定有
2 3
C.该有机物分子中的所有原子在同一平面上 D.该有机物可以由乙烯和氯化氢加成反应得到
14、有关乙烯的下列叙述:①乙烯溶于水后可得乙醇 ②乙烯能发生加聚反应 ③乙烯能与溴水发生加成反应
④乙烯是无色、稍有气味、难溶于水的气体;其中正确的是( )
A.只有② B.①和③ C.②和③ D.②③④
15、下列关于乙烯分子的叙述中错误的是( )
A.乙烯分子中所有原子都在同一平面上 B.CHCH==CH 分子中所有原子都在同一平面上
3 2
C.乙烯分子中碳氢键之间的夹角为120° D.乙烯分子中既有极性键又有非极性键
16、刚摘的猕猴桃往往青涩难吃,但将熟透的红苹果与它共同装入袋内,三天后就香甜可口了,原因是熟透的
苹果挥发出的乙烯对猕猴桃起了催熟作用。下列有关乙烯的说法中不正确的是( )
A.乙烯分子为平面结构,分子中C—H键之间的键角约为120°
B.乙烯与溴发生加成反应后的产物中所有原子都共平面
C.乙烯的产量常用来衡量一个国家石油化工水平的标志
D.乙烯是一种植物生长的调节剂,也可作水果催熟剂
17、甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓HSO B.溴水,浓HSO
2 4 2 4
C.酸性高锰酸钾溶液,浓HSO D.浓HSO ,酸性高锰酸钾溶液
2 4 2 4
18、下列烯烃和HBr发生加成反应所得的产物有两种的是( )A. B. C. D.
19、Ⅰ.如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为CHCHOH――→CH===CH ↑+
3 2 2 2
HO,回答下列问题:
2
(1)图1中仪器①、②的名称分别为______________、______________。
(2)收集乙烯气体最好的方法是_________________________________________________。
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应属于________(填反应类型),反应的
化学方程式为______________________________________________。
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上
述混合气体中有乙烯和二氧化硫。试回答下列问题:
(1)图中①、②、③、④装置盛放的试剂是下列中的:①________;②________;③________;④________
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明二氧化硫气体存在的现象是_________________________________________
(3)使用装置②的目的是____________________________________________________
(4)使用装置③的目的是___________________________________________________
(5)确认含有乙烯的现象是_________________________________________________
20、足球比赛中当运动员肌肉挫伤或扭伤时,队医会迅速对运动员的受伤部位喷射一种药剂——氯乙烷(沸点为
12.27 ℃)进行局部冷冻麻醉应急处理。
(1)氯乙烷用于冷冻麻醉应急处理的原因是____________________________
(2)制取CHCHCl最好的方法是________
3 2
A.乙烷与氯气反应 B.乙烯与氯气反应
C.乙烷与HCl反应 D.乙烯与HCl反应
(3)选择上述方法的理由是_______________________________________________________________________;
制取发生反应的化学方程式为______________________________________
【乙烯】答案
【对点训练1】
1、D
2、D。解析:甲烷是正四面体结构,在一个平面上最多含有3个原子;一溴甲烷分子是甲烷分子中的1个氢原
子被溴原子取代产生的,在一个平面上最多有 3个原子;乙烯分子是平面分子,分子中6个原子在同一个平面
上;2个甲基取代乙烯分子中的2个氢原子,甲基中的碳原子以及该碳原子上的1个氢原子与乙烯面共平面,最
多有8个原子在同一个平面内,D正确。
3、D
【对点训练2】
1、BC
2、B。解析:做这种类型的题时,一定要抓住加成反应的特点:“断一加二,从哪里断,从哪里加”,所以
CH===CH 加成应该是每个碳原子上加一个原子或原子团,所以加成后每个碳原子上至少有两个氢原子,B选
2 2
项不符合。3、B。解析:应把乙烯直接吸收或转化为CO 才能提纯甲烷。方法一:混合气体通过溴水吸收C H ,然后用浓
2 2 4
硫酸干燥CH;方法二:混合气体通过酸性高锰酸钾溶液,然后用澄清石灰水(或NaOH溶液)吸收CO,最后用
4 2
浓硫酸干燥CH。
4
4、C。解析:乙烯使酸性高锰酸钾溶液褪色是发生氧化反应,使溴的四氯化碳溶液褪色是发生加成反应,原理
不同,A错误;乙烯水化法制取乙醇,发生了加成反应,B错误;乙烯是果实的催熟剂,能被酸性高锰酸钾溶
液氧化,所以可以用酸性高锰酸钾溶液除去乙烯,以延长果实成熟期,C正确;乙烯燃烧时火焰明亮,伴有黑
烟,D错误。
5、B
【对点训练3】
1、C。解析:因含 ,故丙烯能使酸性KMnO 溶液褪色,能与Br 、HCl加成,能发生加聚反应,丙烯
4 2
与HCl加成可能得到两种产物。
2、B。解析:A项,1 mol柠檬烯能与2 mol H 发生加成反应,错误;B项,柠檬烯能与气态卤素单质在光照条
2
件下发生取代反应,分子中含有碳碳双键,能与 H 发生加成反应,正确;C项,一个柠檬烯分子中有两个碳碳
2
双键,且分子中含有环状结构,与乙烯的结构不相同,故其不属于乙烯的同系物,错误;D项,柠檬烯分子中
含有碳碳双键,能使酸性高锰酸钾溶液褪色,错误。
3、B。解析:A项,丙烯与氢气的加成产物是CHCHCH ;B项,CHCHCHCl 不可能是丙烯的加成产物;C
3 2 3 3 2 2
项,CHCHCHOH是丙烯与水的加成产物;D项,CHCHCHBr是丙烯与HBr的加成产物。
3 2 2 3 2 2
4、B。解析:烷烃的通式为C H ,烯烃的通式为C H ;烷烃分子中碳原子呈锯齿状,有可能在同一平面内,
n 2n+2 n 2n
烯烃分子中有可能含有烷基碳原子,烷基碳原子呈四面体结构,所有烯烃中碳原子不一定在同一平面内;烯烃
含有碳碳双键,至少含有2个碳原子,乙烯是最简单的烯烃,甲烷是最简单的烷烃,烷烃最少有1个C;含碳
原子数相同的烯烃和烷烃分子式不同,不可能互为同分异构体。
5、C。解析:1 mol丙烯与Cl 发生加成反应需要1 mol Cl ,生成的CHCHCl—CH Cl中含有6 mol H原子,与
2 2 3 2
Cl 发生取代反应,又需要消耗6 mol Cl ,共计7 mol Cl 。
2 2 2
6、C。解析: 与Br 等物质的量反应,若发生1,2-加成反应,生成BrCHC(CH)BrCH===CH ,若发生
2 2 3 2
1,4-加成反应,生成BrCHC(CH)===CHCHBr,若发生3,4-加成反应,生成CH===C(CH )CHBrCH Br,二溴代
2 3 2 2 3 2
烃有3种。
7、B。解析:由图可知该烃的分子式为C H ,中心碳原子连有4个单键,空间构型类似于甲烷,是四面体结构,
5 4
所有碳原子不可能共平面;由于有 2个双键的存在,1 mol该烃最多可与2 mol Br 发生加成反应,可使酸性
2
KMnO 溶液褪色,故选B。
4
【对点训练4】
1、A。解析:由乙烯可使酸性高锰酸钾溶液褪色而乙烷不能,可知乙烯比乙烷活泼,A正确;甲烷和氯气发生
取代反应,而乙烯和氯气发生加成反应,B项不正确;乙烯分子中所有原子在同一平面上,C项不正确;乙烯
分子的碳碳双键中的一个键易断裂,易发生加成反应,而不易发生取代反应, D不正确。
2、D。解析:甲烷和乙烯燃烧现象不同,①错;可燃性气体点燃前都要验纯,②对;甲烷燃烧无黑烟,④错、
③对。
3、B。解析:乙烷和乙烯均是无色气体,但前者易发生取代反应,后者易发生加成反应,若与足量溴作用,乙
烷可以发生取代反应而生成溴代乙烷,乙烯发生加成反应生成二溴乙烷,不仅不易鉴别,还会损失大量的乙烷
且混入大量的溴蒸气杂质,不合理;若在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易
控制,很难得到纯净的乙烷;若分别进行燃烧,无法再得到乙烷;因此只能选B,因为乙烷不和溴水反应,而
乙烯能和溴水发生加成反应而使溴水褪色,且生成的CHBr—CHBr为液体。
2 2
4、C。解析:甲烷不能使溴水褪色,而乙烯可以,因此答案选C。
5、C。解析:A项,乙烯含有碳碳双键,属于不饱和烃,乙烷属于饱和烃,正确;B项,两点决定一条直线,
所以分子中的两个碳原子一定在同一条直线上,正确;C项,乙烯分子中碳碳双键键能小于乙烷分子中碳碳单
键键能的两倍,因此乙烯结构不稳定,导致乙烯能和溴水发生加成反应,错误;D项,甲烷是正四面体结构,
所以乙烷中所有原子不可能在同一平面上;乙烯为平面结构,所有原子都处在同一平面上,正确。
【课后作业】
1、A。解析:水果释放出的乙烯是催熟剂,用KMnO 溶液来吸收乙烯,防止水果早熟。
42、C。解析:乙烷、乙炔均为气体,酒精为液体,三者均不具有催熟作用,只有乙烯是植物体内能够产生的一
种气体激素,是一种植物生长调节剂,能促进果实成熟。
3、B。解析:C H 与酸性高锰酸钾溶液发生氧化反应,A错误;C H 与溴发生加成反应,B正确;C H 燃烧属于氧化
2 4 2 4 2 4
反应,C错误;CH 和Cl 在光照下发生取代反应,D错误。
4 2
4、A。解析:乙烯分子是一种平面结构,2个碳原子和4个氢原子在同一平面上。因为CH 是正四面体结构,所以
4
只要含有—CH 结构的分子就不可能满足所有原子在同一平面上。
3
5、B。解析:乙烯分子为平面结构,6个原子都在同一平面内,A正确;乙烯与酸性KMnO 溶液反应,是乙烯
4
被酸性KMnO 氧化,而不是发生加成反应,B错误;乙烯分子只有两个碳原子,没有同分异构体,C正确;乙
4
烯分子中四个氢原子都是等效的,任何一个被取代所得一氯代物都相同,D正确。
6、C。解析:本题考查乙烯的性质。乙烯分子中含有碳碳双键,决定了它的性质与甲烷、乙烷等烷烃的性质有
所不同。乙烯的加成反应和氧化反应过程中碳碳双键断裂,A对;乙烯能与溴水和酸性KMnO 溶液反应,但是
4
乙烷不能,故能用溴的四氯化碳溶液或酸性KMnO 溶液鉴别乙烯和乙烷,B对;乙烯和甲烷中氢的质量分数不
4
同,故相同质量的乙烯和甲烷完全燃烧后产生的水的质量不同,C错;甲烷燃烧产生淡蓝色火焰,乙烯燃烧火
焰明亮有黑烟,D对。
7、BC。解析:A项,酸性高锰酸钾溶液与C H 发生氧化反应;B项,C H 与溴发生加成反应;C项,C H 与
2 4 2 4 2 4
H 在一定条件下反应生成乙烷;D项,属于取代反应。
2
8、C。解析:乙烯和氯化氢反应的唯一产物是一氯乙烷,没有副产物。
9、C。解析:乙烯的加成反应和氧化反应过程中碳碳双键断裂,A项正确;乙烯能与溴的四氯化碳溶液和酸性
高锰酸钾溶液反应,但是乙烷不能,故能用溴的四氯化碳溶液或酸性KMnO 溶液鉴别乙烯和乙烷,B项正确;
4
乙烯和甲烷中氢的质量分数不同,故相同质量的乙烯和甲烷完全燃烧后产生的水的质量不同,C项错误;乙烯
分子中含有碳碳双键,化学性质比乙烷活泼,D项正确。
10、C
11、B。解析:烷烃不能与溴水反应,乙烯可与Br 发生加成反应,因此,溴水质量增加是因为吸收了乙烯,故
2
乙烯的物质的量为=0.25 mol,则甲烷的物质的量为=0.5 mol,相同条件下气体体积之比等于其物质的量之比,
即CH 与C H 的体积之比为21。
4 2 4
12、B。解析:m mol C H 完全燃烧消耗O 为m(2+)mol=3m mol,n mol H 完全燃烧消耗O 为 mol;m mol
2 4 2 2 2
C H 和n mol H 发生反应后的生成物和剩余的反应物的耗氧量都与m mol C H 和n mol H 的耗氧量相同,B项
2 4 2 2 4 2
正确。
13、D。解析:由该分子的球棍模型可看出,碳碳之间成双键,结合 CH===CH 分子结构特点可推断A、B、C
2 2
正确。
14、D。解析:乙烯需在一定条件下与水加成才能得到乙醇。
15、B。解析:CHCH===CH 的空间结构为 ,共面原子最多为7个。
3 2
16、B。解析:乙烯分子中的6个原子共平面,但与溴发生加成反应后生成BrCHCHBr(1,2二溴乙烷),其结
2 2
构相当于乙烷分子中的两个H原子(位于不同的碳原子上)被Br原子代替,每个碳原子与其相连的4个原子构成
四面体结构,1,2二溴乙烷中的8个原子不共平面。
17、B。解析:应把乙烯转化为CO 或直接吸收才能提纯甲烷。方法一:混合气体通过溴水吸收 C H ,然后用
2 2 4
浓HSO 干燥CH ;方法二:混合气体通过酸性高锰酸钾溶液,然后用澄清石灰水(或NaOH溶液)吸收CO ,最
2 4 4 2
后用浓HSO 干燥CH。
2 4 4
18、D。解析: 与HBr发生加成反应的产物有CHCHCHCHBr和CHCHCHBrCH 两种,D
3 2 2 2 3 2 3
项正确。
19、 Ⅰ.(1)温度计 烧瓶(或圆底烧瓶) (2)排水集气法 (3)加成反应 CH ==CH +Br ―→CH BrCH Br
2 2 2 2 2
Ⅱ.(1)A B A D
(2)装置①中的品红溶液褪色
(3)除去SO 气体,以免干扰乙烯的检验
2
(4)检验SO 是否已被除尽
2(5)装置③中的品红溶液不褪色,装置④中的酸性KMnO 溶液褪色
4
20、(1)氯乙烷的沸点较低,易挥发而吸收热量,使局部冷冻麻醉
(2)D
(3)烷烃的卤代反应是分步进行的,而且反应很难停留在一元取代阶段,所以得到的产物往往是混合物;而
用乙烯和HCl反应只有一种加成产物,所以可以得到相对纯净的产物 CH ===CH +HCl――→CH —
2 2 3
CH Cl
2
解析:为制得纯净的氯乙烷,应用乙烯与HCl的加成反应,而不宜用乙烷与Cl 的取代反应。因为乙烯与HCl
2
的加成产物只有一种,而乙烷与Cl 的取代产物是多种氯代烷的混合物。
2