文档内容
乐山市2019年初中学业水平考试化学试题
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 S—32 Cl—35.5 Fe—56 Cu—64
一、选择题(本大题共14个小题,每题2.5分,共35分,每小题只有一个正确选项。)
1.我们生活在不断变化的物质世界,下列变化只发生了物理变化的是( )
A.米饭在人体中消化成葡萄糖 B.熟石灰改良酸性土壤
C.将矿石研磨成粉末 D.用醋酸清洗水壶中的水垢
【解析】米饭在人体中消化成葡萄糖、熟石灰改良酸性土壤和用醋酸清洗水壶中的水垢均在
发生变化过程中产生新的物质,属于化学变化;将矿石研磨成粉末只是矿石的状态发生变化,
没有生成新的物质,属于物理变化。故选C。
【答案】C
2.“我是碳族的大女儿,让大地充满生机,让地球因我而温暖;我调皮可爱,钻进石灰水,
搅得人家不安宁;我藏在汽水里,小朋友喝了直打嗝。”这里叙述中的“我”是指( )
A.二氧化碳 B.氧气 C.氮气 D.稀有气体
【解析】二氧化碳属于碳的氧化物,可以引起温室效应,使澄清石灰水变浑浊,可以用来制汽
水。故选A。
【答案】A
3.下列物质属于纯净物的是( )
A.浑浊河水 B.番茄蛋汤 C.石蕊溶液 D.液态氢
【解析】浑浊河水、番茄蛋汤、石蕊溶液均属于混合物;液态氢是单质,属于纯净物。故选D。
【答案】D
4.下列物质的用途利用了物质的化学性质的是( )
A.活性炭除去房间中的异味 B. 用煤、石油、天然气作燃料
C.干冰用于冷藏食品 D.用铜或铝制作导线
【解析】活性炭具有吸附性可以除去房间中的异味,利用碳的物理性质;煤、石油、天然气具有
可燃性,可以用作燃料,利用物质的化学性质;干冰升华可以吸收热量,降低温度,可以用于
冷藏食品,利用干冰的物理性质;铜或铝具有导电性,可以用于制作导线,利用金属的物理性
质。故选B。
【答案】B
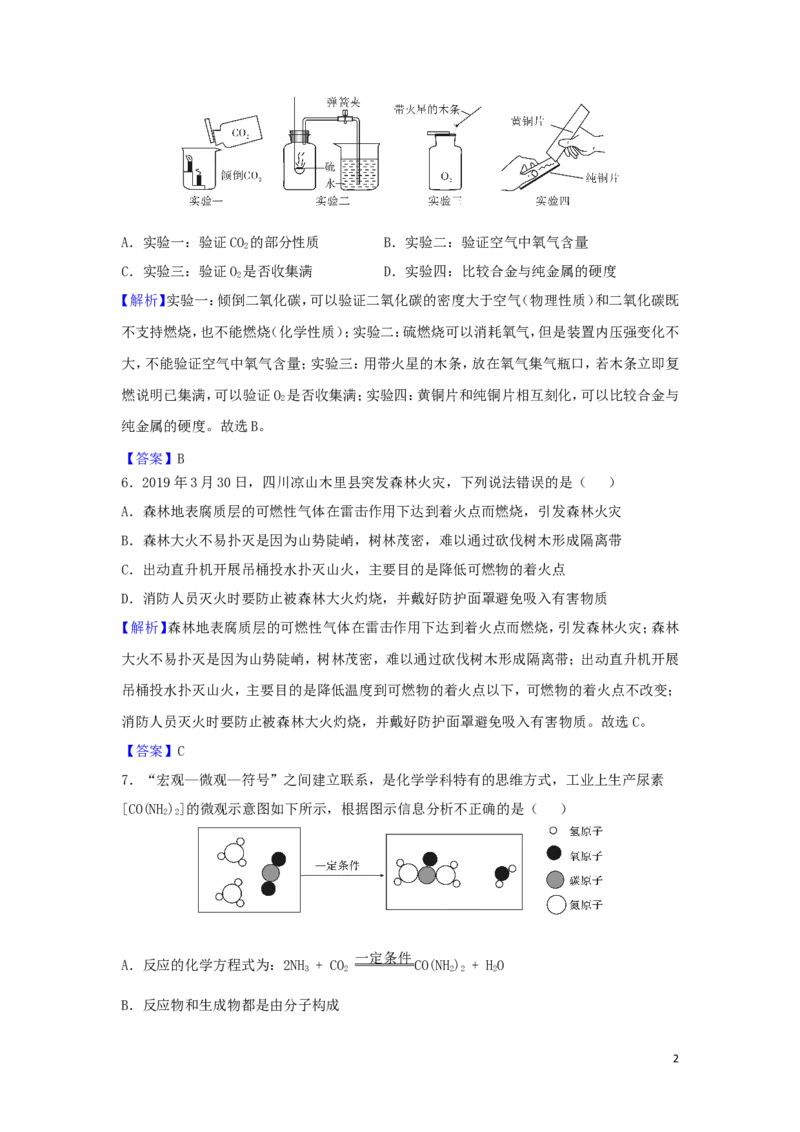
5.下图所示的实验不能达到实验目的的是( )
1A.实验一:验证CO 的部分性质 B.实验二:验证空气中氧气含量
2
C.实验三:验证O 是否收集满 D.实验四:比较合金与纯金属的硬度
2
【解析】实验一:倾倒二氧化碳,可以验证二氧化碳的密度大于空气(物理性质)和二氧化碳既
不支持燃烧,也不能燃烧(化学性质);实验二:硫燃烧可以消耗氧气,但是装置内压强变化不
大,不能验证空气中氧气含量;实验三:用带火星的木条,放在氧气集气瓶口,若木条立即复
燃说明已集满,可以验证O 是否收集满;实验四:黄铜片和纯铜片相互刻化,可以比较合金与
2
纯金属的硬度。故选B。
【答案】B
6.2019年3月30日,四川凉山木里县突发森林火灾,下列说法错误的是( )
A.森林地表腐质层的可燃性气体在雷击作用下达到着火点而燃烧,引发森林火灾
B.森林大火不易扑灭是因为山势陡峭,树林茂密,难以通过砍伐树木形成隔离带
C.出动直升机开展吊桶投水扑灭山火,主要目的是降低可燃物的着火点
D.消防人员灭火时要防止被森林大火灼烧,并戴好防护面罩避免吸入有害物质
【解析】森林地表腐质层的可燃性气体在雷击作用下达到着火点而燃烧,引发森林火灾;森林
大火不易扑灭是因为山势陡峭,树林茂密,难以通过砍伐树木形成隔离带;出动直升机开展
吊桶投水扑灭山火,主要目的是降低温度到可燃物的着火点以下,可燃物的着火点不改变;
消防人员灭火时要防止被森林大火灼烧,并戴好防护面罩避免吸入有害物质。故选C。
【答案】C
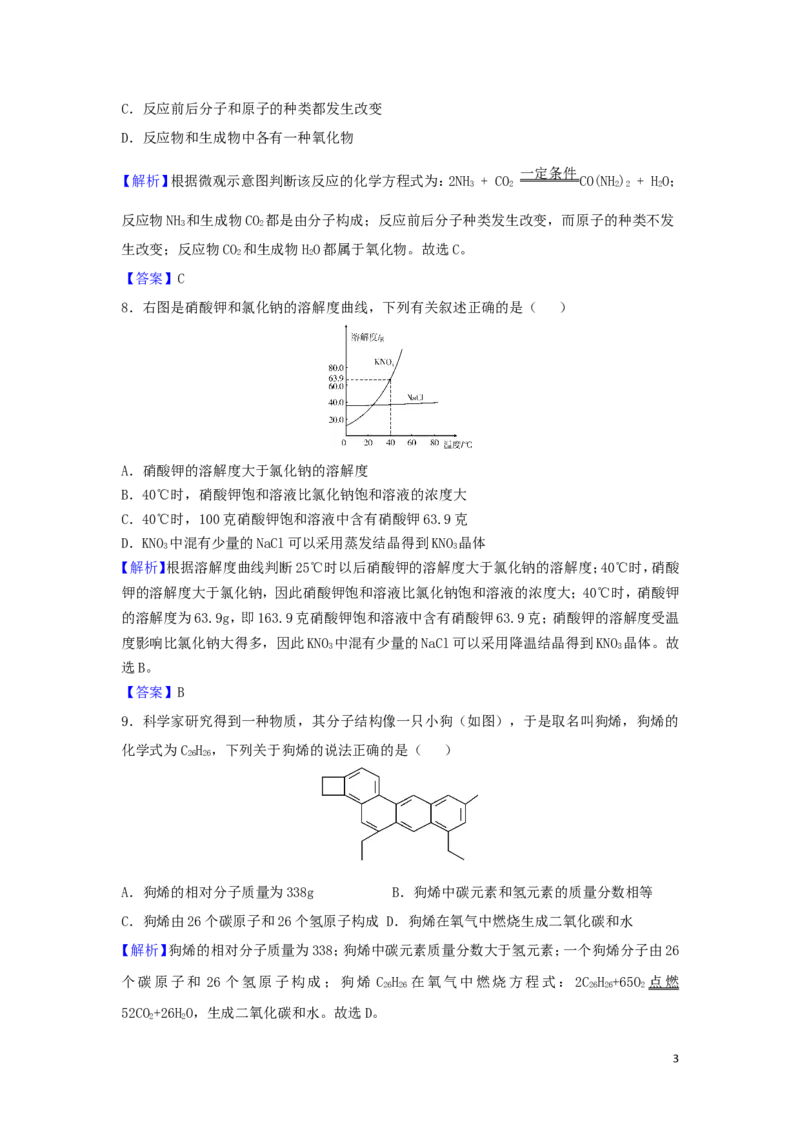
7.“宏观—微观—符号”之间建立联系,是化学学科特有的思维方式,工业上生产尿素
[CO(NH)]的微观示意图如下所示,根据图示信息分析不正确的是( )
2 2
一定条件
A.反应的化学方程式为:2NH + CO CO(NH) + HO
3 2 2 2 2
B.反应物和生成物都是由分子构成
2C.反应前后分子和原子的种类都发生改变
D.反应物和生成物中各有一种氧化物
一定条件
【解析】根据微观示意图判断该反应的化学方程式为:2NH + CO CO(NH) + HO;
3 2 2 2 2
反应物NH 和生成物CO 都是由分子构成;反应前后分子种类发生改变,而原子的种类不发
3 2
生改变;反应物CO 和生成物HO都属于氧化物。故选C。
2 2
【答案】C
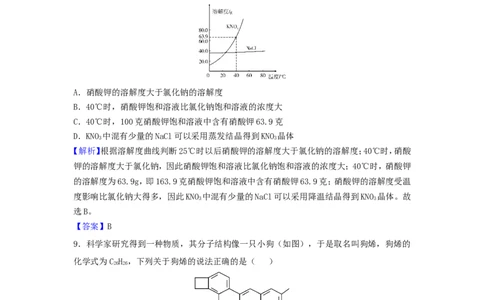
8.右图是硝酸钾和氯化钠的溶解度曲线,下列有关叙述正确的是( )
A.硝酸钾的溶解度大于氯化钠的溶解度
B.40℃时,硝酸钾饱和溶液比氯化钠饱和溶液的浓度大
C.40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克
D.KNO 中混有少量的NaCl可以采用蒸发结晶得到KNO 晶体
3 3
【解析】根据溶解度曲线判断25℃时以后硝酸钾的溶解度大于氯化钠的溶解度;40℃时,硝酸
钾的溶解度大于氯化钠,因此硝酸钾饱和溶液比氯化钠饱和溶液的浓度大;40℃时,硝酸钾
的溶解度为63.9g,即163.9克硝酸钾饱和溶液中含有硝酸钾63.9克;硝酸钾的溶解度受温
度影响比氯化钠大得多,因此KNO 中混有少量的NaCl可以采用降温结晶得到KNO 晶体。故
3 3
选B。
【答案】B
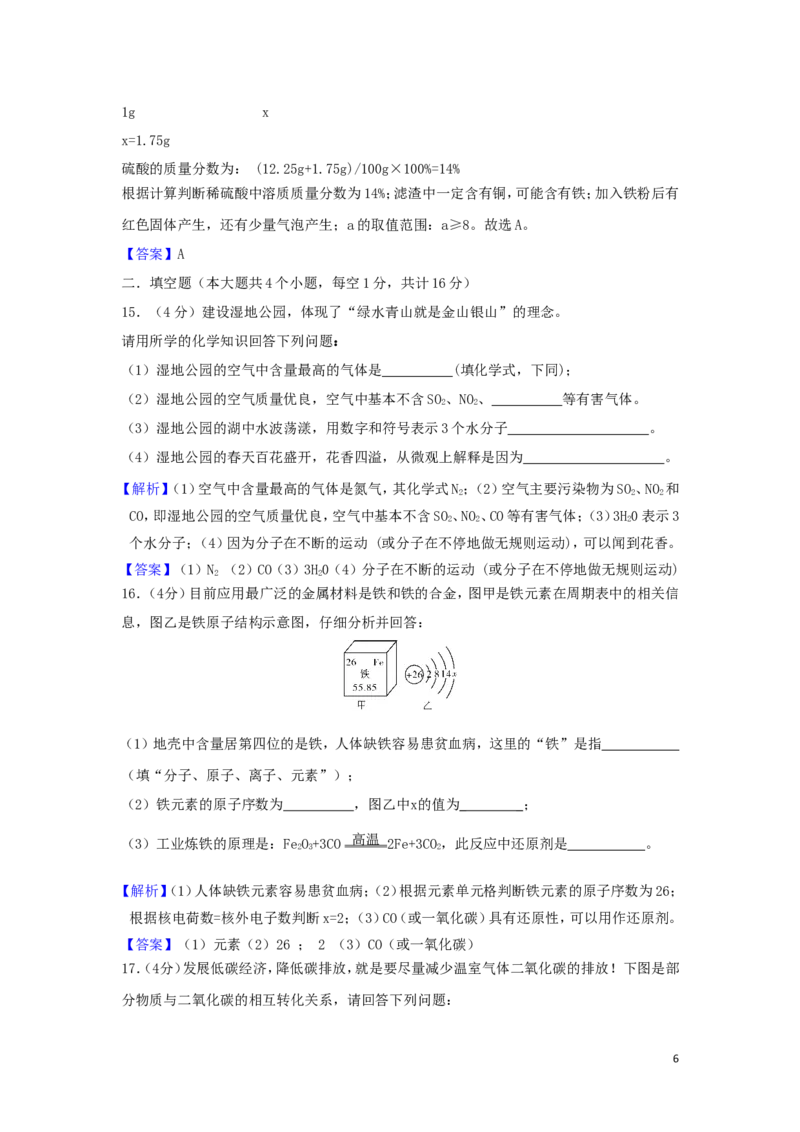
9.科学家研究得到一种物质,其分子结构像一只小狗(如图),于是取名叫狗烯,狗烯的
化学式为C H ,下列关于狗烯的说法正确的是( )
26 26
A.狗烯的相对分子质量为338g B.狗烯中碳元素和氢元素的质量分数相等
C.狗烯由26个碳原子和26个氢原子构成 D.狗烯在氧气中燃烧生成二氧化碳和水
【解析】狗烯的相对分子质量为338;狗烯中碳元素质量分数大于氢元素;一个狗烯分子由26
个碳原子和 26 个氢原子构成;狗烯 C H 在氧气中燃烧方程式:2C H +65O 点燃
26 26 26 26 2
52CO+26HO,生成二氧化碳和水。故选D。
2 2
3【答案】D
10.下列实验方案合理可行的是( )
选项 实验目的 所用试剂或操作方法
A 鉴别稀盐酸、NaCO溶液和蒸馏水 分别滴加无色酚酞溶液,观察颜色
2 3
B 除去生石灰中少量的碳酸钙 加水溶解,过滤
将铜片分别放入到Zn(NO)溶液、
3 2
C 验证Zn、Cu、Ag的金属活动性
AgNO溶液中,观察现象
3
D 除去CO中混有少量的HCl气体 将气体通入足量的NaOH溶液
2
【解析】鉴别稀盐酸、NaCO溶液和蒸馏水,分别滴加无色酚酞溶液,变红的是NaCO溶液,再
2 3 2 3
分别向NaCO溶液滴加其他两种物质,产生气泡的是稀盐酸,另一种是蒸馏水,分别滴加无色
2 3
酚酞溶液,观察颜色,不能鉴别这三种物质;生石灰溶于水且与水反应,加水溶解不能除去生
石灰中少量的碳酸钙;将铜片分别放入到Zn(NO)溶液、AgNO溶液中,Zn(NO)溶液中无现象,
3 2 3 3 2
说明Zn比Cu活泼,AgNO溶液中出现银白色固体,说明Cu比Ag活泼,即三者活泼性:Zn>Cu>Ag,
3
可以验证Zn、Cu、Ag的金属活动性;CO和HCl都与NaOH溶液反应,不能除去CO中混有少量的
2 2
HCl气体。故选C。
【答案】C
11.证据推理是化学学科核心素养的重要内容,下列推理正确的是( )
A.化合物由不同种元素组成,因此含有不同种元素的物质一定是化合物
B.物质与氧气发生反应都会放出热量,因此放热反应都是氧化反应
C.金刚石和石墨都是由碳元素组成,因此金刚石和石墨的性质都相同
D.铜在空气中久置后表面生成铜绿[Cu(OH)CO] ,说明铜的锈蚀可能与空气中的氧气、水
2 2 3
蒸气和二氧化碳有关
【解析】化合物由不同种元素组成,因此含有不同种元素的纯净物一定是化合物;物质与氧
气发生反应都会放出热量,因此放热反应不一定都是氧化反应,如生石灰与水反应放热,不
属于氧化反应;金刚石和石墨都是由碳元素组成,因此金刚石和石墨的化学性质都相同,因
它们碳原子排列方式不同,物理性质差异很大;根据铜绿[Cu(OH)CO]化学式判断铜的锈蚀
2 2 3
可能与空气中的氧气、水。故选D。
【答案】D
12.下列物质之间的转化,只通过一步反应不能实现的是( )
A.FeO →FeCl B.KMnO → MnO C.CO → CO D.CuSO → Cu(OH)
2 3 2 4 2 2 4 2
【解析】FeO →FeCl→FeCl 需要两部反应才能实现;2KMnO 加热 KMnO+MnO +O ↑,一步
2 3 3 2, 4 4 2 2
反应实现;CO+O 加热 2CO,一步反应实现;CuSO+2NaOH=Cu(OH) ↓+ NaSO,一步反
2 2 4 2 2 4
4应实现。故选A。
【答案】A
13.甲、乙、丙、丁分别为1~18号元素中的一种,且核电荷数依次增大,甲的单质是一种
最理想的燃料,乙原子的最外层电子数是电子层数的3倍,丙的离子带一个单位的正电
荷,丁与乙的原子最外层电子数相同。下列有关说法错误的是( )
A.甲和乙元素组成的物质分解能得到氧气B.丙和丁的原子在化学反应中都容易失去电子
C.甲、乙、丙三种元素能组成一种碱 D.丁的单质在乙的单质中燃烧,产生蓝紫色火焰
【解析】根据甲的单质是一种最理想的燃料判断甲为氢气,根据乙原子的最外层电子数是电
子层数的3倍判断乙为氧原子,根据丙的离子带一个单位的正电荷判断丙为钠离子,根据甲、
乙、丙、丁分别为1~18号元素中的一种,且核电荷数依次增大且丁与乙的原子最外层电子
数相同判断丁为硫元素。甲和乙元素组成的物质为水或双氧水分解都能得到氧气;丙的原子
在化学反应中容易失去电子,丁的原子在化学反应中容易得到电子;甲、乙、丙三种元素能组
成一种碱NaOH;硫在氧气中燃烧,产生明亮的蓝紫色火焰。故选B。
【答案】B
14.将10g氧化铜粉末加入到100g一定质量分数的稀硫酸中,微热到氧化铜全部溶解,再向
溶液中加入ag铁粉,使溶液中的溶质完全反应后,过滤,将滤渣在低温下烘干,得到干燥固
体质量仍然为ag,下列分析不正确的是( )
A.稀硫酸中溶质质量分数为12.25% B. 滤渣中一定含有铜,可能含有铁
C. 加入铁粉后有红色固体产生,还有少量气泡产生 D. a的取值范围:a≥8
【解析】设与10g CuO 反应的HSO 的质量为x ,消耗的铁的质量为 y ,生成Cu 的质量为z
2 4
。
CuO ~ HSO ~ Fe ~ Cu
2 4
80 98 56
64
10g
x y z
80/10g=98/x,x= 12. 25g
80/10g=56/y,y =7g
80/10g=64/z,z= 8g
因为生成铜为8g,即a=8g ,那么加入的铁粉也应是8g ,与稀HSO 反应的铁粉的质量
2 4
为8g -7g =1g
Fe + HSO FeSO+ H ↑
2 4 4 2
56 98
51g x
x=1.75g
硫酸的质量分数为: (12.25g+1.75g)/100g×100%=14%
根据计算判断稀硫酸中溶质质量分数为14%;滤渣中一定含有铜,可能含有铁;加入铁粉后有
红色固体产生,还有少量气泡产生;a的取值范围:a≥8。故选A。
【答案】A
二.填空题(本大题共4个小题,每空1分,共计16分)
15.(4分)建设湿地公园,体现了“绿水青山就是金山银山”的理念。
请用所学的化学知识回答下列问题:
(1)湿地公园的空气中含量最高的气体是 (填化学式,下同);
(2)湿地公园的空气质量优良,空气中基本不含SO、NO、 等有害气体。
2 2
(3)湿地公园的湖中水波荡漾,用数字和符号表示3个水分子 。
(4)湿地公园的春天百花盛开,花香四溢,从微观上解释是因为 。
【解析】(1)空气中含量最高的气体是氮气,其化学式N;(2)空气主要污染物为SO、NO 和
2 2 2
CO,即湿地公园的空气质量优良,空气中基本不含SO、NO、CO等有害气体;(3)3H0表示3
2 2 2
个水分子;(4)因为分子在不断的运动 (或分子在不停地做无规则运动),可以闻到花香。
【答案】(1)N (2)CO(3)3H0(4)分子在不断的运动 (或分子在不停地做无规则运动)
2 2
16.(4分)目前应用最广泛的金属材料是铁和铁的合金,图甲是铁元素在周期表中的相关信
息,图乙是铁原子结构示意图,仔细分析并回答:
(1)地壳中含量居第四位的是铁,人体缺铁容易患贫血病,这里的“铁”是指
(填“分子、原子、离子、元素” );
(2)铁元素的原子序数为 ,图乙中x的值为_ _;
高温
(3)工业炼铁的原理是:FeO+3CO 2Fe+3CO,此反应中还原剂是_ 。
2 3 2
【解析】(1)人体缺铁元素容易患贫血病;(2)根据元素单元格判断铁元素的原子序数为26;
根据核电荷数=核外电子数判断x=2;(3)CO(或一氧化碳)具有还原性,可以用作还原剂。
【答案】(1)元素(2)26 ; 2 (3)CO(或一氧化碳)
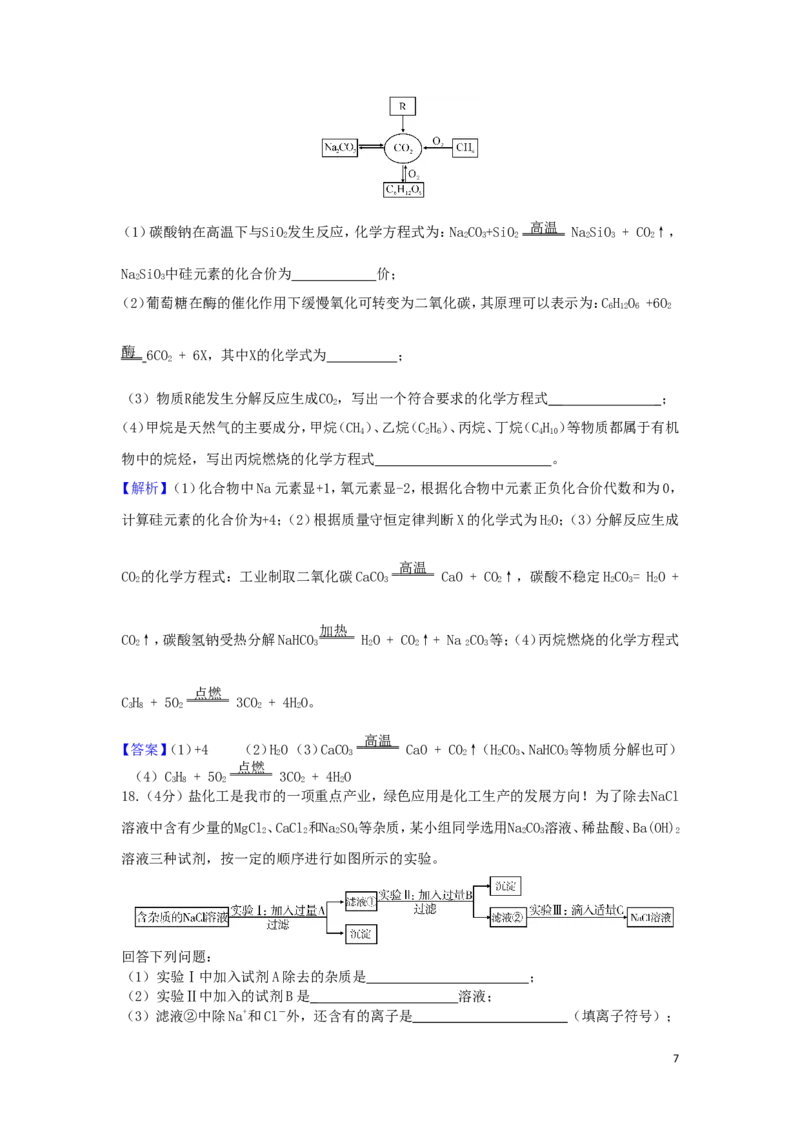
17.(4分)发展低碳经济,降低碳排放,就是要尽量减少温室气体二氧化碳的排放!下图是部
分物质与二氧化碳的相互转化关系,请回答下列问题:
6高温
(1)碳酸钠在高温下与SiO发生反应,化学方程式为:NaCO+SiO NaSiO + CO↑,
2 2 3 2 2 3 2
NaSiO中硅元素的化合价为_ _价;
2 3
(2)葡萄糖在酶的催化作用下缓慢氧化可转变为二氧化碳,其原理可以表示为:CH O +6O
6 12 6 2
酶 6CO + 6X,其中X的化学式为 ;
2
(3)物质R能发生分解反应生成CO,写出一个符合要求的化学方程式__ _;
2
(4)甲烷是天然气的主要成分,甲烷(CH)、乙烷(CH)、丙烷、丁烷(CH )等物质都属于有机
4 2 6 4 10
物中的烷烃,写出丙烷燃烧的化学方程式 。
【解析】(1)化合物中Na元素显+1,氧元素显-2,根据化合物中元素正负化合价代数和为0,
计算硅元素的化合价为+4;(2)根据质量守恒定律判断X的化学式为HO;(3)分解反应生成
2
高温
CO 的化学方程式:工业制取二氧化碳CaCO CaO + CO↑,碳酸不稳定HCO= HO +
2 3 2 2 3 2
加热
CO↑,碳酸氢钠受热分解NaHCO HO + CO↑+ Na CO 等;(4)丙烷燃烧的化学方程式
2 3 2 2 2 3
点燃
CH + 5O 3CO + 4HO。
3 8 2 2 2
高温
【答案】(1)+4 (2)HO (3)CaCO CaO + CO↑(HCO、NaHCO 等物质分解也可)
2 3 2 2 3 3
点燃
(4)CH + 5O 3CO + 4HO
3 8 2 2 2
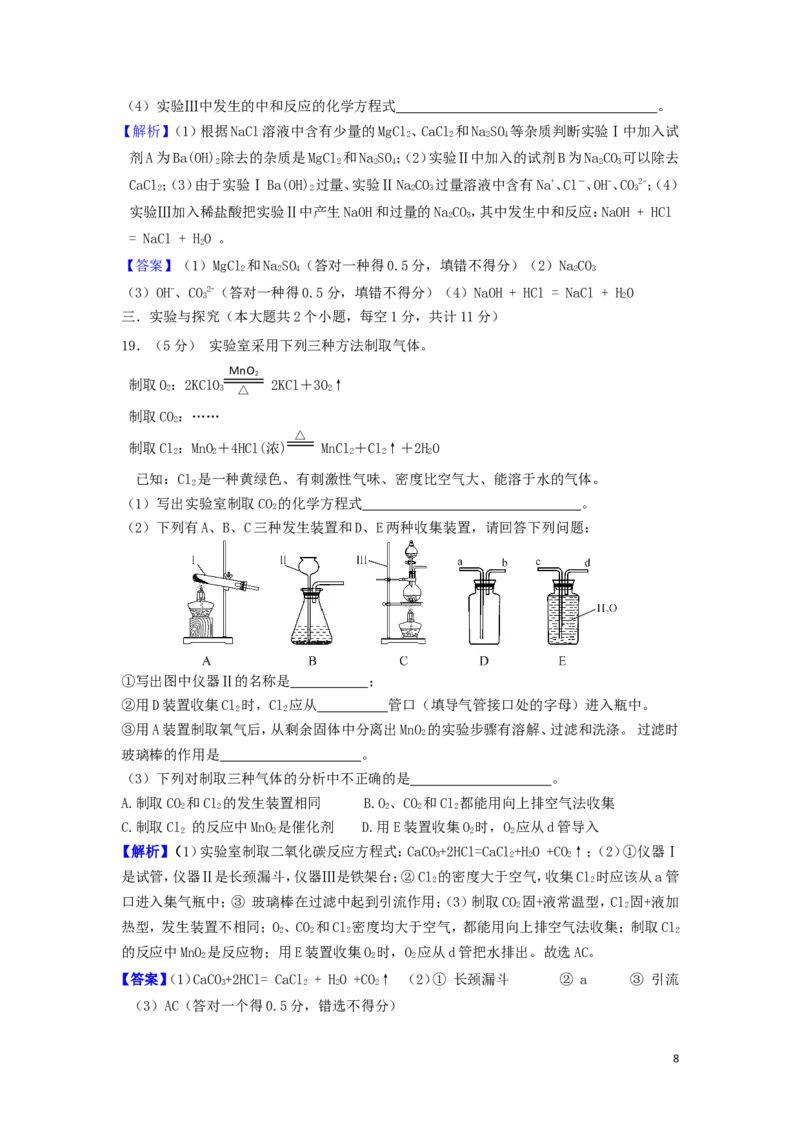
18.(4分)盐化工是我市的一项重点产业,绿色应用是化工生产的发展方向!为了除去NaCl
溶液中含有少量的MgCl、CaCl和NaSO等杂质,某小组同学选用NaCO溶液、稀盐酸、Ba(OH)
2 2 2 4 2 3 2
溶液三种试剂,按一定的顺序进行如图所示的实验。
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是 _;
(2)实验Ⅱ中加入的试剂B是_ 溶液;
(3)滤液②中除Na+和Cl-外,还含有的离子是_ _(填离子符号);
7(4)实验Ⅲ中发生的中和反应的化学方程式_ _。
【解析】(1)根据NaCl溶液中含有少量的MgCl、CaCl 和NaSO 等杂质判断实验Ⅰ中加入试
2 2 2 4
剂A为Ba(OH) 除去的杂质是MgCl 和NaSO;(2)实验Ⅱ中加入的试剂B为NaCO 可以除去
2 2 2 4 2 3
CaCl;(3)由于实验ⅠBa(OH) 过量、实验ⅡNaCO 过量溶液中含有Na+、Cl-、OH-、CO2-;(4)
2 2 2 3 3
实验Ⅲ加入稀盐酸把实验Ⅱ中产生NaOH和过量的NaCO,其中发生中和反应:NaOH + HCl
2 3
= NaCl + HO 。
2
【答案】(1)MgCl 和NaSO(答对一种得0.5分,填错不得分)(2)NaCO
2 2 4 2 3
(3)OH-、CO2-(答对一种得0.5分,填错不得分)(4)NaOH + HCl = NaCl + HO
3 2
三.实验与探究(本大题共2个小题,每空1分,共计11分)
19.(5分) 实验室采用下列三种方法制取气体。
MnO
2
制取O:2KClO 2KCl+3O↑
2 3 △ 2
制取CO:……
2
△
制取Cl:MnO+4HCl(浓) MnCl+Cl↑+2HO
2 2 2 2 2
已知:Cl 是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
2
(1)写出实验室制取CO 的化学方程式 。
2
(2)下列有A、B、C三种发生装置和D、E两种收集装置,请回答下列问题:
①写出图中仪器Ⅱ的名称是 ;
②用D装置收集Cl 时,Cl 应从 管口(填导气管接口处的字母)进入瓶中。
2 2
③用A装置制取氧气后,从剩余固体中分离出MnO 的实验步骤有溶解、过滤和洗涤。 过滤时
2
玻璃棒的作用是 。
(3)下列对制取三种气体的分析中不正确的是 。
A.制取CO 和Cl 的发生装置相同 B.O、CO 和Cl 都能用向上排空气法收集
2 2 2 2 2
C.制取Cl 的反应中MnO 是催化剂 D.用E装置收集O 时,O 应从d管导入
2 2 2 2
【解析】(1)实验室制取二氧化碳反应方程式:CaCO+2HCl=CaCl+HO +CO↑;(2)①仪器Ⅰ
3 2 2 2
是试管,仪器Ⅱ是长颈漏斗,仪器Ⅲ是铁架台;②Cl 的密度大于空气,收集Cl 时应该从a管
2 2
口进入集气瓶中;③ 玻璃棒在过滤中起到引流作用;(3)制取CO 固+液常温型,Cl 固+液加
2 2
热型,发生装置不相同;O、CO 和Cl 密度均大于空气,都能用向上排空气法收集;制取Cl
2 2 2 2
的反应中MnO 是反应物;用E装置收集O 时,O 应从d管把水排出。故选AC。
2 2 2
【答案】(1)CaCO+2HCl= CaCl + HO +CO↑ (2)① 长颈漏斗 ② a ③ 引流
3 2 2 2
(3)AC(答对一个得0.5分,错选不得分)
820.(6分)蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤,课外小组同学决定对蚁酸进行
探究。
【查阅资料】1.蚁酸化学名称叫甲酸,化学式为HCOOH
2.蚁酸在一定条件下会分解生成两种氧化物
3.白色无水硫酸铜粉末遇水变蓝
【提出问题】蚁酸的酸碱性及分解产物是什么?
【猜想与假设】 猜想①:蚁酸的分解产物是水和二氧化碳;
猜想②:蚁酸的分解产物是水和一氧化碳;
猜想③:蚁酸的分解产物是一氧化碳和二氧化碳。
经讨论,小组同学认为猜想③是错误的,理由是 。
【实验探究】 1.探究蚁酸的酸碱性。
用pH试纸测得蚁酸溶液的pH值 7(填“>、<或=”),证明蚁酸溶液呈酸性。
2.探究蚁酸分解的两种产物。
为了确认蚁酸分解的所有产物,小组同学设计实验,将蚁酸分解的产物通入下图所示的实验
装置,并观察现象。
【现象与结论】实验中观察到A中无水硫酸铜变蓝,B中澄清石灰水未变浑浊,D中黑色粉末
逐渐变红,E中澄清的石灰水变浑浊。
(1)写出E中发生的反应的化学方程式 ;
(2)通过对实验现象的分析,上述猜想 正确。
【实验反思】(3)从环保的角度考虑,上述实验装置设计上存在的不足之处是
。
【拓展应用】(4)人们被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒,下列物质中你会选
择的物质是 。A.NaOH溶液 B.食醋 C.食盐水 D.肥皂水
【解析】【猜想与假设】甲酸中含碳、氢元素,分解产物是碳、氢元素,猜想三甲酸的分解产物
生成物中不含氢元素,不符合质量守恒定律;【实验探究】酸性溶液pH<7;(1)二氧化碳通
入澄清石灰水反应方程式:Ca(OH)+CO =CaCO↓+ HO;(2)A中无水硫酸铜变蓝,说明有水
2 2 3 2
生成,B中澄清石灰水未变浑浊,说明没有二氧化碳生成,D中黑色粉末逐渐变红,E中澄清
的石灰水变浑浊,说明有一氧化碳生成。故猜想②正确;(3)一氧化碳有毒,该实验缺少尾
气处理装置(或未进行尾气处理);(4)根据酸碱中和原理判断被蚊虫叮咬后,在叮咬处涂抹
一些碱性物质可减轻痛痒,但不能选择强碱,强碱的腐蚀性强,可以选择肥皂水弱碱性物质。
故选D。
【答案】【猜想与假设】甲酸中含氢元素,而生成物中不含氢元素,不符合质量守恒定律(或不
符合质量守恒定律)
9【实验探究】 <7;(1)Ca(OH)+CO =CaCO↓+ HO(2)②;(3)缺少尾气处理装置(或未进行
2 2 3 2
尾气处理) ;(4)D。
四.计算题(本大题共1个小题,共8分)
21.(8分)生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%~4.3%,钢中碳的含
量为 0.03%~2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在
烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示:
烧杯质量 样品的质量 稀盐酸的质量 烧杯+剩余物的总质量
50g 5.8g 94.6g 150.2g
注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为 g;
(2)样品中碳的质量分数 (计算结果保留到0.1%);
(3)反应后得到的溶液中溶质的质量分数(计算结果保留到0.1%)。
【解析】(1)恰好完全反应时,生成氢气的质量:50g+5.8g+94.6g-150.2g=0.2g … (2分)
(2)解:设样品中铁的质量 x,生成FeCl 的质量为y
2
Fe+2HCl=FeCl+H↑ ……(1分)
2 2
56 127 2
x y 0.2g
56 x
2 0.2g
解得: ………(1分)
x5.6g
127 y
2 0.2g
解得: ……(1分)
y 12.7g
铁合金中碳的质量分数=
5.8g5.6g
3.4 ……(2分)
100%
5.8g
(3)反应后所得溶液中FeCl 的质量分数:
2
12.7g
12.7% ………(1分)
100%
5.6g94.6g0.2g
答:(1)生成氢气的质量是0.2g;(2)样品中碳的质量分数为3.4%;(3)反应后所得溶液中
FeCl 的质量分数12.7%。
2
10【答案】(1)0.2 ;(2)3.4%;(3)12.7%。
1112