文档内容
2024 年中考第一次模拟考试(南京卷)
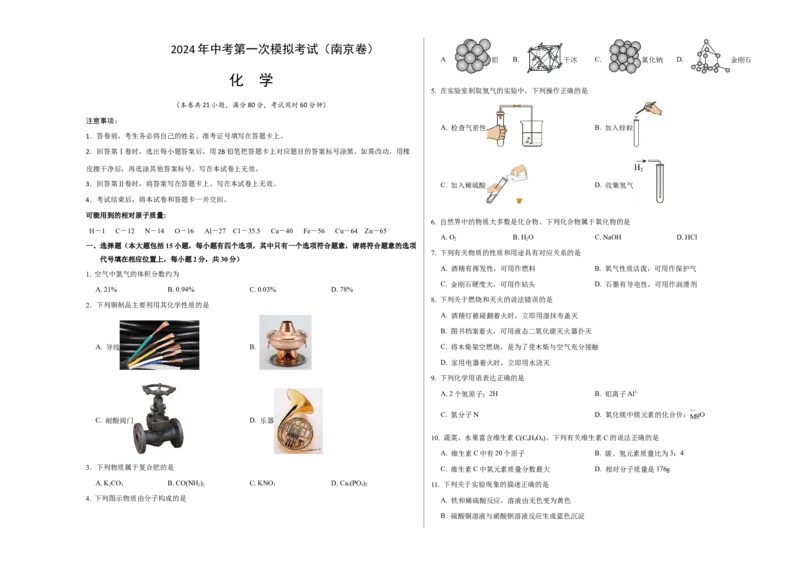
A 铝 B. 干冰 C. 氯化钠 D. 金刚石
.
化 学
5. 在实验室制取氢气的实验中,下列操作正确的是
(本卷共21小题,满分80分,考试用时60分钟)
注意事项:
A. 检查气密性 B. 加入锌粒
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。 C. 加入稀硫酸 D. 收集氢气
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
6. 自然界中的物质大多数是化合物。下列化合物属于氧化物的是
H-1 C-12 N-14 O-16 Al-27 C1-35.5 Ca-40 Fe-56 Cu-64 Zn-65
A. O B. HO C. NaOH D. HCl
2 2
一、选择题(本大题包括15小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的选项
7. 下列有关物质的性质和用途具有对应关系的是
代号填在相应位置上,每小题2分,共30分)
A. 酒精有挥发性,可用作燃料 B. 氧气性质活泼,可用作保护气
1. 空气中氮气的体积分数约为
C. 金刚石硬度大,可用作钻头 D. 石墨有导电性,可用作润滑剂
A. 21% B. 0.94% C. 0.03% D. 78%
8. 下列关于燃烧和灭火的说法错误的是
2.下列铜制品主要利用其化学性质的是
A. 酒精灯被碰翻着火时,立即用湿抹布盖灭
B. 图书档案着火,可用液态二氧化碳灭火器扑灭
A. 导线 B. C. 将木柴架空燃烧,是为了使木柴与空气充分接触
D. 家用电器着火时,立即用水浇灭
9. 下列化学用语表达正确的是
A. 2个氢原子:2H B. 铝离子Al3-
2+
C. 氮分子N D. 氧化镁中镁元素的化合价:MgO
C. 耐酸阀门 D. 乐器
10. 蔬菜、水果富含维生素C(C HO)。下列有关维生素C的说法正确的是
6 8 6
A. 维生素C中有20个原子 B. 碳、氢元素质量比为3:4
3.下列物质属于复合肥的是 C. 维生素C中氧元素质量分数最大 D. 相对分子质量是176g
A. K 2 CO 3 B. CO(NH 2 ) 2 C. KNO 3 D. Ca 3 (PO 4 ) 2 11. 下列关于实验现象的描述正确的是
4. 下列图示物质由分子构成的是 A. 铁和稀硫酸反应,溶液由无色变为黄色
B. 硫酸铜溶液与硝酸钡溶液反应生成蓝色沉淀………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
C. 滴有酚酞试液的蒸馏水中加入Fe(OH) 固体,溶液变红色 二、填空与说明题(本大题包括4小题,化学方程式2分,其余每空1分,共24分)
3
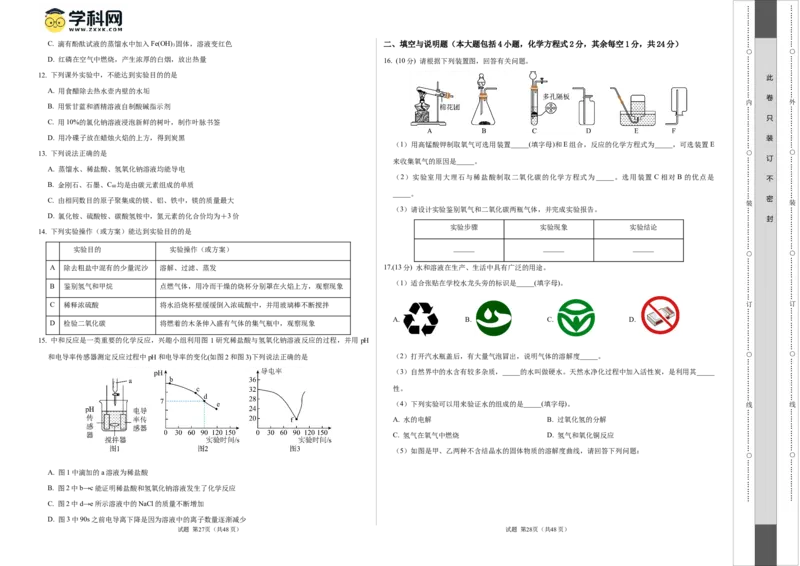
D. 红磷在空气中燃烧,产生浓厚的白烟,放出热量 16. (10分) 请根据下列装置图,回答有关问题。
12. 下列课外实验中,不能达到实验目的的是
此
A. 用食醋除去热水壶内壁的水垢
卷
B. 用紫甘蓝和酒精溶液自制酸碱指示剂
只
C. 用10%的氯化钠溶液浸泡新鲜的树叶,制作叶脉书签
D. 用冷碟子放在蜡烛火焰的上方,得到炭黑 装
(1)用高锰酸钾制取氧气可选用装置_____(填字母)和E组合,反应的化学方程式为_____,可选装置E
13. 下列说法正确的是
订 来收集氧气的原因是_____。
A. 蒸馏水、稀盐酸、氢氧化钠溶液均能导电
(2)实验室用大理石与稀盐酸制取二氧化碳的化学方程式为_____。选用装置 C相对 B的优点是
不
B. 金刚石、石墨、C 均是由碳元素组成的单质
60
_____。
C. 由相同数目的原子聚集成的镁、铝、铁中,镁的质量最大 密
(3)请设计实验鉴别氧气和二氧化碳两瓶气体,并完成实验报告。
D. 氯化铵、硫酸铵、碳酸氢铵中,氮元素的化合价均为+3价
封
实验步骤 实验现象 实验结论
14. 下列实验操作(或方案)能达到实验目的的是
实验目的 实验操作(或方案) ______ ______ ______
A 除去粗盐中混有的少量泥沙 溶解、过滤、蒸发 17.(13分) 水和溶液在生产、生活中具有广泛的用途。
(1)适合张贴在学校水龙头旁的标识是_____(填字母)。
B 鉴别氢气和甲烷 点燃气体,用冷而干燥的烧杯分别罩在火焰上方,观察现象
C 稀释浓硫酸 将水沿烧杯壁缓缓倒入浓硫酸中,并用玻璃棒不断搅拌
A. B. C. D.
D 检验二氧化碳 将燃着的木条伸入盛有气体的集气瓶中,观察现象
15. 中和反应是一类重要的化学反应,兴趣小组利用图 1研究稀盐酸与氢氧化钠溶液反应的过程,并用 pH
和电导率传感器测定反应过程中pH和电导率的变化(如图2和图3)下列说法正确的是 (2)打开汽水瓶盖后,有大量气泡冒出,说明气体的溶解度_____。
(3)自然界中的水含有较多杂质,_____的水叫做硬水。天然水净化过程中加入活性炭,是利用其_____
性。
(4)下列实验可以用来验证水的组成的是_____(填字母)。
A. 水的电解 B. 过氧化氢的分解
C. 氢气在氧气中燃烧 D. 氢气和氧化铜反应
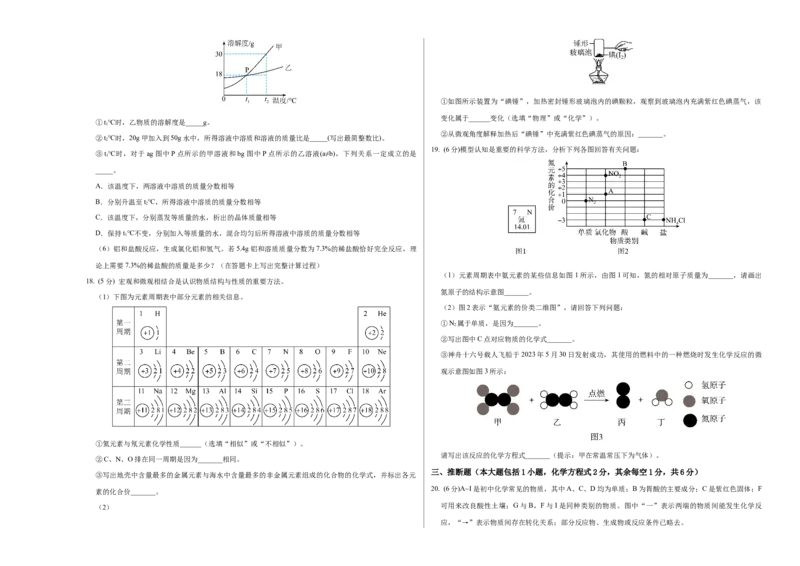
(5)如图是甲、乙两种不含结晶水的固体物质的溶解度曲线,请回答下列问题:
A. 图1中滴加的a溶液为稀盐酸
B. 图2中b→c能证明稀盐酸和氢氧化钠溶液发生了化学反应
C. 图2中d→e所示溶液中的NaCl的质量不断增加
D. 图3中90s之前电导离下降是因为溶液中的离子数量逐渐减少
试题 第27页(共48页) 试题 第28页(共48页)①如图所示装置为“碘锤”,加热密封锤形玻璃泡内的碘颗粒,观察到玻璃泡内充满紫红色碘蒸气,该
变化属于______变化(选填“物理”或“化学”)。
①t℃时,乙物质的溶解度是_____g。
1
②从微观角度解释加热后“碘锤”中充满紫红色碘蒸气的原因:_______。
②t℃时,20g甲加入到50g水中,所得溶液中溶质和溶液的质量比是_____(写出最简整数比)。
2
19. (6分)模型认知是重要的科学方法,分析下列各图回答有关问题:
③t℃时,对于ag图中P点所示的甲溶液和bg图中P点所示的乙溶液(a≠b),下列关系一定成立的是
1
_____。
A.该温度下,两溶液中溶质的质量分数相等
B.分别升温至t℃,所得溶液中溶质的质量分数相等
2
C.该温度下,分别蒸发等质量的水,析出的晶体质量相等
D.保持t℃不变,分别加入等质量的水,混合均匀后所得溶液中溶质的质量分数相等
1
(6)铝和盐酸反应,生成氯化铝和氢气。若5.4g铝和溶质质量分数为7.3%的稀盐酸恰好完全反应,理
论上需要7.3%的稀盐酸的质量是多少?(在答题卡上写出完整计算过程)
(1)元素周期表中氨元素的某些信息如图1所示,由图1可知,氮的相对原子质量为_______,请画出
18. (5分) 宏观和微观相结合是认识物质结构与性质的重要方法。
氮原子的结构示意图_______。
(1)下图为元素周期表中部分元素的相关信息。
(2)图2表示“氨元素的价类二维图”,请回答下列问题:
①N 属于单质,是因为_______。
2
②写出图中C点对应物质的化学式_______。
③神舟十六号载人飞船于2023年5月30日发射成功,其使用的燃料中的一种燃烧时发生化学反应的微
观示意图如图3所示:
①氦元素与氖元素化学性质______(选填“相似”或“不相似”)。
请写出该反应的化学方程式_______(提示:甲在常温常压下为气体)。
②C、N、O排在同一周期是因为_______相同。
三、推断题(本大题包括1小题,化学方程式2分,其余每空1分,共6分)
③写出地壳中含量最多的金属元素与海水中含量最多的非金属元素组成的化合物的化学式,并标出各元
20. (6分)A~I是初中化学常见的物质,其中A、C、D均为单质;B为胃酸的主要成分;C是紫红色固体;F
素的化合价_______。
(2) 可用来改良酸性土壤;G与B,F与I是同种类别的物质。图中“一”表示两端的物质间能发生化学反
应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
( 4 ) “ 还 原 ” 发 生 的 反 应 为 Fe (SO )+Fe═3FeSO ; “ 沉 淀 ” 反 应 的 化 学 方 程 式 为
2 4 3 4
2FeSO +H O+2H O═2FeOOH↓+2H SO 。“沉淀”时会有部分FeOOH与FeSO 反应生成Fe O ,反应的
4 2 2 2 2 4 4 3 4
化学方程式为________。 此
(三)FeOOH的含量测定
卷
已知:FeOOH及铁的氧化物加热分解的温度如下。
只
FeOOH Fe OFe OFeO
2 3 3 4
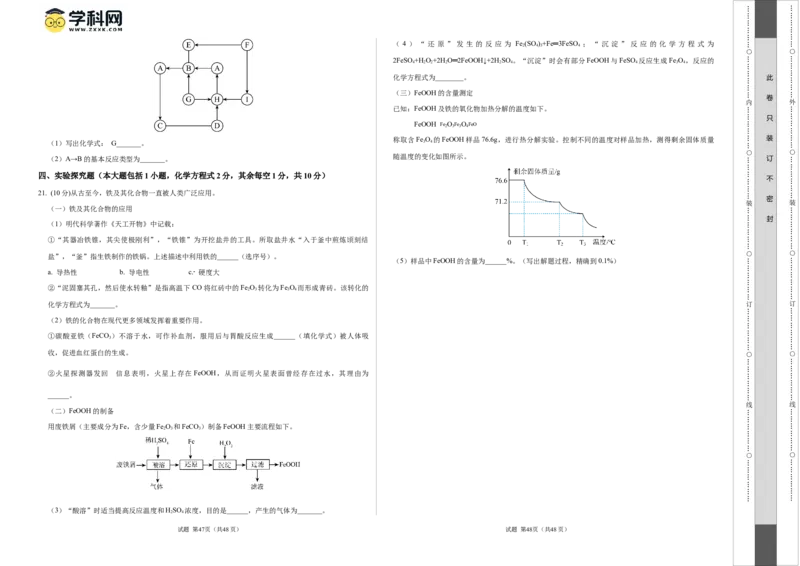
称取含Fe O 的FeOOH样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量 装
(1)写出化学式: G_______。 3 4
随温度的变化如图所示。
(2)A→B的基本反应类型为_______。 订
四、实验探究题(本大题包括1小题,化学方程式2分,其余每空1分,共10分)
不
21. (10分)从古至今,铁及其化合物一直被人类广泛应用。
密
(一)铁及其化合物的应用
封
(1)明代科学著作《天工开物》中记载:
①“其器冶铁锥,其尖使极刚利”,“铁锥”为开挖盐井的工具。所取盐井水“入于釜中煎炼顷刻结
盐”,“釜”指生铁制作的铁锅。上述描述中利用铁的______(选序号)。
(5)样品中FeOOH的含量为______%。(写出解题过程,精确到0.1%)
a. 导热性 b. 导电性 c. 硬度大
②“泥固塞其孔,然后使水转釉”是指高温下 CO将红砖中的Fe O 转化为Fe O 而形成青砖。该转化的
2 3 3 4
化学方程式为_______。
(2)铁的化合物在现代更多领域发挥着重要作用。
①碳酸亚铁(FeCO )不溶于水,可作补血剂,服用后与胃酸反应生成______(填化学式)被人体吸
3
收,促进血红蛋白的生成。
的
②火星探测器发回 信息表明,火星上存在 FeOOH,从而证明火星表面曾经存在过水,其理由为
______。
(二)FeOOH的制备
用废铁屑(主要成分为Fe,含少量Fe O 和FeCO)制备FeOOH主要流程如下。
2 3 3
(3)“酸溶”时适当提高反应温度和HSO 浓度,目的是______,产生的气体为_______。
2 4
试题 第47页(共48页) 试题 第48页(共48页)