文档内容
2026年03⽉20⽇ 4.某化合物A 除在有机合成中有⼴泛应⽤外,还可⽤于聚合引发剂、抗癌药和脑肿瘤的中⼦俘获疗
2026年⾼中毕业年级第⼀次质量检测 法,其结构如下图所示。V、W、X、Y、Z均为原⼦序数依次递增的短周期元素,原⼦半径⼤⼩为Y>Z
>V>X,W、Y基态原⼦电⼦排布中未成对电⼦数相同。下列说法错误的是
化学 A.电负性:X>W>V
B. 最⾼价氧化物的⽔化物酸性:Z>W>V
注意事项: C. VZg、XZ, 空间构型均为平⾯三⻆形
1.答卷前,考⽣务必将⾃⼰的姓名、考⽣号等填写在答题卡上。 D.该结构中所有原⼦均满⾜8电⼦稳定结构
2.回答选择题时,选出每⼩题答案后,⽤铅笔把答题卡上对应题⽬的答案标号涂⿊。如需改动,⽤橡 5.某种合成神经肽抑制剂重要中间体的结构如下图所示。关于该有机物分⼦的说法正确的是
⽪擦⼲净后,再选涂其他答案标号。回答⾮选择题时,将答案写在答题卡上。写在本试卷上⽆效。 A. 分⼦式为Ci,HlB:N,Os
3.考试结束后,将本试卷和答题卡⼀并交回。 B. 官能团种类为3种 Fgl
4. 可能⽤到的相对原⼦质量:H1 C12 016Na 23
C. 能发⽣取代、⽔解、还原、消去等反应
D.⼀定条件下,1 mol该物质最多能与S mol NaOH 发⽣反应
⼀,选择题(本题包括14⼩题,每⼩题3分,共42分。每⼩题只有⼀个选项符合题意)
6. 下列⽅程式错误的是
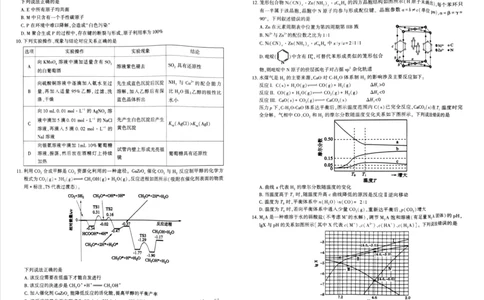
1.⽂物是历史的“时光胶囊”,凝聚着古⼈的智慧与审美。下列⽂物的主要成分为合⾦材料的是
A.⽤氢氟酸雕刻玻璃:Si0,+4 +4F SiF.T+21,0
B. 少量灼热的 CuO 加⼊ CHI, CH, OH 中:CUO + CH, CH,OHf-、 Cu + CH, CHO + H,O
C. NaHSO。 和 Ba(OH),恰好沉淀完全:H+ S0%+ Ba"+ OHf-__ Ba50g + +H,0
D.绿矾(FeSO。 • 7H,0)处理酸性废⽔中的CI20:6Fe~*+CI0 + 14H*—6Fe+2C_ +7H,0
A. “⽗⼄”带盖铜⻆ B.“千秋万岁”画像砖 C. 庙底沟彩陶盆 D.贾湖⻣笛
7.钠离⼦电池具有造价低、安全性能⾼、低温环境下放电稳定等优点,在⼤规模储能领域应⽤前景⼴泛。
外电源或⽤电器
2.下列有关化学⽤语表示错误的是 ⼀种钠离⼦电池的⼯作原理为 NaMO,+C放电 Na-MOat Na,Cn,
A.基态 Br 原⼦简化电⼦排布式:[Ar]3d"4s°4p” 装置如右图所示。下列说法正确的是
A.M可为Ca、Co、Ni 元素
B. ⽔分⼦的 VSEPR 模型: B.放电时,M的化合价降低,Na“嵌⼈负极
C. 充电时,阳极反应为NaMO,-xe—Na-,MO,+ xNa*
Na,MO,电板 Na,C.电极
CH, D.充电时,外电路转移 4 mol e,理论上阴极增重92g
C.亚克⼒(+CH, C-⼠。 )的单体存在顺反异构现象 8.能满⾜下列物质间直接转化关系,且推理成⽴的是
COOCH,
单质X—
”,氧化物1--氧化物211
⼀
0
酸(或碱)
NaOH(或HCI)
灆盐
D.HF 分⼦之间的氢键结构: A.若X为铁,通常⽤ KSCN 溶液检验 Fe*的存在
B. 若X为氮,上述转化中有2个反应属于氧化还原反应
3.下图所示实验装置(夹持装置已省略)能达到实验⽬的的是
C. 若X为硫,标准状况下 44.8 L氧化物2中含氧原⼦的数⽬为6N、
NaOH D.若X为碳,所得盐可能为NaHCO,或Na,CO,,两种盐溶液中存在的微粒种类完全相同
⽯英坩埚
准液 聚四氟
表⾯⽫ 9.可持续⾼分⼦材料在纺织、⽣物医⽤等领域具有⼴阔的应⽤前景。⼀种在温和条件下制备⾼性能
⼄⼆醇 ⼄烯活塞
Na
可持续聚酯P的路线如下图所示。
⾜量酸性 醋酸 25°C,聚合
YKMnO,溶液
(含酚酥)
催化剂
A.制备⼄⼆酸
B.测定醋酸的浓度 C.钠在空⽓中燃烧 D.⾼温熔融烧碱 HCHO
8O°C,解桑
⾼三化学试题 第1⻚(共8⻚) ⾼三化学试题 第2⻚(共8⻚)
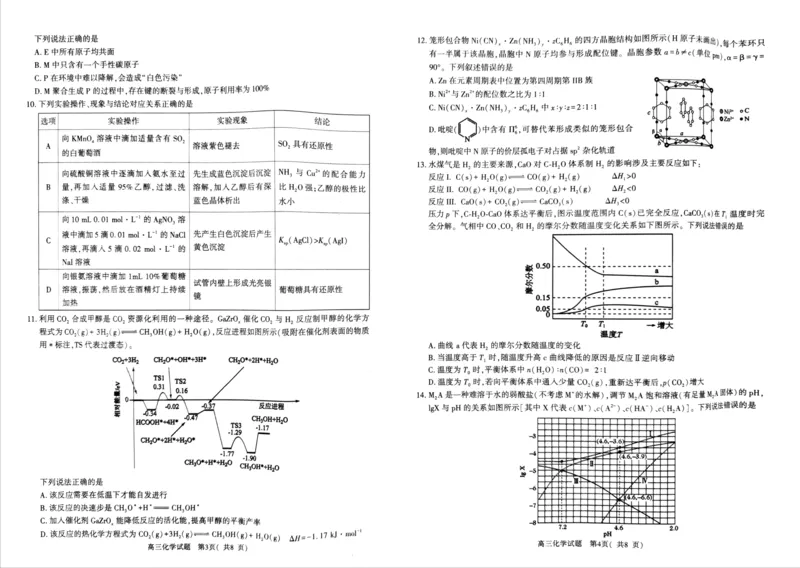
{#{QQABKQAgpgC4kJTACQgqQU1cCUkYsBOjJIgsgQAQuAZCyBFABCA=}#}下列说法正确的是 12.笼形包合物Ni(CN), • Zn(NHL,),•zC。H。的四⽅晶胞结构如图所示(H 原⼦未画出),每个苯环只
A. E 中所有原⼦均共⾯ 有⼀半属于该晶胞,晶胞中N 原⼦均参与形成配位键。晶胞参数a=6*e(单位 pm),Q=B =
B. M 中只含有⼀个⼿性碳原⼦ 90°。下列叙述错误的是
C.P在环境中难以降解,会造成“⽩⾊污染” A. Zn 在元素周期表中位置 第四周期第 IIB 族
D.M聚合⽣成P的过程中,存在键的断裂与形成,原⼦利⽤率为100%
B.N:*与 Zn2*的配位数之⽐为1:1
10. 下列实验操作、现象与结论对应关系正确的是
C. Ni(CN).•Zn(NHs)y•aCH。中 y 2:1:1
②Ni oc
•N
选项 实验操作 实验现象 结论
D.吡啶 中含有 T。,可替代苯形成类似的笼形包合
向KMnO。溶液中滴加适量含有SO,
A 溶液紫⾊褪去 SO2具有还原性
的⽩葡萄酒 物,则吡啶中 N 原⼦的价层孤电⼦对占据sp’杂化轨道
13.⽔煤⽓是H,的主要来源,CaO 对C-H,O体系制H,的影响涉及主要反应如下:
向硫酸铜溶液中逐滴加⼈氨⽔⾄过 先⽣成蓝⾊沉淀后沉淀 NH,与 Cu劲*的配合能⼒
反应1.C(s)+H,0(g) ⼆CO(g)+H2(g) AH,≥0
B 量,再加⼈适量95%⼄醇,过滤、洗 溶解,加⼈⼄醇后有深 ⽐ H0强;⼄醇的极性⽐ 反应I.CO(g)+H,0(g) =COz(g)+Hz(g) AHSO
涤、⼲燥 蓝⾊晶体析出 ⽔⼩ 反应II.CaO(s)+CO(g) CaCOg(s) AHg<0
压⼒p下,C-H,O-CaO体系达平衡后,图示温度范围内C(s)已完全反应,CaCO;(s)在⼯,温度时完
向10mL 0.01 mol•L的AgNO,溶
全分解。⽓相中CO、CO,和⽇,的摩尔分数随温度变化关系如下图所示。下列说法错误的是
液中滴加5滴0.01mol•L 的NaCl 先产⽣⽩⾊沉淀后产⽣
C
K.,(AgCl)>K,(Agl)
溶液,再滴⼊5滴 0.02 mol•L的 ⻩⾊沉淀
Nal 溶液 0.50
向银氨溶液中滴加 1mL 10%葡萄糖
试管内壁上形成光亮银 摩尔分数
D 溶液,振荡,然后放在酒精灯上持续 葡萄糖具有还原性
镜 0.15
加热
0.08
11. 利⽤CO,合成甲醇是CO,资源化利⽤的⼀种途径。GaZrO.催化CO,与H,反应制甲醇的化学⽅
T
⼀增⼤
程式为CO,(8)+3H(8)-CH,OH(8)+ H,0(g),反应进程如图所示(吸附在催化剂表⾯的物质 温度T
⽤*标注,TS代表过疲态)。 A. 曲线a 代表H,的摩尔分数随温度的变化
COnt3i CH,O*+OH*+3H* CHzO"+2H*+HgO B. 当温度⾼于⼯,时,随温度升⾼。曲线降低的原因是反应I逆向移动
C.温度为T。时,平衡体系中n(HO)in(CO)= 2:1
TS1
TS2 D.温度为⼯。时,若向平衡体系中通⼈少量CO,(g),重新达平衡后,P(COz)增⼤
0.31
0.16
14. M,A 是⼀种难溶于⽔的弱酸盐(不考虑M”的⽔解),调节 M,A饱和溶液(有⾜量M,A固体)的pH,
相对能量/eV
-0.02 反应进程 leX 与pH 的关系如图所示[其中X代表。(M')、e(A )、.c(HA )、(H,A)]。下列说法精误的是
-0.34
HCOOH*+4H CHsOH+HO
TS3
-1.17
-1.29
-3
CHyO*+2H*+HgO" +(4.6,-3.6)
-1.77
-1.90
CHsoH*+Eo
-5
下列说法正确的是
A. 该反应需要在低温下才能⾃发进⾏
B. 该反应的决速步是CH』O‘+H‘—CH,OH'
-8l
C. 加⼊催化剂GaZrO,能降低反应的活化能,提⾼甲醇的平衡产率
4.6 2.0
PH
⾼三化学试题 第4⻚(共8⻚)
⾼三化学试题 第3⻚(共8⻚)
{#{QQABKQAgpgC4kJTACQgqQU1cCUkYsBOjJIgsgQAQuAZCyBFABCA=}#}A.曲线I表示lgc(M*)随pH 的变化曲线 (4)Sb 是:51号元素,该元素位于元素周期表 (填“g”“p”“d或“ )区。SbCls分⼦为三⻆
B. Ka. (H,A)数量级为10:2
C.pH=4时,溶液中c(M*)>c(HA)>C(A)20(H,A) 双锥结构( ,请从物质结构⻆度解释 SbCl」 熔沸点⾼于 SbCl,的原因
D.M,A 溶液中,c(M*)=2c(A*)+2c(HAT)+2c(H,A)
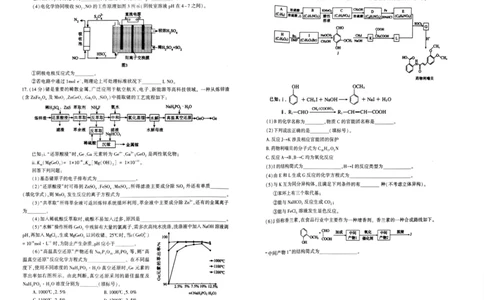
16.(15分)含硫化合物在化⼯⽣产和⽇常⽣活中应⽤⼴泛,关于含硫化合物的研究是⽬前化学⼯业
⼆、⾮选择题(共4⼩题,共58分)。
的热点之⼀。回答下列问题:
15.(15分)三氯化锑(SbCl,)是重要的化⼯原料,实验室先通过氢⽓还原三氧化⼆锑(Sb0,)制备单
(1)家⽤煤⽓中常掺⼊微量具有难闻⽓味的⼄硫醇(CH,SH)作为煤⽓泄鎔的预警⽓。
质锑,再通⼊氯⽓与锑化合制取三氯化锑,实验装置如下图所示(夹持装置省略)。
已知:CH,OH(g)+ H,S(g) CH,SH(g)+H,O(g)AH,=-32.2kJ•mol',120CC时,在⾜量
02中,1mol ⼄醇燃烧放热1409.8 kJ,1 mol 硫化氢燃烧放热562.5 kJ。则反应2G, H,SH(g)+90(g)
4COz(g)+6H,0(g)+250(g)的AH=
(2)已知CH,SH 呈弱酸性,其⽔溶液中的物种分布分数如图1所示。
1.0
C D
数0.8
已知:i.Sb,0;与⽿,在⾼温下反应⽣成 Sb和H,0,反应放热;
:0.6
CAH,SE
0.4
i.Sb 与 Cl,在加热条件下剧烈反应⽣成 SbCls,SbCl,+ Cl, SbCls;
0.2
ii. SbCl,和SbCl,熔沸点:
物质 熔点/° 沸点/°C 性质 1 8 9 10 11 12
pH
图1
223(101kPa)
SbCls 73.4 ①已知K。(H,S)= 9×10,由图可知:K.(H.S) _(填“⼤于”或“⼩于”)K.(GE,SH)。
85.2 (1.86kPa)
均极易⽔解 ②废水中的C,H,SH 可以⽤K,FeO。除去,废⽔ pH =9时,K,FeO,氧化C,E,SE⽣成CgH,S0s
176(101kPa,140CC时分解)
2.8
SbCls
68 (1.86kPa)
(CH,CH§-Or)和Fe(OH)s。若2 mol K,Fe,完全反应,则消耗 —mol CaH,SH。
请回答下列问题:
(1)实验步骤 (3)硫酰氯(S0,Cl,)常⽤作氯化剂和氯磺化剂,其制备原理为S0:(g)+CL.(g) S0,Ch(8)
①组装装置后,首先需进行的操作是
AH =-67.59kJ•mo™。恒容密闭容器中按不同投料⽐充⼊SO.(g)和CL,(g),测定T、72、T;温度下
②打开气阀K,关闭⽓阀K,向⽯英管中通⼈⾜量氩⽓;打开⽓阀K,关闭⽓阀K,点燃酒精喷灯,
体系达平衡时的Ap(Ap = Po-P,P。为体系初始压强,Po=300kPa,p为体系平衡压强)与投料⽐的关
请选择后续正确的操作:_ _ ⼀_ —⼀_ ⼀. _-*c(填字⺟)。 系如图2所示。
a. 改 通氯⽓
75
b.改为通氢⽓⾄⽩⾊固体全部转变成银⽩⾊⾦属
TM(2.60)-
c. 改为通⾜量氩⽓
d.打开⽓阀K」,关闭⽓阀K
e.熄灭酒精喷灯
T!
f. 当观察到 A 装置中固体消失停⽌通⼈氯⽓
(2)装置B 中⼤烧杯⾁冰⽔浴的作⽤是 -。装置C的作⽤是 -。 15 25 3.5 4
n(S0g):n(Cla)
(3)收集的SbCl,中含副产品 SbCl,(⼀种重要的氟化⼯的催化剂),分离⼆者的⽅法是在 图2
⼀(填“101kPa”或“1.86kPe”)压强下蒸馏。选择该压强的理由是 ° ①上图中温度由高到低的顺序为
⾼三化学试题 第5⻚(共8⻚) ⾼三化学试题 第6⻚(#8⻚)
{#{QQABKQAgpgC4kJTACQgqQU1cCUkYsBOjJIgsgQAQuAZCyBFABCA=}#}②M点SO,的转化率为 ,⼯温度下平衡常效K,= (列出⽐例式即可)。 18.(14分)药物利喘⻚具有良好的平喘效果,其以甲苯 起始原料的合成路线如下:
(4)电化学协同吸收SO.、NO 的⼯作原理如图3所示(阴极室溶液pH 在4~7之间)。
直流电源
软液H,80、
吸收
⼆稀旺80,+S02 OH
EISOg
NO 阳离⼦交换膜
图3
①阴极电极反应式为
药物利噹⻉
②若电路中通过1mol e,则理论上可处理标准状况下 L NO。
OH OCHa
17.(14分)销是重要的稀散⾦属,⼴泛应⽤于航空航天、电⼦、新能源等⾼科技领域。⼀种从炼锌渣
(含ZnFe,0。及 MnO.、ZnGeO;、Ga,0s、SiO,)中提取锗的⼯艺流程如下: 已知:1. + CHs1+ NaOH + Nal + H2O
NalPo•FO
NEZF
1. R, CHO CH,(COOH):、 R,-CH-CH-COOH
炼锌渣⼀ 还原酸浸 共萃取~反萃取 中和 氯化蒸馏- 解⼀⾼温真空还原-Ge0•.--Ge
(1)B的化学名称为 —,物质C的官能团名称是_
滤渣 萃余液 反萃取 滤浟 ⽔解⺟液 (2) 下列说法正确的是 (填标号)。
NaHiCOs
A. 反应J⼀K 涉及相应官能团的保护
稀硫酸
沉镓
•⾦属镓
B.药物利喘⻉的分⼦式为CiI8Hp0sN
已知:i“还原酸浸”时,Ge、Ga元素转为Ge*、Ga*;GeO,是两性氧化物;
C.反应 A-B、B-C均內氧化反应
= 1×10"。
i.K,(MgGe0s)= 1×10°,K.,p[Mg(0H),]
(3)I的结构简式为 , ⼀的反应类型为_
回答下列问题:
(4)由E和L⽣成G反应的化学⽅程式为
(1)基态锗原⼦的电⼦排布式为
(5)与K互为同分异构体,且满⾜下列条件的有 种(不考虑⽴体异构)。
(2)“还原酸浸”时可得到ZnSO」、FeSO。、MnSO。,所得滤渣主要成分除SiO,外还有单质
①苯环上有三个取代基;
(填化学式),则MnO,发⽣反应的离⼦⽅程式为
(3)“共萃取”所得萃余液可返回炼锌系统循环利⽤,萃余液中主要成分除 Zn*,还有的⾦属离⼦ ②能与 NaHCO,反应⽣成 COz;
为 ③能与FeCl」溶液发⽣显⾊反应。
(4)加⼊稀硫酸反萃取时,硫酸不易加⼈过多,原因是 (6)]俗称⾹兰素,在⻝品⾏业中主要作为⼀种增⾹剂。⾹兰素的⼀种合成路线如下。
(5)“⽔解“操作所得GeO,中残留有⼤量的氯离⼦,需多次⾼纯⽔洗涤,洗涤液中加⼊ NaOH 溶液调
+CHO 加成 中间 氧化 中间 脫辣。」
pH,再加⼊ MgCh,⽣成 MgGeO,以回收锗。254C时,当c(Ge0g) 1007 OCHsCOOH 产物1
催化剂
产物2
=10~mol •L时,为防⽌产⽣杂质,pH应⼩于
(6)“⾼温真空还原”产物还有Na, P:0.0、H, PO,等,则“⾼ “中间产物1”的结构简式为
温真空还原”反应化学⽅程式为 。在不同温 -1000°C
度下,使⽤不同浓度的 NaH,POz•H0真空还原时,Ge 元素的
~1100°C
1200°C
萃出率如右图所示。由此判断,真空还原采⽤的最佳温度及
NaH,PO•H20 浓度分别为_ —(填标号)。 904
2.5% 5% 7.5% 10% 12.5%
A.1000°C,2.5% B. 1000°CC,5.0% a( NaH,POz H,O)
C. 1100°,2.5% D. 1200CC,2.5%
⾼三化学试题 第7⻚(共8⻚)
⾼三化学忒题第8⻚(共8⻚)
{#{QQABKQAgpgC4kJTACQgqQU1cCUkYsBOjJIgsgQAQuAZCyBFABCA=}#}