文档内容
武汉市 2026届高三年级四月供题
化 学
2026.4
本卷共8页,19题。全卷满分100分。用时75分钟。
注意事项:
1.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号
涂黑。
2.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。
可能用到的相对原子质量:H1 C12 016 Na23 P31 S32 K39 Ca40 Se 79
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.武汉全面推进“氢能城市”建设,氢燃料电池公交车、光储充一体化充电站等绿色交通
。
设施广泛投人使用。下列说法正确的是
A.基态H、D、T的核外电子排布不同
B.镧镍合金能吸收大量氢气生成金属氢化物
C.光储充一体化充电站光伏板主材料为SiO?
D.充电桩壳体聚碳酸酯是一种天然高分子材料
2.下列化学用语表达错误的是
A.SO?~的价层电子对互斥模型:
CE,-=c-CH=cn,化剂+cE?-c-cH-CH?大
B.制备氯丁橡胶:
C.氢氧化铜溶于过量氨水:Cu(OH)?+2NH?=[Cu(NH?)?]2++20H-
D.0.5 mol H?O晶体中氢键的数目为N
3.化学与人体健康密切相关。下列说法错误的是
A.铁、锌、氟、氮等是维持人体正常生命活动所必需的微量元素
B.维生素C主要存在于蔬菜和水果中,能促进人体生长发育
C.人工合成蛋白质可以为人们提供性能优异的药物和生物催化剂
D.粮食中的淀粉属于糖类,糖类是人体主要的供能物质
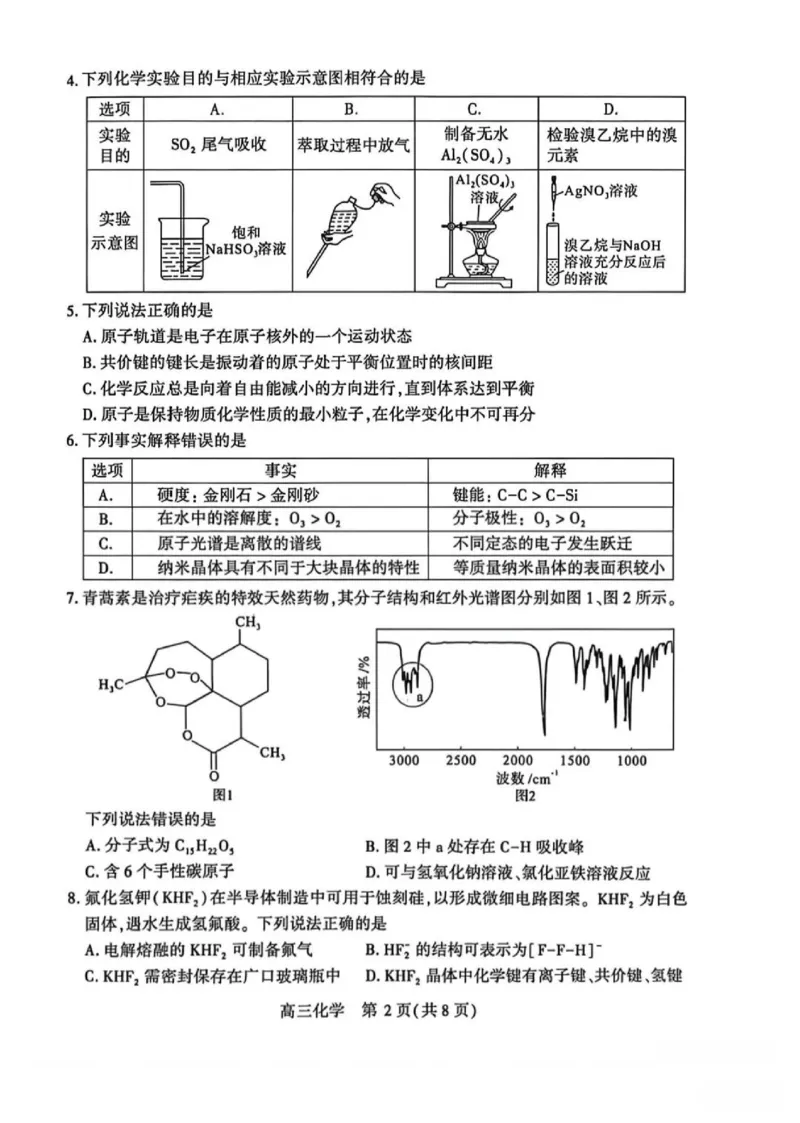
高三化学 第1页(共8页)4.下列化学实验目的与相应实验示意图相符合的是
A. B. C. D.
选项
实验 制备无水 检验溴乙烷中的溴
SO?尾气吸收 萃取过程中放气
目的 Al?(SO?)? 元素
Al?(SO?)?
AgNO?溶液
溶液
实验
饱和
示意图 溴乙烷与NaOH
NaHSO?溶液
溶液充分反应后
的溶液
5.下列说法正确的是
A.原子轨道是电子在原子核外的一个运动状态
B.共价键的键长是振动着的原子处于平衡位置时的核间距
C.化学反应总是向着自由能减小的方向进行,直到体系达到平衡
D.原子是保持物质化学性质的最小粒子,在化学变化中不可再分
6.下列事实解释错误的是
选项 事实 解释
A.
硬度:金刚石>金刚砂 键能:C-C>C-Si
B. 在水中的溶解度:0?>O? 分子极性:O?>0?
C.
原子光谱是离散的谱线 不同定态的电子发生跃迁
mr
D.
纳米晶体具有不同于大块晶体的特性 等质量纳米晶体的表面积较小
7.青蒿素是治疗疟疾的特效天然药物,其分子结构和红外光谱图分别如图1、图2所示。
CH?
透过率/%
0-
O、
H?C
0- a
O
CH?
3000 2500 2000 1500 1000
O 波数/cm'
图1 图2
下列说法错误的是
A.分子式为C??H??O? B.图2中a处存在C-H吸收峰
C.含6个手性碳原子 D.可与氢氧化钠溶液、氯化亚铁溶液反应
8.氟化氢钾(KHF?)在半导体制造中可用于蚀刻硅,以形成微细电路图案。KHF?为白色
固体,遇水生成氢氟酸。下列说法正确的是
A.电解熔融的KHF?可制备氟气 B.HF2的结构可表示为[F-F-H]-
C. KHF?需密封保存在广口玻璃瓶中D. KHF?晶体中化学键有离子键、共价键、氢键
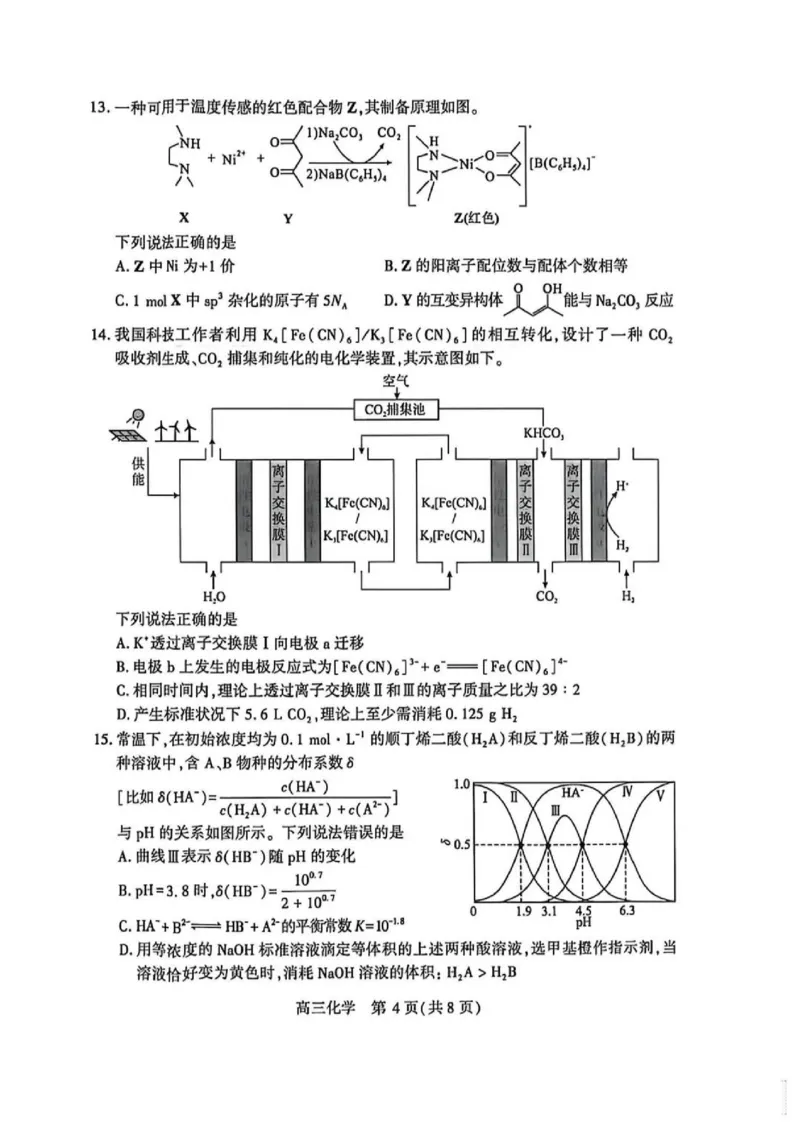
高三化学 第2页(共8页)9.某药物分子结构如图所示,其中X、Y、Z、M、W是原子序数依次增大的短周期主族元
素。下列说法错误的是
A.该分子具有两性
B.电负性:M>Z>W
。○○0○
C.第一电离能:M>Z>W
D.简单氢化物的键角:Y>Z>M X Y Z M W
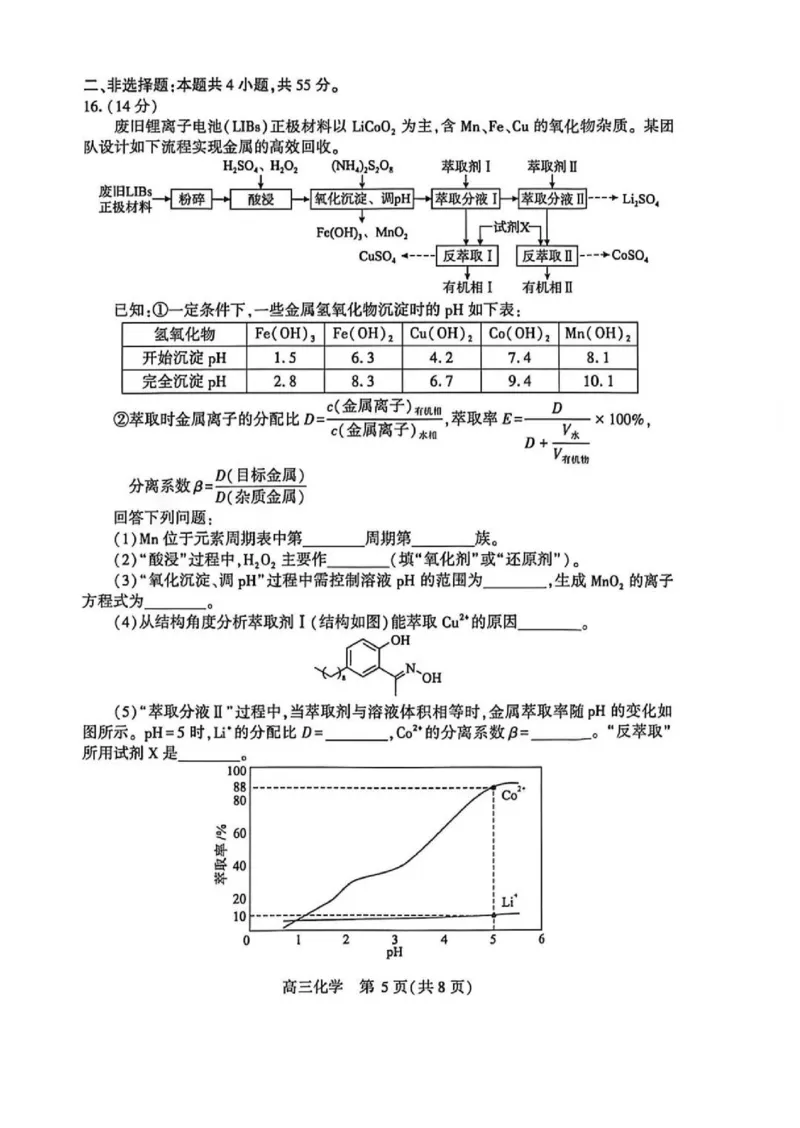
10.部分含碳或钙元素的物质转化关系如图所示。化合物甲是发热包内物质的主要成分
之一,在发热时起重要作用。丁易与血红蛋白结合。己可以发生加成反应。下列说法
错误的是
戊
A.乙的同素异形体可为分子晶体
水
甲 丙
B.实验室制取己可选用启普发生器
已
C.甲、乙、己均能与水发生反应 Z
丁
D.丙、丁、己中均含有三键
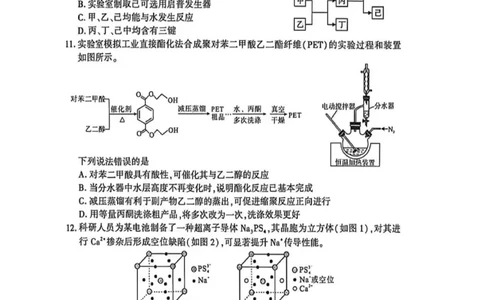
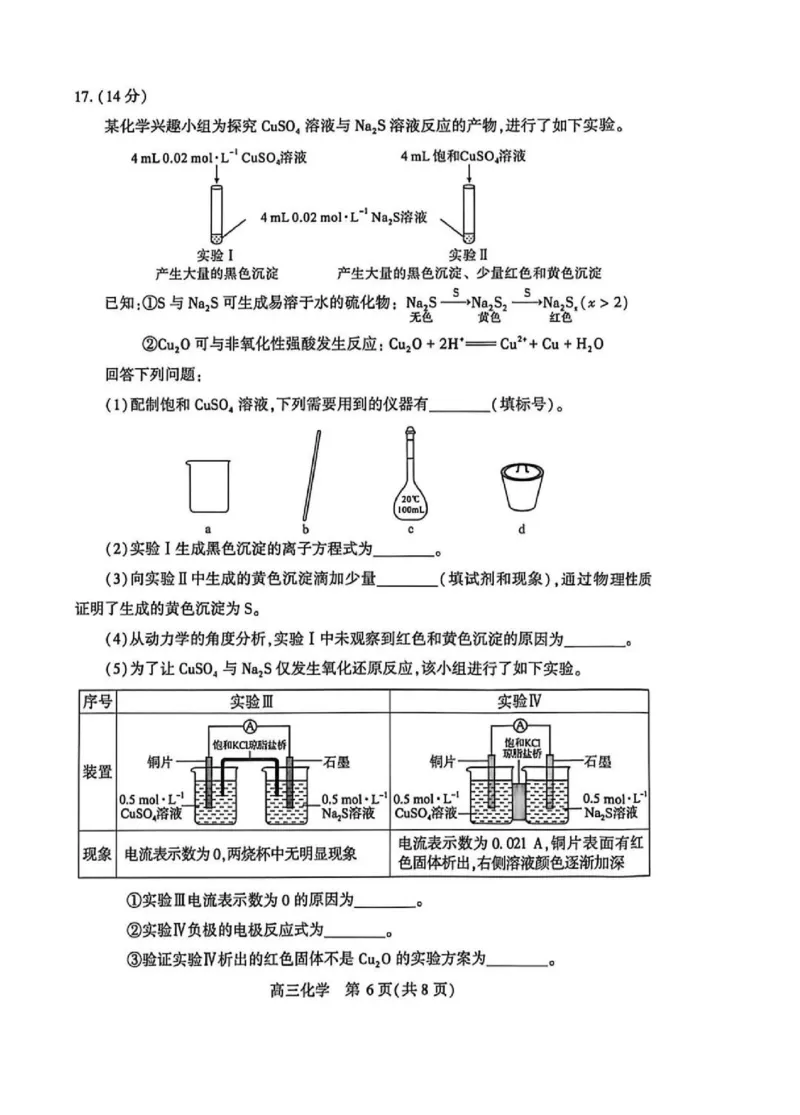
11.实验室模拟工业直接酯化法合成聚对苯二甲酸乙二酯纤维(PET)的实验过程和装置
如图所示。
二m
-
对苯二甲酸
电动搅拌器 分水器
-N?
安
下列说法错误的是
恒温加热装置
A.对苯二甲酸具有酸性,可催化其与乙二醇的反应
B.当分水器中水层高度不再变化时,说明酯化反应已基本完成
C.减压蒸馏有利于副产物乙二醇的蒸出,可促进缩聚反应正向进行
D.用等量丙酮洗涤粗产品,将多次改为一次,洗涤效果更好
12.科研人员为某电池制备了一种超离子导体Na?PS?,其晶胞为立方体(如图1),对其进
行Ca2掺杂后形成空位缺陷(如图2),可显著提升Na传导性能。
O
…·… PS ●
OPS
o· o
●Na' ● Na’或空位
◎
0 o Ca3
O·
…白
a nm
白
图1 图2
下列说法正确的是
28×0°8·m
A.图1晶体密度为
B.图2中空位数与Na'数目之比为1:4
C.导电时,空位移动方向与电流方向相同
D.将Na,PS.中S换为Se,该电池的比能量将增大
高三化学 第3页(共8页)13.一种可用于温度传感的红色配合物 Z,其制备原理如图。
X Y
Z(红色)
下列说法正确的是
A.Z中Ni为+1价 B.Z的阳离子配位数与配体个数相等
H
C.1 mol X中sp3杂化的原子有5N D.Y的互变异构体 能与Na?CO?反应
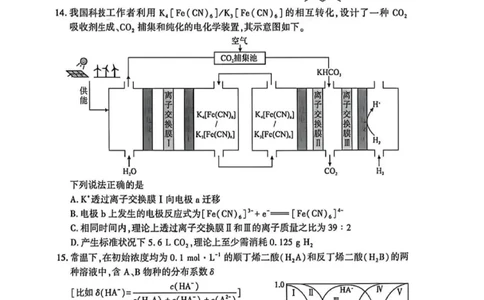
14.我国科技工作者利用K?[Fe(CN)?]/K?[Fe(CN)?]的相互转化,设计了一种CO?
吸收剂生成、CO?捕集和纯化的电化学装置,其示意图如下。
空气
CO?捕集池
十十个
KHCO,
供能
离子交换膜I 离子交换映Ⅱ 离子交换膜Ⅲ
H·
K.[Fe(CN)。] K[Fe(CN)]
/
K,[Fe(CN)] K,[Fe(CN)]
H,
H?O CO? H?
下列说法正确的是
A.K*透过离子交换膜I向电极a迁移
B.电极b上发生的电极反应式为[Fe(CN)?]3?+e?=[Fe(CN)?]?-
C.相同时间内,理论上透过离子交换膜Ⅱ和Ⅲ的离子质量之比为39:2
D.产生标准状况下5.6L CO?,理论上至少需消耗0.125g H?
15.常温下,在初始浓度均为0.1mol·L?1的顺丁烯二酸(H?A)和反丁烯二酸(H?B)的两
种溶液中,含A、B物种的分布系数δ
1.0
IV
8(HA”)=c(HA)+c(HA)+c(A2- I Ⅱ HA V
[比如
Ⅲ
与pH的关系如图所示。下列说法错误的是
0.5
A.曲线Ⅲ表示δ(HB~)随pH的变化
8(HB)=2+10°
B.pH=3.8时,
5
0 1.9 3.1 6.3
C.HA"+B2-—HB?+A2-的平衡常数K=10-1.8
D.用等浓度的NaOH标准溶液滴定等体积的上述两种酸溶液,选甲基橙作指示剂,当
溶液恰好变为黄色时,消耗NaOH溶液的体积:H?A>H?B
高三化学 第4页(共8页)二、非选择题:本题共4小题,共55分。
16.(14分)
废旧锂离子电池(LIBs)正极材料以LiCoO?为主,含Mn、Fe、Cu的氧化物杂质。某团
队设计如下流程实现金属的高效回收。
H?SO?、H?O?
(NH?)?S?O? 萃取剂I 萃取剂Ⅱ
废旧LIBs_
粉碎 酸浸 氧化沉淀、调pH- 萃取分液I 萃取分液Ⅱ ---→Li?SO
正极材料
试剂X-
Fe(OH)?、MnO?
CuSO?- ---→CoSO?
反萃取I 反萃取Ⅱ
有机相I 有机相Ⅱ
已知:①一定条件下,一些金属氢氧化物沉淀时的pH如下表:
氢氧化物 Fe(OH)? Fe(OH)? Cu(OH)? Co(OH)? Mn(OH)?
开始沉淀 pH 1.5 6.3 4.2 7.4 8.1
2.8 8.3 6.7 9.4 10.1
完全沉淀pH
D=“(金属离子)n
,萃取率ED+×100%,
②萃取时金属离子的分配比
D(余质金属)
分离系数β=
回答下列问题:
(1)Mn位于元素周期表中第_______周期第_______族。
(2)“酸浸”过程中,H?O?主要作_______(填“氧化剂”或“还原剂”)。
(3)“氧化沉淀、调pH”过程中需控制溶液pH的范围为____,生成MnO?的离子
方程式为_______。
(4)从结构角度分析萃取剂I(结构如图)能萃取Cu2的原因______。
(5)“萃取分液Ⅱ”过程中,当萃取剂与溶液体积相等时,金属萃取率随pH的变化如
图所示。pH=5时,Li"的分配比D=___,Co2的分离系数β=____。“反萃取”
所用试剂X是_______。
100
88 Co2
80
萃取率%60
如
20 Li
10
0 1 2 3 4 5 6
pH
高三化学 第5页(共8页)17.(14分)
某化学兴趣小组为探究CuSO?溶液与Na?S溶液反应的产物,进行了如下实验。
4mL0.02 mol·L?'CuSO?溶液 4mL饱和CuSO?溶液
4mL0.02 mol·L?1Na?S溶液
实验I 实验Ⅱ
产生大量的黑色沉淀 产生大量的黑色沉淀、少量红色和黄色沉淀
一S一Na5(> 2)
已知:①S与Na?S可生成易溶于水的硫化物:
②Cu?0可与非氧化性强酸发生反应:Cu?O+2H?=Cu2?+Cu+H?O
回答下列问题:
(1)配制饱和CuSO?溶液,下列需要用到的仪器有______(填标号)。
合
20℃
100mL)
a c
b d
(2)实验I生成黑色沉淀的离子方程式为_______。
(3)向实验Ⅱ中生成的黄色沉淀滴加少量________(填试剂和现象),通过物理性质
证明了生成的黄色沉淀为S。
(4)从动力学的角度分析,实验I中未观察到红色和黄色沉淀的原因为______。
(5)为了让CuSO?与Na?S仅发生氧化还原反应,该小组进行了如下实验。
序号 实验Ⅲ 实验IV
A A-
饱和KC
饱和KCL琼脂盐桥
铜片 石墨 铜片· 琼脂盐桥 石墨
装置
0.5mol·L-1 0.5 mol·L-10.5 mol·L?1 0.5mol·L
CuSO?溶液 Na?S溶液 CuSO?溶液- Na?S溶液
电流表示数为0.021 A,铜片表面有红
现象 电流表示数为0,两烧杯中无明显现象
色固体析出,右侧溶液颜色逐渐加深
①实验Ⅲ电流表示数为0的原因为______。
②实验IV负极的电极反应式为___。
③验证实验IV析出的红色固体不是Cu?O的实验方案为___。
高三化学 第6页(共8页)一
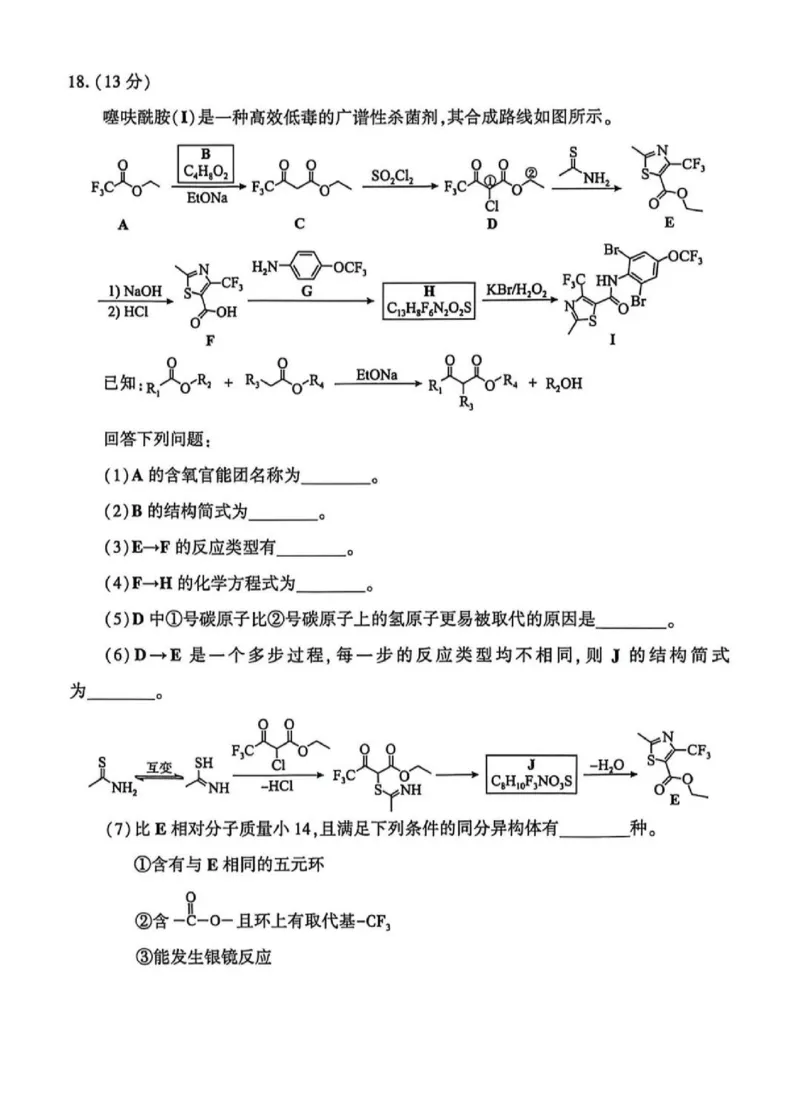
18.(13分)
噻呋酰胺(I)是一种高效低毒的广谱性杀菌剂,其合成路线如图所示。
—B
F
已知R,。B,+几,是R EoONe,R+BOH
回答下列问题:
(1)A的含氧官能团名称为_____。
(2)B的结构简式为_________。
(3)E→F的反应类型有____。
(4)F→H的化学方程式为____。
(5)D中①号碳原子比②号碳原子上的氢原子更易被取代的原因是_______。
(6)D→E是一个多步过程,每一步的反应类型均不相同,则J的结构简式
为___。
(7)比E相对分子质量小14,且满足下列条件的同分异构体有____种。
①含有-°与-Eo相-同的五元环
②含 且环上有取代基-CF?
③能发生银镜反应19.(14分)
甲醇高选择性转化制乙烯是煤化工领域的重要研究方向,是保证能源安全的重要手
段。其涉及反应如下。
主反应:2CH?OH(g)一C?H?(g)+2H?O(g) △H
副反应:C?H?(g)+CH?OH(g)一C?H?(g)+H?O(g) △H?=-51.0kJ·mol?1
回答下列问题:
△H?=-19.9kJ·mol-1
(1)已知:2CH?OH(g)一CH?OCH?(g)+H?O(g)
CH?OCH?(g)一C?H?(g)+H?O(g) △H?=-3.2 kJ·mol?1
则主反应的△H=_____kJ·mol?1。
(2)对于主反应,加压会使平衡向______(填“正反应”或“逆反应”)方向移动,但
是实际生产中仍选择适度加压,其目的是______。
(3)分子筛可为气体提供活性位点,以达催化的目的。分子筛上的甲醇转化的部分
反应路径如图所示。
CHOo CHDH
H?O CH,OH H?O n CH?OH n H?O
高碳烯烃
(ii) (ii)
(i)
①该反应路径中过程(ii)的化学方程式为____。
②随温度升高,乙烯的平衡选择性升高的原因是_____。
S(C?H,)=总转化的甲物物质的×100%]
[乙烯选择性:
③500℃时,100 kPa恒压条件下通人1mol CH?OH(g)和4 mol H?O(g),平衡时
a(CH?OH)=90?(C?H?)=40只考虑副产物为丙烯,则平衡时n(H?O)=_____mol,
主反应的K。=_______kPa(列出计算式)。
④研究发现,进料中添加一定量的H?O(g)可以提高乙烯的选择性,从催化剂角度
分析可能原因是___。
高三化学 第8页(共8页)