文档内容
2026届高三四月第一次检测(二模)
一、单选题(每小题3分,共39分)
1.古代壁画中常用的蓝色颜料是石青[2CuCO Cu(OH) ],黑色颜料是铁黑(Fe O )。下列元
3 2 3 4
素位于元素周期表中 ds区的是 ∙
A.Cu B.C C.Fe D.O
2.过氧化钠用于呼吸面罩的供氧剂,其反应原理为2Na O 2CO 2Na CO O 。下列
2 2 2 2 3 2
说法正确的是
A.Na O 中含极性共价键 B.CO 的电子式为
2 2 2
C.CO2的空间构型为正四面体形 D.O原子结构示意图为
3
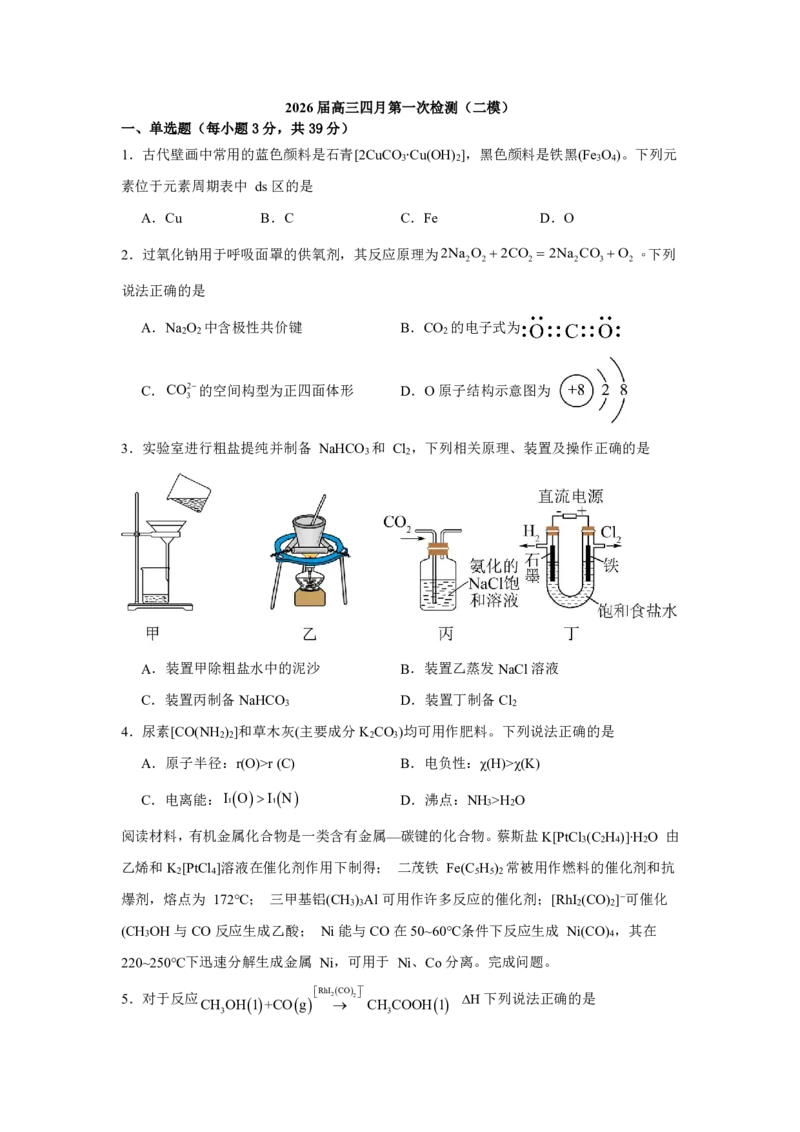
3.实验室进行粗盐提纯并制备 NaHCO 和 Cl ,下列相关原理、装置及操作正确的是
3 2
A.装置甲除粗盐水中的泥沙 B.装置乙蒸发NaCl溶液
C.装置丙制备NaHCO D.装置丁制备Cl
3 2
4.尿素[CO(NH ) ]和草木灰(主要成分K CO )均可用作肥料。下列说法正确的是
2 2 2 3
A.原子半径:r(O)>r(C) B.电负性:χ(H)>χ(K)
C.电离能:I₁OI₁N D.沸点:NH >H O
3 2
阅读材料,有机金属化合物是一类含有金属—碳键的化合物。蔡斯盐K[PtCl (C H )]∙H O 由
3 2 4 2
乙烯和K [PtCl ]溶液在催化剂作用下制得; 二茂铁 Fe(C H ) 常被用作燃料的催化剂和抗
2 4 5 5 2
爆剂,熔点为 172℃; 三甲基铝(CH ) Al可用作许多反应的催化剂;[RhI (CO) ]−可催化
3 3 2 2
(CH OH与CO反应生成乙酸; Ni能与CO在50~60℃条件下反应生成 Ni(CO) ,其在
3 4
220~250℃下迅速分解生成金属 Ni,可用于 Ni、Co分离。完成问题。
5.对于反应 CH OH1+COg RhI2 CO 2 CH COOH1 H下列说法正确的是
3 3A.该反应的△H<0
B.CO在反应过程中共价键未断裂
C.[RhI (CO) ]−提高该反应的活化能
2 2
D.及时分离CH COOH 能加快化学反应速率
3
6.下列化学反应表示正确的是
A.溴乙烷制备乙烯的反应:CH CH Br浓硫酸CH =CH ↑+HBr
3 2 2 2
点燃
B.过量铁与氯气反应:FeCl FeCl
2 2
C.合成蔡斯盐的反应: C 2 H 4 K 2 PtCl 4 H 2 OK PtCl 3 C 2 H 4 H 2 OKCl
220250℃
D.生成 Ni(CO) 的反应:Ni4CO NiCO
4 4
7.下列说法正确的是
A.(CH ) Al中 Al 原子轨道的杂化类型为 sp3
3 3
B.K[PtCl (C H )]中 Pt的化合价为+3
3 2 4
C.Fe(C H ) 属于离子化合物
5 5 2
D.1molNi(CO) 中 σ 键数目为 8mol
4
8.在给定条件下,下列制备过程涉及的物质转化均可实现的是
A.工业制高纯Si:SiO CSi(s)HClSiHCl (s)H2Si(s)
2 高温 高温 3 高温
B.侯氏制碱法:NaCl(aq)CO2NaHCO (s) ΔNa CO (s)
3 2 3
C.工业制硝酸:NH O2 NO(g)H2OHNO (aq)
3 催化剂、Δ 3
D.海水中提取镁:Mg(OH) (s)稀盐酸MgCl (aq)电解Mg(s)
2 2
9.一种可充放电Li-O 电池的结构示意图如图所示。该电池放电时,产物为Li O和Li O ,
2 2 2 2
随着反应温度升高,Q(消耗1mol O 转移的电子数)增大。下列说法不正确的是
2A.放电时, Li向上通过固态电解质膜
B.随温度升高放电时,正极电极反应为O 2e O2
2 2
C.充电时,锂电极接电源负极,发生还原反应
D.熔融盐中LiNO 的质量分数大小影响充放电速率
3
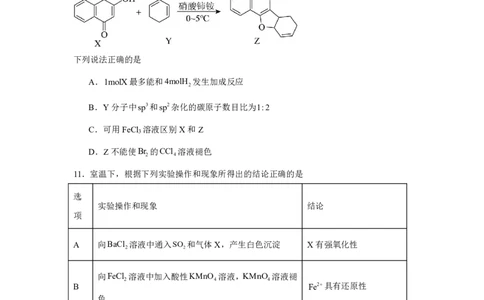
10.化合物Z是一种具有生理活性的多环呋喃类化合物,部分合成路线如下:
下列说法正确的是
A.1molX最多能和4molH 发生加成反应
2
B.Y分子中sp3和sp2杂化的碳原子数目比为1:2
C.可用FeCl 溶液区别X和Z
3
D.Z不能使Br 的CCl 溶液褪色
2 4
11.室温下,根据下列实验操作和现象所得出的结论正确的是
选
实验操作和现象 结论
项
A 向BaCl 溶液中通入SO 和气体X,产生白色沉淀 X有强氧化性
2 2
向FeCl 溶液中加入酸性KMnO 溶液,KMnO 溶液褪
2 4 4
B Fe2具有还原性
色
向Na SO 溶液中先滴加酚酞,再滴加BaCl 溶液至过 Na SO 溶液中SO2水解
2 3 2 2 3 3
C
量,溶液红色变浅至消失 使溶液呈碱性
在2mL0.01 molL1 Na S溶液中先滴入几滴0.01
2
D K ZnSK CuS
sp sp
molL1 CuSO 溶液有黑色沉淀生成,再滴入0.01
4molL1 ZnSO 溶液,又有白色沉淀生成
4
A.A B.B C.C D.D
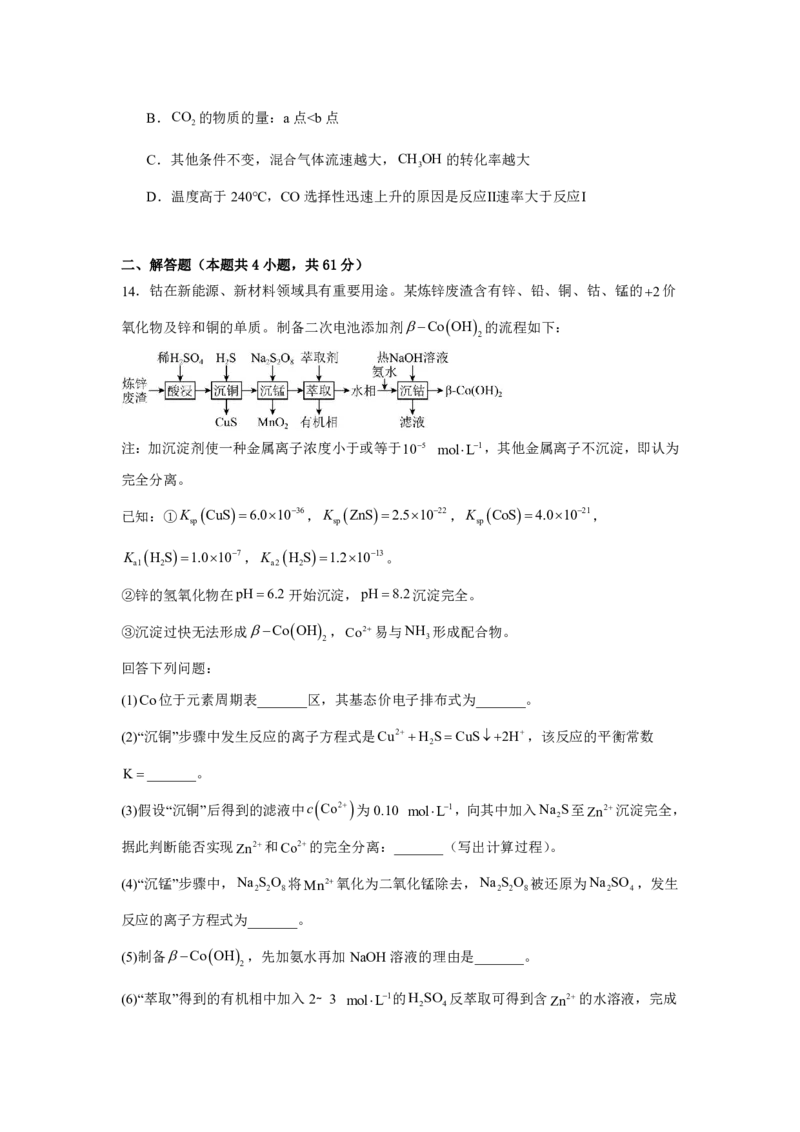
12.实验室通过下列过程制取草酸亚铁晶体:
已知:K H C O 5.6102、K H C O 1.5104、K FeC O 3.2107。下列
a1 2 2 4 a2 2 2 4 sp 2 4
说法不正确的是
A.pH4的H C O 溶液中:c
C
O2
c
HC
O
2 2 4 2 4 2 4
B.“酸化”后的溶液中:c
NH
2c
Fe2
2c
SO2
4 4
C.“沉淀”后的上层清液中:c Fe2 c C O2 3.2107
2 4
D.水洗后,再用乙醇洗涤有利于晶体快速干燥
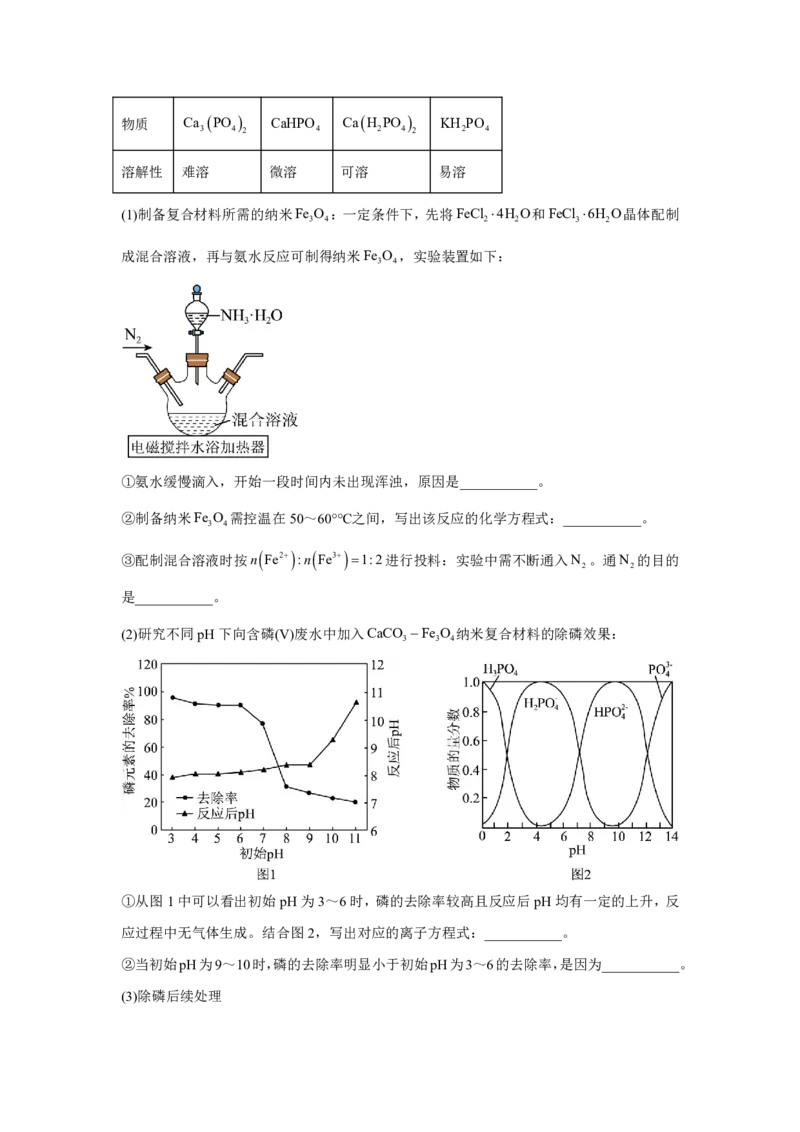
13.甲醇水蒸气重整制氢是生产氢气的重要途径,其主要反应为:
Ⅰ.CH OHgH Og CO g3H g H 49.4kJmol1
3 2 2 2 1
Ⅱ.CH OHg COg2H g H 90.6kJmol1
3 2 2
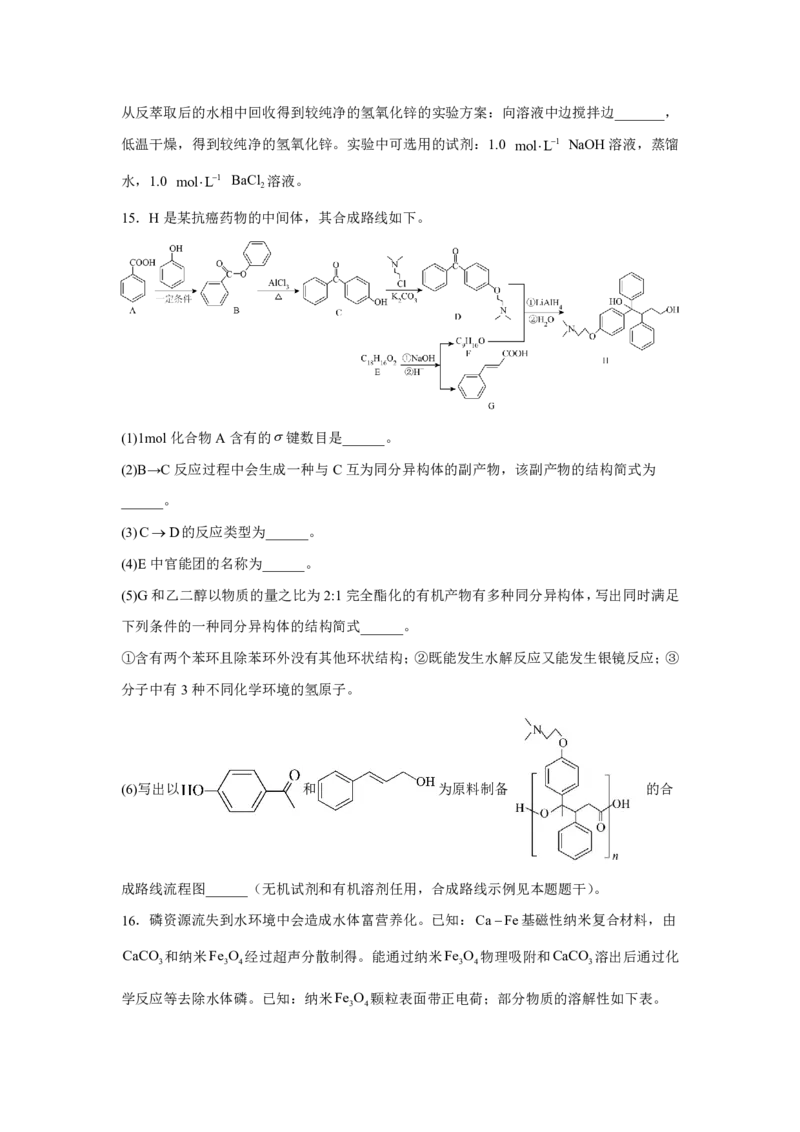
1.01105Pa、n H O:n CH OH1.2:1时,混合气体以一定流速通过反应管,在催
起始 2 起始 3
n CO
化剂作用下反应一段时间后测得CH OH转化率、CO选择性 生成 100%随温度
3 n
反应
CH
3
OH
的变化如图所示。
下列说法正确的是
A.反应Ⅱ的平衡常数:K K
220℃ 280℃B.CO 的物质的量:a点