文档内容
二月阶段性测试 2023 级高三化学试卷 B.[Fe(CN) 6 ]3- 中的 C 原子杂化方式为: sp 杂化
C. Co [Ar]3d74s2
基态 原子的价层电子排布式为:
(本试卷满分100分,考试时间 75分钟)
D.Ni
的价电子排布图为:
H 1 O 16 As 75 Ni 59
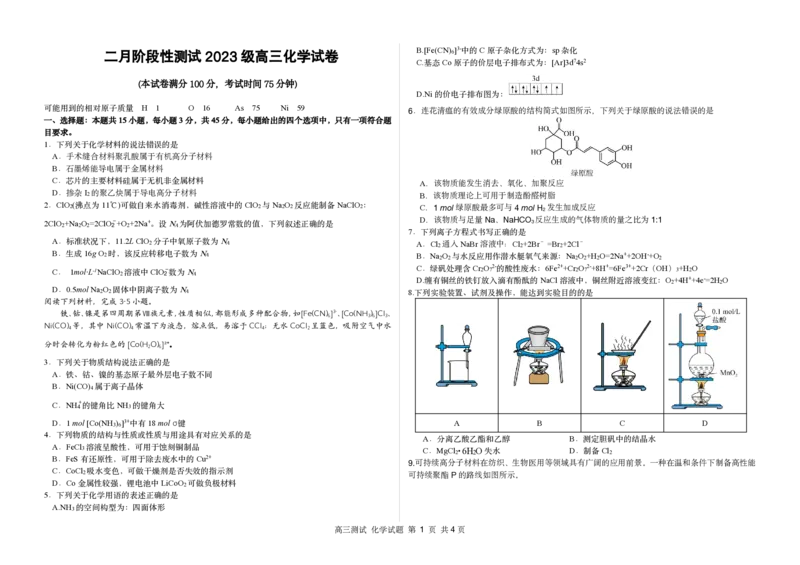
可能用到的相对原子质量 6. 连花清瘟的有效成分绿原酸的结构简式如图所示,下列关于绿原酸的说法错误的是
15 3 45
一、选择题:本题共 小题,每小题 分,共 分,每小题给出的四个选项中,只有一项符合题
目要求。
1
.下列关于化学材料的说法错误的是
A 手术缝合材料聚乳酸属于有机高分子材料
.
B 石墨烯能导电属于金属材料
.
C
.芯片的主要材料硅属于无机非金属材料 A.该物质能发生消去、氧化、加聚反应
D
.
掺杂I 2的聚乙炔属于导电高分子材料
B.该物质理论上可用于制造酚醛树脂
2 ClO ( 11 ) ClO Na O NaClO
. 2 沸点为 ℃ 可做自来水消毒剂,碱性溶液中的 2与 2 2反应能制备 2: C.1mol绿原酸最多可与4molH 发生加成反应
2
2ClO +Na O =2ClO - +O +2Na+ N D.该物质与足量Na、NaHCO 3 反应生成的气体物质的量之比为1:1
2 2 2 2 2 。设 A为阿伏加德罗常数的值,下列叙述正确的是
7
.下列离子方程式书写正确的是
A .标准状况下, 11.2LClO 2分子中氧原子数为 N A A . Cl 2 通入NaBr溶液中:Cl 2 +2Br- =Br 2 +2Cl-
B .生成 16gO 2时,该反应转移电子数为 N A B . Na 2 O 2与水反应用作潜水艇氧气来源: Na 2 O 2 +H 2 O=2Na++2OH-+O 2
C 1mol∙L-1NaClO ClO - N C .绿矾处理含 Cr 2 O 7 2- 的酸性废水: 6Fe2++Cr 2 O 7 2-+8H+=6Fe3++2Cr ( OH )3 +H 2 O
. 2溶液中 2数为 A
D. NaCl O +4H++4e-=2H O
缠有铜丝的铁钉放入滴有酚酞的 溶液中,铜丝附近溶液变红: 2 2
D 0.5molNa O N
. 2 2固体中阴离子数为 A 8.
下列实验装置、试剂及操作,能达到实验目的的是
阅读下列材料,完成3-5小题。
铁、钴、镍是第四周期第Ⅷ族元素,性质相似,都能形成多种配合物,如[Fe(CN) ]3-、[Co(NH ) ]Cl 、
6 36 3
Ni(CO) 等,其中Ni(CO) 常温下为液态,熔点低,易溶于CCl ;无水CoCl 呈蓝色,吸附空气中水
4 4 4 2
分时会转化为粉红色的[Co(H O) ] ⁺。
2 6 ²
3
.下列关于物质结构说法正确的是
A
.铁、钴、镍的基态原子最外层电子数不同
B Ni(CO)
. 4属于离子晶体
+
C NH NH
. 4的键角比 3的键角大
D 1mol[Co(NH ) ]3+ 18mol A B C D
. 3 6 中有 键
4
.下列物质的结构与性质或性质与用途具有对应关系的是 A B
.分离乙酸乙酯和乙醇 .测定胆矾中的结晶水
A FeCl
. 3溶液呈酸性,可用于蚀刻铜制品 C
.
MgCl 2●6H
2
O
失水
D
.制备
Cl
2
B FeS Cu2+
. 有还原性,可用于除去废水中的 9.可持续高分子材料在纺织、生物医用等领域具有广阔的应用前景。一种在温和条件下制备高性能
C CoCl
. 2吸水变色,可做干燥剂是否失效的指示剂 可持续聚酯P的路线如图所示。
D Co LiCoO
. 金属性较强,锂电池中 2可做负极材料
5
.下列关于化学用语的表述正确的是
A.NH
3的空间构型为:四面体形
高三测试 化学试题 第 1 页 共4页
{#{QQABDQi1wwCYkIRACS77AUnqCQgYkJAQJAgmwQCYuAxLSQFABAA=}#}“盐浸”过程ZnO转化为
ZnNH
3
4
2 ,并有少量Fe2和Fe3浸出。下列说法错误的是
A.“盐浸”过程若浸液pH下降,需补充NH
3
B.“沉锌”过程发生反应
ZnNH
3
4
2 4H
2
OS2 ZnS4NH
3
H
2
O
C.“滤渣”的主要成分为Fe(OH)
3
D.应合理控制 NH S用量,以便滤液循环使用
4 2
下列说法错误的是
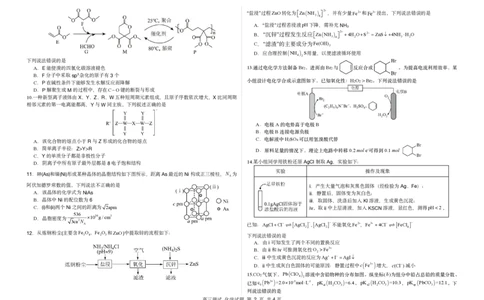
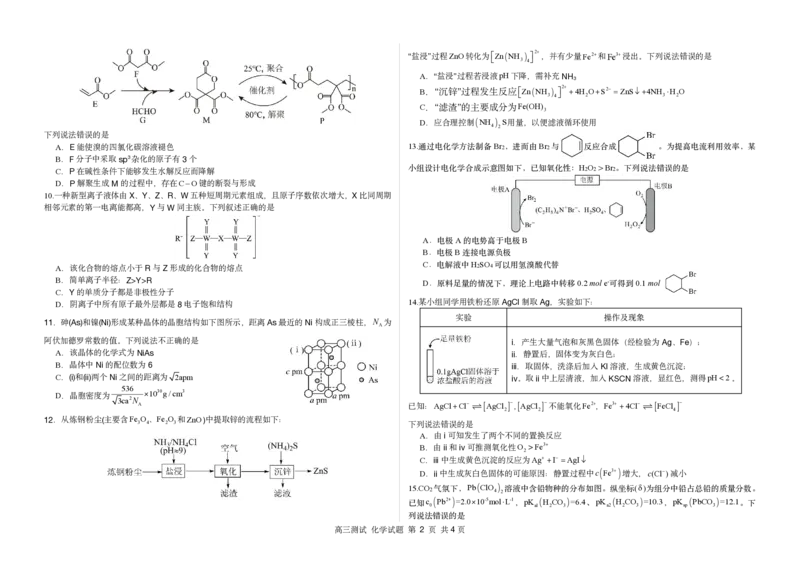
A.E能使溴的四氯化碳溶液褪色 13. 通过电化学方法制备 Br 2,进而由 Br 2与 反应合成 。为提高电流利用效率,某
B.F分子中采取sp3杂化的原子有3个
H O >Br
C.P在碱性条件下能够发生水解反应而降解 小组设计电化学合成示意图如下,已知氧化性: 2 2 2。下列说法错误的是
D.P解聚生成M的过程中,存在CO键的断裂与形成
10.一种新型离子液体由X、Y、Z、R、W五种短周期元素组成,且原子序数依次增大,X比同周期
相邻元素的第一电离能都高,Y与W同主族。下列叙述正确的是
A A B
.电极 的电势高于电极
B B
.电极 连接电源负极
C H SO
A.该化合物的熔点小于R与Z形成的化合物的熔点 .电解液中 2 4可以用氢溴酸代替
B.简单离子半径:Z>Y>R D 0.2mole- 0.1mol
.原料足量的情况下,理论上电路中转移 可得到
C.Y的单质分子都是非极性分子
D.阴离子中所有原子最外层都是8电子饱和结构 14.某小组同学用铁粉还原AgCl制取Ag,实验如下:
实验 操作及现象
11.砷(As)和镍(Ni)形成某种晶体的晶胞结构如下图所示,距离As最近的Ni构成正三棱柱,N
A
为
阿伏加德罗常数的值。下列说法不正确的是 i.产生大量气泡和灰黑色固体(经检验为Ag、Fe);
A.该晶体的化学式为NiAs ii.静置后,固体变为灰白色;
B.晶体中Ni的配位数为6 iii.取固体,洗涤后加入KI溶液,生成黄色沉淀;
C.(ⅰ)和(ⅱ)两个Ni之间的距离为 2apm iv。取ii中上层清液,加入KSCN溶液,显红色,测得pH2。
536
D.晶胞密度为
1030g/cm3
3ca2N
A 已知:AgClCl AgCl , AgCl 不能氧化Fe2,Fe3 4Cl FeCl
2 2 4
12.从炼钢粉尘(主要含Fe
3
O
4
、Fe
2
O
3
和ZnO)中提取锌的流程如下:
下列说法错误的是
A.由i可知发生了两个不同的置换反应
B.由ii和iv可推测氧化性O Fe3
2
C.iii中生成黄色沉淀的反应为Ag I AgI
D.ii中生成灰白色固体的可能原因:静置过程中c Fe3 增大,c(Cl)减小
15.CO
PbClO
(δ)
2气氛下, 4 2溶液中含铅物种的分布如图。纵坐标 为组分中铅占总铅的质量分数。
c Pb2+ =2.010-5molL-1 pK H CO =6.4 pK H CO =10.3 pK PbCO =12.1
已知 0 , al 2 3 、 a2 2 3 , sp 3 。下
列说法错误的是
高三测试 化学试题 第 2 页 共4页
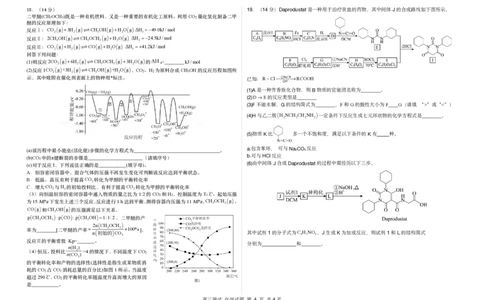
{#{QQABDQi1wwCYkIRACS77AUnqCQgYkJAQJAgmwQCYuAxLSQFABAA=}#}17. ( 13 分)正丁醚 CH 3 CH 2 CH 2 CH 2 2 O 可用作溶剂,电子级清洗剂。实验室制备原理如下:
Δ
2CH CH CH CH OHCH CH CH CH O H O
3 2 2 2 H 3 2 2 22 2 。
制备步骤:
I ( )
步骤 选择仪器并组装 夹持装置略 。
15.5mL 2.5mL 100 115
步骤Ⅱ.加入 正丁醇、 浓硫酸,摇匀,在磁力搅拌器上加热至 ~ ℃,
A pH=6.5 c CO2- ”或“<”)
(4)H与乙二胺 H
2
NCH
2
CH
2
NH
2
一定条件下反应生成七元环状物的化学方程式是 。
(5)物质K比 多一个不饱和度,满足以下条件的K有_____种。
(a) ( ) a.包含苯环, 可与Na 2 CO 3 反应
该历程中最小能垒 活化能 步骤的化学方程式为 。
(b)CO π
b.可与HCl反应
2中的 键断裂的步骤是 (请填序号)
(c) I ( )
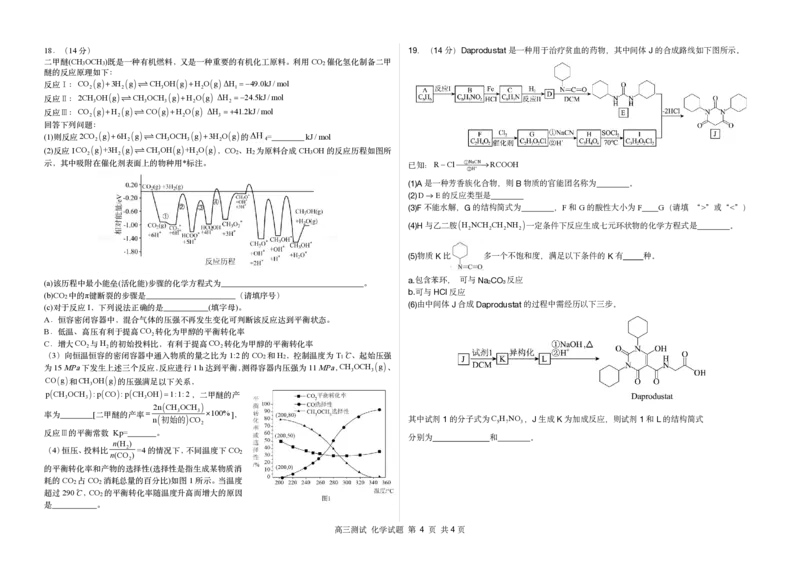
(6)由中间体J合成Daprodustat的过程中需经历以下三步。
对于反应 ,下列说法正确的是 填字母 。
A
.恒容密闭容器中,混合气体的压强不再发生变化可判断该反应达到平衡状态。
B CO
.低温、高压有利于提高 2转化为甲醇的平衡转化率
C CO H CO
.增大 2与 2的初始投料比,有利于提高 2转化为甲醇的平衡转化率
3 1:2 CO H T
( )向恒温恒容的密闭容器中通入物质的量之比为 的 2和 2,控制温度为 1℃、起始压强
15MPa 1h 11MPa CH OCH g
为 下发生上述三个反应,反应进行 达到平衡,测得容器内压强为 , 3 3 、
COg CH OHg
和 3 的压强满足以下关系,
pCH OCH :pCO:pCH OH1:1:2
3 3 3 ,二甲醚的产
2nCH OCH
率为 [ 二甲醚的产率
n 初始的
3
CO
3
2
100%]
, 其中试剂1的分子式为C
5
H
7
NO
3
,J生成K为加成反应,则试剂1和L的结构简式
Kp=
反应Ⅲ的平衡常数 。 分别为 和 。
n(H )
4 2 =4 CO
( )恒压、投料比n(CO ) 的情况下,不同温度下 2
2
(
的平衡转化率和产物的选择性 选择性是指生成某物质消
CO CO ) 1
耗的 2占 2消耗总量的百分比 如图 所示。当温度
290 CO
超过 ℃, 2的平衡转化率随温度升高而增大的原因
是 。
高三测试 化学试题 第 4 页 共4页
{#{QQABDQi1wwCYkIRACS77AUnqCQgYkJAQJAgmwQCYuAxLSQFABAA=}#}