文档内容
第1 页共4 页
重庆市2026 届高考模拟调研卷(三)
化学答案
1~5
CADAD
6~10
BCCAB
11~14
ACDD
1.
C.【
—解析】发电所用核心材料为硅单质,A 不符合题意;均苯三甲酸不属于高分子化合物,B
不符合题意;石墨属于混合晶体,C 符合题意;砷化镓属于无机非金属材料,D 不符合题意。
2.
A.【
—解析】N 原子p 轨道半充满,因此第一电离能N>O>S,A 正确,符合题意;H2O 能形
成分子间氢键,常温下为液体,H2S 不能形成分子间氢键,B 错误;电负性:O>P>C,C 错误;电子空间
运动状态数是指电子所在的轨道数,因此电子空间运动状态数S=P=Si,D 错误。
3.
D【
—解析】A 项,乙醇也能与金属钠反应生成氢气,不能证明医用酒精中含水,A 不符合题意;
B 项,碘盐中添加的是KIO3,加入淀粉溶液没有颜色变化,B 不符合题意;C 项,高锰酸钾溶液具有强氧
化性,会氧化碱式滴定管的橡胶管,C 不符合题意;D 项,配制FeSO4 溶液需要防水解,也需要防氧化,加
硫酸是防水解,加铁粉是防氧化,D 符合题意。
4.
A【
—解析】B 项:在0.1 mol·L
-1 氯化钠溶液中,pH=7,Fe3+不能大量共存;C 项:在0.1 mol·L
-1碳酸氢钠溶液中,OH
-会与HCO
-
3 反应生成CO
2-
3 ,不能大量共存;D 项:在0.1 mol·L
-1稀硫酸中,[Ag(NH3)2]
+在酸性条件下会反应,且[Ag(NH3)2]
+与I
-生成AgI 沉淀,不能共存。
5.
D.【
—解析】A 项,分子式应该为C12H12O6,A 不符合题意;B 项,分子中含有3 种官能团,B
不符合题意;C 项,能发生取代、加成、氧化反应,不能发生加聚、消去反应,C 不符合题意;D 项,与足
量H2 反应的产物中含有4 个手性碳原子,D 符合题意。
6.
B.【
—解析】A 项,SO2 和H2O 均为极性分子,A 不符合题意;B 项,NO
-
3 和SO
2-
3 的中心原子
的杂化类型分别为sp2、sp3,B 符合题意;C 项,SO
2-
4 为正四面体结构,O-S-O 键角为109°28',NH2OH
的N 原子为sp3 杂化,同时N 原子上有1 对孤电子对,孤电子对对成键电子对斥力较大,使H-N-H 键角
小于109°28',故O-S-O 键角大于H-N-H,C 不符合题意;D 项,H2O 和NH3 各自分子间的O-H…O
氢键键能大于N-H…N,D 不符合题意。
7.
C【
—解析】A 项,SiC 硬度很大,但其硬度小于金刚石,因此不能用于切割金刚石,A 不符合
题意;B 项,Cl2 有较强氧化性,但Cl2 没有漂白性,B 不符合题意;C 项,丙三醇能与水形成分子间氢键,
易溶于水,也因此可用于皮肤护理的保湿剂,C 符合题意;D 项,苯酚有弱酸性,但苯酚与甲醛制酚醛树脂
发生的是缩聚反应,D 不符合题意。
8.
C.【
—解析】A 项,图①还需要有玻璃棒引流;C 项:应将反应后的混合物加入水中稀释;D
项,图④装置应使用环形玻璃搅拌棒。
9.
A【
—解析】A 项,1mol P4 中含共价键数目为6NA,A 错误;B 项,由于NH
+
4 水解,溶液中所含
NH
+
4 数小于NA,B 正确;C 项,1mol Fe 与1mol Cl2 反应,铁过量,Cl2 完全反应,转移2 NA 电子,C 正确;
D 项,标况下11.2L 气体的物质的量为0.5 mol,1mol CO2 和N2O 中含有的电子数均为22 NA,故D 正确。
10. B.【
—解析】A 项,用均摊法计算,该晶胞中含有4 个Na
+,A 不符合题意;B 项,该晶体属于离
子晶体,不是混合晶体,B 符合题意;C 项,两个Na
+之间的最短距离刚好是边长为a nm 的正方形对角线长
度的一半,即
2 a
2
nm,C 不符合题意;D 项,Na
+周围紧邻且等距的BH
-
4 数为8,D 不符合题意。
11. A.【
—解析】W、X、Y 分别为C、Al、Cl,由于W、X、Y、Z 价层电子数之和为17,Z 为
Ga。A 项:碳有多种氢化物,例如苯,常温下为液体,沸点比HCl 高;B 项:Ga 与Al 同主族,可能具有
类似性质,与NaOH 溶液反应;C 项:AlCl3 溶液中Al3+会水解,溶液呈酸性;D 项:原子半径Ga>Al>Cl。
12. C【
—解析】A 项,b 电极为阴极,发生还原反应;B 项,b 电极反应为:O2+4H
++4e
-=2H2O,
b 极附近溶液pH 增大;D 项,电极反应式为:2CH3OH+CO-2e
-=(CH3O)2CO+2H
+。
13. D【
—解析】A 项:实验1 得到的是KHA 和KCl 物质的量浓度比为1∶1 的混合溶液,HA
-在溶
液中电离大于水解,溶液呈酸性,所以pH<7;B 项:阴离子浓度最大的是Cl
-;D 项:实验3 所得溶液中
c(H
+)>c(HA
-)>c(SO
2-
4 )。
14. D.【
—解析】由方程式知,图中a,b,c 分别为H2S、H2、S2 的体积分数随温度变化的曲线。A
正确;B 选项,由图可知,温度升高,H2S 的体积分数减小,说明平衡向正反应方向移动,该反应为吸热反
第2 页共4 页
应,△H>0,根据△G=△H-T△S,△S>0,所以在高温下反应可能自发进行,B 正确;C 选项,反应温
度为1400℃时,H2S 的体积分数等于H2 的体积分数为40%,S2 的体积分数为20%,C 正确;D 选项,若
H2S 高温裂解反应在刚性密闭容器中进行,增大H2S 的投入量相当于增大压强,平衡向逆反应方向移动,
H2 的物质的量分数减小,D 不正确,符合题意。
15. (14 分,除标注外每空2 分)
(1)第四周期第ⅢA 族(1 分)
4(1 分)
(2)SiO
2-
3 、OH
-
GaAs+4K2O2+4H2O=K[Ga(OH)4]+K3AsO4+4KOH
(3)使[Ga(OH)4]
-与H
+反应生成Ga(OH)3沉淀,从而实现[Ga(OH)4]
-和AsO
3-
4 的分离
硅酸(或H2SiO3)
(4)蒸发皿(1 分)
酒精灯(1 分)
(5)28
【
—解析】
(2)根据废料中成分GaAs、Fe2O3、SiO2 和流程后面成分分析,GaAs 与K2O2 和H2O 反应生成KGa(OH)4、
K3AsO4、KOH,成分中不溶于KOH 溶液的是Fe2O3,因此浸渣是Fe2O3,浸取液含有Na+、Ga(OH)
-
4 、
AsO
3-
4 、SiO
2-
3 、OH
-,故GaAs 发生的化学反应方程式为GaAs+4K2O2+4H2O=K[Ga(OH)4]+K3AsO4+
4KOH。
(4)从溶液中获得晶体,一般经过:蒸发浓缩溶液、冷却结晶、过滤、洗涤、干燥,因此还需要的玻璃仪器有
蒸发皿、酒精灯。
(5)当c(Ga3+)<10
-5 mol/L 时,Ga3+沉淀完全,将此浓度代入Ga(OH)3 的Ksp 表达式中,计算可得
c(OH
-)>10
-9.7 mol/L,由此可知此时溶液中的c(H
+)<10
-4.3 mol/L,根据溶液混合后c(H
+)的计算等式,
可计算出加入的KOH 溶液体积约为28 mL。
16. (15 分,除标注外每空2 分)
(1)恒压滴液漏斗
检漏
(2)冷凝、回流和导气
(3)温度低于60℃,反应速率太慢,温度高于60℃,硫酸羟胺会分解
(4)放气
200δ
10
2δ
(5)否(1 分)
Ba2+要除去过量的SO
2-
4
17. (14 分,除标注外每空2 分)
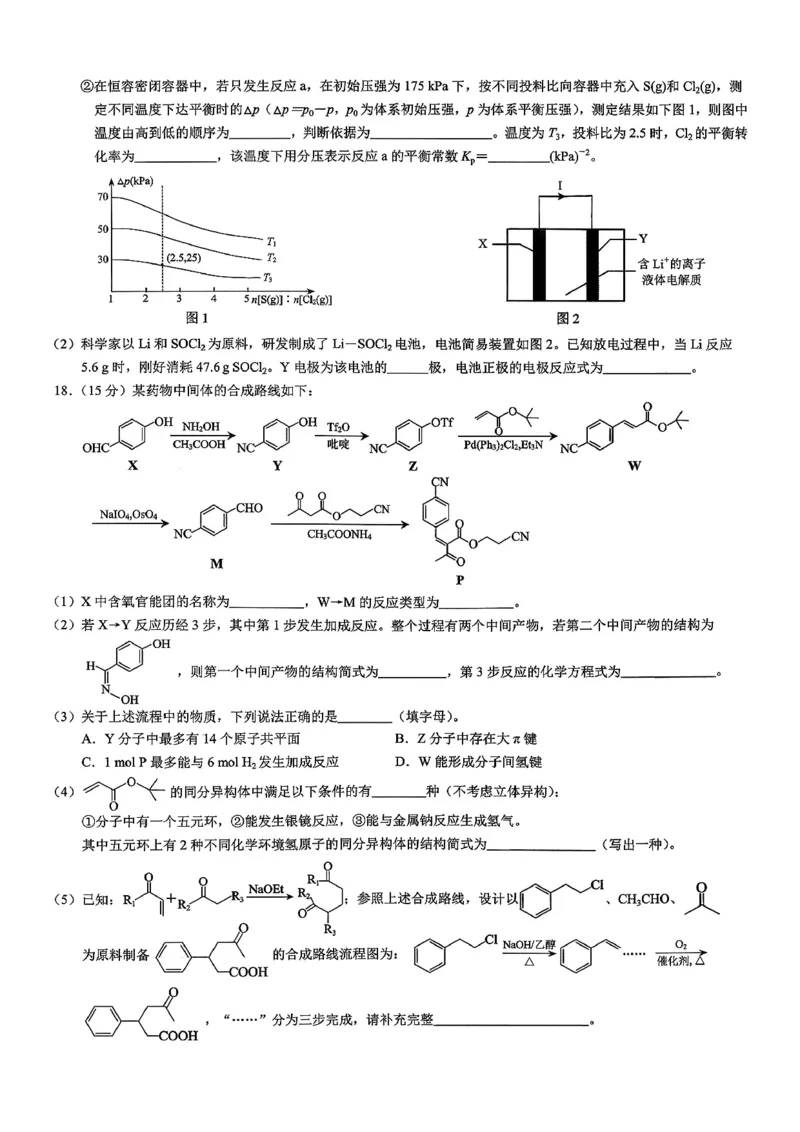
(1)①正向(1 分)
减小
②T3>T2>T1
反应放热,恒容且进料比相同的条件下,温度升高平衡逆向移动,平衡时p
增大,△p 减小,因此T3 温度最高,则T3>T2>T1
25%
1
30000
(2)负(1 分)
2SOCl2+4Li
++4e
-=S+SO2+4LiCl
【
—解析】
(1)①其他条件不变时,压缩容器容积,容器压强增大,使反应a 向正向移动,使S2Cl2(g)的浓度在因压缩容器
容积而增大的情况下,进一步增大,从而使反应b 的平衡向右移动。根据勒夏特列原理,S2Cl2(g)的平衡
体积分数将增大。
(2)温度为T3,投料比为2.5 时,△p=25;以压强为计算依据,初始压强175kPa,则p(Cl2)=50 kPa,
p(S)=125 kPa,设平衡时S2Cl2 的压强为x kPa,列三段式:
2S(g)
+
Cl2(g)
S2Cl2(g)
起始/kPa
125
50
0
转化/kPa
2x
x
x
平衡/kPa
125-2x
50-x
x
投料比为2.5 时,时△p=25kPa,则175-(175-2x)=25,x=12.5,Cl2 的转化率为12.5
50 ×100%=25%;
T3 温度下用分压表示的平衡常数Kp=
1
30000 (kPa)
-2;
(3)由电池装置可知,X 极为电池的正极,Y 极为电池的负极;根据题中数据计算可知,放电时,正极上SOCl2
转化为S、SO2,正极电极反应为2SOCl2+4Li
++4e
-=S+SO2+4LiCl。
第3 页共4 页
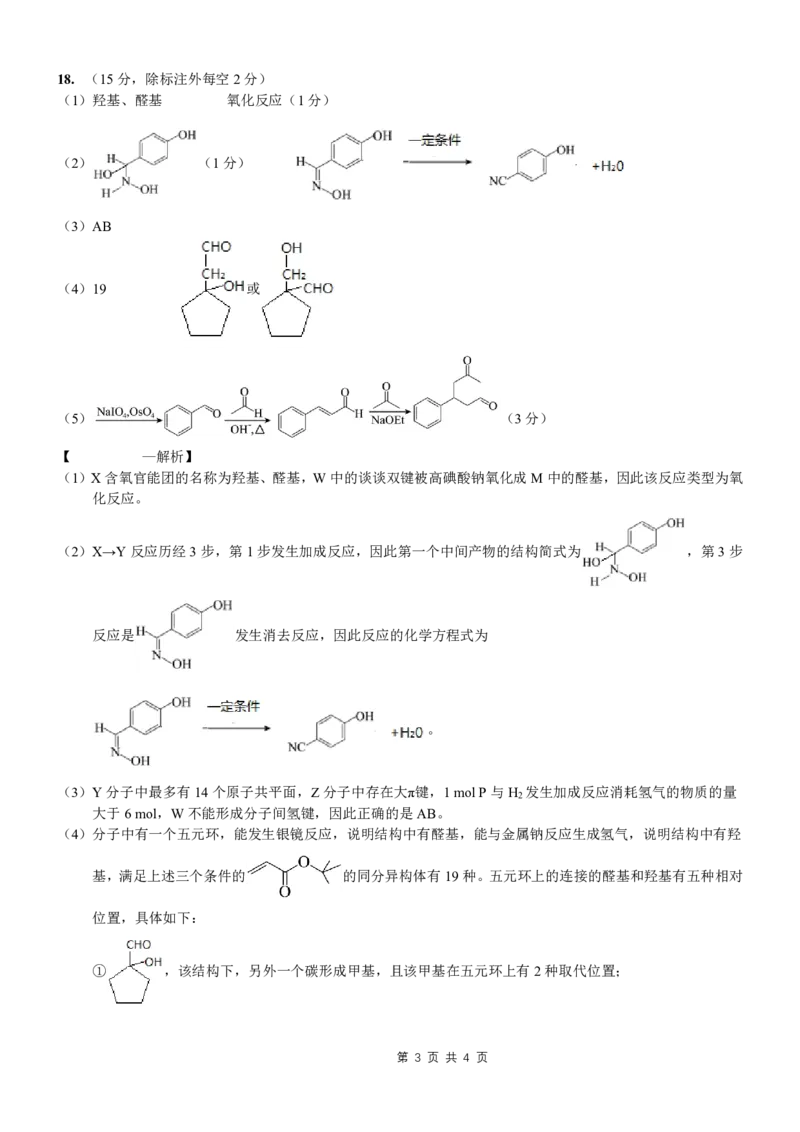
18. (15 分,除标注外每空2 分)
(1)羟基、醛基
氧化反应(1 分)
(2)
(1 分)
(3)AB
(4)19
或
(5)
(3 分)
【
—解析】
(1)X 含氧官能团的名称为羟基、醛基,W 中的谈谈双键被高碘酸钠氧化成M 中的醛基,因此该反应类型为氧
化反应。
(2)X→Y 反应历经3 步,第1 步发生加成反应,因此第一个中间产物的结构简式为
,第3 步
反应是
发生消去反应,因此反应的化学方程式为
。
(3)Y 分子中最多有14 个原子共平面,Z 分子中存在大π键,1 mol P 与H2 发生加成反应消耗氢气的物质的量
大于6 mol,W 不能形成分子间氢键,因此正确的是AB。
(4)分子中有一个五元环,能发生银镜反应,说明结构中有醛基,能与金属钠反应生成氢气,说明结构中有羟
基,满足上述三个条件的
的同分异构体有19 种。五元环上的连接的醛基和羟基有五种相对
位置,具体如下:
①
,该结构下,另外一个碳形成甲基,且该甲基在五元环上有2 种取代位置;
第4 页共4 页
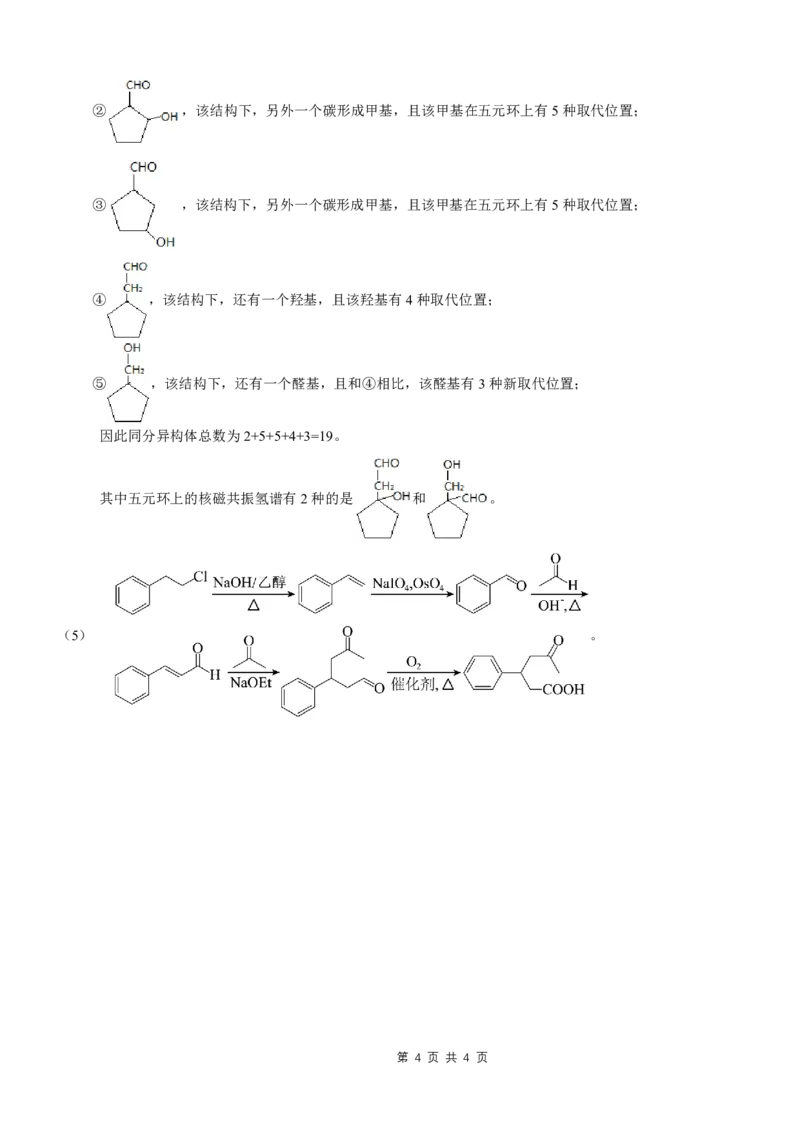
②
,该结构下,另外一个碳形成甲基,且该甲基在五元环上有5 种取代位置;
③
,该结构下,另外一个碳形成甲基,且该甲基在五元环上有5 种取代位置;
④
,该结构下,还有一个羟基,且该羟基有4 种取代位置;
⑤
,该结构下,还有一个醛基,且和④相比,该醛基有3 种新取代位置;
因此同分异构体总数为2+5+5+4+3=19。
其中五元环上的核磁共振氢谱有2 种的是
和
。
(5)
。