文档内容
陕西省咸阳市 2026 年高考模拟检测(二)化学试题
注意事项: 2026.03
1.本试卷共8页,满分100分,考试时间75 分钟。
2.答卷前,考生务必将自己的姓名和准考证号填写在答题卡上。
3.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,监考员将答题卡按顺序收回,装袋整理;试卷不回收。
可能用到的相对原子质量:H—1 Li—7 C—12 N—14 O—16 Cl—35.5
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.新质生产力以科技创新为引领,以高科技、高效能、高质量为特征。下述科技成果及发现中属于有机高分
子材料的是
A.光伏与新能源“工业黄金”——聚烯烃弹性体
B.北京科技大学研发的超高强度马氏体合金材料
C.西安交通大学研发的超级压电陶瓷
D.月壤中存在的天然单壁碳纳米管
2.下列化学用语及图示表达错误的是
A. CaO 电子式:
B.丙炔的₂键线式:
C. O 为极性分子,其空间结构为:
₃
D. Cl 分子中σ键的形成:
3.习总书
₂
记说“要在学生中弘扬劳动精神”。下列有关解释不合理的是
A.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
B.制作面点时加入食用纯碱,利用Na CO 中和发酵过程产生的酸
C.鱼缸清洁时加入 K FeO ,有杀菌消 ₂ 毒、 ₃ 净水及增氧作用
D.日常清洁中,可向 ₂84消
₄
毒液(含 NaClO)中滴加少量洁厕灵(含盐酸)
咸阳市2026年高考化学模拟检测(二)-1-(共8页)4.如图所示的有机物在抗炎、抗病毒等方面具有一定的生物活性。
下列有关该有机物的说法错误的是
A.该有机物分子中含4个手性碳原子
B.1 mol 该有机物与足量氢氧化钠溶液反应,最多消耗
2mol NaOH
C.1 mol该有机物与足量溴水反应,最多消耗3mol Br
D.该有机物发生消去反应,有机产物最多有1种(不含立体异构)
5.氢键的缔合方式为形成超分子自组装体系提供了理论基₂础。下列为2-丙烯酰胺基吡啶(M)以双重氢
键形成二聚体(N)的过程,以下说法错误的是
A.超分子晶体能够识别并吸附气体分子
B. M在酸性或碱性条件下均可发生水解
C. N中存在共价键、范德华力、氢键
D.氢键是一种较弱的化学键,在空间具有一定的方向性
6.根据下列实验陈述所得出的结论正确的是
选项 实验陈述 结论
向 FeCl 和 MgCl 的混合溶液中滴加 NaOH 溶
A
液,溶液中有红褐色沉淀产生 K [Fe(OH)₃]< K [Mg(OH)₂]
sp sp
₃ ₂
向某钾盐中滴加浓盐酸有气体产生,将该气体通入该钾盐为K SO 或 KHSO 中的至
B
品红溶液,品红溶液褪色 少一种
₂ ₃ ₃
甲苯( )、硝基苯( )一定条件
甲基、硝基对苯环不同位置氢原子
C 下分别进行硝化反应,所得主要产物分别为
的取代反应影响不同
将I (g)和H (g)的混合气体充入密闭容器中发生反
D 平衡向生成I (g)的方向移动
应,达平衡后压缩容器,混合气体颜色加深
₂ ₂
7.下列方程式错误的是
₂
A.乙酰胺在盐酸中发生反应的化学方程式: CH CON H +HCl→CH CON H Cl
3 2 3 3
B.用 CuSO 溶液除去乙炔中的 H S:Cu2++H S=CuS↓+2H+
2 2
C. NaClO 溶液中通入少量 CO :ClO−+CO +H O=HCO−+HClO
₄ 2 2 2 3
D.常温浓硝酸中以铜、铝为两极形成原电池的正极反应: NO−+2H++e−=NO ↑+H O
3 2 2
咸阳市2026年高考化学模拟检测(二)-2-(共8页)8. CCUS(CO 的捕集、利用与封存)是“十五五”碳达峰决胜期的核心技术抓手。下列灼烧 NaHCO 固
3
体并利用产物进行的实验中正确的是
₂
9.下列表格中 X 既满足如图所示转化关系,推理又正确的是
选项 X 推理
A Fe 实验室保存盐 N溶液时常加入X
B Al 反应①可用作家庭厨卫管道的疏通
C NaHSO 电解熔融盐 N时阳极得到金属钠
D (NH₄)₂S 盐 M溶液中的阴离子种类有2 种
₃
10.脑机接口(BCI)实现了人脑与机器的直接信息交流,一种信号感知与采集的共轭
导电高分子活性材料的单体结构如图所示。X、Y、Z、W是原子序数依次增大的
短周期元素,Z的最外层电子数是内层的3倍,Y、W未成对电子数相等。下列
说法正确的是
A.原子半径:W>Z>Y
B.最简单氢化物的键角:Y>W>Z
C. X、Y、Z形成的酸为二元弱酸
D. Y、Z的氢化物中可能含非极性键
11.电子级对氯甲苯可用作芯片蚀刻液的添加剂。其制备反应机理(部分物质已省略)如图所示。已知:重氮
盐超过10℃易分解;生成时需在强酸性条件下进行,以免发生副反应。
下列说法正确的是
A.加浓盐酸或用酒精灯加热可加快重氮盐生成速率
B. CuCl能降低反应活化能,但反应历程和ΔH不变
C.加入过量的 NaNO 溶液不能得到更多的重氮盐
D.过程中有极性键的断裂,但无非极性键的形成
₂
咸阳市2026年高考化学模拟检测(二)-3-(共8页)12.磷酸铁锂半固态电池在无人机供能领域有广泛应用。磷酸铁锂电池放电时工作原理如图所示(铝箔、
铜箔集流体是汇集电流的金属薄片,不参与电极反应),下列说法正确的是
放电
A.电池总反应为: xLiFePO + C xFePO +Li C
4 6 4 x 6
❑
B.放电一段时间后,LiPF₆的 DMC 有机溶液中 Li⁺浓度减小
C.充电时,电子由 M 通过导线流向 N
D.充电时通过1 mol e⁻,阴极嵌入的 Li 质量为7 g
13. Hofmann型氰氨金属笼形包合物是人形机器人感知系统的一种前沿研究材料。其四方晶胞结构如
⁺
图所示(摩尔质量为 Mg⋅mol−1,H原子均未画出,晶胞中 N原子均参与形成配位键,苯分子均处
于面心位置),NA 为阿伏加德罗常数的值。下列说法错误的是
A.化学式为 Ni(CN) ⋅Zn(N H ) ⋅2C H (C H 代表苯)
4 3 2 6 6 6 6
(1 b−c)
B. E原子的分数坐标为 ,1,
2 2
C.加热该物质时首先脱离出来的是苯
M
D.该晶体的密度为
×1030g⋅cm−3
a2bN
A
14.室温下,向含有 SnSO 的酸性溶液中通入 H S 生成 SnS 沉淀,若始终保持 H S的浓度为0.1m
2
ol/L, 体 系 中 pX[pX=-lgX,X 为 与 pH 的 关 系 如 图 所 示 , 已 知
₄ ₂
K (SnS)=10−25。下列说法错误的是
ap
c(HS−)
A.线②表示 p 随pH的变化曲线
c(H S)
2
B. Sn2++H S=SnS+2H+平衡常数为106.5
2
C. H S的K 数量级为 10−13
D. A点(c(HaS-)=10-6.2 mol/L
₂ ₂咸阳市2026年高考化学模拟检测(二)-4-(共8页)二、非选择题:本题共4 小题,共58分。
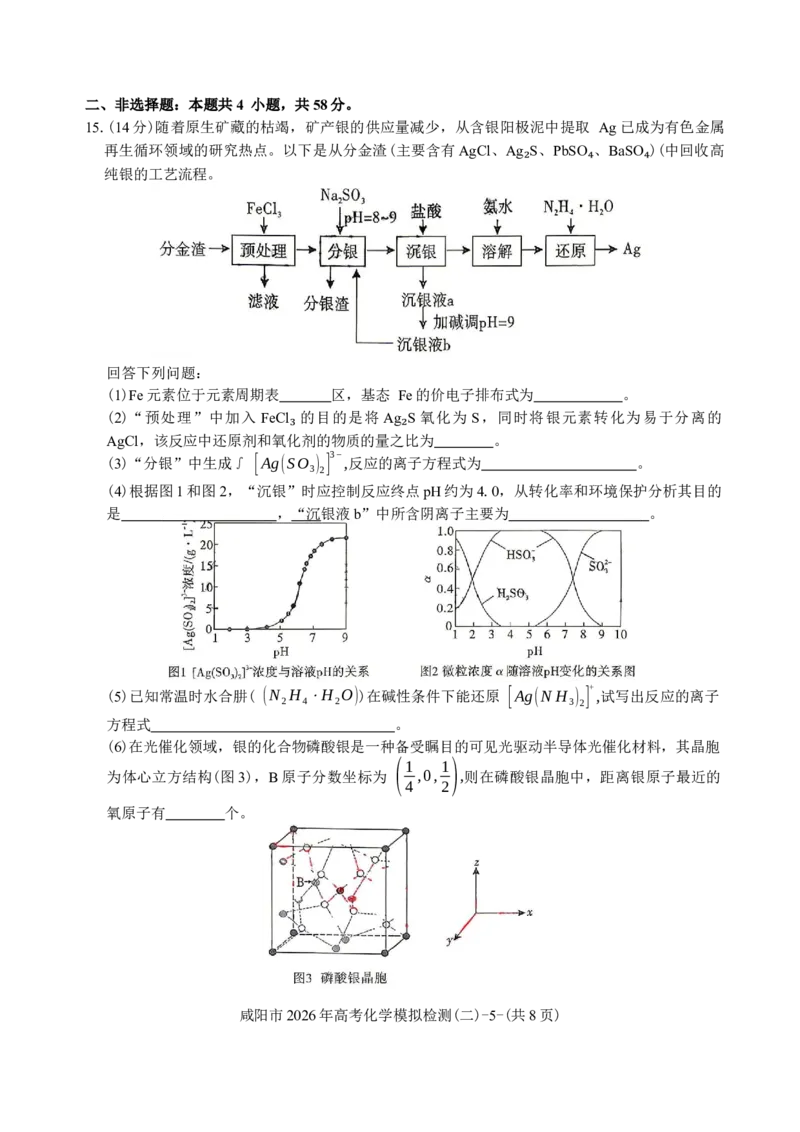
15.(14分)随着原生矿藏的枯竭,矿产银的供应量减少,从含银阳极泥中提取 Ag已成为有色金属
再生循环领域的研究热点。以下是从分金渣(主要含有AgCl、Ag S、PbSO 、BaSO )(中回收高
纯银的工艺流程。
₂ ₄ ₄
回答下列问题:
(1)Fe元素位于元素周期表 区,基态 Fe的价电子排布式为 。
(2)“预处理”中加入 FeCl 的目的是将 Ag S 氧化为 S,同时将银元素转化为易于分离的
AgCl,该反应中还原剂和氧化剂的物质的量之比为 。
₃ ₂
3−
(3)“分银”中生成∫ [Ag(SO ) ] ,反应的离子方程式为 。
3 2
(4)根据图1和图2,“沉银”时应控制反应终点pH约为4.0,从转化率和环境保护分析其目的
是 ,“沉银液b”中所含阴离子主要为 。
+
(5)已知常温时水合肼( (N H ⋅H O))在碱性条件下能还原 [Ag(N H ) ] ,试写出反应的离子
2 4 2 3 2
方程式 。
(6)在光催化领域,银的化合物磷酸银是一种备受瞩目的可见光驱动半导体光催化材料,其晶胞
(1 1)
为体心立方结构(图3),B原子分数坐标为 ,0, ,则在磷酸银晶胞中,距离银原子最近的
4 2
氧原子有 个。
咸阳市2026年高考化学模拟检测(二)-5-(共8页)16.(14分)苯甲醛是一种重要的化工原料。在 Na WO ⋅2H O催化下,用 H O 氧化苯甲醇制备苯
2 4 2 2 2
甲醛是一种环境友好的合成路线,其实验室制备原理如下:
物质 相对分子质量 熔点/℃ 沸点/℃ 溶解性
苯甲醇 108 -15.3 205.7 微溶于水,易溶于醇、醚
苯甲醛 106 -26 178 微溶于水,易溶于醇、醚
甲基叔丁基醚 88 -114.3 55 不溶于水,易溶于醇、醚
已知: (C H ) NHSO 为相转移催化剂,其作用机制是“离子的搬运”。
4 9 4 4
反应装置(加热、夹持等装置略)如图:
实验步骤:
①向反应容器 A 中,依次加入( (C H ) NHSO 0.2g,,钨酸钠0.2g,30% H O 7.5
4 9 4 4
mL(0.069 mol)和H O10 mL,磁力搅拌5m in,再加入苯甲醇6.5mL(6.5g),90℃水
₂ ₂
浴搅拌反应3h。
₂
②反应完成后,冷却,分出油层,用甲基叔丁基醚萃取水层2~3次。
③合并油层与醚层,用10 mL饱和 Na S O 溶液洗涤除去未反应的 H O ,再用
2 2 3 2 2
MgSO 进行干燥。
4
④常压蒸馏回收甲基叔丁基醚。用真空泵抽气减压蒸馏收集馏分,即可得到产品,约
0.5g。
回答以下问题:
(1)仪器B的名称是 ,进水口为 (填“a”或“b”)。
(2)步骤①中使用( (C H ) NHSO ,,其原因可能是 (填字母)。
4 9 4 4
A. (C H ) NHSO 作为氧化剂,参与苯甲醇的氧化反应
4 9 4 4
B. (C H ) N+ 与 WO2−在水相结合得到 [(C H ) N+] WO
4 9 4 4 4 9 4 2 4
C. (C H ) N+ 具有亲油性,可以将 WO2−从水相转移至有机相,加快反应
4 9 4 4
D. (C H ) NHSO 能改变反应平衡常数,使反应正向进行程度增大
4 9 4 4
(3)步骤②中萃取过程中所使用的玻璃仪器有 。用甲基叔丁基醚萃取水层的目
的是 。
(4)检验步骤③中是否残留 H O 的方法是:取出少量洗涤后的溶液于试管中,加入少量淀粉-KI溶
2 2
液(酸性),观察到溶液变蓝,其反应的离子方程式为 。
(5)步骤④使用减压蒸馏收集产品,其优势可能是 。
(6)本实验中苯甲醛的产率为 %(保留一位小数)。
17.(15分)甲醇水蒸气重整(MSR)是重要的制氢反应(反应Ⅰ),可分解为两个半反应(甲醇脱氢和水煤
气转化反应即反应Ⅱ和反应Ⅲ)。已知:
反应Ⅰ: CH OH(g)+H O(g)CO (g)+3H (g) △H =+49.5kJ·mol−1
3 2 2 2 1
反应Ⅱ: CH OH(g)CO(g)+2H (g) △H =+90.7kJ·mol−1
3 2 2
反应Ⅲ: CO(g)+H O(g)CO (g)+H (g) △H =−41.2kJ·mol−1
2 2 2 3
咸阳市2026年高考化学模拟检测(二)-6-(共8页)回答下列问题:
(1) 若 反 应 Ⅰ 的 正 反 应 活 化 能 为 akJ⋅mol−1,则 逆 反 应 的 活 化 能 为
kJ·mol⁻¹。反应Ⅰ在 (填“高温”“低温”或“任意温度”)下可自发进行。
(2)CH OH和 CO 分子中C 原子与下列物质中心原子杂化轨道类型对应的是 (填
3 2
字母)。
A. H S和H O B. PCl 和 HCN G. SO 和SO D. NH 和O
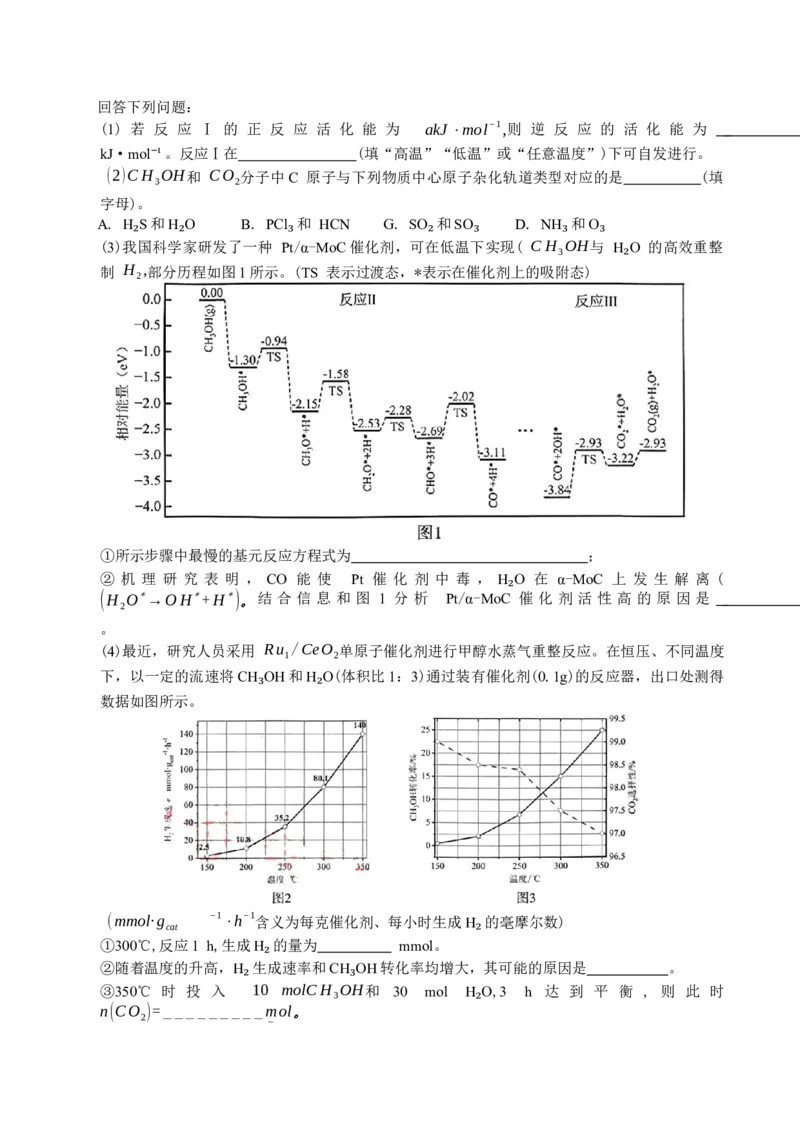
(3)我国科学家研发了一种 Pt/α-MoC催化剂,可在低温下实现( CH OH与 H O 的高效重整
₂ ₂ ₃ ₂ ₃ 3₃ ₃
制 H ,部分历程如图1所示。(TS 表示过渡态,*表示在催化剂上的吸附态)
2 ₂
①所示步骤中最慢的基元反应方程式为 ;
② 机 理 研 究 表 明 , CO 能 使 Pt 催 化 剂 中 毒 , H O 在 α-MoC 上 发 生 解 离 (
(H O∗→OH∗+H∗)。结 合 信 息 和 图 1 分 析 Pt/α-MoC 催 化 剂 活 性 高 的 原 因 是
2
₂
。
(4)最近,研究人员采用 Ru /CeO 单原子催化剂进行甲醇水蒸气重整反应。在恒压、不同温度
1 2
下,以一定的流速将CH OH和H O(体积比1:3)通过装有催化剂(0.1g)的反应器,出口处测得
数据如图所示。
₃ ₂
(mmol·g −1 ⋅h−1含义为每克催化剂、每小时生成H 的毫摩尔数)
cat
①300℃,反应1 h,生成H 的量为 mmol。
₂
②随着温度的升高,H 生成速率和CH OH转化率均增大,其可能的原因是 。
₂
③350℃ 时 投 入 10 molCH OH和 30 mol H O,3 h 达 到 平 衡 , 则 此 时
₂ 3 ₃
n(CO )=_________mol。
2
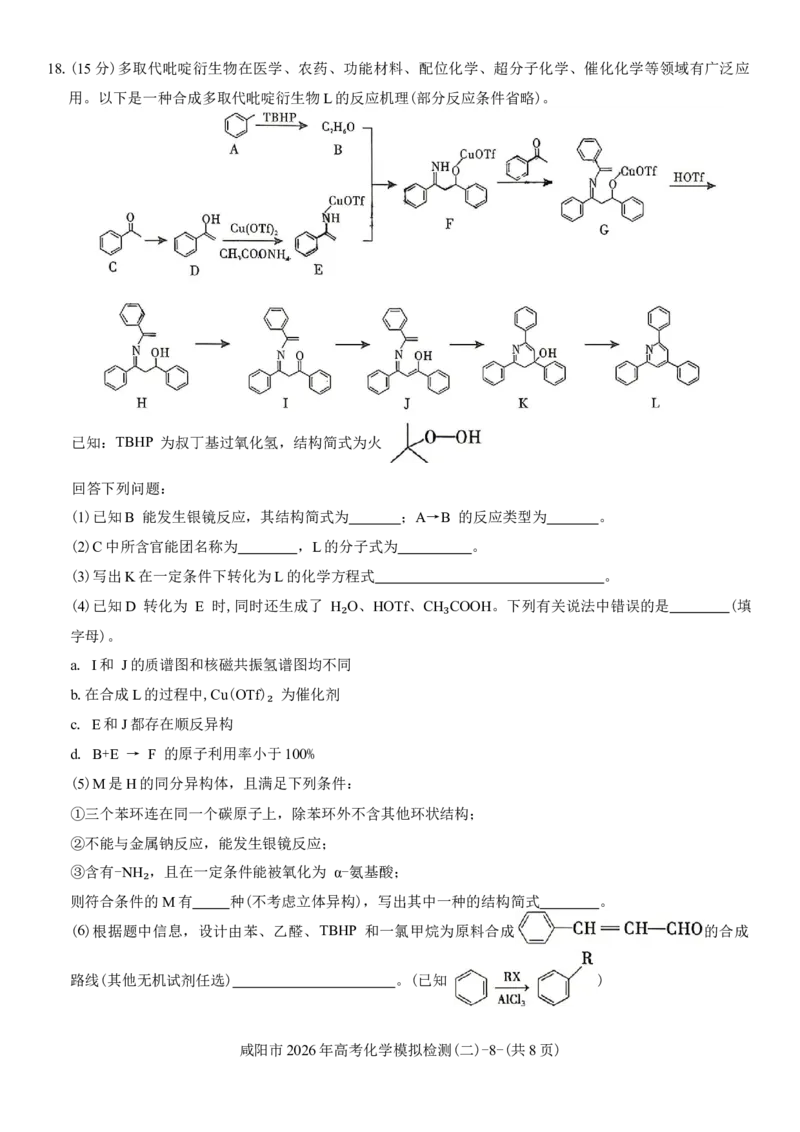
¯ ₂咸阳市2026年高考化学模拟检测(二)-7-(共8页)18.(15分)多取代吡啶衍生物在医学、农药、功能材料、配位化学、超分子化学、催化化学等领域有广泛应
用。以下是一种合成多取代吡啶衍生物L的反应机理(部分反应条件省略)。
已知:TBHP 为叔丁基过氧化氢,结构简式为火
回答下列问题:
(1)已知B 能发生银镜反应,其结构简式为 ;A→B 的反应类型为 。
(2)C中所含官能团名称为 ,L的分子式为 。
(3)写出K在一定条件下转化为L的化学方程式 。
(4)已知D 转化为 E 时,同时还生成了 H O、HOTf、CH COOH。下列有关说法中错误的是 (填
字母)。 ₂ ₃
a. I和 J的质谱图和核磁共振氢谱图均不同
b.在合成L的过程中,Cu(OTf) 为催化剂
c. E和J都存在顺反异构
₂
d. B+E → F 的原子利用率小于100%
(5)M是H的同分异构体,且满足下列条件:
①三个苯环连在同一个碳原子上,除苯环外不含其他环状结构;
②不能与金属钠反应,能发生银镜反应;
③含有-NH ,且在一定条件能被氧化为 α-氨基酸;
则符合条件
₂
的M有 种(不考虑立体异构),写出其中一种的结构简式 。
(6)根据题中信息,设计由苯、乙醛、TBHP 和一氯甲烷为原料合成 的合成
路线(其他无机试剂任选) 。(已知 )
咸阳市2026年高考化学模拟检测(二)-8-(共8页)2026 年高考模拟检测(二)
化学试题参考答案及评分标准
一、选择题:本题共14小题,每小题3分,共42分。
1. A 2. B 3. D 4. C 5. D 6. C 7. A 8. C 9. B 10. D11.
C 12. D 13. B 14. B
二、非选择题:本题共4小题,共58分。
15.(14分)
(1)d(1分) 3d⁶4s²(1分)
(2)1:2(2分)
(3)AgCl+2SO2−[Ag(SO ) ] 3− +Cl−(2分)
3 3 2
3−
(4)使溶液中的 [Ag(SO ) ] 尽可能转化为 AgCl沉淀,同时不产生污染性气体SO (2
3 2
分)SO²⁻(2分) ₂
(5)4[Ag(N H ) ] + +N H ⋅H O+4OH−4 Ag↓+N ↑+8N H ↑+5H O
3 2 2 4 2 2 3 2
(或 4[Ag(N H ) ] + +N H +4OH−4 Ag↓+N ↑+8N H ↑+4H O
3 2 2 4 2 3 2
4[Ag(N H ) ] + +N H +4OH−+4H O 4 Ag↓+N ↑+8N H ⋅H O
3 2 2 4 2 2 3 2
4[Ag(N H ) ] + +N H +4OH−+4H O 4 Ag↓+N ↑+8N H ⋅H O(2分)(6)4(2
3 2 2 4 2 2 3 2
分)
16.(14分)
(1)恒压滴液漏斗(1分)b(1分)
(2)BC(2分)
(3)分液漏斗、烧杯(2分)将水层中溶解的苯甲醛提取到有机相,减少产物损失(2分)
(4)H O +2I−+2H+ I +2H O(2分)
2 2 2 2
(5)苯甲醛沸点较高,减压蒸馏可降低其沸点,避免其热分解或被氧化(2分)
(6)7.8(2分)
17.(15分)
(1)a-49.5(2分) 高温(1分)
(2)B(2分)
(3)CO∗+2OH∗=CO∗+H O∗(2分)
2 2
②Pt/α-MoC催化剂中,水解离生成OH⁺,OH⁺与CO反应生成CO ,防止 Pt中毒,提高了催化活性(2分)
(4)①8.01(2分)
₂
②温度升高,反应速率加快,单位时间生成的H 增多;流速一定下转化的CH OH也越多,即转化率增大
(2分)
₂ ₃
③2.425(2分)
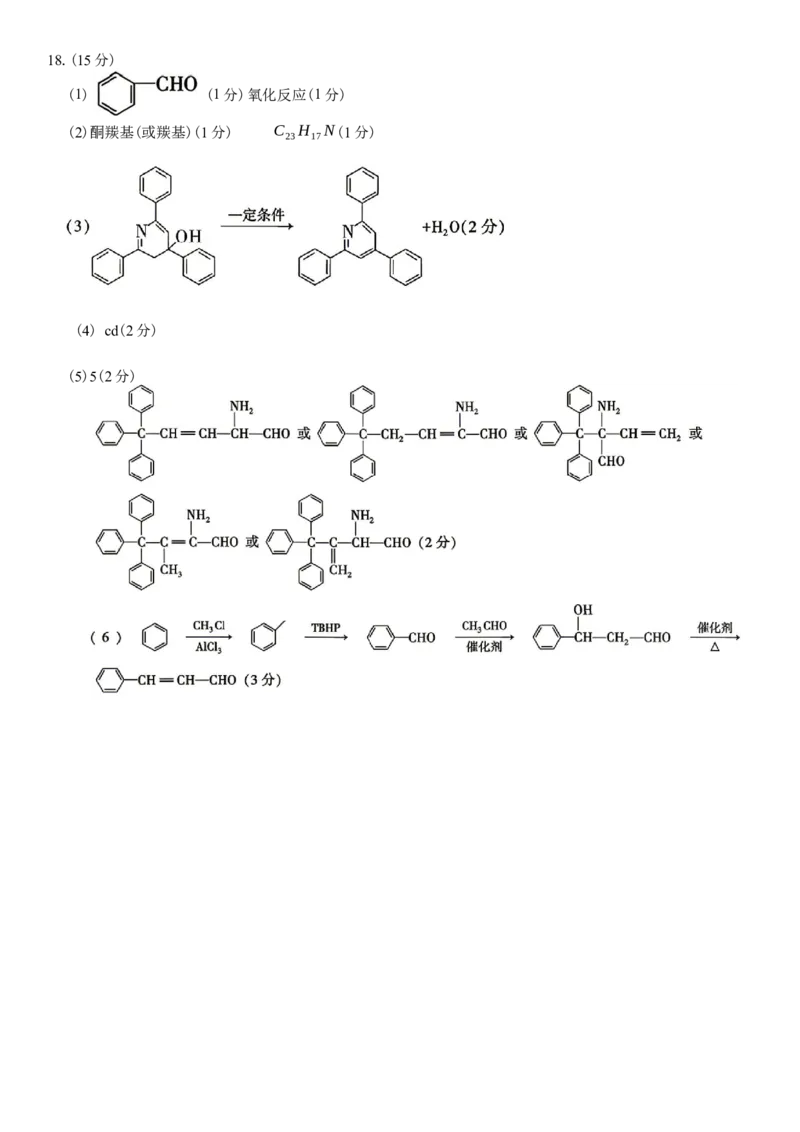
2026年高考化学模拟检测(二)-答案-1(共2页)18.(15分)
(1) (1分)氧化反应(1分)
(2)酮羰基(或羰基)(1分) C H N(1分)
23 17
(4) cd(2分)
(5)5(2分)