文档内容
第1 页共3 页
重庆市2026 届高考模拟调研卷(四)
化学答案
1~5 DCAAC
6~10 DBCDD
11~14 ACCD
1.
略
2.
C【
—解析】A.丁达尔效应不能用于分离提纯物质;B.纯净的H2 在Cl2 中燃烧产生苍白色的
火焰;C.用稀硝酸可与银反应,生成硝酸银、NO 和H2O;D.酸性KMnO4 溶液可以与FeCl2 溶液中的Cl
-发生氧化还原反应。
3.
A【
—解析】B.基态原子第一电离能:F>N;C.C 原子的杂化方式有2 种;D.基态Cu 原子
的价层电子排布式为3d104s1。
4.
A【
—解析】A.Na
+、K
+、MnO
-
4 、SO
2-
4 四种离子之间不反应,虽MnO
-
4 有色,但是澄清透明,
A 符合题意;B.H2O2 和HSO
-
3 会反应,HSO
-
3 和[Al(OH)4]
-也会反应,不能大量共存,B 不符合题意;C.使
酚酞变红的溶液显碱性,Fe2+和OH
-反应会生成Fe(OH)2 沉淀,不能大量共存,C 不符合题意;D.pH<7
的溶液显酸性,H
+和CH3COO
-会发生反应生成CH3COOH,不能大量共存,D 不符合题意。
5.
C【
—解析】HClO 的电子式为:
。
6.
D【
—解析】A.溶液体积未知,无法计算。B.11.2 g Fe 为0.2 mol,反应中Fe 从0 价升至+2 价,
转移电子0.4 mol,即0.4 NA。C.未注明6.72 L 气体的外界条件,无法计算。D.每个[Fe(CN)6]4-中,含6 个
Fe-C σ键和6 个C≡N σ键,每个C≡N 含1 个σ键,共12 个σ键,0.5 mol [Fe(CN)6]4-含6 mol σ键,即6 NA。
7.
B【
—解析】A.温度、催化剂均能加快反应速率,由探究实验变量唯一化的原则可知,装置①
不能达到验证氯化铁对过氧化氢分解反应有催化作用的实验目的,A 不符合题意;B.Al2(SO4)3 水解生成氢
氧化铝和硫酸,加热虽促进水解但硫酸属于难挥发性酸,氢氧化铝会溶于硫酸,则蒸发Al2(SO4)3 溶液制备
无水Al2(SO4)3,B 符合题意;C.用盐酸滴定含有酚酞的NaOH 溶液时,应该用左手操作酸式滴定管的旋钮,
右手慢慢摇晃锥形瓶,图中用右手拧旋钮,C 不符合题意;D.H2(g)+I2(g)
2HI(g)为反应前后气体总物
质的量不变的反应,改变压强平衡不移动,D 不符合题意。
8.
C【
—解析】D.Y 和Z 在酸性条件下完全水解得到的产物结构简式为
。
9.
D【
—解析】由题意推得元素X、Y(Z)、W、M 分别为C、H、N、O。A.非金属性:O>C>H;
B.O 无最高正价;
C.Y 与Z 互为同位素;D.由C、H、N、O 可形成(NH4)2CO3、NH4HCO3 等离子化
合物。
10. D【
—解析】D.IO
-
3 与I
-需在酸性条件下才能发生反应。
11. A【
—解析】A.晶胞中Cs
+位于体心,Pb2+位于顶点,I
-位于棱心,化学式为CsPbI3;B.与Cs
+
等距离且最近的Cs
+应为6 个;C.掺杂M2+取代Pb2+后,配位数应为6(八面体配位),不是8;D.NA=
24
3
2.163 10
3
8a
ρ
。
12. C【
—解析】A.NO
-
3 +8e
-+10H
+=NH
+
4 +3H2O 是还原反应,应该在正极上发生;
B.双极
膜中H
+在电场作用下移向正极;
C.催化电极区域,pH 变大;
D.产生0.1 mol NH
+
4 时,转移0.8 mol
电子,锌电极区Zn2+增加0.4 mol,质量增加0.4×65+0.8×17=39.6 g。
13. C【
—解析】根据题意可知I 为X2-的分布系数,II 为HX
-的分布系数。A.a 点数据计算可知Ka2
=10
-4.2;B.a、b、c 三点随加入NaOH 溶液增加,NaHX 逐渐消耗,到c 点完全反应生成Na2X,水的电离
程度逐渐增大;C.c 点溶液中的溶质为Na2X:c(Na
+)=2[c(HX
-)+c(X2-)+c(H2X)]
D.b 点溶液中为物质的
量浓度1∶1 的Na2X 与NaHX 溶液,根据电荷守恒有:c(Na
+)+c(H
+)=c(OH
-)+c(HX
-)+2c(X2-),b 点溶液
pH<7,c(H
+)>c(OH
-),故c(Na
+)<c(HX
-)+2c(X2-)。
14. D
—解析】平衡时通入Ar,气体的物质的量浓度不变,平衡不移动;体积变大,平衡正向移动,
达平衡时气体的物质的量浓度不变,c[CO2(g)]=0.4 mol/L,若c[CO2(g)]=0.3 mol/L 时已达平衡,说明固体反
应完全,故此时a=0.3×2×222=133.2;体积压缩为0.5L,平衡逆向移动,平衡时c[CO2(g)]=0.4 mol/L,固
第2 页共3 页
体增加的质量为反应的气体质量,即为12.4g;通入等物质的量的H2O 和CO2,平衡逆向移动,再次平衡时
c[H2O(g)]=c[CO2(g)]=0.4 mol/L。
15.(14 分,除标注外每空2 分)
(1)增长(1 分)
6(1 分)
(2)搅拌、适当升温、适当增大硫酸浓度等
(3)CaF2、MgF2
平面三角形(1 分)
(4)RuO4+2SO
2-
3 +4H
+=Ru4++2SO
2-
4 +2H2O
(5)排除空气,防止Ru 被氧化(1 分)
Ru(C2O4)2
4CO2↑+Ru
(6)0.01
16.(15 分,除标注外每空2 分)
(1)检查装置的气密性
直形冷凝管(1 分)
(2)平衡气压,防止堵塞
缓冲作用
(3)[Cu(NH3)4]2+
(4)防止NH3 挥发
(5)B4O
2-
7 +2H
++5H2O=4H3BO3
(6)3.28
【
—解析】(6)15mL 中,n(N)=n(NH3)=n(HCl)=22.5×10
-3×0.01000=2.25×10
-4 mol
250mL 中,n(N)=2.25×10
-4× 250
15 =3.75×10
-3 mol
w(蛋白质)=3.75×10
-3×14× 100
10 ×
1
16% =3.28g/100g。
17.(14 分,除标注外每空2 分)
(1)bd(1 分)
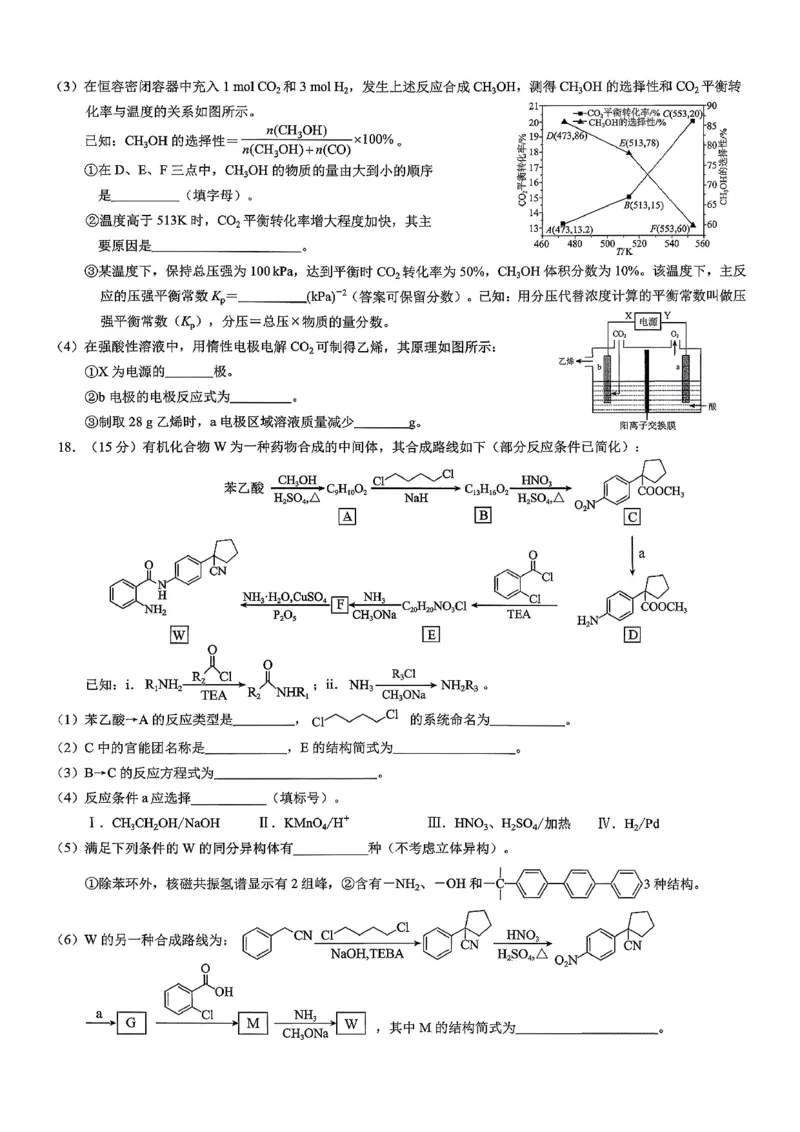
(2)增大体系压强、增大CO2 和H2 的进气量、及时分离出CH3OH
(3)①F>E>D
②随着温度升高,主反应向右移动的程度大于副反应向左移动的程度
③
3
10
55
(4)①负(1 分)
②2CO2+12e
-+12H
+=C2H4+4H2O
③108
解析:(3)③设反应生成CH3OH 的物质的量为x mol,生成CO 的物质的量为y mol。
CO2(g)+3H2(g)
CH3OH(g)+H2O(g)
起始(mol)
1
3
转化(mol)
x
3x
x
x
CO2(g)+H2(g)
CO(g)+H2O(g)
转化(mol)
y
y
y
y
气体总物质的量为4-2x,由题意得:
0.5
0.1
4
2
x
y
x
x
,解得x=1
3
,y=1
6
,
则达平衡时各物质的物质的量:n(CO2)=0.5mol,n(H2)=11
6
mol,n(H2O)=0.5mol,
n(CH3OH)=1
3
mol,n(CO)=1
6
mol,n 总=10
3
mol。
第3 页共3 页
Kp
3
3
1
0.5
3
(
100)
(
100)
10
10
10
3
3
11
55
0.5
6
(
100)
(
100)
10
10
3
3
。
(4)因为左侧电极反应为:2CO2+12e
-+12H
+=C2H4+4H2O ,生成28 g 乙烯转移12 mol e
-,右侧电极反应
式为:2H2O-4e
-=O2↑+4H
+,右侧电极区域溶液质量减少为放出的O2 质量与移到左侧的H
+质量之和,
即3×32+12=108g。
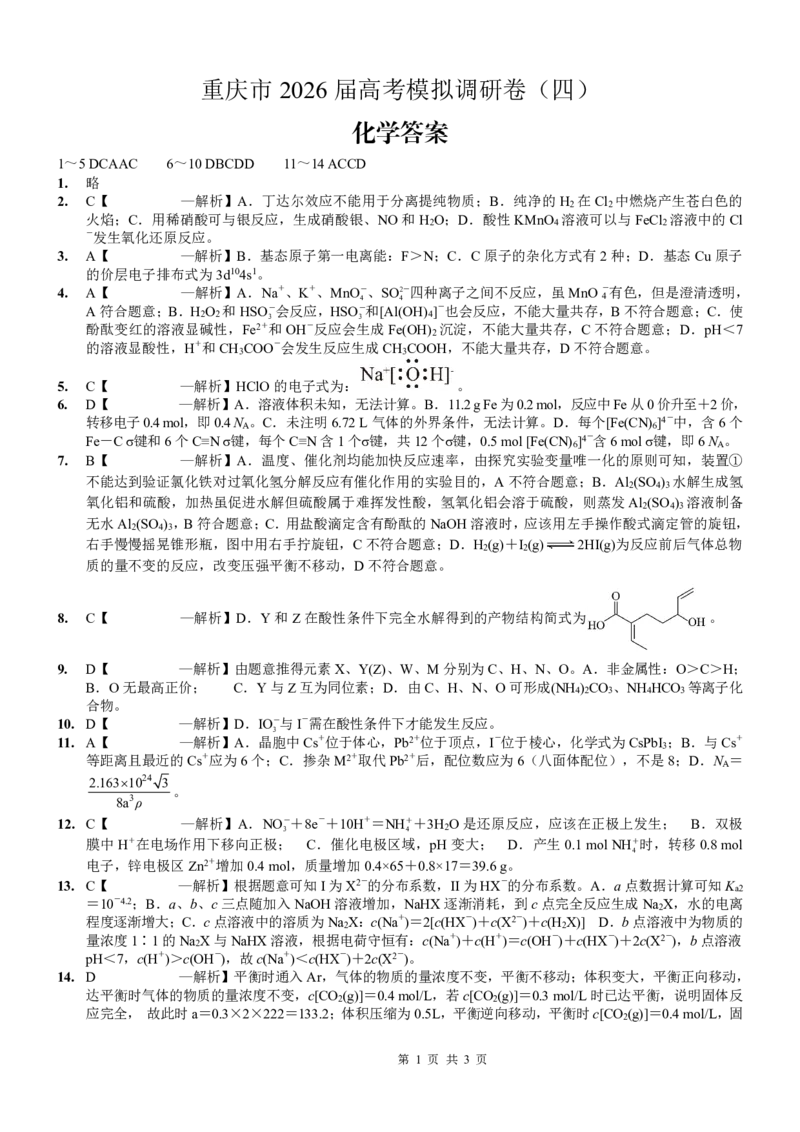
18.(15 分,除标注外每空2 分)
(1)取代反应或酯化反应(1 分)
1,4-二氯丁烷
(2)硝基、酯基;
(3)
(4)Ⅳ
(5)7
(6)
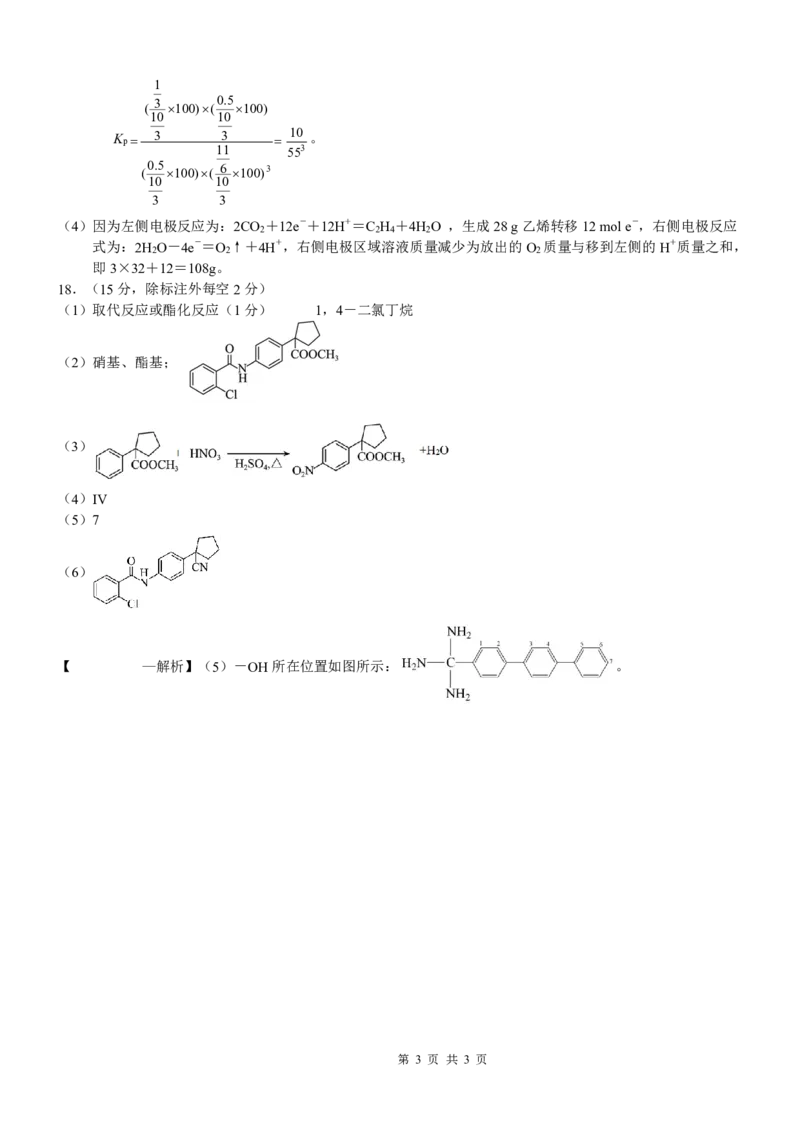
【
—解析】(5)-OH 所在位置如图所示:
。