文档内容
2025-2026 学年度秋学期期中联考试卷
高一化学
1.本试卷分为选择题和非选择题两部分,共100分,考试时间75分钟。
2.请把选择题和非选择题的答案均填写在答题卷的指定栏目内。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5
第Ⅰ卷 选择题(共39分)
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.中国科学家首次发现Ni O,高温超导体系Ni O 属于
x y x y
A. 氧化物 B. 酸 C. 碱 D. 盐
2.下列化学用语使用正确的是
A. Na+的结构示意图 B. 明矾的化学式: KAlSO •12H O
4 2
C. O 与O 互为同素异形体 D. Al (SO ) 的电离:Al (SO ) === Al3++SO
2 3 2 4 3 2 4 3
3.氧化还原反应与四种基本反应的关系如图。则下列化学反应中属于阴影部分的是
A.C+O ===== CO
2 2
B.Zn+CuSO === Cu+ZnSO
4 4
C.2NO+2CO ===== N+2CO
2
D.NH HCO ==== NH ↑+H O+CO↑
4 3 3 2 2
4.下列实验装置能达到实验目的的是
A B C D
将剩余钠放回试剂 比较NaCO、NaHCO 的稳
制备氧化钠 除去CO 中的HCl 2 3 3
瓶 2 定性
5.下列变化需要加入还原剂才能完成的是
A.Fe O → Fe B.NO → NO C.Fe → FeCl D.HCO → CO
2 3 3 2
6.在给定条件下,下列选项所示物质间转化能实现的是A. CuO ——————→Cu(OH) B. Cl ————→FeCl
2 2 3
C. Fe ————→Fe O D. 熔融NaCl ———→Na
2 3
7.下列有关物质性质与用途具有对应关系的是
A. 钠有还原性,可用于冶炼金属钛
B. Cl 具有氧化性,可使干燥有色布条褪色
2
C. 过氧化钠为淡黄色固体,可用作呼吸面具中的供氧剂
D. 次氯酸具有酸性,可用于杀菌消毒
8.下列各组离子能大量共存的是
A. OH-、NO、K+、HCO B. NH、Mg2+、Cl-、SO
C. H+、Na+、CO、Cl- D. Mg2+、OH-、NO 、 Cl-
9.下列离子方程式书写正确的是
A.硫酸与Ba(OH) 溶液反应:Ba2++OH-+H++SO = BaSO↓+HO
2 4 2
B.钠与硫酸铜溶液的反应:2Na+2HO = 2OH-+2Na++H↑
2 2
C.NaO 与HO反应制备O:2NaO+2HO = 4Na++4OH-+O↑
2 2 2 2 2 2 2 2
D.氯气溶于水的反应:Cl+HO = 2H++Cl-+ClO-
2 2
10.下列实验操作得出实验结论不正确的是
选项 实验操作与现象 实验结论
将硫的酒精溶液滴入一定量的热水中得淡蓝色透明
A 淡蓝色液体属于胶体
液体,用激光笔照射,有光亮的通路
B 湿润 淀的粉碘化钾试纸遇氯气变蓝 氯气的氧化性比碘强
C 向某溶液中滴加BaCl 溶液,产生白色沉淀 该溶液中一定含有
2
用洁净铂丝蘸取某样品在酒精灯火焰上灼烧,透过
D 样品可能为钾盐
蓝色钴玻璃观察,火焰显紫色
11. N 为阿伏加德罗常数的值。下列说法正确的是
A
A.水的摩尔质量为18g
B.32 g O 与O 的混合气体中,氧原子数为2N
2 3 A
C.将1mol NaSO 溶于水配成溶液,溶液中的氧原子数4N
2 4 A
D.22.4LN 的质量为28g
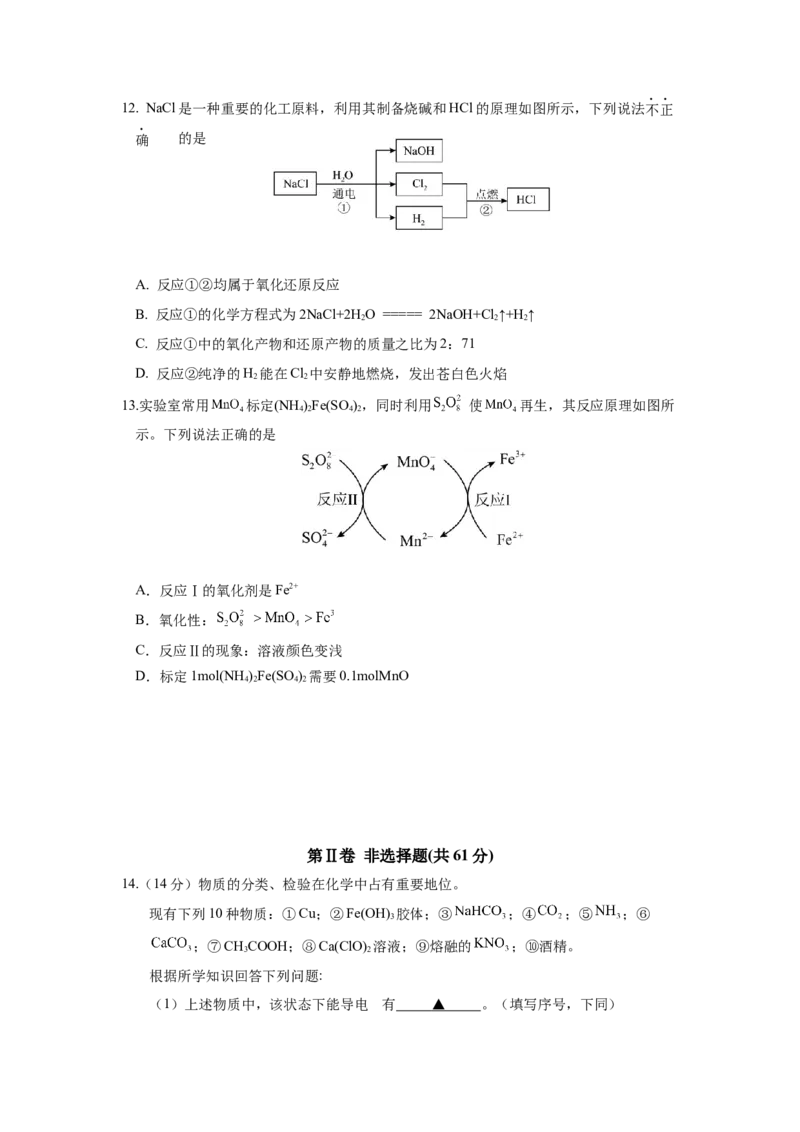
212. NaCl是一种重要的化工原料,利用其制备烧碱和HCl的原理如图所示,下列说法不正
确 的是
A. 反应①②均属于氧化还原反应
B. 反应①的化学方程式为2NaCl+2H O ===== 2NaOH+Cl ↑+H ↑
2 2 2
C. 反应①中的氧化产物和还原产物的质量之比为2:71
D. 反应②纯净的H 能在Cl 中安静地燃烧,发出苍白色火焰
2 2
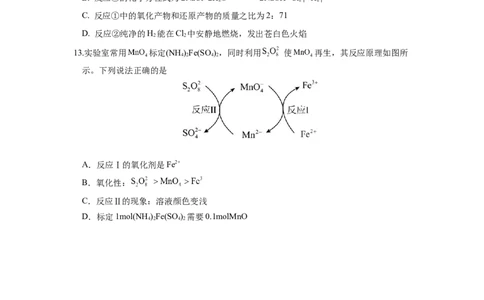
13.实验室常用 标定(NH )Fe(SO ),同时利用 使 再生,其反应原理如图所
4 2 4 2
示。下列说法正确的是
A.反应Ⅰ的氧化剂是Fe2+
B.氧化性:
C.反应Ⅱ的现象:溶液颜色变浅
D.标定1mol(NH)Fe(SO ) 需要0.1molMnO
4 2 4 2
第Ⅱ卷 非选择题(共61分)
14.(14分)物质的分类、检验在化学中占有重要地位。
现有下列10种物质:①Cu;②Fe(OH) 胶体;③ ;④ ;⑤ ;⑥
3
;⑦CHCOOH;⑧Ca(ClO) 溶液;⑨熔融的 ;⑩酒精。
3 2
根据所学知识回答下列问题:
(1)上述物质中,该状态下能导电 有的 ▲ 。(填写序号,下同)(2)属于电解质的是 ▲ 。
(3)写出⑧在水中的电离方程式 ▲ 。
(4)制备物质②的方法是:在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中
滴入几滴饱和FeCl ,继续煮沸至溶液呈红褐色,即制得 胶体。
3
化学反应方程式 ▲
胶体和溶液的本质区别是 ▲ (填选项)
a. 分散剂不同 b. 丁达尔效应 c. 分散质粒子直径大小不同
(5)在标准状况下,17g 所含的电子数约为 ▲ ,它与标准状况下与 ▲
L硫化氢含有相同数目的氢原子。
15.(15分)国际化学年的中国宣传口号是“化学−我们的生活,我们的未来”。学习化学
应该明白“从生活中来,到生活中去”道理。请填空:
(1)小苏打可治疗胃酸过多,其反应的离子反应方程式为 ▲ 。
(2)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2HS+O=2Ag S+2HO。
2 2 2 2
用双线桥标出上述方程式的电子转移方向和数目 ▲ 。
(3)火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应
2KNO+3C+S===KS+N↑+3CO ↑,其中还原产物是 ▲ 。
3 2 2 2
(4)人体内铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,
可使Fe3+转化成Fe2+,说明维生素C具有 ▲ 。(填“氧化性”或“还原
性”)。
(5)在潜水艇和消防员的呼吸面具中都有NaO,NaO 与CO 所发生反应的化学方
2 2 2 2 2
程式为 ▲ 。
(6)配平的化学方程式。
▲ Fe(NO ) + ▲ HNO = ▲ NO ↑ + ▲ Fe(NO ) + ▲ HO
3 2 3 3 3 2
16.(16分)联合制碱法(又称侯氏制碱法),因其提高了食盐的转化率,减少了对环境的
污染,从而赢得了国际化工界的高度评价。联合制碱法的主要过程如图所示:已知:沉淀池中的反应原理如下:NH +CO +H O+NaCl === NaHCO ↓+NHCl
3 2 2 3 4
(1)“侯氏制碱法”中从沉淀池分离出母液的操作是 ▲ ,从母液中提取的副产
品为 ▲ 。(填化学式)
(2)煅烧炉中反应的化学方程式为 ▲ 。
(3)在饱和食盐水中先通入NH ,再通入CO,这样操作的目的是 ▲ 。(填选
3 2
项)
a.NH 比CO 更易制取
3 2
b.NH 极易溶于水,使CO 更易被吸收,加快反应速率
3 2
c.CO 的密度比NH 大
2 3
(4)制得的碳酸钠样品中往往含有少量的NaCl,检验样品中含有NaCl的操作及现象为
▲ 。
(5)将0.84gNaHCO 和1.06gNa CO 混合并配成溶液,向溶液中滴加稀盐酸至过量。计
3 2 3
算标准状况下产生CO 的体积 ▲ 。(写出计算过程)
2
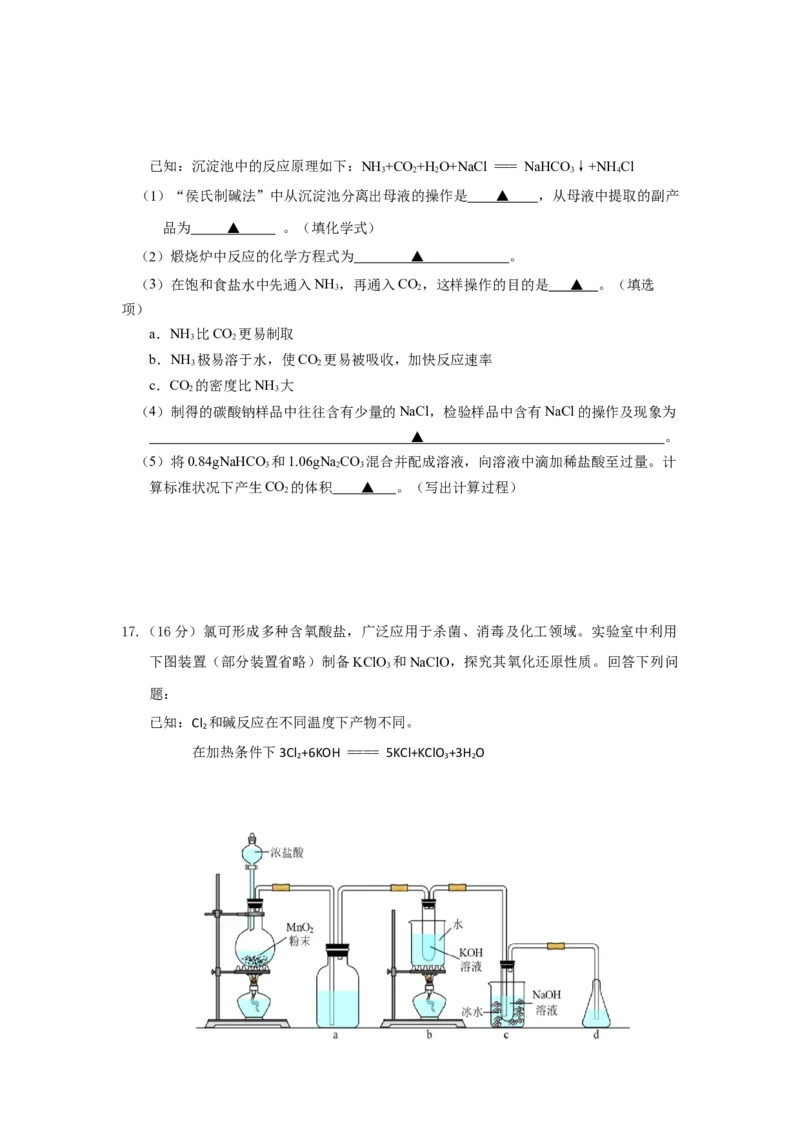
17.(16分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用
下图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。回答下列问
3
题:
已知:Cl 和碱反应在不同温度下产物不同。
2
在加热条件下3Cl +6KOH ==== 5KCl+KClO +3H O
2 3 2图1
(1)制备氯气的化学方程式为 ▲ ,a中的试剂为 ▲ 。
(2)b中发生的反应为3Cl +6KOH ==== 5KCl+KClO +3H O,每生产1molKClO 转移的电子
2 3 2 3
的物质的量为 ▲ 。
(3)c中发生化学反应的离子方程式是 ▲ 。
c的采用冰水浴冷却的目的是 ▲ 。
(4)d的作用是 ▲ 。
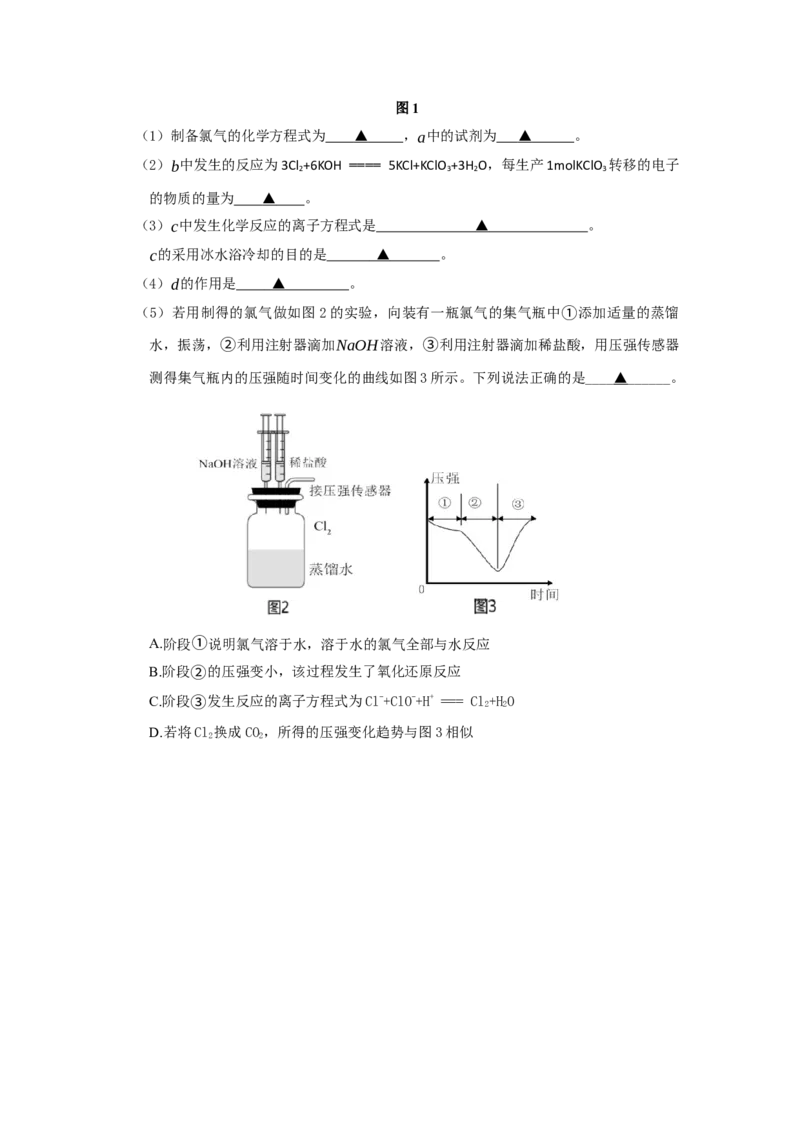
(5)若用制得的氯气做如图2的实验,向装有一瓶氯气的集气瓶中①添加适量的蒸馏
水,振荡,②利用注射器滴加NaOH溶液,③利用注射器滴加稀盐酸,用压强传感器
测得集气瓶内的压强随时间变化的曲线如图3所示。下列说法正确的是____▲______。
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③发生反应的离子方程式为Cl-+ClO-+H+ === Cl
2
+H
2
O
D.若将Cl 换成CO,所得的压强变化趋势与图3相似
2 2