文档内容
2025—2026 学年度上学期 2025 级
9 月月考化学试卷
时间:75分钟 分数:100分
可能用到的相对原子质量: H-1 C-12 O-16 S-32 Ca-40 Ba-137
第Ⅰ卷(选择题 共45分)
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.我国传统文化源远流长,对下列古文或诗词的解读错误的是
A.“方以类聚,物以群分”表达了对于世界体系的分类概念
B.“野火烧不尽”涉及氧化还原反应
C.“日照澄洲江雾开,淘金女伴满江隈”涉及丁达尔效应
D.“曾青得铁则为铜”过程发生了复分解反应
2.多角度认识物质的性质是化学研究的基本任务。下列有关酸、碱、盐的认识正确的是
A.实验:用pH试纸测得某溶液呈强酸性,其溶质不一定是酸
B.微观:盐的水溶液中一定含有金属元素
C.变化:反应后只生成盐和水的两种物质一定是酸和碱
D.宏观:复分解反应一定有气体、沉淀或水生成
3.实验室用饱和FeCl 溶液和蒸馏水制 胶体,下列说法正确的是
3
A.实验要注意的安全图标有
B.FeCl 溶液和 胶体的本质区别是能否发生丁达尔效应
3
C.溶液变成红褐色后继续加热能得到更多胶体D.向 胶体中加入稀硫酸,红褐 色的
胶体会立刻变成黄色溶液
4.氧化还原反应与四种基本反应类型的关系 如图
所示,则下列化学反应属于区域3的是
A.2 F + 2 HO ═ 4 HF+ O
2 2 2
B.AgNO + NaCl ═ AgCl↓ + NaNO
3 3
C.3CO + Fe O 2Fe + 3CO
2 3 2
D.MgCl (熔融) Mg + Cl↑
2 2
5.下列说法正确的是
A.金属阳离子被还原一定得到金属单质
B. 可表示所有的酸碱中和反应
C.失电子越多,还原性越强,得电子越多,氧化性越强
D. 个 与沸水完全反应转化为 胶体, 胶粒的数目少于
个
6.下列物质转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不
可能全部实现的是
A.
B. 溶液
C.
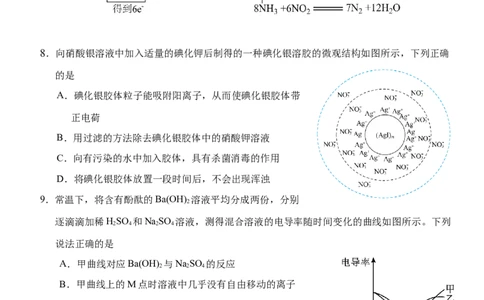
D.7.下列化学方程式中,电子转移的方向和数目都正确的是
A. B.
C. D.
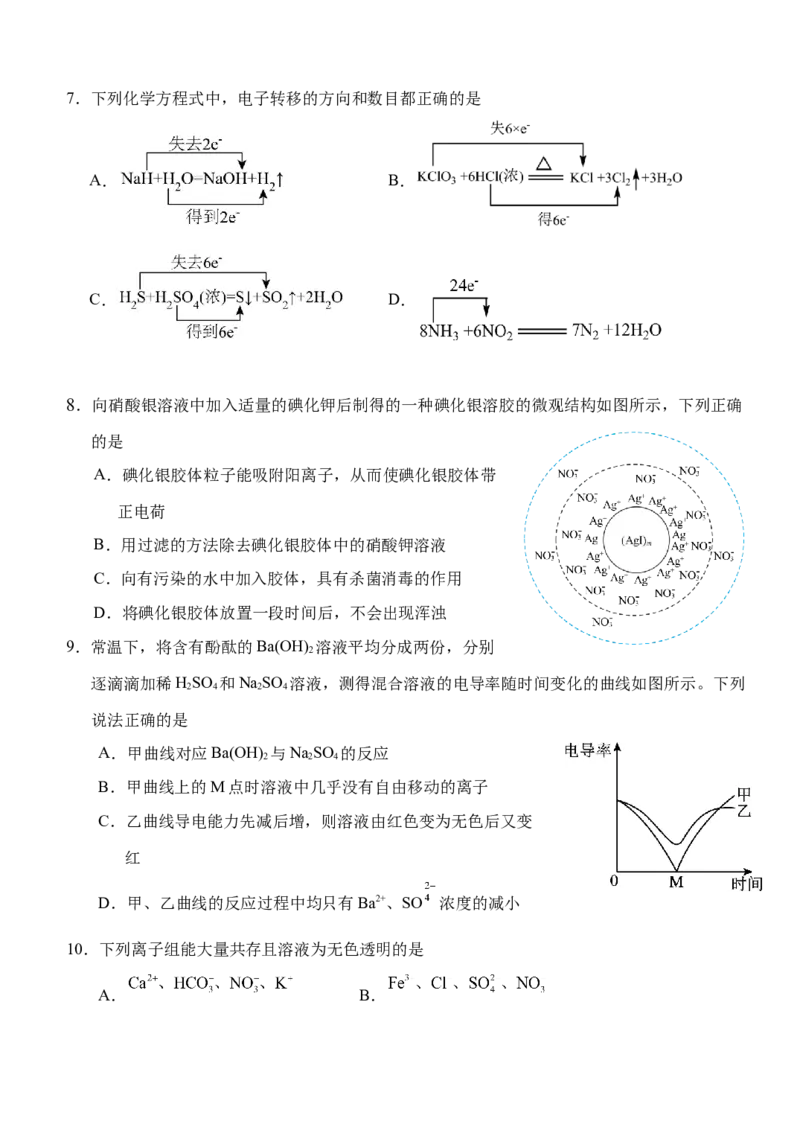
8.向硝酸银溶液中加入适量的碘化钾后制得的一种碘化银溶胶的微观结构如图所示,下列正确
的是
A.碘化银胶体粒子能吸附阳离子,从而使碘化银胶体带
正电荷
B.用过滤的方法除去碘化银胶体中的硝酸钾溶液
C.向有污染的水中加入胶体,具有杀菌消毒的作用
D.将碘化银胶体放置一段时间后,不会出现浑浊
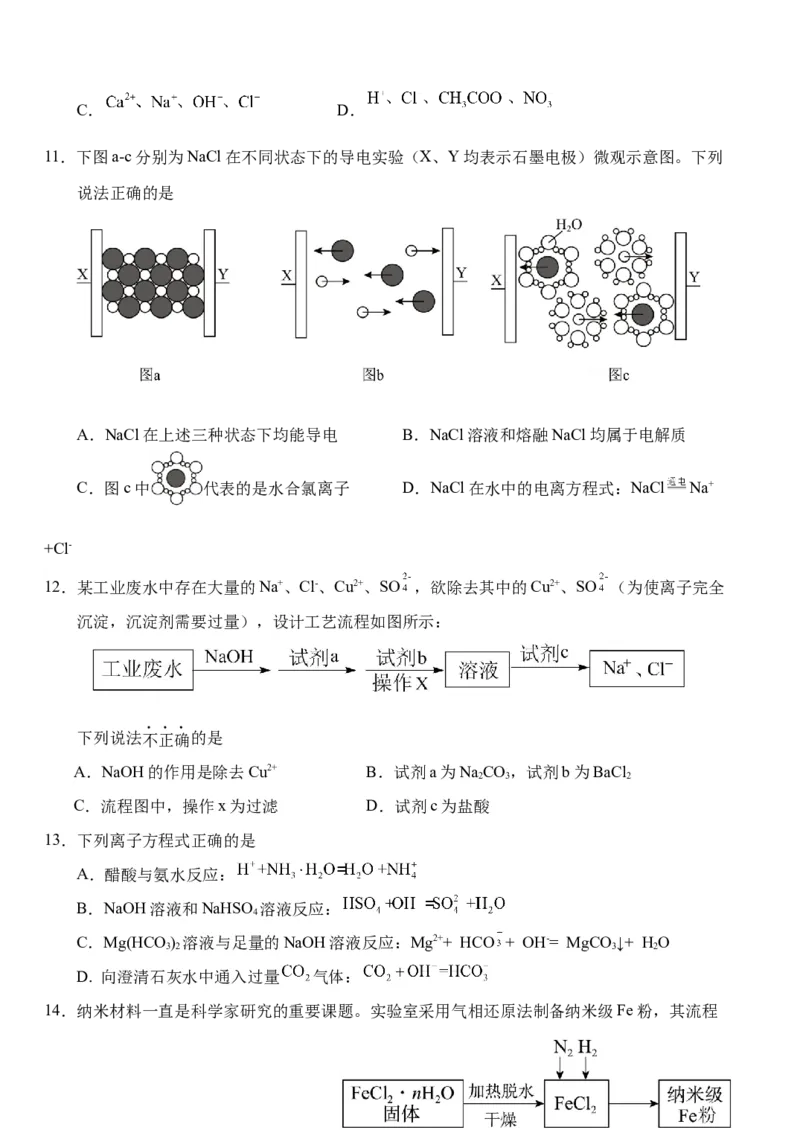
9.常温下,将含有酚酞的Ba(OH) 溶液平均分成两份,分别
2
逐滴滴加稀HSO 和NaSO 溶液,测得混合溶液的电导率随时间变化的曲线如图所示。下列
2 4 2 4
说法正确的是
A.甲曲线对应Ba(OH) 与NaSO 的反应
2 2 4
B.甲曲线上的M点时溶液中几乎没有自由移动的离子
C.乙曲线导电能力先减后增,则溶液由红色变为无色后又变
红
D.甲、乙曲线的反应过程中均只有Ba2+、SO 浓度的减小
10.下列离子组能大量共存且溶液为无色透明的是
A. B.C. D.
11.下图a-c分别为NaCl在不同状态下的导电实验(X、Y均表示石墨电极)微观示意图。下列
说法正确的是
A.NaCl在上述三种状态下均能导电 B.NaCl溶液和熔融NaCl均属于电解质
C.图c中 代表的是水合氯离子 D.NaCl在水中的电离方程式:NaCl Na+
+Cl-
12.某工业废水中存在大量的Na+、Cl-、Cu2+、SO ,欲除去其中的Cu2+、SO (为使离子完全
沉淀,沉淀剂需要过量),设计工艺流程如图所示:
下列说法不正确的是
A.NaOH的作用是除去Cu2+ B.试剂a为NaCO,试剂b为BaCl
2 3 2
C.流程图中,操作x为过滤 D.试剂c为盐酸
13.下列离子方程式正确的是
A.醋酸与氨水反应:
B.NaOH溶液和NaHSO 溶液反应:
4
C.Mg(HCO ) 溶液与足量的NaOH溶液反应:Mg2++ HCO + OH-= MgCO ↓+ HO
3 2 3 2
D. 向澄清石灰水中通入过量 气体:
14.纳米材料一直是科学家研究的重要课题。实验室采用气相还原法制备纳米级Fe粉,其流程如图所示,下列说法错误的是
A. 固体加热脱水的过程属于化学变化
B.获得的纳米级Fe粉属于胶体
C.纳米级Fe粉比普通铁粉更易与氧气反应
D.高温制备纳米级Fe粉的过程中通入N 可以防止爆炸,也可作保护气
2
15.已知有下列四个反应:
①
②
③
④
下列有关说法错误的是
A.反应②③④中的氧化产物分别是 、 、
B.根据①②③可以得到还原性:
C.可以发生反应
D.在反应④中参加反应的 和体现还原性的HCl个数比为1∶2
第II卷(填空题 共55分)
16.(14分)生活中离不开化学,家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的
主要成分:
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④碱面( );⑤小苏打(
);⑥84消毒液(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾KAl(SO )·12H O
4 2 2
);⑨铁锅(Fe) 。
回答下列问题:
(1)上述厨卫商品的主要成分(括号内的物质)属于非电解质的是 (填序号,
下同),①④⑤⑨中能够导电的有 。
(2)小苏打的主要成分 ,在水溶液的电离方程式: 。(3)向小苏打溶液中滴加少量澄清石灰水,写离子方程式:
(4)酒店的保洁阿姨不小心将⑥⑦混合使用生成有毒的氯气(Cl)导致中毒,除外产物还
2
有:NaCl和水,请大家试着写出该反应的化学方程式:
。
(5)已知 和碱反应生成 ,故 为酸性氧化物, 与酸反应生成Fe3+,故
为碱性氧化物. 可以形成两种盐: 、 (微溶物),则 属于 氧
化物(填“酸性”或“碱性”、“两性”、“不成盐”).写出 与浓NaOH溶液反应的化学
方程式: 。
(6)在水处理过程中,⑧明矾转化为Al(OH) 胶体,Al(OH) 胶体具有很大的表面积,
3 3
可 悬浮于水中的杂质,使之从水中沉降出来。证明有 Al(OH) 胶体生成的方法是
3
。
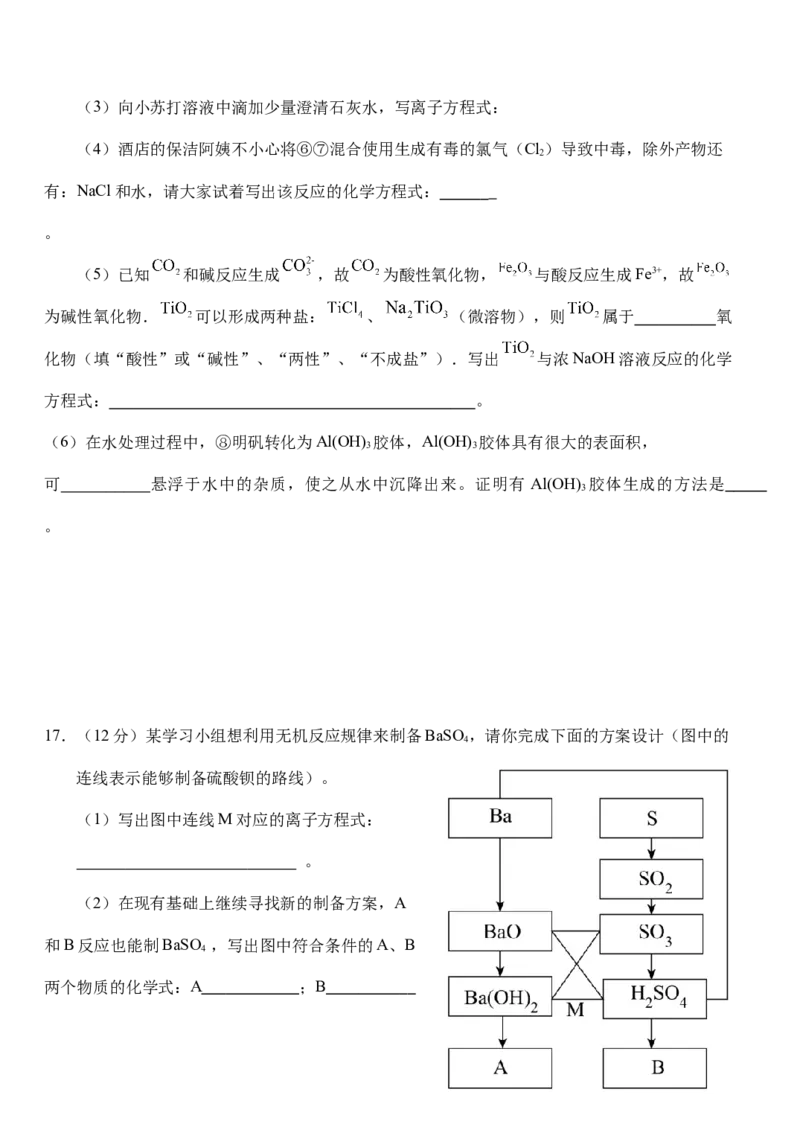
17.(12分)某学习小组想利用无机反应规律来制备BaSO,请你完成下面的方案设计(图中的
4
连线表示能够制备硫酸钡的路线)。
(1)写出图中连线M对应的离子方程式:
。
(2)在现有基础上继续寻找新的制备方案,A
和B反应也能制BaSO ,写出图中符合条件的A、B
4
两个物质的化学式:A ;B(各写出一种即可)。
(3)向NaHSO 溶液中加Ba也可生成BaSO,对应的离子方程式 。
4 4
(已知:金属活动性Ba>Ca)
(4)上述方案中SO 有多种性质,将SO 气体通入紫色的酸性高锰酸钾溶液中,溶液紫色褪
2 2
去。已知上述反应中MnO 转化为Mn2+,该反应的离子方程式为
。
(5)下列叙述中正确的是 。
a.硫酸钡在水中几乎不导电,所以硫酸钡是非电解质
b.硫酸钡不溶于水和酸,且不容易被X射线透过,故在医疗上可用作消化系统X射线
检查的内服药剂,俗称“钡餐”
c.碳酸钡也可用于“钡餐”
18.(14分)实验室有一瓶无色透明的溶液,可能含有Na+、Ba2+、Cu2+、Mg2+、H+、SO 、CO
、NO 、OH-、Cl-中的若干种离子,且每种离子的个数一样多。化学兴趣小组设计了一系
列实验来探究该溶液的成分。
(1)通过观察,该溶液中一定不存在 (填写离子符号,下同)。
为鉴别该溶液的成分,对该溶液进行了以下实验。
①取少量溶液,加入紫色石蕊,溶液变红。②取样,向溶液中加入过量的BaCl 溶液,生成白色沉淀。
2
③将②得到的浊液过滤,再加入AgNO 溶液,生成白色沉淀。
3
(2)实验①证明溶液含有 。
(3)写出实验②发生的离子方程式 。
(4)有同学认为,实验③不能证明原溶液中含有氯离子,理由是
。
(5)改正实验后,证明了溶液中含有氯离子,请写出证明含有Cl-的离子方程式:
;结合上述实验,溶液中一定存在的离子是 ,可能存在的离子是
。
19.(15分)化学兴趣小组对牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:牙膏摩擦剂由 ① CaCO ② CaHPO ③ SiO ④ Al(OH) 组成 。
3 4 2 3
(1)推测SiO、Al(OH) 的溶解性: (填写“易溶于水”、“难溶于
2 3水”)。
(2)若Al(OH) 属于碱,Al(OH) 与盐酸反应的离子方程式是 。
3 3
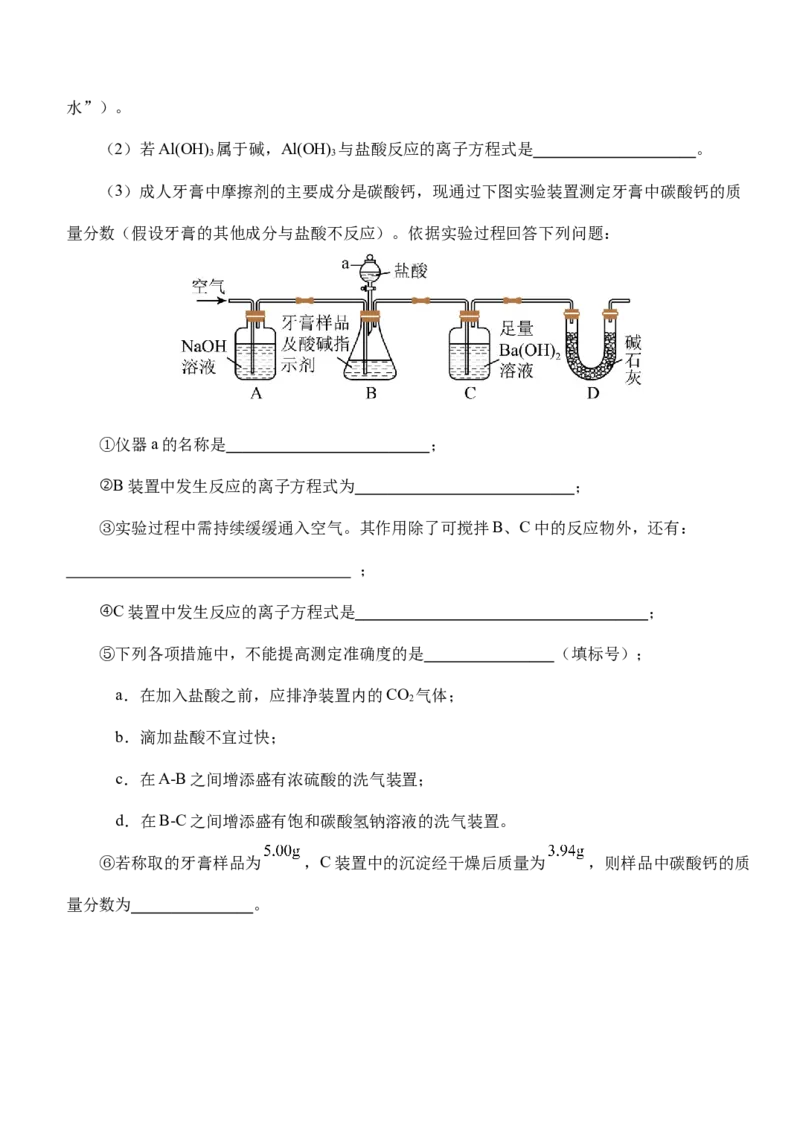
(3)成人牙膏中摩擦剂的主要成分是碳酸钙,现通过下图实验装置测定牙膏中碳酸钙的质
量分数(假设牙膏的其他成分与盐酸不反应)。依据实验过程回答下列问题:
①仪器a的名称是 ;
②B装置中发生反应的离子方程式为 ;
③实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
;
④C装置中发生反应的离子方程式是 ;
⑤下列各项措施中,不能提高测定准确度的是 (填标号);
a.在加入盐酸之前,应排净装置内的CO 气体;
2
b.滴加盐酸不宜过快;
c.在A-B之间增添盛有浓硫酸的洗气装置;
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置。
⑥若称取的牙膏样品为 ,C装置中的沉淀经干燥后质量为 ,则样品中碳酸钙的质
量分数为 。