文档内容
成都外国语学校 2025-2026 学年度上期 12 月月考
高一化学试卷
注意事项:
1、本试卷分 I 卷(选择题)和 II 卷(非选择题)两部分。
2、本堂考试 75 分钟,满分 100 分。
3、答题前,考生务必先将自己的姓名、学号、班级填写在答卷上
4、考试结束后,将答题卡交回。
可能用到的相对原子质量: H -1 C -12 N-14 O -16 Na -23
第 I 卷(选择题,共 45 分)
一、选择题(本题包括 15 小题,每小题 3 分,共 45 分。每小题只有一个选项符合题意)
1. 化学与生活息息相关,下列有关物质的性质、用途的叙述,正确的是
A. 碳酸钠俗名小苏打,可用作糕点膨松剂
B. 钢铁腐蚀、胶体的制备都与氧化还原反应有关
C. Na O 用于呼吸面具,活性炭用于防毒面具,两者原理不相同
2 2
D. 漂白粉、漂白液既可用作游泳池的消毒剂,又可作食品漂白剂
2. 下图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是
X Y Z
A CuSO ·5H O 盐 纯净物
4 2
B 胶体 分散系 混合物
C 碱性氧化物 氧化物 化合物
D 置换反应 氧化还原反应 离子反应
A. A B. B C. C D. D
第 1页/共 8页3. 下列物质在标准状况下体积最大的是
A. 6 g B. 2.5 mol C. 11.2 L D. 个
4. 下列各组物质间的转化,在指定条件下均能一步实现的是
A.
B.
C.
D.
5. 下列有关氯及其化合物的说法正确的是
A. Cl →Cl-的转化过程,必须加入还原剂才能实现
2
B. 新制氯水中可以使 K
2
CO
3
溶液产生气泡的微粒是 H+
C. 往待测液中滴加 AgNO 溶液,若产生白色沉淀,则一定有 Cl-
3
D. 实验室可以用 pH 试纸来测量新制氯水的 pH
6. 一定量 与 溶液反应,所得产物中含有 和 ,且其物质的量之比为 ,则
参加反应的 与 的物质的量之比为
A. B. C. D.
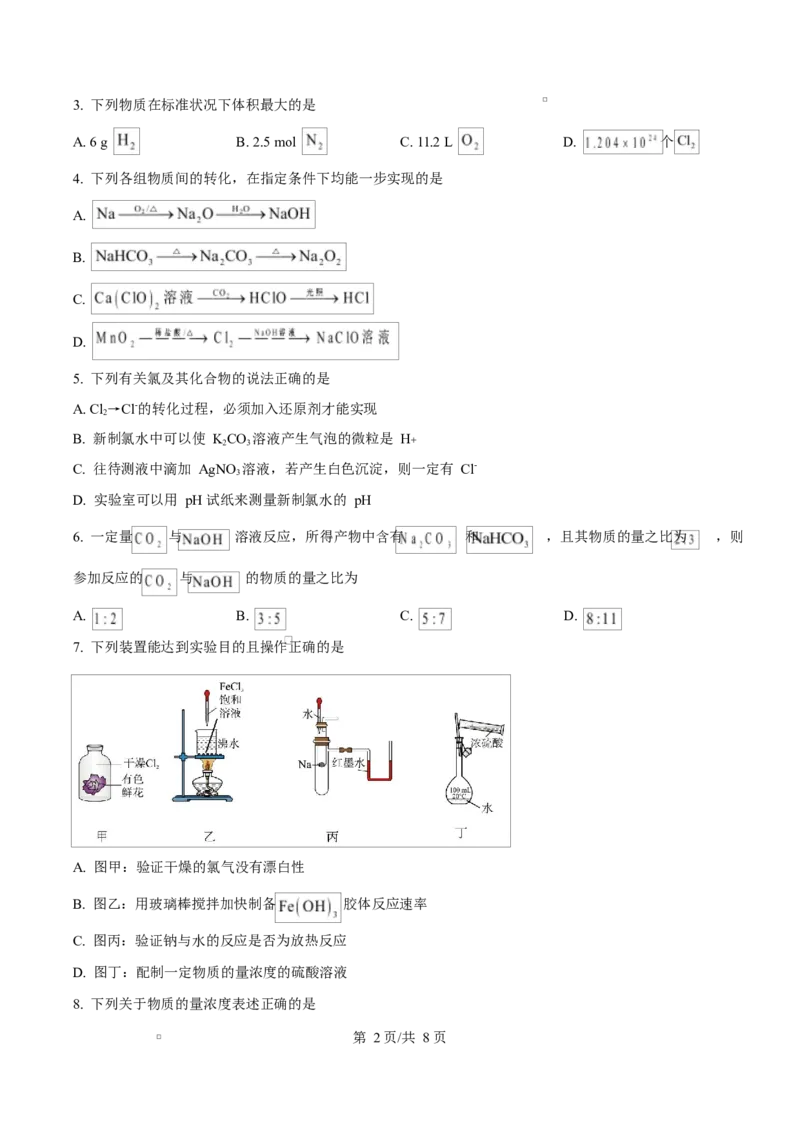
7. 下列装置能达到实验目的且操作正确的是
A. 图甲:验证干燥的氯气没有漂白性
B. 图乙:用玻璃棒搅拌加快制备 胶体反应速率
C. 图丙:验证钠与水的反应是否为放热反应
D. 图丁:配制一定物质的量浓度的硫酸溶液
8. 下列关于物质的量浓度表述正确的是
第 2页/共 8页A. 10g98%的硫酸(密度为 1.84g cm-3)与 10mL18.4mol/L 的硫酸浓度相等
B. 将 62gNaO 溶于水中,配成 1L 溶液,所得溶质的物质的量浓度为 1mol/L
2
C. 用 1L 水吸收 22.4L 氯化氢(标况下)所得盐酸的浓度是 1mol/L
D. 0.2mol/LNa
2
SO
4
溶液中含有 Na+ 和 总物质的量为 0.6mol
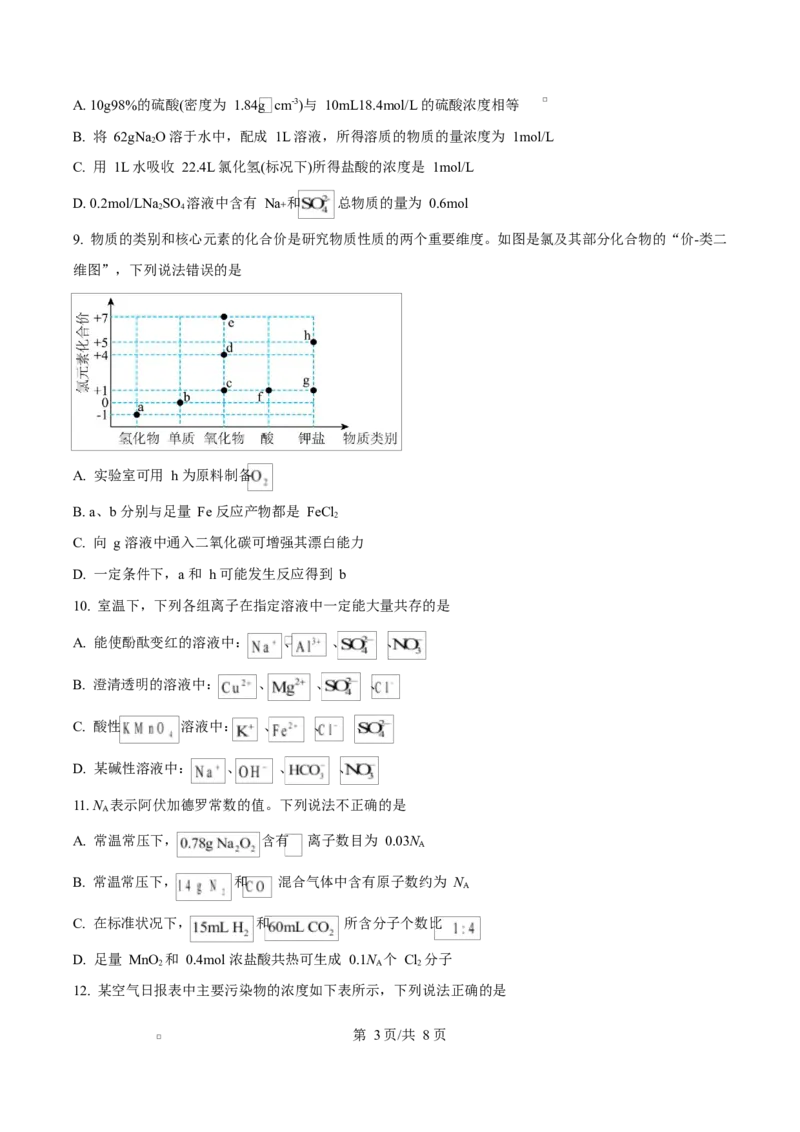
9. 物质的类别和核心元素的化合价是研究物质性质的两个重要维度。如图是氯及其部分化合物的“价-类二
维图”,下列说法错误的是
A. 实验室可用 h 为原料制备
B. a、b 分别与足量 Fe 反应产物都是 FeCl
2
C. 向 g 溶液中通入二氧化碳可增强其漂白能力
D. 一定条件下,a 和 h 可能发生反应得到 b
10. 室温下,下列各组离子在指定溶液中一定能大量共存的是
A. 能使酚酞变红的溶液中: 、 、 、
B. 澄清透明的溶液中: 、 、 、
C. 酸性 溶液中: 、 、 、
D. 某碱性溶液中: 、 、 、
11. N 表示阿伏加德罗常数的值。下列说法不正确的是
A
A. 常温常压下, 含有 离子数目为 0.03N
A
B. 常温常压下, 和 混合气体中含有原子数约为 N
A
C. 在标准状况下, 和 所含分子个数比
D. 足量 MnO 和 0.4mol 浓盐酸共热可生成 0.1N 个 Cl 分子
2 A 2
12. 某空气日报表中主要污染物的浓度如下表所示,下列说法正确的是
第 3页/共 8页主要污染物 PM2.5 CO
浓度(ug/m3) 32 14 42 0
(已知:1g=1×106 )
A. CO 和 互为同素异形体
B. 相同体积的 和 中所含氧原子数一定相同
C 该空气中含有 3.125×10-5 molO
3
D. 常温下,相同质量的 和 CO 所含的分子个数比为
13. 下列离子方程式书写正确的是
A. 氯气溶于水:Cl
2
+H
2
O=2H++Cl-+ClO-
B. “84”消毒液与洁厕灵混合后产生气体:
C. 向 溶液中通入少量 :
D. 溶液与少量的 溶液混合:
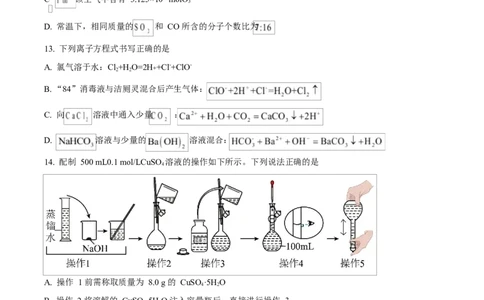
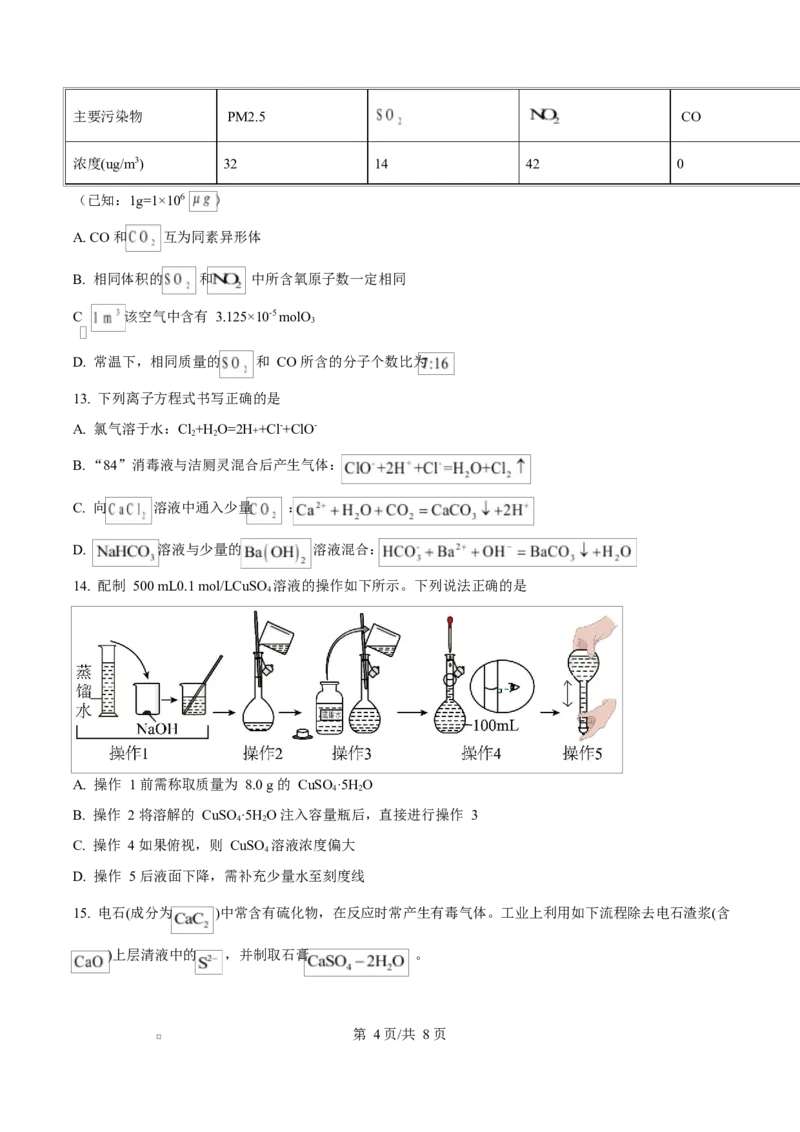
14. 配制 500 mL0.1 mol/LCuSO 溶液的操作如下所示。下列说法正确的是
4
A. 操作 1 前需称取质量为 8.0 g 的 CuSO ·5H O
4 2
B. 操作 2 将溶解的 CuSO ·5H O 注入容量瓶后,直接进行操作 3
4 2
C. 操作 4 如果俯视,则 CuSO 溶液浓度偏大
4
D. 操作 5 后液面下降,需补充少量水至刻度线
15. 电石(成分为 )中常含有硫化物,在反应时常产生有毒气体。工业上利用如下流程除去电石渣浆(含
)上层清液中的 ,并制取石膏 。
第 4页/共 8页下列说法不正确的是
A. 过程Ⅰ中的反应会使溶液的碱性减弱
B. 过程Ⅱ 离子方程式为
C. 将上层清液中 的 转化为 ,理论上总共需要 的
D. 由上述转化过程可知,氧化性:
第Ⅱ卷(非选择题,共 55 分)
16 按照要求回答下列问题:
Ⅰ.①CO ②Cl ③ ④ ⑤NaOH 溶液 ⑥NaCO 溶液 ⑦熔融 NaCl
2 2 2 3
(1)上述物质中属于电解质的是________(填序号,下同),属于非电解质的是________。
(2)写出①与④反应的化学反应方程式________。
(3)将 NaOH 溶液与 NaCO 溶液相混合,则混合溶液中 的物
2 3
质的量浓度为________(忽略混合前后溶液体积的变化)。
Ⅱ.已知:
(4)0.3 mol NH Cl 分子中所含氢原子数与________molNH 分子中所含氢原子数相等,这些 在标准状
4 3
况下的体积约为________L。
(5)反应中氧化剂和还原剂的物质的量之比为________。
(6)有 0.8mol 的 NH 参与反应,转移的电子数为________。
3
(7)等质量的下列气体 、 、 三种气体中,在同温同压条件下,体积最大的是________。
17. 某兴趣小组拟在实验室用 12 mol/L 浓盐酸配制 1mol/L 的稀盐酸溶液 250 mL。
(1)①需要量筒量取________mL 的浓盐酸。
②配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、胶头滴管、________。
③下列是该配制过程的操作图示,其正确的操作顺序应是________(填字母)。
第 5页/共 8页④C 操作中用胶头滴管滴加蒸馏水至溶液________。
⑤在配制过程中,下列操作会导致所配制溶液的浓度偏低的是________(填序号)。
A.未洗涤烧杯和玻璃棒
B.向容量瓶中转移溶液前,容量瓶中有少量蒸馏水
C.定容时俯视刻度线
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
(2)现有某食用碱,测定其中碳酸钠的含量的操作如下(该食用碱中的其他成分不与盐酸反应):
①取 5.3 g 该食用碱溶于 50 mL 蒸馏水中;
②加入 100 mL 1mol/L 稀盐酸;
③用 1mol/L 氢氧化钠溶液中和过量稀盐酸,记录所消耗氢氧化钠溶液的体积是 15 mL.
则该食用碱中碳酸钠的纯度为________。
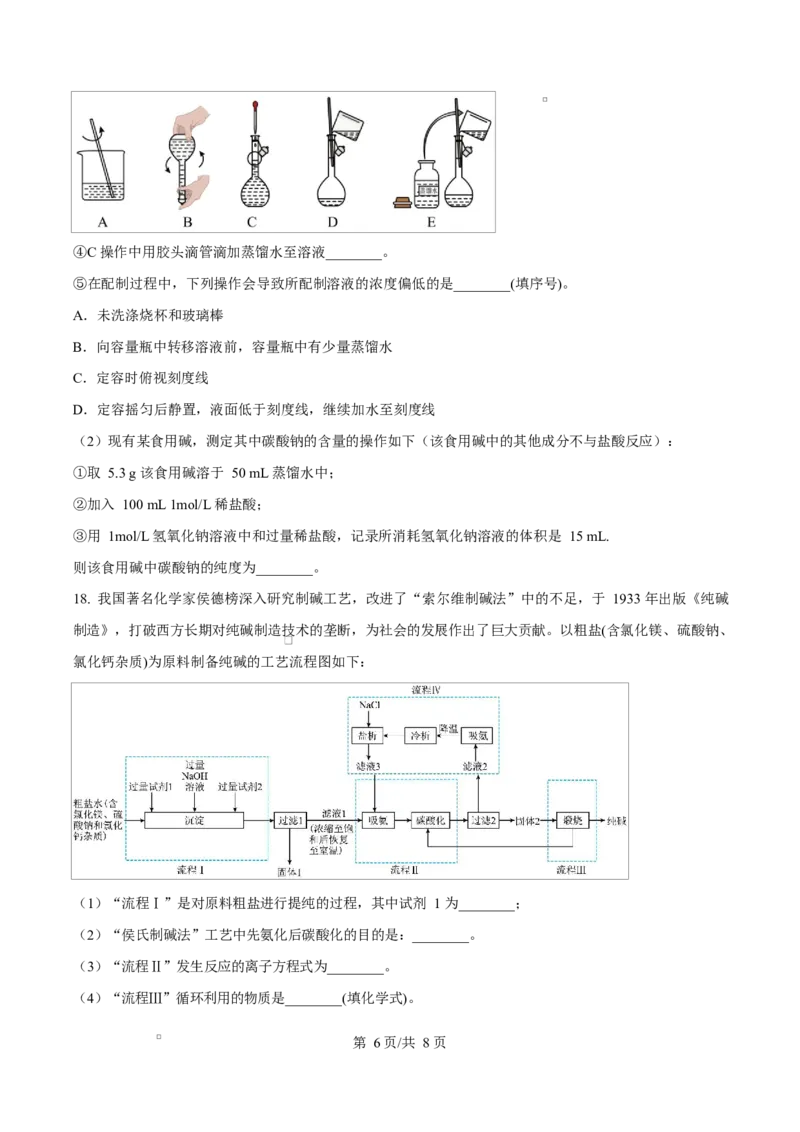
18. 我国著名化学家侯德榜深入研究制碱工艺,改进了“索尔维制碱法”中的不足,于 1933 年出版《纯碱
制造》,打破西方长期对纯碱制造技术的垄断,为社会的发展作出了巨大贡献。以粗盐(含氯化镁、硫酸钠、
氯化钙杂质)为原料制备纯碱的工艺流程图如下:
(1)“流程Ⅰ”是对原料粗盐进行提纯的过程,其中试剂 1 为________;
(2)“侯氏制碱法”工艺中先氨化后碳酸化的目的是:________。
(3)“流程Ⅱ”发生反应的离子方程式为________。
(4)“流程Ⅲ”循环利用的物质是________(填化学式)。
第 6页/共 8页(5)固体 2 加热分解的化学方程式为________。
(6)从 A~E 中选择合适的仪器制备 ,其中 D 装置的作用是________。
(7)二氧化碳在氨盐水里溶解度较低,则 B 中使用雾化装置的优点是_______。
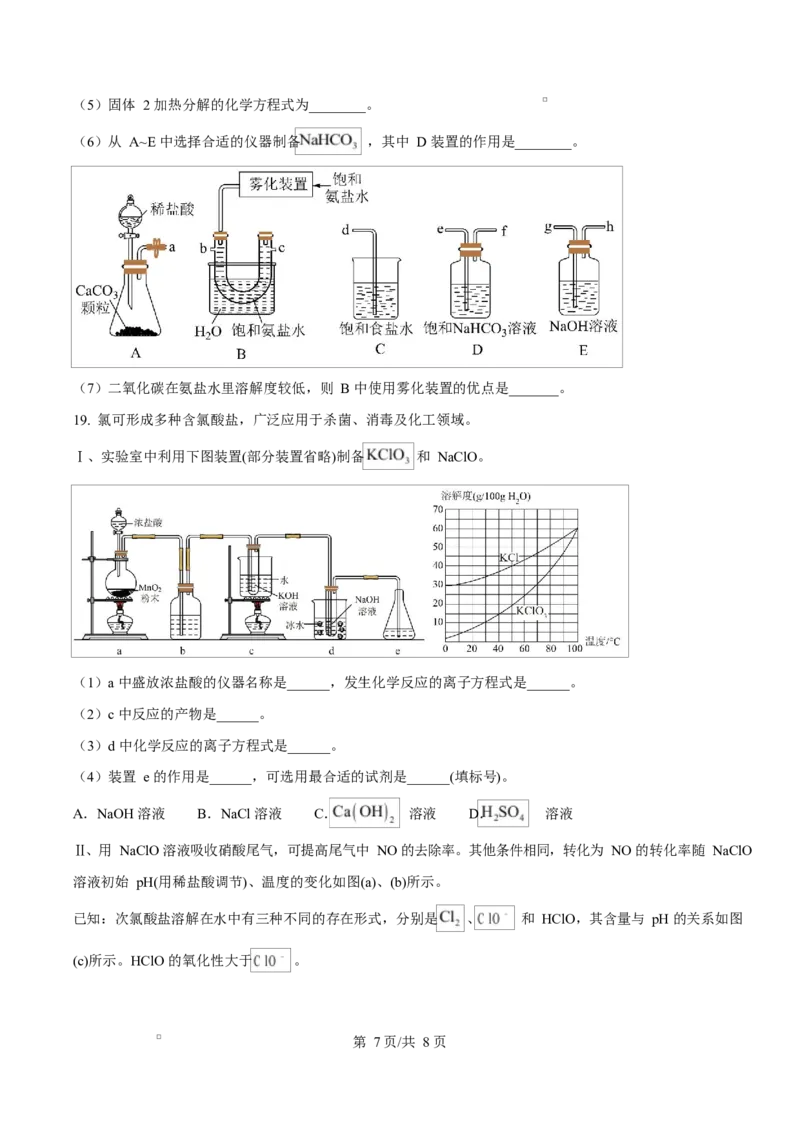
19. 氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。
Ⅰ、实验室中利用下图装置(部分装置省略)制备 和 NaClO。
(1)a 中盛放浓盐酸的仪器名称是______,发生化学反应的离子方程式是______。
(2)c 中反应的产物是______。
(3)d 中化学反应的离子方程式是______。
(4)装置 e 的作用是______,可选用最合适的试剂是______(填标号)。
A.NaOH 溶液 B.NaCl 溶液 C. 溶液 D. 溶液
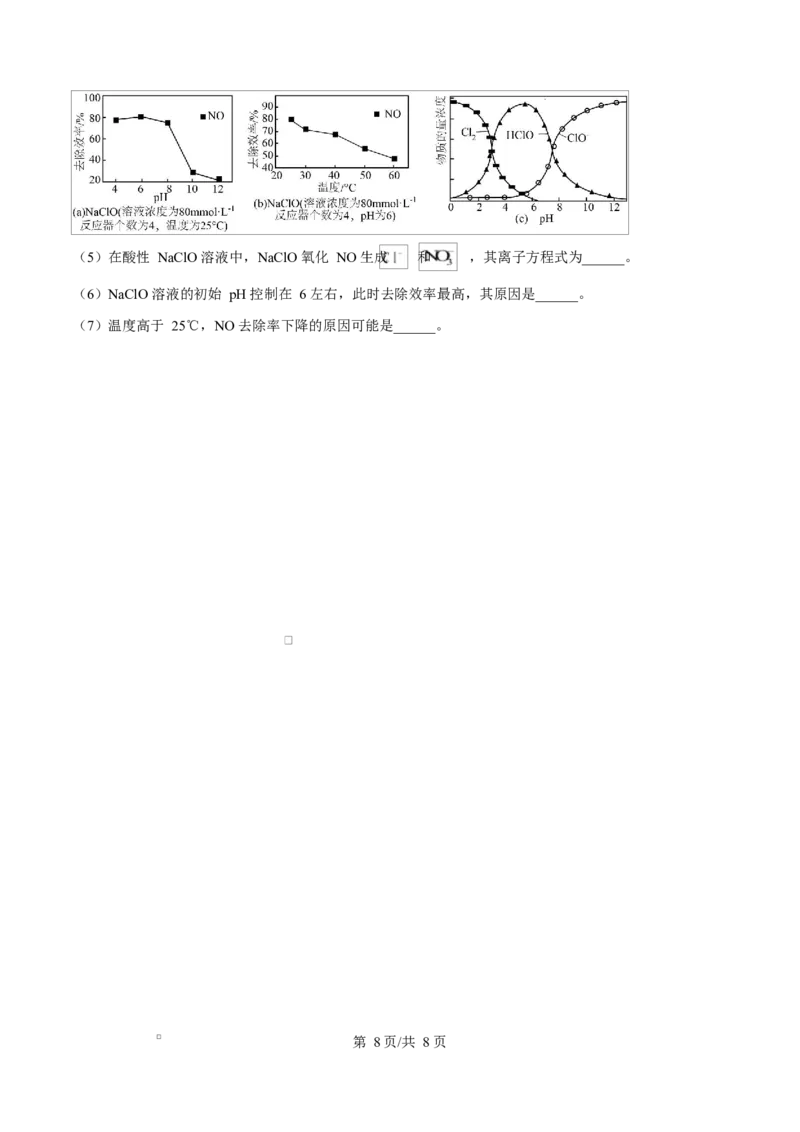
Ⅱ、用 NaClO 溶液吸收硝酸尾气,可提高尾气中 NO 的去除率。其他条件相同,转化为 NO 的转化率随 NaClO
溶液初始 pH(用稀盐酸调节)、温度的变化如图(a)、(b)所示。
已知:次氯酸盐溶解在水中有三种不同的存在形式,分别是 、 和 HClO,其含量与 pH 的关系如图
(c)所示。HClO 的氧化性大于 。
第 7页/共 8页(5)在酸性 NaClO 溶液中,NaClO 氧化 NO 生成 和 ,其离子方程式为______。
(6)NaClO 溶液的初始 pH 控制在 6 左右,此时去除效率最高,其原因是______。
(7)温度高于 25℃,NO 去除率下降的原因可能是______。
第 8页/共 8页