文档内容
东莞实验中学 2024-2025 学年第二学期第一次段考
高一年级 化学
可能用到的相对原子质量:N 14 O 16 S 32 Zn 65 Pb 207
注意事项:
1.答卷前,考生务必用黑色字迹钢笔或签字笔将自己的姓名、考生号、考场号和座位号填写在答题卡
上。用2B铅笔将试卷类型(A)填涂在答题卡相应位置上。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑;如需
改动,用橡皮擦干净后,再选涂其他答案。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;
如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作
答的答案无效。
4.考生必须保持答题卡整洁。考试结束后,只需将答题卡交回。
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分:第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列文物的主要材质为金属材料的是
选
A B C D
项
物
质
名 元青花釉里红瓷盖
错金杜虎符 东汉玉环 石犀
称 罐
A.A B.B C.C D.D
2.下列化学用语表示错误的是
A.S2-的结构示意图: B.N 的结构式:
2
C.CO 分子结构模型: D.中子数为10的氟原子:
2
3.纵观古今,化学与环境、材料、生产、生活关系密切,下列说法不正确的是
A.“玉兔号”月球车帆板太阳能电池的材料是氮化硅或二氧化硅B.“神舟”系列飞船使用的碳纤维材料、光导纤维都是新型无机非金属材料
C.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
D.“神舟”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分不是硅酸盐
4.下列关于物质性质的描述正确的是
A.SO 能使酸性高锰酸钾溶液褪色,说明SO 具有漂白性
2 2
B.SO 与H S气体混合产生淡黄色固体,说明SO 具有还原性
2 2 2
C.常温下,浓硫酸可以用铁罐储存和运输,说明铁在常温下与浓硫酸不反应
D.SO 可溶于H SO ,所以浓H SO 可用于实验室除去SO 中混有的SO
3 2 4 2 4 2 3
5.在 反应中,下列表示该反应速率最快的是
A. B.
C. D.
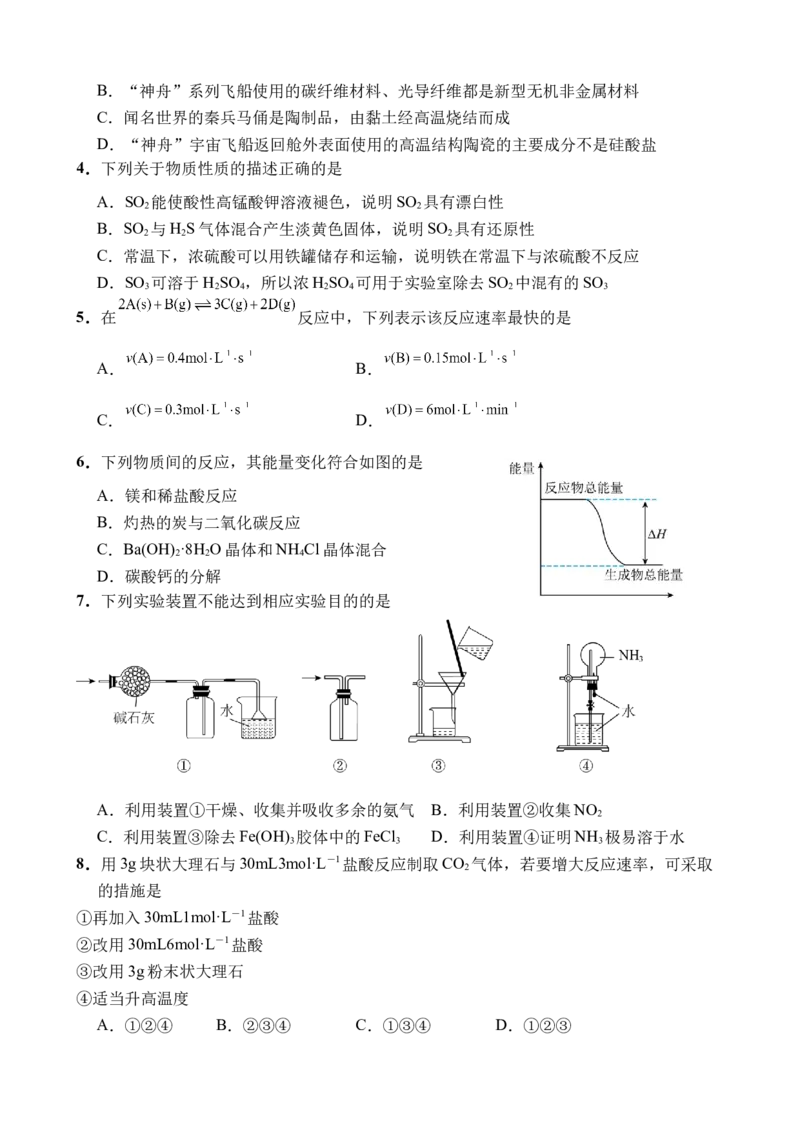
6.下列物质间的反应,其能量变化符合如图的是
A.镁和稀盐酸反应
B.灼热的炭与二氧化碳反应
C.Ba(OH) ·8H O晶体和NH Cl晶体混合
2 2 4
D.碳酸钙的分解
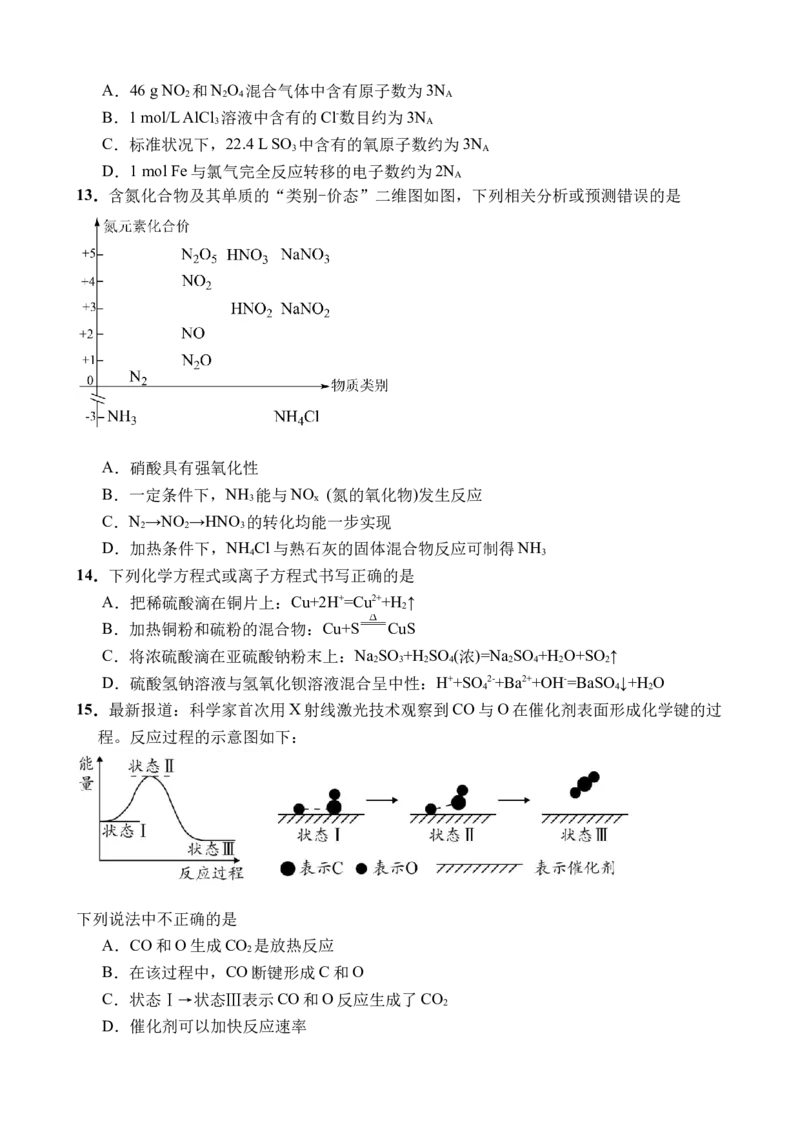
7.下列实验装置不能达到相应实验目的的是
A.利用装置①干燥、收集并吸收多余的氨气 B.利用装置②收集NO
2
C.利用装置③除去Fe(OH) 胶体中的FeCl D.利用装置④证明NH 极易溶于水
3 3 3
8.用3g块状大理石与30mL3mol·L-1盐酸反应制取CO 气体,若要增大反应速率,可采取
2
的措施是
①再加入30mL1mol·L-1盐酸
②改用30mL6mol·L-1盐酸
③改用3g粉末状大理石
④适当升高温度
A.①②④ B.②③④ C.①③④ D.①②③9.如图是化学课外活动小组设计的用化学电源使LED灯发光的装置。下列说法正确的是
A.铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生
B.如果将锌片换成铜片,电路中的电流方向将改变
C.其能量转化的形式主要是“化学能→电能→光能”
D.如果将稀硫酸换成柠檬汁,LED灯将不会发光
10.下列叙述I和II均正确并有因果关系的是
选
叙述I 叙述II
项
常温下,SiO 与氢氟酸和NaOH溶液均可
A 2 SiO 是两性氧化物
反应 2
往饱和Na CO 溶液中通入CO 产生沉
B 常温下,NaHCO 的溶解度比Na CO 小 2 3 2
3 2 3 淀
SO 气体通入Ba(NO ) 溶液中产生沉
C BaSO 难溶于水 2 3 2
3 淀
D 非金属性:Cl>C 酸性:HClO>H CO
2 3
A.A B.B C.C D.D
11.CaCO 与100ml稀盐酸反应生成CO 的量与反应时间的关系如图所示,下列结论不正确
3 2
的是( )
A.反应在2~4min内平均反应速率最大
B.反应在2~4min内用盐酸表示平均反应速率为v(HCl)=0.1mol·L-1·min-1
C.反应开始阶段反应速率逐渐上升是由于温度比浓度对反应速率的影响大
D.4min后,反应速率减小的主要原因是c(H+)减小
12.N 表示阿伏加德罗常数,下列说法正确的是
AA.46 g NO 和N O 混合气体中含有原子数为3N
2 2 4 A
B.1 mol/L AlCl 溶液中含有的Cl-数目约为3N
3 A
C.标准状况下,22.4 L SO 中含有的氧原子数约为3N
3 A
D.1 mol Fe与氯气完全反应转移的电子数约为2N
A
13.含氮化合物及其单质的“类别-价态”二维图如图,下列相关分析或预测错误的是
A.硝酸具有强氧化性
B.一定条件下,NH 能与NO (氮的氧化物)发生反应
3 x
C.N →NO →HNO 的转化均能一步实现
2 2 3
D.加热条件下,NH Cl与熟石灰的固体混合物反应可制得NH
4 3
14.下列化学方程式或离子方程式书写正确的是
A.把稀硫酸滴在铜片上:Cu+2H+=Cu2++H ↑
2
B.加热铜粉和硫粉的混合物:Cu+S CuS
C.将浓硫酸滴在亚硫酸钠粉末上:Na SO +H SO (浓)=Na SO +H O+SO ↑
2 3 2 4 2 4 2 2
D.硫酸氢钠溶液与氢氧化钡溶液混合呈中性:H++SO 2-+Ba2++OH-=BaSO ↓+H O
4 4 2
15.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过
程。反应过程的示意图如下:
下列说法中不正确的是
A.CO和O生成CO 是放热反应
2
B.在该过程中,CO断键形成C和O
C.状态Ⅰ→状态Ⅲ表示CO和O反应生成了CO
2
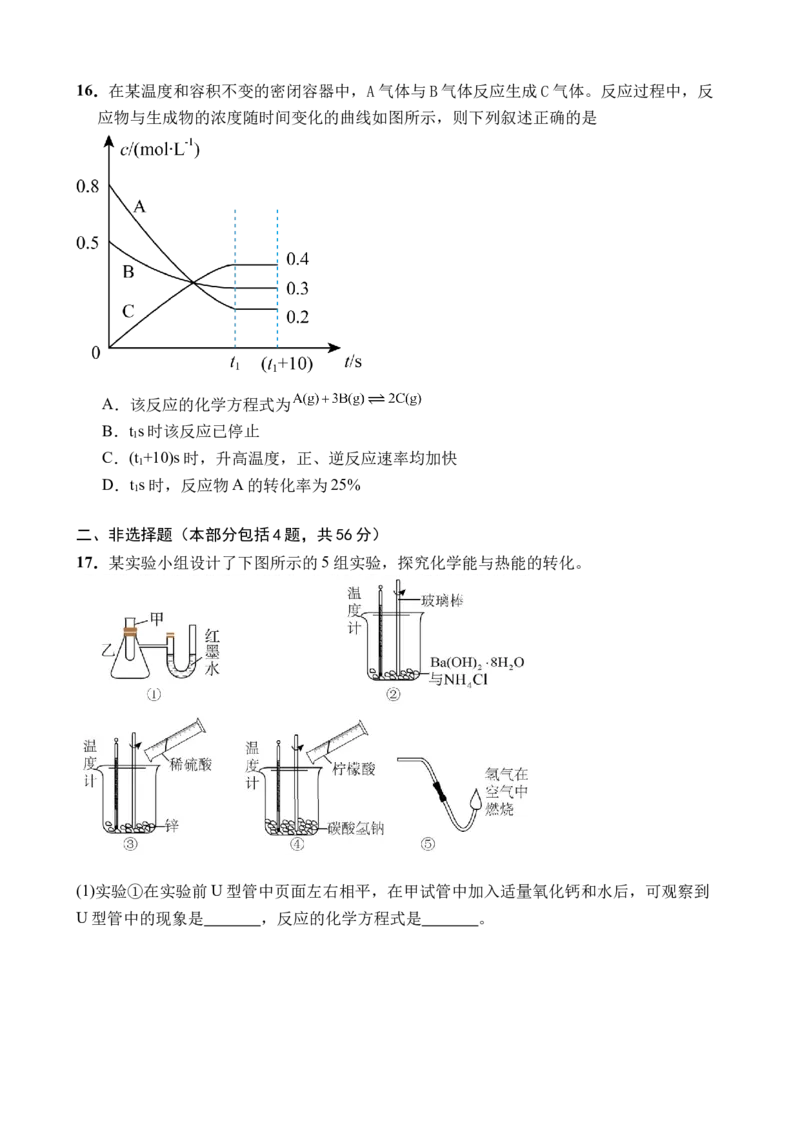
D.催化剂可以加快反应速率16.在某温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反
应物与生成物的浓度随时间变化的曲线如图所示,则下列叙述正确的是
A.该反应的化学方程式为
B.t s时该反应已停止
1
C.(t +10)s时,升高温度,正、逆反应速率均加快
1
D.t s时,反应物A的转化率为25%
1
二、非选择题(本部分包括4题,共56分)
17.某实验小组设计了下图所示的5组实验,探究化学能与热能的转化。
(1)实验①在实验前U型管中页面左右相平,在甲试管中加入适量氧化钙和水后,可观察到
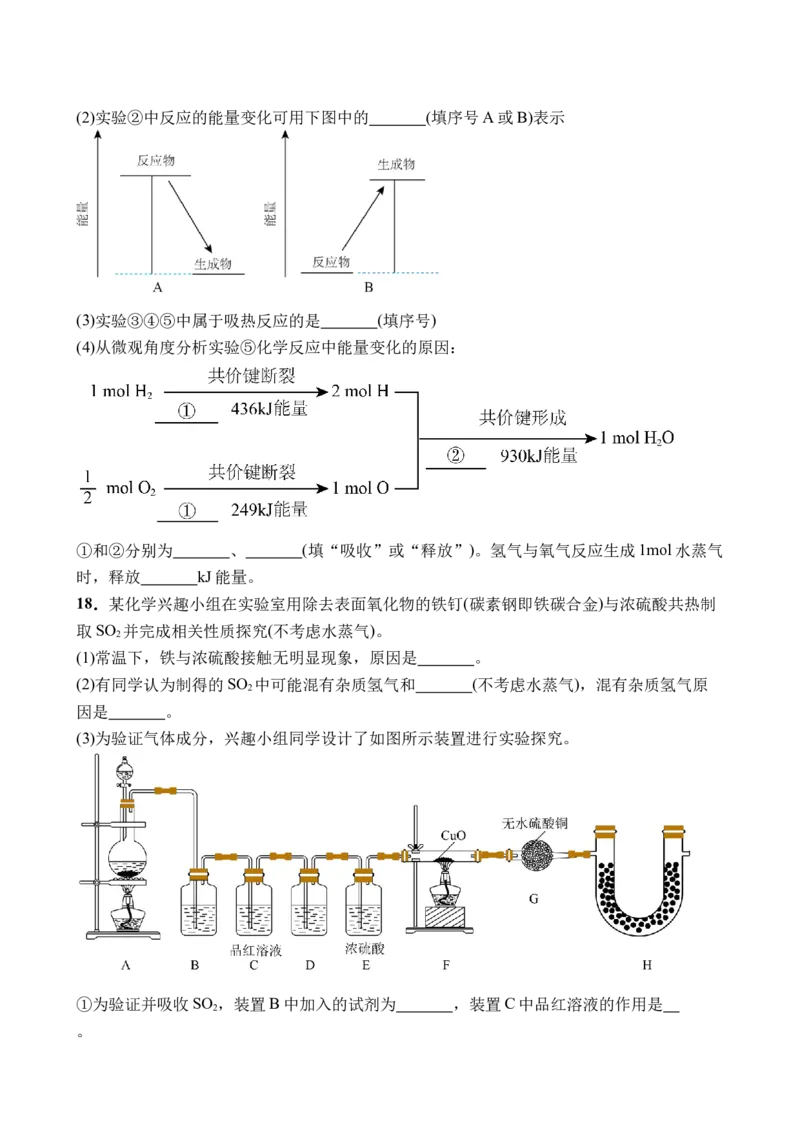
U型管中的现象是 ,反应的化学方程式是 。(2)实验②中反应的能量变化可用下图中的 (填序号A或B)表示
(3)实验③④⑤中属于吸热反应的是 (填序号)
(4)从微观角度分析实验⑤化学反应中能量变化的原因:
①和②分别为 、 (填“吸收”或“释放”)。氢气与氧气反应生成1mol水蒸气
时,释放 kJ能量。
18.某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢即铁碳合金)与浓硫酸共热制
取SO 并完成相关性质探究(不考虑水蒸气)。
2
(1)常温下,铁与浓硫酸接触无明显现象,原因是 。
(2)有同学认为制得的SO 中可能混有杂质氢气和 (不考虑水蒸气),混有杂质氢气原
2
因是 。
(3)为验证气体成分,兴趣小组同学设计了如图所示装置进行实验探究。
①为验证并吸收SO ,装置B中加入的试剂为 ,装置C中品红溶液的作用是
2
。②装置D中试剂为 。
③装置H的作用为 。
19.I.把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应
速率为0.1mol/(L·min),计算:
(1)B的转化率 。
(2)恒温达平衡时容器内的压强与开始时压强比 。
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
,碱性锌锰干电池的负极材料是 (填名
称),负极上发生的电极反应为 。若反应消耗13g负极材料,则电池中转移电子
的物质的量为 mol。
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为
。下列说法正确的是___________(填标号)。
A.电解液中H SO 的浓度始终保持不变
2 4
B.放电时正极上的电极反应式为
C.放电时,当外电路通过1mol电子时,理论上负极质量增加48g
D.放电时,溶液中的SO 2-向正极移动
420.Na S O ·5H O俗称“大苏打”,它是一种常用的试剂.
2 2 3 2
(1)工业上,常用Na S O 溶液吸收尾气中的Cl ,氧化产物为SO 2-.写出离子方程式:
2 2 3 2 4
.理论上,能发生的氧化还原反应都可以设计成原电池.如果将上述反应设计成原电池,则
正极反应式为 .
(2)已知:
某小组设计实验探究影响化学反应速率的外界因素:
序号 溶液 溶液 蒸馏水 温度 变浑浊时间
I 20ml 20ml 0 35℃ a s
II 20ml 16ml V mL 35℃ b s
III 20ml 20ml 0 45℃ c s
IV 20ml 15ml 5 mL 40℃ d s
①V= ,设计实验I,Ⅱ的目的是 .
②实验测得:a>c.由实验I、Ⅲ得出结论是 .
③根据表格信息, (填“能”或“不能”)比较a和d的大小,原因是
.
(3)已知:BaS O 是白色难溶物.大苏打易变质生成Na SO .设计实验证明某大苏打样品是
2 3 2 4
否变质: .