文档内容
2024~2025 学年度第一学期高一六校联合学业质量检
测
化 学
注意事项:
1.本试卷满分100分,考试时间60分钟。
2.答题前,考生务必将自己的姓名、准考证号等填写在答题卡的相应位置。
3.全部答案在答题卡上完成,答在本试题卷上无效。
4.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。
5.考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H1 O 16 Na 23 Mg 24 S32 Cl 35.5 Fe 56
一、选择题:本题共 16小题,共44分。第1~10小题,每小题 2分;第11~16 小题,每小题 4
分。每小题给出的四个选项中,只有一项是符合题目要求的。
1.五千年中华文化不仅能彰显民族自信、文化自信,还蕴含着许多化学知识。下列说法错误的是
A. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
B. “火树银花合,星桥铁锁开”中“火树银花”与金属的“焰色试验”相关
C. “司南之杓(勺),投之于地,其柢(勺柄)指南”,司南的“杓”中含有Fe₂O₃
D.战国时期的“长方形铁炉”标志着我国当时已经初步掌握冶铁技术
2.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述错误的是
A.通常状况下,干燥的氯气和 Fe不反应,可以用钢瓶运输液氯
B.苏打、小苏打的水溶液均显碱性,可用作食用碱
C.水果罐头中添加维生素C作抗氧化剂,是因为维生素C易被氧化
D.漂白粉在空气中久置变质,是因为其中的CaCl₂与空气中的CO₂反应生成CaCO₃
3.表中对于相关物质的分类全部正确的是
编号 纯净物 混合物 酸性氧化物 碱性氧化物 电解质 非电解质
A 液氯 氨水 CO Na₂O NH₃·H₂O NH₃
B 纯碱 冰水混合物 SO₂ CaO NaHCO₃ Cl₂
C 熟石灰 碘酒 SiO₂ FeO Na₂CO₃ 乙醇
D 氢气 盐酸 CO₂ Na₂O₂ K₂SO₄ CO
4.常温下,下列各组离子在溶液中一定能大量共存的是
A.M g2+ 、SO2−,Cl− 、K+ B.Na+ 、OH− 、NO− 、HCO−
4 3 3
C.Ca²⁺、ClO⁻、H⁺、Fe²⁺ D.Na⁺、Fe³⁺、SCN⁻,Cl⁻【高一六校联合学业质量检测 化学卷 第1页(共6页)】 5213A5.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 用盐酸去除公园铁护栏的铁锈(Fe₂O₃) Fe₂O₃ 是碱性氧化物
B 更换球场高压钠灯 钠单质具有强还原性
C 用“84”消毒液(NaClO)对衣物进行消毒 NaClO 具有氧化性
D 用NaHCO₃作膨松剂制作面包 NaHCO₃受热分解产生CO₂
6.在生产、生活中铁盐与亚铁盐有重要应用。下列有关离子方程式正确的是
A.铁粉与 FeCl₃溶液反应制备 FeCl₂:Fe+Fe³⁺ =2Fe²⁺
B.FeCl₃溶液与铜片反应制作印刷电路板: 2Fe³⁺ +3Cu=2Fe+3Cu²⁺
C.FeCl₃溶液与氨水反应制备 Fe(OH)₃:Fe³⁺ +3OH⁻ =Fe(OH)₃↓
D.双氧水与酸性的 FeCl₂溶液反应: 2Fe²⁺ +H₂O₂+2H⁺ =2Fe³⁺ +2H₂O
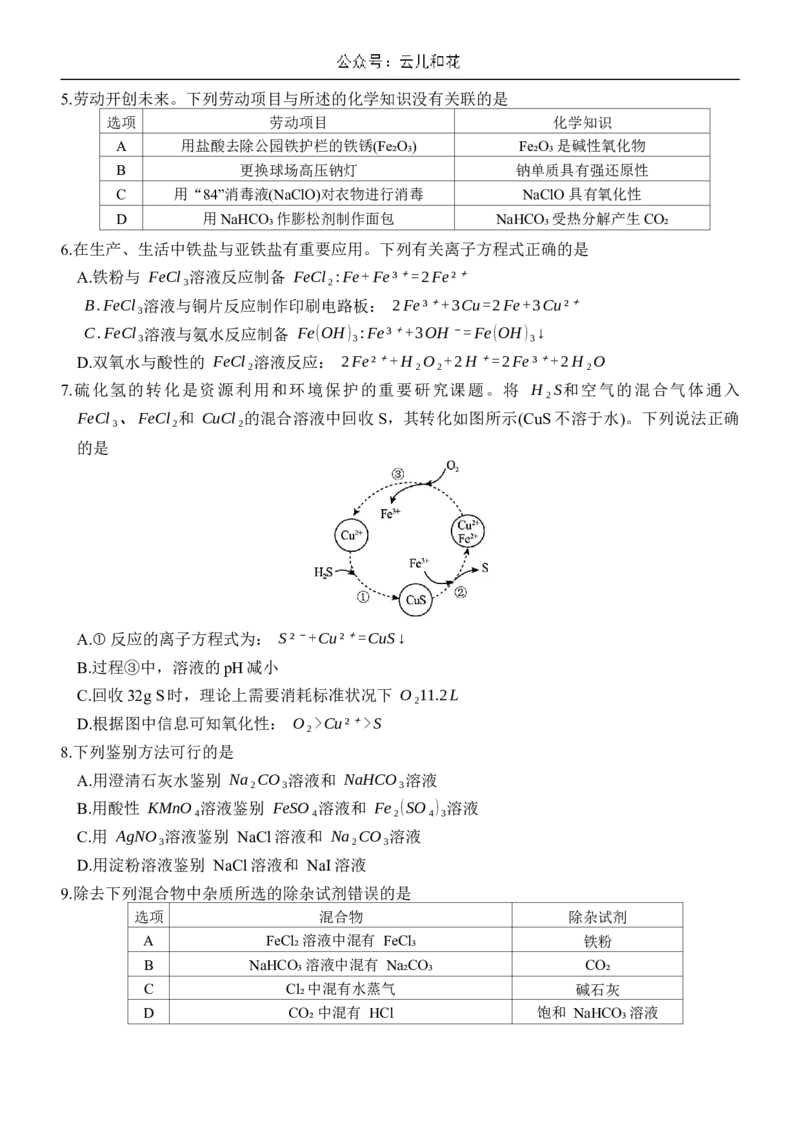
7.硫化氢的转化是资源利用和环境保护的重要研究课题。将 H₂S和空气的混合气体通入
FeCl₃、FeCl₂和 CuCl₂的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确
的是
A.①反应的离子方程式为: S²⁻ +Cu²⁺ =CuS↓
B.过程③中,溶液的pH减小
C.回收32g S时,理论上需要消耗标准状况下 O₂11.2L
D.根据图中信息可知氧化性: O₂>Cu²⁺ >S
8.下列鉴别方法可行的是
A.用澄清石灰水鉴别 Na₂CO₃溶液和 NaHCO₃溶液
B.用酸性 KMnO₄溶液鉴别 FeSO₄溶液和 Fe₂(SO₄)₃溶液
C.用 AgNO₃溶液鉴别 NaCl溶液和 Na₂CO₃溶液
D.用淀粉溶液鉴别 NaCl溶液和 NaI溶液
9.除去下列混合物中杂质所选的除杂试剂错误的是
选项 混合物 除杂试剂
A FeCl₂溶液中混有 FeCl₃ 铁粉
B NaHCO₃溶液中混有 Na₂CO₃ CO₂
C Cl₂中混有水蒸气 碱石灰
D CO₂ 中混有 HCl 饱和 NaHCO₃溶液【高一六校联合学业质量检测 化学卷 第2页(共6页)】 5213A10.下列各组物质中,物质之间通过一步反应能实现如图所示转化的是
选项 a b c
A Fe Fe₂O₃ Fe(OH)₃
B Na Na₂O₂ Na₂CO₃
C Cl₂ HClO HCl
D Na NaOH NaHCO₃
11.用下列装置或操作进行相应实验,不能达到实验目的的是
A.用图①探究氧化性: KMnO₄>Cl₂>I₂
B.用图②测新制氯水的 pH
C.用图③制备少量 Fe(OH)₂并能较长时间看到其白色
D.用图④验证 Na 和水反应是否为放热反应
12. NA表示阿伏加德罗常数,下列判断正确的是
A.常温常压下,32 g O₂和O₃混合气体中氧原子总数为4N
A
B.7.8gNa₂O₂与足量 H₂O反应转移电子总数为0.2N
A
C.足量的Cl₂与5.6g Fe完全反应时,转移的电子数为0.3N
A
D.含 NA个Na⁺的Na₂O溶解于1 L水中,Na⁺的物质的量浓度为 1mol⋅L⁻¹
13. “细菌冶金”是近代湿法治金的一种新工艺。例如氧化亚铁硫杆菌能利用空气中的氧气将黄铁
矿氧化,其原理为 FeS₂+O₂+H₂O→Fe₂(SO₄)₃+H₂SO₄(未配平)。下列说法错误的是
A. FeS₂中硫元素化合价为-1价
B.氧气在反应中做氧化剂,被还原
C.每1 mol FeS₂被氧化,转移 14 mol 电子
D. “细菌冶金”工艺符合绿色环保理念
14.部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.通过化合反应和复分解反应均能直接得到 d
B.a→f→g→d的每步转化均可一步实现
C. h具有强氧化性,在日常生活中可用于生活用水的消毒与
净化
D.可将g加入浓碱液中制得 d的胶体
【高一六校联合学业质量检测 化学卷 第3页(共6页)】 5213A15.某同学结合所学知识探究 Na₂O₂与 H₂能否反应,设计装置如图,下列说法正确的是
A.装置A气密性的检查方法:直接向长颈漏斗中加水,当漏斗中液面高于试管中液面且高度
不变,说明气密性良好
B.为达到实验目的需在装置B中盛放无水CaCl₂
C.装置A也可直接用于碳酸钠与稀硫酸反应制取CO₂
D.反应结束后,将玻璃管C处固体加水溶解,滴加酚酞变红,不能证明C中生成了NaOH
16.2020年9月,研究人员在金星大气中探测到了磷化氢 (PH₃)气体。 PH₃常作为一种熏蒸剂,
在贮粮中用于防治害虫,一种制备 PH₃的流程如图所示,下列说法正确的是
A.流程中,每一步均属于氧化还原反应
B.次磷酸的分子式为 H₃PO₂,,属于三元酸
C.理论上,1m ol白磷可生产 2.5molPH₃
D.白磷与浓 NaOH溶液反应的化学方程式为: P +3NaOH(浓)≜PH ↑+3NaH PO
4 3 2 2
二、非选择题:本题共3小题,共56分。
17.(20分)“84”消毒液是家居常用品,某小组同学查看包装说明,得到如下信息:
该小组同学进行了如下实验,回答下列问题:
(1)稀释:将“84”消毒液原液稀释配制成480 mL c(NaClO)=0.10 mol·L⁻¹的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。
②稀释时,需要取用 mL“84”消毒液原液。
③下列操作会使溶液中 NaClO浓度偏低的是 (填标号)。
A.取用久置的“84”消毒液原液进行稀释
B.定容时,俯视刻度线
C.量取“84”消毒液原液时,俯视读数
D.转移溶液前容量瓶内有少量蒸馏水
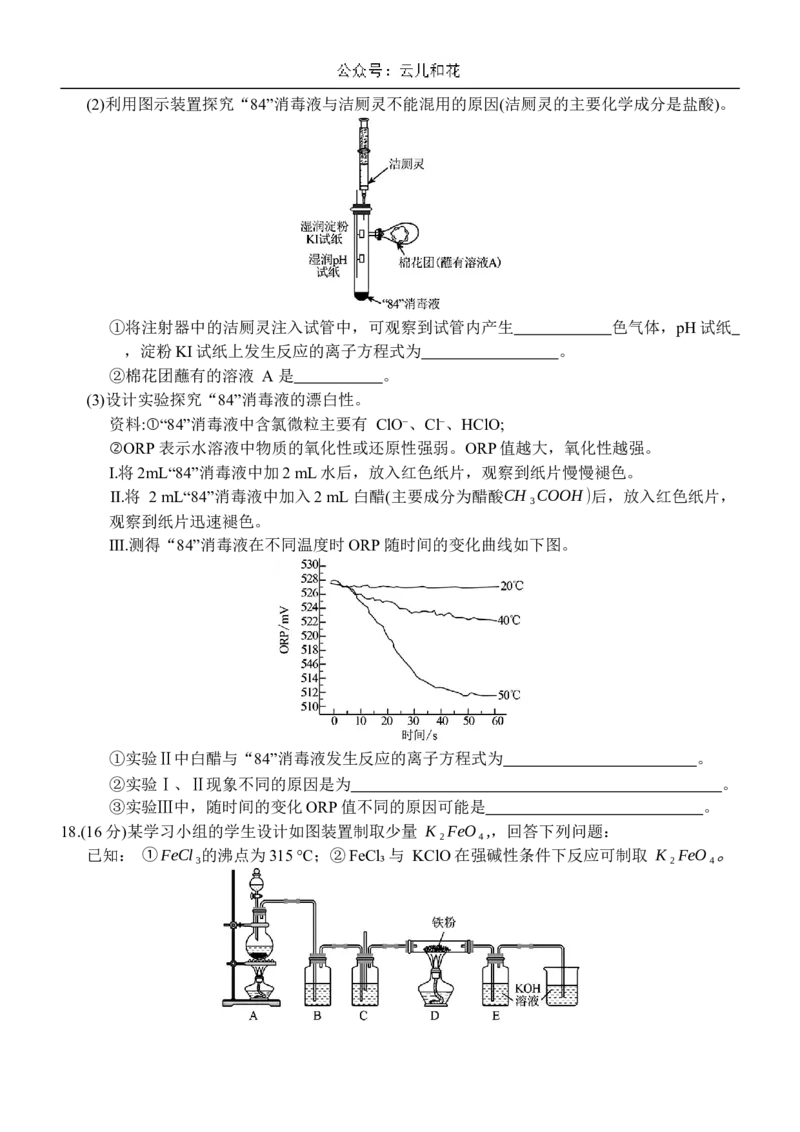
【高一六校联合学业质量检测 化学卷 第4页(共6页)】 5213A(2)利用图示装置探究“84”消毒液与洁厕灵不能混用的原因(洁厕灵的主要化学成分是盐酸)。
①将注射器中的洁厕灵注入试管中,可观察到试管内产生 色气体,pH试纸
,淀粉KI试纸上发生反应的离子方程式为 。
②棉花团蘸有的溶液 A 是 。
(3)设计实验探究“84”消毒液的漂白性。
资料:①“84”消毒液中含氯微粒主要有 ClO⁻、Cl⁻、HClO;
②ORP 表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
Ⅰ.将2mL“84”消毒液中加2 mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.将 2 mL“84”消毒液中加入2 mL 白醋(主要成分为醋酸CH₃COOH)后,放入红色纸片,
观察到纸片迅速褪色。
Ⅲ.测得“84”消毒液在不同温度时ORP 随时间的变化曲线如下图。
①实验Ⅱ中白醋与“84”消毒液发生反应的离子方程式为 。
②实验Ⅰ、Ⅱ现象不同的原因是为 。
③实验Ⅲ中,随时间的变化ORP值不同的原因可能是 。
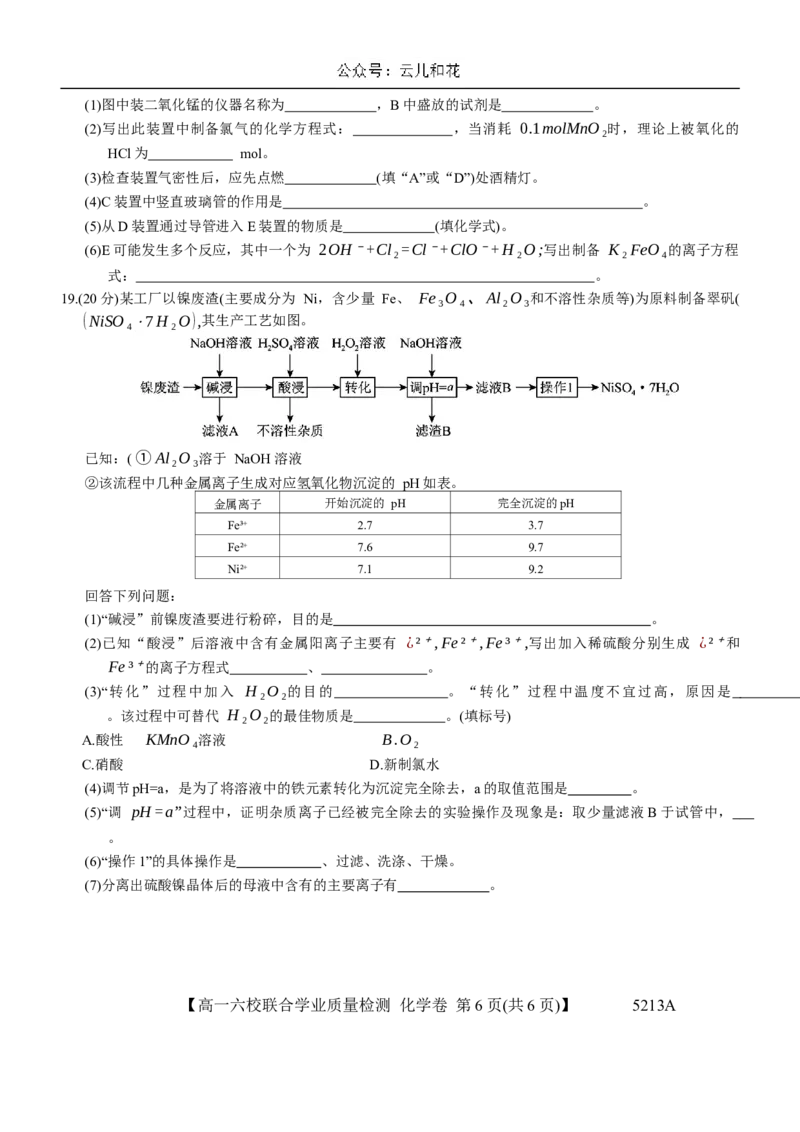
18.(16分)某学习小组的学生设计如图装置制取少量 K₂FeO₄,,回答下列问题:
已知: ①FeCl₃的沸点为315 ℃;②FeCl₃与 KClO在强碱性条件下反应可制取 K₂FeO₄。【高一六校联合学业质量检测 化学卷 第5页(共6页)】 5213A(1)图中装二氧化锰的仪器名称为 ,B中盛放的试剂是 。
(2)写出此装置中制备氯气的化学方程式: ,当消耗 0.1molMnO₂时,理论上被氧化的
HCl为 mol。
(3)检查装置气密性后,应先点燃 (填“A”或“D”)处酒精灯。
(4)C装置中竖直玻璃管的作用是 。
(5)从D装置通过导管进入E装置的物质是 (填化学式)。
(6)E可能发生多个反应,其中一个为 2OH⁻ +Cl₂=Cl⁻ +ClO⁻ +H₂O;写出制备 K₂FeO₄的离子方程
式: 。
19.(20分)某工厂以镍废渣(主要成分为 Ni,含少量 Fe、 Fe₃O₄、Al₂O₃和不溶性杂质等)为原料制备翠矾(
(NiSO₄⋅7H₂O),其生产工艺如图。
已知:( ①Al₂O₃溶于 NaOH 溶液
②该流程中几种金属离子生成对应氢氧化物沉淀的 pH如表。
金属离子 开始沉淀的 pH 完全沉淀的pH
Fe³⁺ 2.7 3.7
Fe²⁺ 7.6 9.7
Ni²⁺ 7.1 9.2
回答下列问题:
(1)“碱浸”前镍废渣要进行粉碎,目的是 。
(2)已知“酸浸”后溶液中含有金属阳离子主要有 ¿²⁺,Fe²⁺,Fe³⁺,写出加入稀硫酸分别生成 ¿²⁺和
Fe³⁺的离子方程式 、 。
(3)“转化”过程中加入 H₂O₂的目的 。“转化”过程中温度不宜过高,原因是
。该过程中可替代 H₂O₂的最佳物质是 。(填标号)
A.酸性 KMnO₄溶液 B.O₂
C.硝酸 D.新制氯水
(4)调节pH=a,是为了将溶液中的铁元素转化为沉淀完全除去,a的取值范围是 。
(5)“调 pH=a”过程中,证明杂质离子已经被完全除去的实验操作及现象是:取少量滤液B于试管中,
。
(6)“操作1”的具体操作是 、过滤、洗涤、干燥。
(7)分离出硫酸镍晶体后的母液中含有的主要离子有 。
【高一六校联合学业质量检测 化学卷 第6页(共6页)】 5213A