文档内容
学科⽹(北京)股份有限公司
⼴东省2025—2026 学年领航⾼中联盟12 ⽉⾼⼀检测考试
化学参考答案及评分细则
1. 【答案】C
【解析】不锈钢盆的主要成分为铁和铬,天然磁铁的主要成分为Fe3O4,⾚铁矿的主
要成分为Fe2O3,铸铁井盖的主要成分为铁,C 项符合题意,A、B、D 项不符合题
意。
2. 【答案】D
【解析】同素异形体的研究对象是单质,C2H5OH 和CH3COOH 都是化合物,⼆者不
互为同素异形体,A 项错误;CO 不属于酸性氧化物,B 项错误;雪融化为⽔属于物
理变化,C 项错误;Cu 的活动性弱于H,常温下不会与稀盐酸发⽣置换反应,D 项正
确。
3. 【答案】A
【解析】Fe3+、H+、
三者不会发⽣反应,能⼤量共存,A 项符合题意;H+、Cl-、
ClO-三者会发⽣氧化还原反应⽣成Cl2 等⽽不能⼤量共存,B 项不符合题意;HC
和OH-会发⽣反应⽣成
和H2O ⽽不能⼤量共存,C 项不符合题意;Fe2+会与ClO-
发⽣氧化还原反应⽽不能⼤量共存,D 项不符合题意。
4. 【答案】D
【解析】溶解FeSO4 固体时,搅拌可以加快溶解速率,A 项正确;煮沸NaOH 溶液可
除去溶解在NaOH 溶液中的氧⽓,B 项正确;将NaOH 溶液挤⼊FeSO4 溶液中制备
Fe(OH)2,植物油膜可以隔绝空⽓,C 项正确;振荡会使Fe(OH)2 被空⽓中的氧
⽓氧化,D 项错误。
5. 【答案】B
【解析】还原铁粉易与O2 反应,且⽆毒⽆害,常⽤作⻝品脱氧剂,A 项正确;NaCl
的焰⾊呈⻩⾊不是发⽣化学反应导致的,B 项错误;H2O 的相对分⼦质量为18,则
H2O 的摩尔质量为18 g· mol-1,C 项正确;Fe 与CH3COOH 反应⽣成Fe2+,Fe2+能
补充⼈体所需要的铁元素,D 项正确。
6. 【答案】C
学科⽹(北京)股份有限公司
【解析】摩尔是物质的量的单位,物质的量表示含有⼀定数⽬粒⼦的集合体的物理
量,A 项错误;固态物质粒⼦之间的距离⾮常⼩,等物质的量的固态物质的体积主要
取决于粒⼦的⼤⼩,B 项错误;6. 02× 1022 个O3 分⼦的物质的量约为0. 1 mol,质量
约为4. 8 g,C 项正确;传统杆秤(由⽊制秤杆、⾦属秤砣、提纽组成)是利⽤杠杆
原理称量物质的质量,称量原理与量筒不相同,D 项错误。
7. 【答案】C
【解析】往容量瓶中转移溶液前,容量瓶刻度线下内壁可以残留⽔珠,不会影响最终
所配制的溶液的体积,因为定容过程需要添加⽔⾄溶液的凹液⾯最低处与刻度线⻬
平,C 项错误。
8. 【答案】B
【解析】FeSO4 易被氧化,保存FeSO4 溶液时需加⼊适量铁粉,A 项不符合题意;将
Cl2 通⼊冷的⽯灰乳中,发⽣反应:2Ca(OH)2+2Cl2
CaCl2+Ca(ClO)2+
2H2O,制得有效成分为Ca(ClO)2 的漂⽩粉,B 项符合题意;覆铜板放到FeCl3 溶
液中制作印刷电路板,反应的离⼦⽅程式为2Fe3++Cu
2Fe2++Cu2+,C 项不符
合题意;⽤主要成分为CaCO3 的抗胃酸药物治疗胃酸过多,反应的离⼦⽅程式为
CaCO3+2H+
Ca2++CO2↑+H2O,D 项不符合题意。
9. 【答案】A
【解析】根据n=
可知,等质量的CH4、N2、CO2 和Cl2 的物质的量⼤⼩为n
(CH4)>n(N2)>n(CO2)>n(Cl2),同温同压条件下,⽓体的物质的量之⽐等
于⽓体的体积之⽐,故V(CH4)>V(N2)>V(CO2)>V(Cl2),①②③④四室
的⽓体分别为Cl2、CH4、N2 和CO2,A 项符合题意。
10. 【答案】B
【解析】未说明溶液体积,⽆法计算0. 5 mol· L-1 Na2SO4 溶液中Na+的数⽬,A 项
错误;1 mol H2O 含有2 mol H 原⼦,B 项正确;23 g Na+含有的核外电⼦总数为
10NA,C 项错误;未说明温度和压强,⽆法确定1. 12 L H2 含有的分⼦数⽬,D 项错
误。
11. 【答案】A
学科⽹(北京)股份有限公司
【解析】100 mL 1 mol· L-1 NaCl 溶液、0. 05 L 1 mol· L-1 NaCl 溶液、0. 1 L 1
mol· L-1 盐酸、10 mL 5 mol· L-1 盐酸分别含有0. 1 mol NaCl、0. 05 mol NaCl、0. 1
mol HCl 和0. 05 mol HCl,溶质的质量分别为5. 85 g、2. 925 g、3. 65 g 和1. 825 g,A
项符合题意。
12. 【答案】D
【解析】反应①不属于氧化还原反应,反应②属于氧化还原反应,A 项错误;反应②
的电⼦转移情况可表示为
,B 项错误;反应①为SO2+
2NH3· H2O
(NH4)2SO3+H2O,1 L 5 mol· L-1 氨⽔中含有5 mol 溶质,最多能
与2. 5 mol SO2 反应⽣成2. 5 mol (NH4)2SO3,C 项错误;根据质量守恒定律和得失
电⼦守恒规律可知总反应⽅程式为2SO2+4NH3· H2O+O2
2(NH4)2SO4+
2H2O,D 项正确。
13. 【答案】B
【解析】未说明温度和压强,A 项错误;H2 能在Cl2 中燃烧说明燃烧不⼀定需要O2,
B 项正确;在FeCl3 溶液中加⼊⾜量铁粉,发⽣反应的离⼦⽅程式为2Fe3++Fe
3Fe2+,C 项错误;FeCl2 溶液使酸性KMnO4 溶液褪⾊体现了FeCl2 溶液的还原性,D
项错误。
14. 【答案】C
【解析】蚀刻废液中含有的CuCl2 和HCl 会与Fe 反应,“ 反应” 不能在铁制容器中
进⾏,A 项正确;“ 操作1” 为过滤,实验室进⾏过滤操作时需⽤玻璃棒引流,B 项
正确;氯化铜蚀刻废液中Cu2+含量为160 g· L-1,1 L 溶液中含有2. 5 mol Cu 元
素,理论上可制备1. 25 mol Cu2O,C 项错误;颗粒直径为20 nm 的Cu2O 形成的分散
系为胶体,能产⽣丁达尔效应,D 项正确。
15. 【答案】C
【解析】浓盐酸与⾼锰酸钾发⽣反应:16HCl(浓)+2KMnO4
5Cl2↑+2KCl+
2MnCl2+8H2O,体现了浓盐酸的还原性和酸性,A 项正确;NaOH 溶液可吸收多余的
学科⽹(北京)股份有限公司
Cl2,防⽌污染环境,B 项正确;Cu 和Cl2 在加热时会反应⽣成CuCl2,C 项错误;根
据⽅程式:16HCl(浓)+2KMnO4
5Cl2↑+2KCl+2MnCl2+8H2O,⽣成1 mol
Cl2 时,有0. 4 mol KMnO4 被还原,D 项正确。
16. 【答案】D
【解析】根据图中转化关系及题⼲信息可知,a、b、c、d 分别为NaClO、HCl、Na、
Fe。Cl2 与NaOH 溶液反应⽣成NaClO、Cl2 与H2O 反应⽣成HClO 时,体现了Cl2 的
氧化性和还原性,Cl2 与Na、Fe 的反应中,Cl2 均体现了氧化性,A 项错误;铁与少
量Cl2 反应⽣成FeCl3,B 项错误;Fe 与⽔蒸⽓在⾼温条件下反应⽣成Fe3O4 和H2,C
项错误;常温下,NaClO 和HCl 能发⽣化学反应⽣成Cl2、NaCl 和H2O,D 项正确。
17. 【答案】(1)氧化(1 分)
(2)①检验装置⽓密性(1 分)
浓硫酸(1 分)
②E 处硬质玻璃管内⿊⾊固体变红(2 分)
(3)①玻璃棒、胶头滴管(2 分,1 个1 分)
20. 0(2 分,写“ 20” 扣1 分)
偏
⼩(1 分)
②KSCN(2 分)
2Fe2++H2O2+2H+
2Fe3++2H2O(2 分,物质正确1 分,配
平1 分)
【解析】(1)铁⽣锈时,铁作还原剂,发⽣了氧化反应。
(2)①加药品前需要检验装置⽓密性;H2 还原CuO 前需要⼲燥H2,故试剂a 为浓
硫酸。②E 处硬质玻璃管内⿊⾊固体变红说明有还原性的H2 产⽣。
(3)①⽤1. 0 mol· L-1 硫酸配制50 mL 0. 4 mol· L-1 硫酸,需要使⽤的玻璃仪器
有量筒、烧杯、50 mL 容量瓶、玻璃棒(⽤于搅拌和引流)和胶头滴管(⽤于定
容),需要⽤量筒量取
=20. 0 mL 1. 0 mol· L-1 硫酸;配制过程中,若
定容时仰视刻度线,则最终配制的溶液体积偏⼤,所配制的硫酸浓度偏⼩。②KSCN
溶液与Fe3+反应会使溶液变红,可⽤来检验Fe3+;强酸性条件下,Fe2+被氧化为Fe3
+,H2O2 被还原为H2O,反应的离⼦⽅程式为2Fe2++H2O2+2H+
2Fe3++
2H2O。
18. 【答案】(1)0. 1NA(2 分)
学科⽹(北京)股份有限公司
(2)1(2 分)
2(2 分)
(3)1:2(2 分)
16:1(2 分)
(4)0. 8(2 分)
8. 8(2 分)
【解析】(1)标准状况下,1. 12 L O2 的物质的量为
=0. 05 mol,含有0. 05
mol× 2× NA mol-1=0. 1NA 个O 原⼦。
(2)71 g Cl2 的物质的量为1 mol,根据反应:Cl2+2FeCl2
2FeCl3 可知1 mol Cl2
最多能消耗2 mol FeCl2,即71 g Cl2 最多能消耗2 L 1 mol· L-1FeCl2 溶液。
(3)同温同压下,⽓体的体积之⽐等于⽓体的物质的量之⽐,⽓体的密度之⽐等于
⽓体的摩尔质量之⽐,所以常温常压下,1 L 的O2 和2 L 的H2 的物质的量之⽐为
1:2,密度之⽐为32:2=16:1。
(4)设1 mol CO 和CO2 的混合⽓体中有x mol CO 和y mol CO2,则x+y=1 且28x
+44y=31. 2,求出x=0. 8、y=0. 2。则1 mol 该混合⽓体中CO 的物质的量为0. 8
mol,CO2 的质量为0. 2 mol× 44 g· mol-1=8. 8 g。
19. 【答案】(1)分解反应(2 分,未写“ 反应” 扣1 分)
(2)4. 48(2 分)
BC(2 分,1 个1 分,多选、错选不得分)
(3)Cl2+2Br-
2Cl-+Br2(2 分,物质正确1 分,配平1 分)
96(2 分)
(4)加⼊稀硝酸酸化的AgNO3 溶液(2 分,合理表述均可)
(5)24(2 分)
【解析】(1)⻉壳的主要成分为CaCO3,CaCO3 ⾼温分解为CaO 和CO2,属于分解
反应。
(2)电解饱和⻝盐⽔的反应⽅程式为2NaCl+2H2O
Cl2↑+H2↑+2NaOH,转移
0. 4 mol e-的同时可⽣成0. 2 mol H2,换算成标准状况下的体积为4. 48 L。饱和⻝盐
⽔为混合物,既不属于电解质也不属于⾮电解质,A 项错误;NaCl 在⽔中全部电离为
Na+和Cl-:NaCl
Na++Cl-,B 项正确;实验室中可⽤饱和⻝盐⽔除去Cl2 中混
有的HCl,C 项正确;钾的活泼性强于钠,向饱和⻝盐⽔中加⼊钾,钾会与⽔发⽣反
应,D 项错误。
学科⽹(北京)股份有限公司
(3)反应①为Cl2 氧化Br-,反应的离⼦⽅程式为Cl2+2Br-
2Cl-+Br2;反应
②的离⼦⽅程式为
+5Br-+6H+
3Br2+3H2O,消耗1 mol Br-时,理论上⽣
成× 160 g=96 g Br2。
(4)检验最后⼀次洗涤液中⽆Cl-的操作为取最后⼀次洗涤液,加⼊稀硝酸酸化的
AgNO3 溶液,溶液中⽆⽩⾊沉淀产⽣。
(5)反应:2MgO+Si
2Mg↑+SiO2 中,MgO 为氧化剂,Mg 为还原产物,消耗1
mol MgO,⽣成24 g Mg。
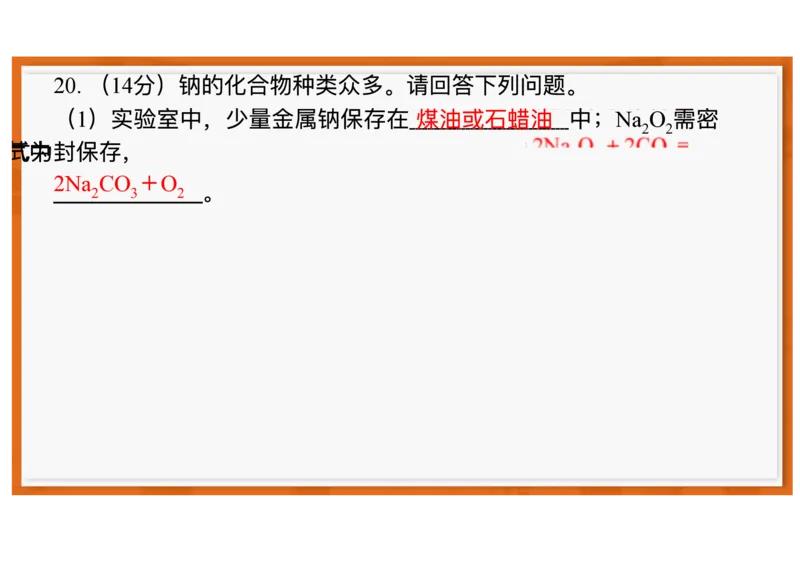
20. 【答案】(1)煤油(或⽯蜡油,2 分)
2Na2O2+2CO2
2Na2CO3+O2(2
分,物质正确1 分,配平1 分)
(2)A(1 分)
A(1 分)
0. 02 mol(2 分,未写单位扣1 分)
(3)①2NaHCO3+CaCl2
CaCO3↓+2NaCl+H2CO3 (2 分,物质正确1 分,未
配平、未写“ ↓” 扣1 分,写NaHCO3+CaCl2
CaCO3↓+NaCl+HCl 得1 分)
②CO2(2 分)
(4)往溶液中通⼊⾜量的CO2(2 分,类似表述均可)
【解析】(1)为了隔绝空⽓,钠常常保存在⽯蜡油或煤油中。
(2)NaHCO3 与盐酸反应产⽣CO2 的速率更快,故A 装置⽓球胀⼤速率更快;n(HCl)=
0. 02 mol、n(NaHCO3)=
mol、n(Na2CO3)=
mol,盐酸过量,A 装置产⽣
mol CO2,B 装置产⽣
mol CO2,充分反应后恢复⾄室温,A 装置中的⽓球体积
更⼤。
(3)①实验2 中,1 mol· L-1 NaHCO3 溶液与0. 5 mol· L-1 CaCl2 溶液反应,溶液
中产⽣⽩⾊沉淀但没有产⽣⽓体,说明没有产⽣CO2,反应的化学⽅程式为2NaHCO3
+CaCl2
CaCO3↓+2NaCl+H2CO3。②实验3 中,⽣成了较多的H2CO3,H2CO3
分解产⽣了CO2,故⽓体为CO2。
(4)往含有Na2CO3 杂质的NaHCO3 溶液中通⼊⾜量CO2,发⽣反应:Na2CO3+CO2
+H2O
2NaHCO3,即可除去Na2CO3。
⼴东省2025—2026学年领航⾼中联盟12⽉⾼⼀检测考试
化学试卷
⼀、选择题:本题共16⼩题,共44分,第1~10⼩题,每⼩题2分;第
11~16⼩题,每⼩题4分。在每⼩题给出的四个选项中,只有⼀项是
符合题⽬要求的。
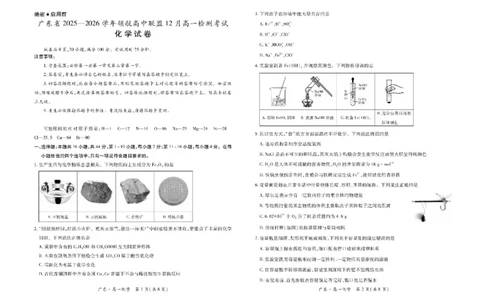
1. ⽣产⽣活与化学物质息息相关。下列物质的主要成分为Fe2O3的是
A. 不锈钢盆
B. 天然磁铁
C. ⾚铁矿
D. 铸铁井盖
【答案】C
【解析】不锈钢盆的主要成分为铁和铬,天然磁铁的主要成分为
Fe3O4,⾚铁矿的主要成分为Fe2O3,铸铁井盖的主要成分为铁,C项
符合题意,A、B、D项不符合题意。
2. “绿蚁新醅酒,红泥⼩⽕炉。晚来天欲雪,能饮⼀杯⽆?”中的意境
美不胜收,更蕴含了丰富的化学知识。下列说法正确的是
A. ⻩酒中含有的C2H5OH和CH3COOH互为同素异形体
B. ⽊炭在缺氧条件下燃烧会⽣成CO,CO属于酸性氧化物
C. 雪融化为⽔属于化学变化
D. 古代⻘铜酒杯中含有⾦属Cu,Cu常温下不会与稀盐酸发⽣置换反
应
【答案】D
【解析】同素异形体的研究对象是单质,C2H5OH和CH3COOH都是
化合物,⼆者不互为同素异形体,A项错误;CO不属于酸性氧化
物,B项错误;雪融化为⽔属于物理变化,C项错误;Cu的活动性弱
于H,常温下不会与稀盐酸发⽣置换反应,D项正确。
3. 下列离⼦在溶液中能⼤量共存的是
A. Fe3+、H+、
B. H+、Cl-、ClO-
C. K+、HC
、OH
-
D. Na+、Fe2+、ClO-
【答案】A
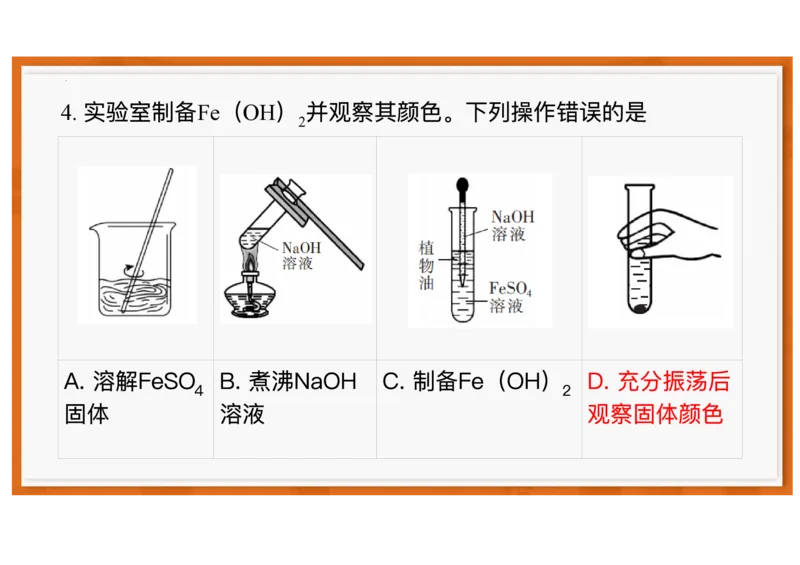
4. 实验室制备Fe(OH)2并观察其颜⾊。下列操作错误的是
A. 溶解FeSO4
固体
B. 煮沸NaOH
溶液
C. 制备Fe(OH)2 D. 充分振荡后
观察固体颜⾊
【答案】D
【解析】溶解FeSO4固体时,搅拌可以加快溶解速率,A项正确;煮沸
NaOH溶液可除去溶解在NaOH溶液中的氧⽓,B项正确;将NaOH溶液
挤⼊FeSO4溶液中制备Fe(OH)2,植物油膜可以隔绝空⽓,C项正确;
振荡会使Fe(OH)2被空⽓中的氧⽓氧化,D项错误。
5. ⺠以⻝为天,“⻝”的⽅⽅⾯⾯都离不开化学。下列说法错误的是
A. 还原铁粉常⽤作⻝品脱氧剂
B. NaCl是必不可少的调味品,其在⽕焰上灼烧会发⽣化学反应⽽使⽕焰
呈特殊颜⾊
C. H2O是⼈体不可或缺的营养物质,H2O的摩尔质量为18 g·mol-1
D. 铁锅烹制酸甜⻥时,⻝醋会与铁锅反应⽣成Fe2+,能帮助⻝⽤者补铁
【答案】B
【解析】还原铁粉易与O2反应,且⽆毒⽆害,常⽤作⻝品脱氧剂,A项
正确;NaCl的焰⾊呈⻩⾊不是发⽣化学反应导致的,B项错误;H2O的
相对分⼦质量为18,则H2O的摩尔质量为18 g·mol-1,C项正确;Fe与
CH3COOH反应⽣成Fe2+,Fe2+能补充⼈体所需要的铁元素,D项正确。
6. 度量衡是指在⽇常⽣活中计量物体⻓度、容积、重量的统称。下列
说法正确的是
A. 摩尔是表示含有⼀定数⽬粒⼦的集合体的物理量
B. 等物质的量的固态物质的体积主要取决于固体粒⼦之间的距离
C. 6.02×1022个O3分⼦的总质量约为4.8 g
D. 传统杆秤(如图)的称量原理与量筒相同
【答案】C
【解析】摩尔是物质的量的单位,物质的量表示含有⼀定数⽬粒⼦的
集合体的物理量,A项错误;固态物质粒⼦之间的距离⾮常⼩,等物
质的量的固态物质的体积主要取决于粒⼦的⼤⼩,B项错误;6.02×1022
个O3分⼦的物质的量约为0.1 mol,质量约为4.8 g,C项正确;传统杆秤
(由⽊制秤杆、⾦属秤砣、提纽组成)是利⽤杠杆原理称量物质的质量,
称量原理与量筒不相同,D项错误。
7. 容量瓶是细颈、梨形的平底玻璃瓶,下列关于容量瓶的说法错
误的是
A. 容量瓶上标有温度和容积,瓶⼝配有磨⼝玻璃塞或塑料塞
B. 实验室使⽤容量瓶来配制⼀定体积、⼀定物质的量浓度的溶液
C. 往容量瓶中转移溶液前,容量瓶刻度线下内壁不能残留⽔珠
D. 在使⽤前,⾸先要检查容量瓶是否完好,瓶⼝处是否漏⽔
【答案】C
【解析】往容量瓶中转移溶液前,容量瓶刻度线下内壁可以残留⽔珠,
不会影响最终所配制的溶液的体积,因为定容过程需要添加⽔⾄溶液的
凹液⾯最低处与刻度线⻬平,C项错误。
8. 劳动精神是中华⽂明⽣⽣不息的精神密码。下列所述化学知识正确且
与劳动项⽬有关联的是
选
项
劳动项⽬
化学知识
A 保存FeSO4溶液时加⼊适量铁粉
FeSO4⻅光易分解
B 将Cl2通⼊冷的⽯灰乳中制得漂⽩粉2Ca(OH)2+2Cl2 CaCl2
+Ca(ClO)2+2H2O
C 覆铜板放到FeCl3溶液中制作印刷电
路板
Fe3++Cu
Fe2++Cu2+
D ⽤主要成分为CaCO3的抗胃酸药物
治疗胃酸过多
+2H+ CO2↑
+H2O
【答案】B
9. ⼀密闭容器被隔板分成四室,隔板与器壁之间⽆间隙但隔板可⾃
由滑动,将等质量的CH4、N2、CO2和Cl2四种⽓体分别充⼊某⼀室,
待容器内温度恢复⾄室温,各隔板的位置最终如图所示,则②室的
⽓体为
①
②
③
④
A. CH4
B. N2
C. CO2
D. Cl2
【答案】A
10. 设NA为阿伏加德罗常数的值,下列说法正确的是
A. 0.5 mol·L-1 Na2SO4溶液中含有的Na+数⽬为NA
B. 1 mol H2O含有的H原⼦数⽬为2NA
C. 23 g Na+含有的核外电⼦总数为 NA
D. 1.12 L H2含有的分⼦数⽬为0.05NA
【答案】B
【解析】未说明溶液体积,⽆法计算0.5 mol·L-1 Na2SO4溶液中Na+的
数⽬,A项错误;1 mol H2O含有2 mol H原⼦,B项正确;23 g Na+含
有的核外电⼦总数为10NA,C项错误;未说明温度和压强,⽆法确定
1.12 L H2含有的分⼦数⽬,D项错误。
11. 下列溶液中,溶质的质量最⼤的是
A. 100 mL 1 mol·L-1 NaCl溶液
B. 0.05 L 1 mol·L-1 NaCl溶液
C. 0.1 L 1 mol·L-1 盐酸
D. 10 mL 5 mol·L-1 盐酸
【答案】A
【解析】100 mL 1 mol·L-1 NaCl溶液、0.05 L 1 mol·L-1 NaCl溶液、0.1 L
1 mol·L-1 盐酸、10 mL 5 mol·L-1 盐酸分别含有0.1 mol NaCl、0.05 mol
NaCl、0.1 mol HCl和0.05 mol HCl,溶质的质量分别为5.85 g、2.925 g、
3.65 g和1.825 g,A项符合题意。
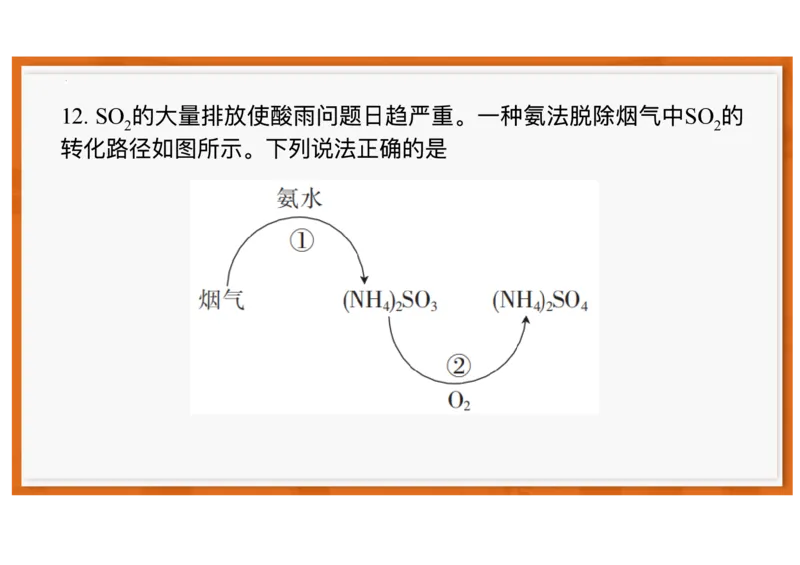
12. SO2的⼤量排放使酸⾬问题⽇趋严重。⼀种氨法脱除烟⽓中SO2的
转化路径如图所示。下列说法正确的是
A. 反应①和②均为氧化还原反应
B. 反应②的电⼦转移情况可表示为
C. 1 L 5 mol·L-1氨⽔能吸收10 mol SO2⽣成(NH4)2SO3
D. 总反应的化学⽅程式为2SO2+4NH3·H2O+O2 2
(NH4)2SO4
+2H2O
【答案】D
13. 下列由实验操作及现象得出的实验结论正确的是
选项
实验操作及现象
实验结论
A
2.4 g镁与⾜量稀硫酸反应,最终产⽣
V L H2
标准状况下,⽓体的摩
尔体积为10V L·mol-1
B
在空⽓中点燃氢⽓,然后把导管缓慢伸
⼊盛满氯⽓的集⽓瓶中,纯净的H2在Cl2
中安静地燃烧,发出苍⽩⾊⽕焰
燃烧不⼀定需要O2参与
C
在FeCl3溶液中加⼊⾜量铁粉,铁粉逐渐
溶解,溶液由棕⻩⾊变为浅绿⾊
Cl-被氧化为Cl2
D
向酸性KMnO4溶液中滴⼊FeCl2溶液,溶
液紫红⾊褪去
FeCl2溶液具有漂⽩性
【答案】B
14. 纳⽶氧化亚铜(Cu2O)是⼀种重要的光电材料,具有⼴泛的应⽤前
景。⼀种利⽤氯化铜蚀刻废液(溶质主要为CuCl2和HCl,Cu2+含量为
160 g·L-1)制备氧化亚铜的⼯艺如图所示。下列说法错误的是
A. “反应”不能在铁制容器中进⾏
B. 实验室进⾏“操作1”时需⽤玻璃棒引流
C. 理论上1 L上述氯化铜蚀刻废液可制备2.5 mol Cu2O
D. 颗粒直径为20 nm的Cu2O形成的分散系能产⽣丁达尔效应
【答案】C
【解析】蚀刻废液中含有的CuCl2和HCl会与Fe反应,“反应”不能在铁制
容器中进⾏,A项正确;“操作1”为过滤,实验室进⾏过滤操作时需⽤
玻璃棒引流,B项正确;氯化铜蚀刻废液中Cu2+含量为160 g·L-1,1 L
溶液中含有2.5 mol Cu元素,理论上可制备1.25 mol Cu2O,C项错误;
颗粒直径为20 nm的Cu2O形成的分散系为胶体,能产⽣丁达尔效应,D
项正确。
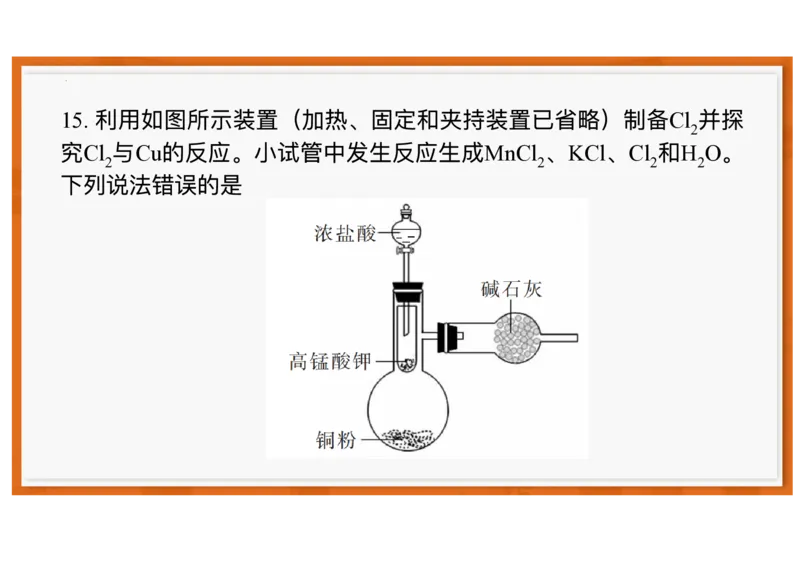
15. 利⽤如图所示装置(加热、固定和夹持装置已省略)制备Cl2并探
究Cl2与Cu的反应。⼩试管中发⽣反应⽣成MnCl2、KCl、Cl2和H2O。
下列说法错误的是
A. 与⾼锰酸钾反应,体现了浓盐酸的还原性和酸性
B. 球形⼲燥管内的碱⽯灰可⽤浸有⾜量饱和NaOH溶液的棉花代替
C. 当容器内充满⻩绿⾊⽓体时,若⽤酒精灯加热铜粉,会发⽣反
应:2Cu+Cl2 2CuCl
D. 当⼩试管内⽣成1 mol Cl2时,有0.4 mol KMnO4被消耗
【答案】C
16. a~d是中学中常⻅物质,a为“84”消毒液的有效成分,b为“洁厕灵
”的有效成分,c和d均为⾦属单质,c的焰⾊呈⻩⾊,d是⽬前产量最
⼤、使⽤最⼴泛的⾦属。各物质转化关系如图所示,“ ”中表示相连
的两种物质能发⽣反应,“→”表示⼀种物质能转化成另⼀种物质。下
列说法正确的是
A. Cl2→a、Cl2→HClO、c Cl2、d Cl2的反应中,均体现了Cl2的还原性
B. d在少量Cl2中燃烧的化学⽅程式为Fe+Cl2 FeCl2
C. d与⽔蒸⽓反应⽣成的化合物为Fe2O3
D. 常温下,a与b可以发⽣反应⽣成Cl2
【答案】D
【解析】根据图中转化关系及题⼲信息可知,a、b、c、d分别为
NaClO、HCl、Na、Fe。Cl2与NaOH溶液反应⽣成NaClO、Cl2与H2O
反应⽣成HClO时,体现了Cl2的氧化性和还原性,Cl2与Na、Fe的反应
中,Cl2均体现了氧化性,A项错误;铁与少量Cl2反应⽣成FeCl3,B项
错误;Fe与⽔蒸⽓在⾼温条件下反应⽣成Fe3O4和H2,C项错误;常温
下,NaClO和HCl能发⽣化学反应⽣成Cl2、NaCl和H2O,D项正确。
⼆、⾮选择题:本题共4⼩题,共56分。
17. (14分)⼈类在很久以前就开始使⽤铁器,铁制品为社会进步做出
了巨⼤贡献。
(1)铁在潮湿的空⽓中易⽣锈。该过程中,铁发⽣了
(填“氧化”或“还原”)反应。
氧化
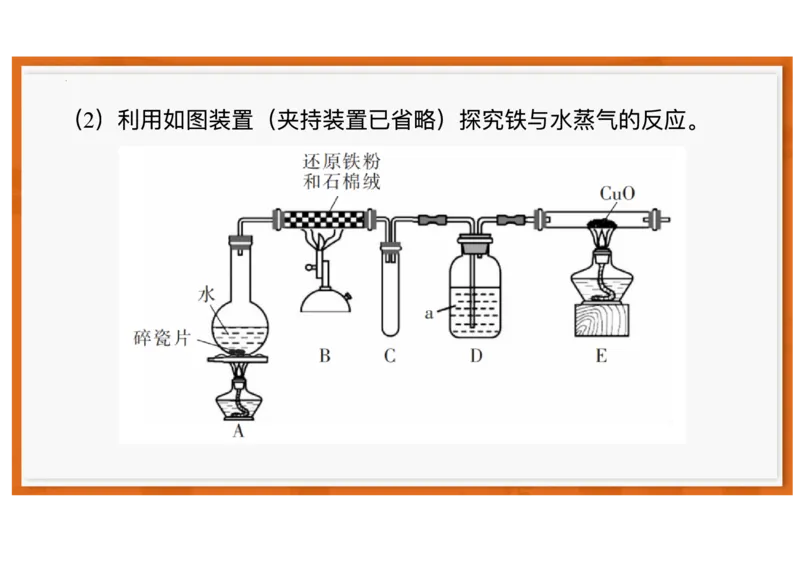
(2)利⽤如图装置(夹持装置已省略)探究铁与⽔蒸⽓的反应。
①组装好装置后,在加⼊试剂前应进⾏的操作为
;试剂a为 (填试剂名称)。
②实验过程中能证明有
。
检验装置⽓密性
浓硫酸
E处硬质玻璃管内⿊⾊固体
变红
(3)铁是⼈体必需的微量元素。菠菜是含铁元素较多的蔬菜,探究⼩
组利⽤实验测定菠菜中的铁含量。实验步骤如下:
a.⽤1.0 mol·L-1硫酸配制50 mL 0.4 mol·L-1硫酸。
b.将晒⼲的菠菜去杆后剪成碎块,准确称取菠菜碎块30 g,然后将其研
碎,灼烧成灰。
c.将冷却后的灰分转移⾄烧杯中,然后加⼊20 mL 0.4 mol·L-1 H2SO4溶
液,溶解后过滤,往滤液中加⼊⾜量H2O2溶液使其充分反应。
d.经仪器测得滤液中总含铁量为8.4×10-4 g。
①步骤a中,需要使⽤的玻璃仪器除量筒、烧杯、50 mL容量瓶外,还
有 (填仪器名称),需要⽤量筒量取
mL 1.0 mol·L-1硫酸;配制过程中,若定容时仰视容量瓶刻度线,会导
致配制的硫酸浓度 (填“偏⼤”“偏⼩”或“不变”)。
②步骤c中,过滤后的滤液中含有Fe2+和Fe3+,检验滤液中含有Fe3+的
操作及现象为:取适量滤液于试管中,滴加 (填化学式)
溶液,观察到溶液变为红⾊,说明滤液中含有Fe3+。步骤c中,加⼊
⽅程式为
被氧化为
Fe
H2O2溶液,
2+
。
玻璃棒、胶头滴管
20.0
偏⼩
KSCN
2Fe2++H2O2+2H+
【答案】(1)氧化(1分)
(2)①检验装置⽓密性(1分) 浓硫酸(1分)
②E处硬质玻璃管内⿊⾊固体变红(2分)
(3)①玻璃棒、胶头滴管(2分,1个1分) 20.0(2分,写“20”扣1
分) 偏⼩(1分)
【解析】(1)铁⽣锈时,铁作还原剂,发⽣了氧化反应。
(2)①加药品前需要检验装置⽓密性;H2还原CuO前需要⼲燥H2,故
试剂a为浓硫酸。②E处硬质玻璃管内⿊⾊固体变红说明有还原性的H2
产⽣。
18. (14分)物质的量建⽴了宏观物质与微观粒⼦间的联系,可以帮
助我们从定量的⻆度认识物质及其变化。请回答下列问题。
(1)设NA为阿伏加德罗常数的值,则标准状况下,1.12 L O2含有
(⽤含NA的代数式表示)个O原⼦。
(3)常温常压下,1 L的O2和2 L的H2的物质的量之⽐为 (填
最简整数⽐,下同),密度之⽐为 。
(4)1 mol CO和CO2的混合⽓体的质量为31.2 g,则1 mol该混合⽓体中,
CO的物质的量为 mol,CO2的质量为 g。
0.1NA
1
2
1∶2
16∶1
0.8
8.8
【答案】(1)0.1NA(2分)
(2)1(2分)
2(2分)
(3)1∶2(2分)
16∶1(2分)
(4)0.8(2分)
8.8(2分)
(3)同温同压下,⽓体的体积之⽐等于⽓体的物质的量之⽐,⽓体
的密度之⽐等于⽓体的摩尔质量之⽐,所以常温常压下,1 L的O2和
2 L的H2的物质的量之⽐为1∶2,密度之⽐为32∶2=16∶1。
(4)设1 mol CO和CO2的混合⽓体中有x mol CO和y mol CO2,则x+
y=1且28x+44y=31.2,求出x=0.8、y=0.2。则1 mol该混合⽓体中
CO的物质的量为0.8 mol,CO2的质量为0.2 mol×44 g·mol-1=8.8 g。
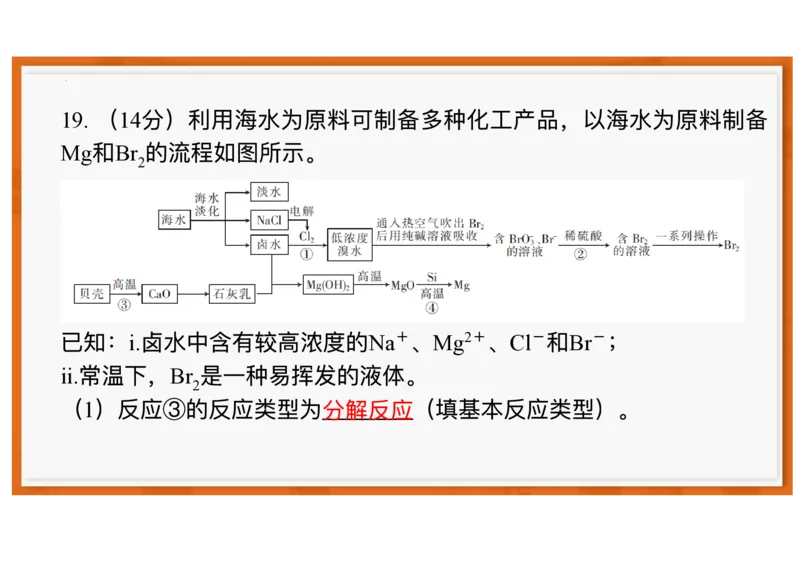
19. (14分)利⽤海⽔为原料可制备多种化⼯产品,以海⽔为原料制备
Mg和Br2的流程如图所示。
已知:i.⻧⽔中含有较⾼浓度的Na+、Mg2+、Cl-和Br-;
ii.常温下,Br2是⼀种易挥发的液体。
(1)反应③的反应类型为 (填基本反应类型)。
分解反应
A. 饱和⻝盐⽔能导电是因为饱和⻝盐⽔是电解质
B. NaCl在⽔中的电离⽅程式为NaCl
Na++Cl-
C. 实验室中可⽤饱和⻝盐⽔除去Cl2中混有的HCl
D. 向饱和⻝盐⽔中加⼊钾会发⽣反应:K+Na+ K
++Na
4.48
BC
应
(
;反应②中,消耗1 mol Br-时,理论上⽣成 g Br2
。
(4)在⻧⽔中加⼊⽯灰乳,经沉降、过滤、洗涤操作可得到
Mg(OH)2。检验最后⼀次洗涤液中⽆Cl-的操作为:取最后
⼀次洗涤液, ,⽆明
显现象。
+Br2
96
加⼊稀硝酸酸化的AgNO3溶液
24
【答案】(1)分解反应(2分,未写“反应”扣1分)
(2)4.48(2分) BC(2分,1个1分,多选、错选不得分)
(4)加⼊稀硝酸酸化的AgNO3溶液(2分,合理表述均可)
(5)24(2分)
【解析】(1)⻉壳的主要成分为CaCO3,CaCO3⾼温分解为CaO和
CO2,属于分解反应。
(4)检验最后⼀次洗涤液中⽆Cl-的操作为取最后⼀次洗涤液,加
⼊稀硝酸酸化的AgNO3溶液,溶液中⽆⽩⾊沉淀产⽣。
20. (14分)钠的化合物种类众多。请回答下列问题。
(1)实验室中,少量⾦属钠保存在 中;Na2O2需密
式为
⽓中封保存,
。
煤油或⽯蜡油
2Na2CO3+O2
(2)按图组装好装置并添加好试剂。将⽓球内的固体(两⽓球内固体
颗粒⼤⼩基本⼀致)同时倒⼊试管中,⽓球胀⼤速率更快的是
(填字⺟,下同);充分反应后恢复⾄室温,理论上⽓球体积更⼤的为
;充分反应后,试管B中Cl-的物质的量为 。
A
A
0.02 mol
(3)⼩组同学探究能否⽤CaCl2溶液鉴别Na2CO3溶液和NaHCO3溶液。实验
操作和现象如下表。
编号
实验操作
实验现象
1
分别取4.0 mL 0.05 mol·L-1 CaCl2溶液于两⽀试管中,
⽤胶头滴管向两⽀试管中分别滴加0.1 mol·L-1
Na2CO3溶液和0.1 mol·L-1 NaHCO3溶液
盛装Na2CO3溶液的试管中
产⽣⽩⾊沉淀,盛装
NaHCO3溶液的试管中⽆
明显现象
2
分别取4.0 mL 1 mol·L-1 Na2CO3溶液和1 mol·L-1
NaHCO3溶液于两⽀试管中,⽤胶头滴管向两⽀试管
中分别滴加⼏滴0.5 mol·L-1 CaCl2溶液
两⽀试管中均产⽣⽩⾊沉
淀,⽆⽓泡产⽣,振荡后
沉淀不消失
3
分别取4.0 mL 6.0 mol·L-1 CaCl2溶液于两⽀试管中,
⽤胶头滴管向两⽀试管中分别滴加0.5 mol·L-1
Na2CO3溶液和0.5 mol·L-1 NaHCO3溶液
两⽀试管中均产⽣⽩⾊沉
淀,且滴加NaHCO3溶液
的试管中有⽓泡产⽣
①实验2中,1 mol·L-1 NaHCO3溶液与0.5 mol·L-1 CaCl2溶液反应
的化学⽅程式为
。
②实验3中,盛装NaHCO3溶液的试管内产⽣的⽓体为
(填化学式)。
H2CO3
CO2
实验结论:不宜⽤CaCl2溶液鉴别浓度较⼤的Na2CO3溶液和NaHCO3
溶液。
4(NaHCO
)请设计实验,除去
3Na
溶液中的
2
CO3 杂质:
(写出必要的试剂和操作⽅法)。
往溶液中通
⼊⾜量的CO2
(2)A(1分) A(1分) 0.02 mol(2分,未写单位扣1分)
②CO2(2分)
(4)往溶液中通⼊⾜量的CO2(2分,类似表述均可)
【解析】(1)为了隔绝空⽓,钠常常保存在⽯蜡油或煤油中。
感谢观看
THANK YOU FOR YOUR WATCHING
序号题号
试题形式题型分值
知识模块
知识板块
知识点
认知⽔平
考查能⼒
预计难度答案
1
1
客观题选择题2 常⻅的⽆机物及其应⽤
⾦属及其化合物
铁及其化合物
了解接受、吸收、整合化学信息的能⼒0.90
C
2
2
客观题选择题2 常⻅的⽆机物及其应⽤
⾦属及其化合物
铜及其化合物
了解接受、吸收、整合化学信息的能⼒0.80
D
3
3
客观题选择题2 常⻅的⽆机物及其应⽤
物质及其变化
离⼦共存
了解接受、吸收、整合化学信息的能⼒0.85
A
4
4
客观题选择题2
化学科学与实验探究
化学实验
化学实验装置的选择
探究
化学实验与探究的能⼒
0.65
D
5
5
客观题选择题2 常⻅的⽆机物及其应⽤
⾦属及其化合物
焰⾊试验
理解接受、吸收、整合化学信息的能⼒0.60
B
6
6
客观题选择题2 常⻅的⽆机物及其应⽤
物质的量
物质的量的计算
了解接受、吸收、整合化学信息的能⼒0.60
C
7
7
客观题选择题2 常⻅的⽆机物及其应⽤
物质的量
配制⼀定物质的量浓度的溶液
了解接受、吸收、整合化学信息的能⼒0.60
C
8
8
客观题选择题2 常⻅的⽆机物及其应⽤
物质及其变化
离⼦⽅程式正误判断
理解接受、吸收、整合化学信息的能⼒0.55
B
9
9
客观题选择题2 常⻅的⽆机物及其应⽤
物质的量
理想⽓体状态⽅程
理解接受、吸收、整合化学信息的能⼒0.55
A
10
10
客观题选择题2 常⻅的⽆机物及其应⽤
物质的量
阿伏加德罗常数的应⽤及其计算
掌握接受、吸收、整合化学信息的能⼒0.55
B
11
11
客观题选择题4 常⻅的⽆机物及其应⽤
物质的量
溶质质量的计算
理解接受、吸收、整合化学信息的能⼒0.60
A
12
12
客观题选择题4 常⻅的⽆机物及其应⽤
物质及其变化
氧化还原反应
应⽤
分析和解决化学问题的能⼒0.50
D
13
13
客观题选择题4
化学科学与实验探究
化学实验
化学实验设计与评价
探究
化学实验与探究的能⼒
0.55
B
14
14
客观题选择题4 常⻅的⽆机物及其应⽤
⾦属及其化合物
⾦属及其化合物的性质
应⽤
分析和解决化学问题的能⼒0.50
C
15
15
客观题选择题4 常⻅的⽆机物及其应⽤
⾮⾦属及其化合物
氯⽓的性质
探究
化学实验与探究的能⼒
0.50
C
16
16
客观题选择题4 常⻅的⽆机物及其应⽤
物质及其变化
物质的分类及转化
应⽤
分析和解决化学问题的能⼒0.50
D
17 17(1-2)
主观题填空题5
化学科学与实验探究
化学实验
探究铁与⽔蒸⽓反应
探究
化学实验与探究的能⼒
0.70
18
17(3)
主观题填空题9
化学科学与实验探究
化学实验
测定菠菜中铁的含量
探究
化学实验与探究的能⼒
0.55
19
18
主观题填空题14 常⻅的⽆机物及其应⽤
物质的量
阿伏加德罗常数的应⽤及其计算
掌握接受、吸收、整合化学信息的能⼒0.50
20 19(1-2)
主观题填空题6 常⻅的⽆机物及其应⽤
元素及其化合物
元素及其化合物的性质
应⽤
分析和解决化学问题的能⼒0.55
21 19(3-5)
主观题填空题8 常⻅的⽆机物及其应⽤
元素及其化合物
元素及其化合物的性质
应⽤
分析和解决化学问题的能⼒0.45
22 20(1-2)
主观题填空题8 常⻅的⽆机物及其应⽤
⾦属及其化合物
钠及其化合物
探究
化学实验与探究的能⼒
0.50
23 20(3-4)
主观题填空题6 常⻅的⽆机物及其应⽤
⾦属及其化合物
钠及其化合物
探究
化学实验与探究的能⼒
0.35
.