文档内容
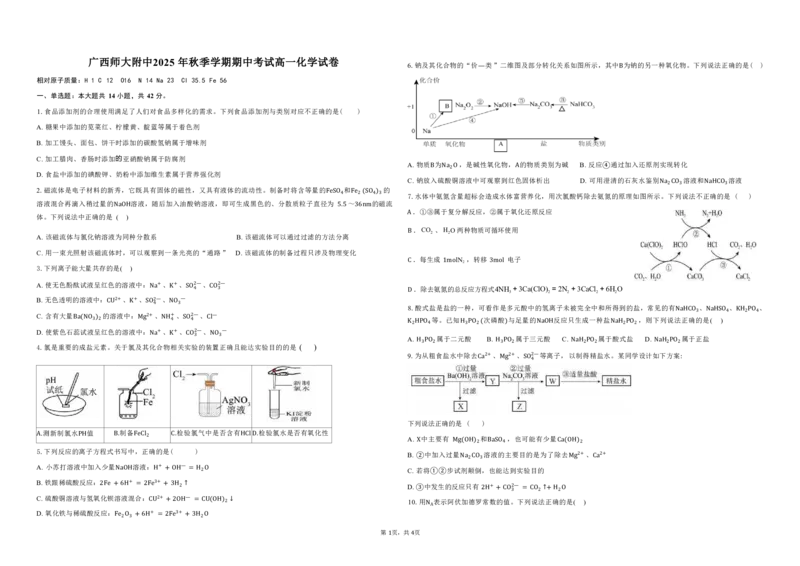
广西师大附中2025 年秋季学期期中考试高一化学试卷
6.钠及其化合物的“价 类”二维图及部分转化关系如图所示,其中 为钠的另一种氧化物。下列说法正确的是( )
相对原子质量:H 1 C 12 O16 N 14 Na 23 Cl 35.5 Fe 56 — B
一、单选题:本大题共 14 小题,共 42 分。
1.食品添加剂的合理使用满足了人们对食品多样化的需求。下列食品添加剂与类别对应不正确的是( )
A. 糖果中添加的苋菜红、柠檬黄、靛蓝等属于着色剂
B. 加工馒头、面包、饼干时添加的碳酸氢钠属于增味剂
C. 加工腊肉、香肠时添加的亚硝酸钠属于防腐剂
A. 物质 为 ,是碱性氧化物, 的物质类别为碱 B. 反应 通过加入还原剂实现转化
D. 食盐中添加的碘酸钾、奶粉中添加维生素属于营养强化剂
C. 钠放入B 硫N酸a2铜O溶液中可观察到红色A 固体析出 D. 可用④澄清的石灰水鉴别 溶液和 溶液
2.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性。制备时将含等量的 和 的
7.水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示N。a2下C列O3说法不正Na确H的CO是3 ( )
溶液混合再滴入稍过量的 溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径F为eSO4 ~ Fe2(SO的4)磁3 流
.①③属于复分解反应,②属于氧化还原反应
体。下列说法中正确的是 N(aOH) 5.5 36nm
A
.CO 、H O两种物质可循环使用
2 2
A. 该磁流体与氯化钠溶液为同种分散系 B. 该磁流体可以通过过滤的方法分离
B
C. 用一束光照射该磁流体时,可以观察到一条光亮的“通路” D. 该磁流体的制备过程只涉及物理变化
.每生成 N ,转移 电子
2
3.下列离子能大量共存的是( )
C 1mol 3mol
A. 使无色酚酞试液呈红色的溶液中: 、 、 、
.除去氨氮的总反应方程式4NH +3Ca(ClO) =2N +3CaCl +6H O
+ + 2— 2— 3 2 2 2 2
B. 无色透明的溶液中: 、 、 Na 、K SO4 CO3
D
2+ + 2— — 8.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 、 、 、
C. 含有大量 的C溶U液中K: SO4、 NO、3 、
等。已知 次磷酸 与足量的 反应只生成一种盐 ,则下列说法 Na 正 HC 确 O 的3 是 N ( aHS ) O4 KH2PO4
2+ + 2— —
D. 使紫色石蕊Ba试(N液O3 呈)2 红色的溶液中M:g N、H4 、SO4 、Cl K2HPO4 H3PO2( ) NaOH NaH2PO2
+ + 2— — A. 属于二元酸 B. 属于三元酸 C. 属于酸式盐 D. 属于正盐
4.氯是重要的成盐元素。关于氯及其化Na合物K相关实CO验3的装N置O3正确且能达实验目的的是 ( )
9.为H3 从PO粗 2 食盐水中除去 、H3PO2 、 等离子,以Na制H得 2P精O2 盐水。某同学设计如Na下H方 2P案O2
2+ 2+ 2—
Ca Mg SO4 :
下列说法正确的是 ( )
测新制氯水 值 制备 检验氯气中是否含有 检验氯水是否有氧化性
A. 中主要有 和 ,也可能有少量
A. PH B. FeCl2 C. HClD.
5.下列反应的离子方程式书写中,正确的是( ) B. X 中加入过M量g(OH)2 溶B液aS的O4 主要目的是为了除Ca去(OH)2 、
A. 小苏打溶液中加入少量 溶液: C. 若②将 步试N剂a颠2C倒O3,也能达到实验目的 Mg 2+ Ca 2+
+ —
B. 铁跟稀硫酸反应: NaOH H + OH = H2O
D.
中①发生②的反应只有
+ 3+
C. 硫酸铜溶液与氢氧2化F钡e +溶6液H混合=:2Fe + 3H2 ↑ 10.③用 表示阿伏加德罗2常H数 + +的C值O。 2 3 — 下=列C说O2法↑正+确H2的O是( )
2+ —
D. 氧化铁与稀硫酸反应: CU +2OH = CU(OH)2 ↓ NA
+ 3+
Fe2O3 +6H = 2Fe + 3H2O
第 页,共 页
学科网(北京)股份有限公司 1 4A. 标准状况下, H2O 所含有的分子数为 A.装置①应先打开 K,再通入 N2 ,后滴加浓硫酸
B. 液态 11.中2所L 含 数为 0.5NA B.装置①通N2 的主要目的是排净空气并使生成的 ClO2 进入后续装置
C. 0.1mol H与Cl足量 C反l
—
应电子0.转1N移A总数为
C.装置②可起到缓冲气流并防止倒吸的作用
D. 1常m温o常l N压a2下O,2 H和2O 的混合气体中含有的2氧NA原子数为
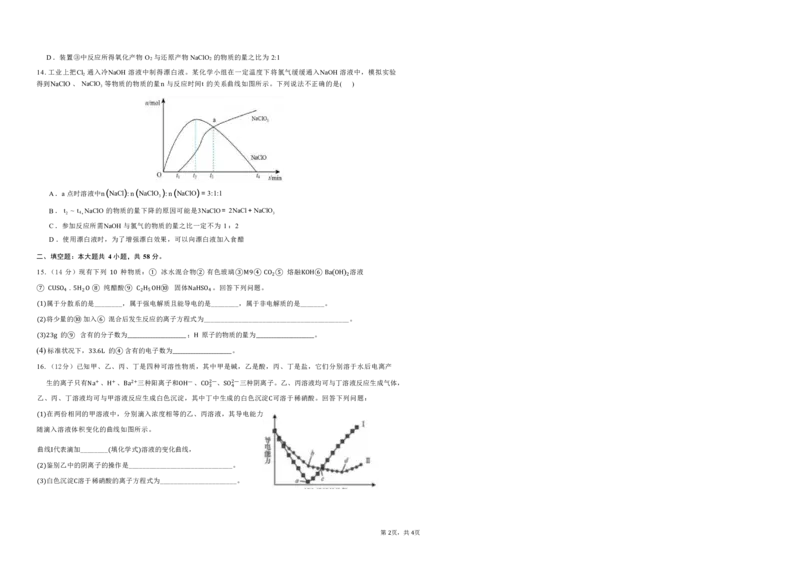
11.如图横坐标、4纵89坐O标 3 分O别 2 表示一定条件下氧化剂的氧化性、3N还 A 原剂的还原性由弱到强的变化, 、 、 点表示了
横纵坐标对应微粒在水溶液中反应的产物。下列说法正确的是( )
1 2 3
A. 反应 中 的 失电子表现氧化性 B. 反应 的离子方程式为:
3+ — 2+
C.反应 1 的产SO物2 是S D. 从图2可推得 能氧化 、Fe + 2I = Fe +I2
— —
12.钠在3液氨中溶a解速Cl度O 极快,形成一种蓝色溶液,研究认Cl2 为蓝色是I 生成SO氨 2 合电子 的缘故,如图所示。将钠
—
投入液氨中,钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气体。下列有关说e 法(N不H正3)确X 的是 ( )
A. 钠的密度比液氨大
B. 溶液的导电性增强
C. 氨合电子 具有强的氧化性
—
D.
钠和液氨e可发(N生H3以)X下反应:
13.ClO2 是一种黄绿色气体,在2空NH气3中+浓2度Na超=过2N10aN%H时2会+有H很2 ↑强的爆炸性。制备
ClO 可依据反应3NaClO +2H SO (浓)= NaClO +2ClO ↑+2NaHSO +H O ,实验室可用 ClO 制备少量NaClO 溶
2 3 2 4 4 2 4 2 2 2
液。下列说法不正确的是 ( )
第 页,共 页
学科网(北京)股份有限公司 2 4D.装置③中反应所得氧化产物 O2 与还原产物NaClO2 的物质的量之比为 2:1
14.工业上把Cl 通入冷NaOH 溶液中制得漂白液。某化学小组在一定温度下将氯气缓缓通入NaOH 溶液中,模拟实验
2
得到NaClO 、 NaClO 等物质的物质的量n 与反应时间t 的关系曲线如图所示。下列说法不正确的是( )
3
A.a 点时溶液中n(NaCl):n(NaClO ):n(NaClO)=3:1:1
3
B.t
2
~ t 4,NaClO 的物质的量下降的原因可能是3NaClO= 2NaCl+NaClO
3
C.参加反应所需NaOH 与氯气的物质的量之比一定不为 1:2
D.使用漂白液时,为了增强漂白效果,可以向漂白液加入食醋
二、填空题:本大题共 4小题,共 58 分。
15.(14 分)现有下列 种物质: 冰水混合物 有色玻璃 熔融 溶液
纯1醋0酸 ① 固体 ② 。回答下③列M问9④题。CO2⑤ KOH⑥ Ba OH 2
⑦属CU于SO分 4 散. 5系H的2O是⑧________,⑨属于C2强H5 电OH解⑩质且能导N电aH的SO是 4 ________,属于非电解质的是_______。
(1)将少量的 加入 混合后发生反应的离子方程式为__________________________________________。
(2) 的 ⑩含有的⑥分子数为 ; 原子的物质的量为 。
((43))2标3g准状⑨况下, 的 含__有___的___电__子___数___为_______ H 。 _______________________
16.(12分)已知3甲3.、6L乙、④丙、丁是四种可溶_性___物___质__,___其___中___甲__是___碱,乙是酸,丙、丁是盐,它们分别溶于水后电离产
生的离子只有 、 、 三种阳离子和 、 、 三种阴离子。乙、丙溶液均可与丁溶液反应生成气体,
+ + 2+ — 2— 2—
乙、丙、丁溶液均Na可与H甲溶液Ba反应生成白色沉淀OH,其中CO丁3中生S成O4的白色沉淀 可溶于稀硝酸。回答下列问题:
在两份相同的甲溶液中,分别滴入浓度相等的乙、丙溶液,其导电能力 C
随(1滴) 入溶液体积变化的曲线如图所示。
曲线Ⅰ代表滴加________ 填化学式 溶液的变化曲线,
鉴别乙中的阴离子的操( 作是___)___________________________。
(2)白色沉淀 溶于稀硝酸的离子方程式为______________________。
(3) C
第 页,共 页
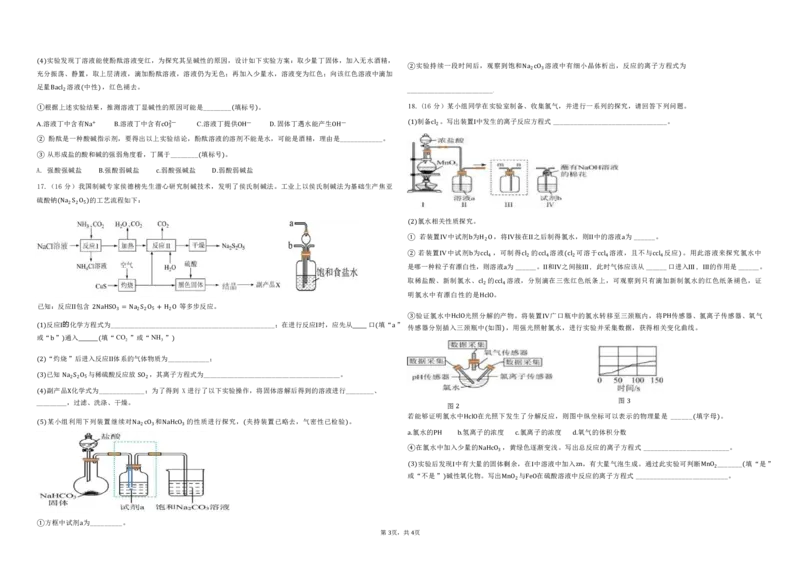
学科网(北京)股份有限公司 2 4实验发现丁溶液能使酚酞溶液变红,为探究其呈碱性的原因,设计如下实验方案:取少量丁固体,加入无水酒精,
实验持续一段时间后,观察到饱和 溶液中有细小晶体析出,反应的离子方程式为
充分振荡、静置,取上层清液,滴加酚酞溶液,溶液仍为无色;再加入少量水,溶液变为红色;向该红色溶液中滴加
(4)
② Na2cO3
足量 溶液 中性 ,红色褪去。
_________________________
。
Bacl2 ( )
根据上述实验结果,推测溶液丁显碱性的原因可能是________ 填标号 。 18.(16 分)某小组同学在实验室制备、收集氯气,并进行一系列的探究,请回答下列问题。
A ① .溶液丁中含有 溶液丁中含有 C.溶液丁提供( ) 固体丁遇水能产生 制备 。写出装置Ⅰ中发生的离子反应方程式 _________________________________。
酚酞是一种酸Na碱 + 指示剂B,. 要得出以上实cO验 2 3 — 结论,酚酞溶液的溶剂OH不 — 能是水D,. 可能是酒精,理由O是H_ — ___________。 (1) cl2
② 从形成盐的酸和碱的强弱角度看,丁属于________ 填标号 。
A③. 强酸强碱盐 强酸弱碱盐 弱酸强碱盐 ( 弱)酸弱碱盐
17.(16 分)我国制B碱.专家侯德榜先生潜c.心研究制碱技术,D.发明了侯氏制碱法。工业上以侯氏制碱法为基础生产焦亚
硫酸钠 的工艺流程如下:
(Na2S2O5)
氯水相关性质探究。
(2)若装置Ⅳ中试剂 为 ,将Ⅳ接在Ⅱ之后制得氯水,则Ⅱ中的溶液 为 ______。
① 若装置Ⅳ中试剂b为H2O,可制得 的 溶液 可溶于 溶液a,且不与 反应 。用此溶液来探究氯水中
②是哪一种粒子有漂白b性,c则cl4溶液 为__c_l_2__。ccⅡl4和Ⅳ之(c间l2接Ⅲ, 此cc时l4 气体应该从__c_c_l_4_口进)入Ⅲ, Ⅲ的作用是______。
取稀盐酸、新制氯水、 的 a溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证
明氯水中有漂白性的是cl2 。ccl4
已知:反应Ⅱ包含 等多步反应。
HclO
验证氯水中 光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将 传感器、氯离子传感器、氧气
2NaHSO3 = Na2S2O5 + H2O
反应Ⅰ的化学方程式为_______________________________________________;在进行反应Ⅰ时,应先从 口 填“ ”
传感器分别插入三颈瓶中 如图 ,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。
③ HclO PH
或“ ” 通入 填“CO ”或“NH ”
(1) 2 3 ( a ( )
b ) ( )
“灼烧”后进入反应Ⅱ体系的气体物质为____________;
(2)已知 与稀硫酸反应放 ,其离子方程式为________________________________________。
(3)副产品Na2 化S2 学O5 式为____________SO_; 2 为了得到 X 进行了以下实验操作,将固体溶解后得到的溶液进行________、
_________,过滤、洗涤、干燥。 图
(4) X 图
若能够证明氯水中 在光照下发生了分解反应,则图中纵坐标可以表示3 的物理量是 ______ 填字母 。
某小组利用下列装置继续对 和 的性质进行探究, 夹持装置已略去,气密性已检验 。 2
氯水的 氢Hc离lO子的浓度 氯离子的浓度 氧气的体积分数 ( )
(5) Na2cO3 NaHcO3 ( )
a. 在氯水P中H加入b少. 量的 ,黄c绿. 色逐渐变浅。写出d.总反应的离子方程式 ________________________。
④ 实验后发现Ⅰ中有大量N的aH固cO体 3 剩余,在Ⅰ中溶液中加入 ,有大量气泡生成。通过此实验可判断 _______ 填“是”
或
(3
“
)
不是” 碱性氧化物。写出 与 在硫酸溶液中
z
反
n
应的离子方程式 ___________________
M
_
n
_
O
__2___。
(
) MnO2 FeO
方框中试剂 为_________。
第 页,共 页
① a
学科网(北京)股份有限公司 3 4高一期中考试化学答案
1. 2. 3. 4. 5. 6. 7.C 8.D9. 10. 11. 12.
15B.(每C 空A2分D ,D共 A14分) A D D C 13.D 14.A
(1)②⑥ ⑤ ④⑨
2+ — + 2—
((2))Ba +或OH +×H +S,O4 = BaSO4 ↓+H2O
23
A
(3)0.5N 3.01 10 3mol
A
164.(每33N空 2分,共 12分)
;
(1)H取 2 少SO量 4 样品于试管中,加入盐酸无现象,加入氯化钡溶液产生白色沉淀,则有硫酸根离子
(2)
+ 2+
(3) BaCO3 + 2H = Ba +H2O + CO2 ↑
(4)若①酚D酞的溶剂是水,则在碳酸钠的酒精溶液中滴加酚酞溶液就会显红色
②
③C
17.(除了特别标注外,每空 2分,共 16分)
a(1分) ( 分)
(1) NaCl + CO2 + NH3 + H2O = NaHCO3 ↓+ NH4Cl ; NH3 1
(2)SO2
2— +
(3)S2O5 + 2H = 2SO蒸2发↑+(H加2O热)浓缩( 分),降温(冷却)结晶( 分)
(4) CuS饱O4和. 5的H碳2O酸氢;钠溶液( ) 1 1
(5) ① NaHCO3
+ 2—
②
18
2 .(Na除了+特C别O3 标注+ H外 2O,+每C空O2
2
=分2N,aH共CO
1
3
6
↓分)
+ — 2+
(1)MnO饱 2 和+食4H盐水+ 2Cl Mn + Cl2 ↑+ 2H2O
(2)浓①硫酸; 分);安全瓶,防倒吸
② n(1 ③ bcd
— —
④ 不Cl2是+(H1CO分3)=;Cl + HClO + CO2 ↑
+ 2+ 3+
(3) MnO2 + 2FeO +8H = Mn +2Fe +4H2O
第 页,共 页
学科网(北京)股份有限公司 4 4