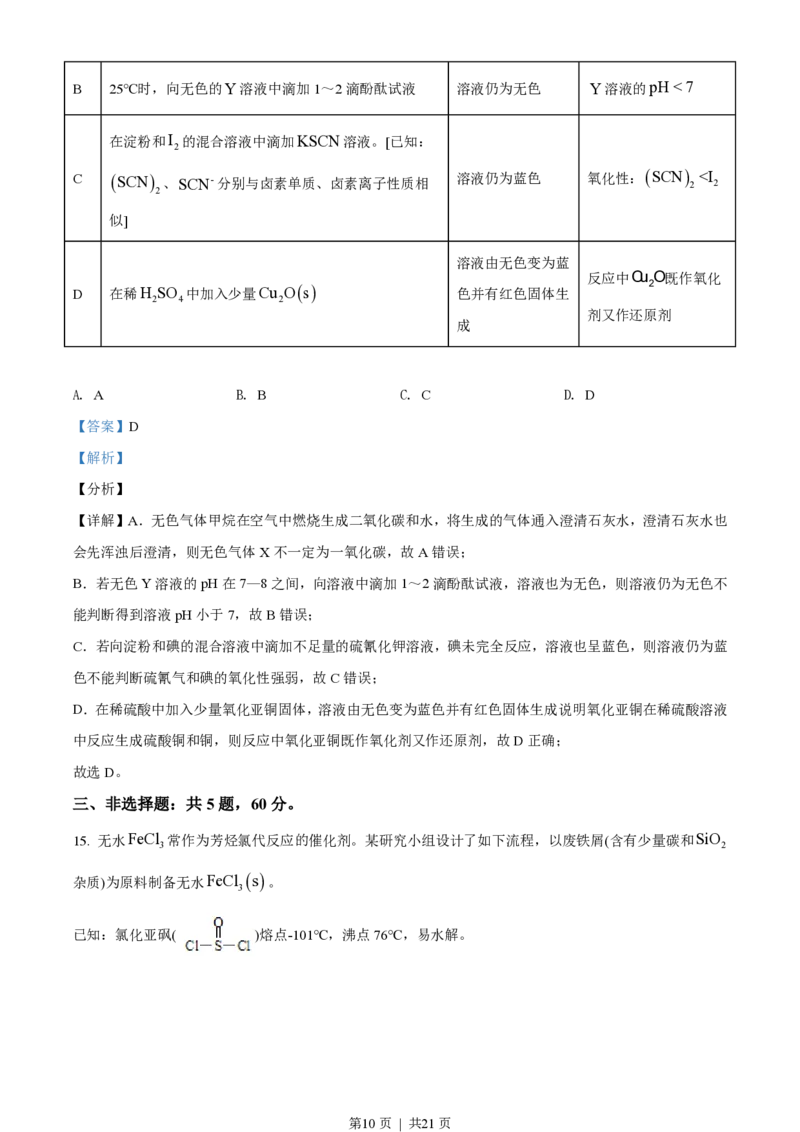文档内容
海南省 2021 年普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23
一、选择题:本题共 8小题,每小题 2分,共 16 分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1. 2020年9月22日,中国向全世界宣布,努力争取2060年前实现碳中和。下列措施不利于大气中CO 减
2
少的是
A. 用氨水捕集废气中的CO ,将其转化为氮肥
2
B. 大力推广使用风能、水能、氢能等清洁能源
C. 大力推广使用干冰实现人工增雨,缓解旱情
D. 通过植树造林,利用光合作用吸收大气中的CO
2
【答案】C
【解析】
【分析】
【详解】A.氨水能与酸性氧化物二氧化碳反应生成碳酸铵或碳酸氢铵,则用氨水捕集废气中的二氧化碳,
将其转化为氮肥有利于大气中二氧化碳的减少,故A不符合题意;
B.大力推广使用风能、水能、氢能等清洁能源可以减少化石能源的使用,从而减少二氧化碳气体的排放,
有利于大气中二氧化碳的减少,故B不符合题意;
C.大力推广使用干冰实现人工增雨,会增加大气中二氧化碳的量,不利于大气中二氧化碳的减少,故C符
合题意;
D.通过植树造林,利用光合作用吸收大气中的二氧化碳有利于大气中二氧化碳的减少,故D不符合题意;
故选C。
2. 元末陶宗仪《辍耕录》中记载:“杭人削松木为小片,其薄为纸,熔硫磺涂木片顶端分许,名日发
烛……,盖以发火及代灯烛用也。”下列有关说法错误的是
A. 将松木削薄为纸片状有助于发火和燃烧
B. “发烛”发火和燃烧利用了物质的可燃性
C. “发烛”发火和燃烧伴随不同形式的能量转化
D. 硫磺是“发烛”发火和燃烧反应的催化剂
【答案】D
第1页 | 共21页【解析】
【分析】
【详解】A.将松木削薄为纸片状可以增大可燃物与氧气接触面积,有助于发火和燃烧,A正确;
B.发烛具有可燃性,“发烛”发火和燃烧利用了物质的可燃性,B正确;
C.“发烛”发火和燃烧伴随不同形式的能量转化,如化学能转化为光能、热能等,C正确;
D.硫磺也燃烧,不是催化剂,D错误;
选D。
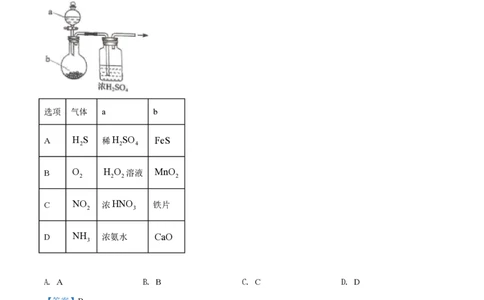
3. 用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是
选项 气体 a b
A H S 稀H SO FeS
2 2 4
B O H O 溶液 MnO
2 2 2 2
C NO 浓HNO 铁片
2 3
D NH 浓氨水 CaO
3
A. A B. B C. C D. D
【答案】B
【解析】
【分析】
【详解】A.H S与浓硫酸反应,故不能用浓硫酸干燥,故A错误;
2
MnO
2
B.发生反应2H O 2H O+O ,浓硫酸干燥氧气,故B正确;
2 2 2 2
C.铁片和浓硝酸常温下发生钝化,故不能制取二氧化氮气体,故C错误;
第2页 | 共21页D.氨气与浓硫酸反应,故不能用浓硫酸干燥氨气,故D错误;
故选B。
4. 生活中处处有化学。下列说法错误的是
A. 天然橡胶的主要成分是聚苯乙烯 B. 天然气的主要成分是甲烷
C. 乙烯可用作水果催熟剂 D. 苯酚可用作消毒剂
【答案】A
【解析】
【分析】
【详解】A.天然橡胶的主要成分聚异戊二烯,故A错误;
B.天然气的主要成分是甲烷,故B正确;
C.乙烯具有植物生成调节作用,可以用作水果催熟剂,故C正确;
D.苯酚能使蛋白质的变性、具有消毒防腐作用,低浓度时可用作杀菌消毒剂,D正确;
故选A。
5. SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关SF 的说法正确的是
6 6
A. 是非极性分子 B. 键角∠FSF都等于90°
C. S与F之间共用电子对偏向S D. S原子满足8电子稳定结构
【答案】A
【解析】
【分析】
【详解】A.结构对称、正负电荷重心重合的分子为非极性分子,SF 分子呈正八面体结构,S 原子位于正
6
八面体的中心,该分子结构对称、正负电荷重心重合,所以为非极性分子,A正确;
B.SF 是结构对称、正负电荷重心重合的分子,确切地说角FSF可以是90度,但也有处于对角位置的角
6
FSF为180度,故键角∠FSF不都等于90°,B错误;
C.由于F的电负性比S的大,S与F之间共用电子对偏向F,C错误;
D.中心元素价电子数+化合价的绝对值=8时该分子中所有原子都达到8电子稳定结构,但氢化物除外,该
化合物中S元素化合价+价电子数=6+6=12,则S原子不是8电子稳定结构,D错误;
故答案为:A。
第3页 | 共21页6. 一次性鉴别等浓度的KNO 、NH Cl、Na CO 三种溶液,下列方法不可行的是
3 4 2 3
A. 测定pH B. 焰色试验
C. 滴加AlCl 溶液 D. 滴加饱和CaOH 溶液,微热
3 2
【答案】C
【解析】
【分析】
【详解】A.KNO 溶液显中性,NH Cl溶液显酸性,Na CO 溶液显碱性,故可以用测定pH的方法鉴
3 4 2 3
别,故A正确;
B.KNO 的焰色试验中现象为透过蓝色钴玻璃为紫色,NH Cl的焰色试验中无现象,Na CO 的焰色
3 4 2 3
试验中现象为黄色,故可以用焰色试验的方法鉴别,故B正确;
C.KNO 、NH Cl、Na CO 中只有Na CO 能与AlCl 反应有现象,故KNO 和NH Cl不能鉴别,
3 4 2 3 2 3 3 3 4
故C错误;
D
D.2NH Cl+CaOH CaCl2+2NH +2H O有刺激性气味气体产生,
4 2 3 2
Na CO +CaOH =CaCO +2NaOH有白色沉淀产生,而KNO 不反应无现象,故可以鉴别,故D正确;
2 3 2 3 3
故选C。
7. N 代表阿伏加德罗常数的值。下列说法正确的是
A
A. 0.1mol 27Al3+中含有的电子数为1.3N
A
B. 3.9g Na O 中含有的共价键的数目为0.1N
2 2 A
C. 0.1mol肼 H N-NH 含有的孤电子对数为0.2N
2 2 A
D. CH =CH +H ®CH CH ,生成1mol乙烷时断裂的共价键总数为N
2 2 2 3 3 A
【答案】C
【解析】
【分析】
【详解】A.1个27Al3+的电子数为10,故0.1mol 27Al3+中含有的电子数为1.0N ,故A错误;
A
B.Na O 的电子式为 ,含有1个共价键,3.9g Na O 的物质的量为
2 2 2 2
第4页 | 共21页3.9g
=0.05mol,故3.9g Na O 中含有的共价键的数目为0.05N ,故B错误;
78g/mol 2 2 A
C.肼 H N-NH 中每个N原子上各有1个孤电子对,故0.1mol肼 H N-NH 含有的孤电子对数为0.2
2 2 2 2
N ,故C正确;
A
D.发生CH =CH +H ®CH CH 反应时,C=C中的一个键和H-H键都断裂,故生成1mol乙烷时断裂
2 2 2 3 3
的共价键总数为2N ,故D错误;
A
故选C。
8. 制备水煤气的反应Cs+H 2 Og ƒ H 2 g+COg ΔH>0,下列说法正确的是
A. 该反应ΔS<0
B. 升高温度,反应速率增大
C. 恒温下,增大总压,H O(g)的平衡转化率不变
2
D. 恒温恒压下,加入催化剂,平衡常数增大
【答案】B
【解析】
【分析】
【详解】A.该反应的正反应是气体体积增大的反应,所以△S>0,A错误;
B.升高温度,物质的内能增加,分子运动速率加快,有效碰撞次数增加,因此化学反应速率增大,B正确;
C.恒温下,增大总压,化学平衡向气体体积减小的逆反应方向移动,使H O(g)的平衡转化率减小,C错误;
2
D.恒温恒压下,加入催化剂,化学平衡不移动,因此化学平衡常数不变,D错误;
故合理选项是B。
二、选择题:本题共 6小题,每小题 4分,共 24 分。每小题有一个或两个选项符合题意。若
正确答案只包括一个选项,多选得 0分;若正确答案包括两个选项,只选一个且正确得 2分,
选两个且都正确得 4分,但只要选错一个就得 0分。
9. 液氨中存在平衡:2NH ƒ NH++NH- 。如图所示为电解池装置,以KNH 的液氨溶液为电解液,电
3 4 2 2
解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
第5页 | 共21页A. b电极连接的是电源的负极 B. a电极的反应为2NH +2e-=H +2NH-
3 2 2
C. 电解过程中,阴极附近K+浓度减小 D. 理论上两极产生的气体物质的量之比为1:1
【答案】B
【解析】
【分析】
【详解】A.根据图示可知:在b电极上产生N ,N元素化合价升高,失去电子,发生氧化反应,所以b
2
电极为阳极,连接电源的正极,A错误;
B.电极a上产生H ,H元素化合价降低得到电子,发生还原反应,所以a电极为阴极,电极反应式为:
2
2NH +2e-=H +2NH- ,B正确;
3 2 2
C.电解过程中,阴极附近产生NH- ,使附近溶液中阴离子浓度增大,为维持溶液电中性,阳离子K+会向
2
阴极区定向移动,最终导致阴极附近K+浓度增大,C错误;
D.每反应产生1 mol H ,转移2 mol电子,每反应产生1 mol N ,转移6 mol电子,故阴极产生H 与阳极
2 2 2
产生的N 的物质的量的比是3:1,D错误;
2
选B。
10. 短周期主族元素X、Y、Z、W的原子序数依次增大,XY-离子与Y 分子均含有14个电子;习惯
2
上把电解饱和ZW水溶液的工业生产称为氯碱工业。下列判断正确的是
A. 原子半径:W>Z B. 最高价氧化物对应的水化物的酸性:Y>X
C. 化合物ZXY的水溶液呈中性 D. XY 分子中既有σ键又有π键
2
【答案】BD
【解析】
【分析】XY-离子与Y 分子均含有14个电子,则X为C,Y为N;习惯上把电解饱和ZW水溶液的工业
2
生产称为氯碱工业,则Z为Na,W为Cl。
【详解】A.同周期元素原子半径随核电荷数的增大半径逐渐减小,故Na>Cl,故A错误;
第6页 | 共21页B.同周期元素随核电荷数的增大非金属性逐渐增强,其最高价氧化物对应的水化物的酸性越强,故HNO
3
>H CO ,故B正确;
2 3
C.NaCN为强碱弱酸盐,显碱性,故C错误;
D.(CN) 的结构简式为NºC-Cº N,分子中单键为σ键,三键中含有1个σ键和2个π键,故D正确;
2
故选BD。
11. 关于NH 性质的解释合理的是
3
选项 性质 解释
A 比PH 容易液化 NH 分子间的范德华力更大
3 3
B 熔点高于PH N-H键的键能比P-H大
3
C 能与Ag+以配位键结合 NH 中氮原子有孤电子对
3
D 氨水中存在NH+ NH ×H O是离子化合物
4 3 2
A. A B. B C. C D. D
【答案】C
【解析】
【分析】
【详解】A.NH 和PH 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但氨气中
3 3
含有氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;
3
B.NH 熔点高于PH ,是因为氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是N-H键的键能比
3 3
P-H大,故B错误;
C.NH 中氮原子有孤电子对,使Ag+和NH 以配位键结合形成[Ag(NH ) ]+,故C正确;
3 3 3 2
D.NH ×H O是共价化合物,是弱碱,在水溶液中部分电离出NH+和OH-,故D错误;
3 2 4
答案选C。
12. 我国化工专家吴蕴初自主破解了“味精”的蛋白质水解工业生产方式。味精的主要成分为谷氨酸单钠盐。
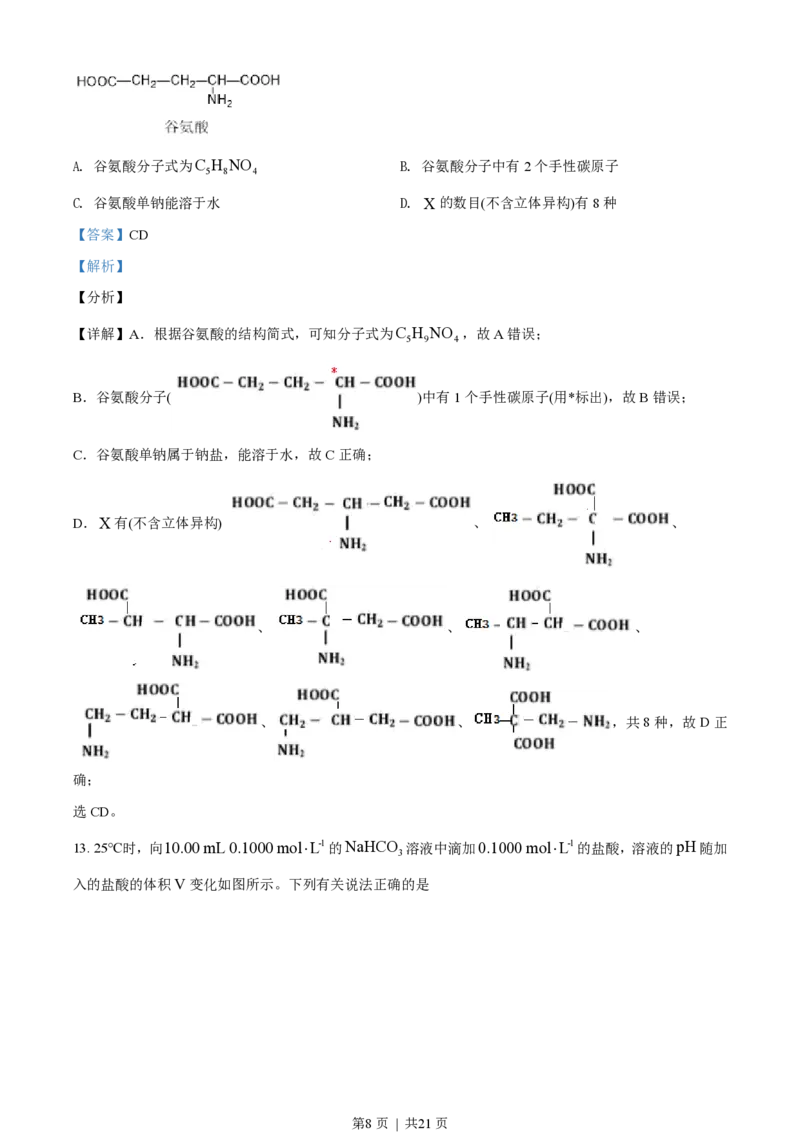
X 是谷氨酸(结构简式如下)的同分异构体,与谷氨酸具有相同的官能团种类与数目。下列有关说法正确的
是
第7页 | 共21页A. 谷氨酸分子式为C H NO B. 谷氨酸分子中有2个手性碳原子
5 8 4
C. 谷氨酸单钠能溶于水 D. X 的数目(不含立体异构)有8种
【答案】CD
【解析】
【分析】
【详解】A.根据谷氨酸的结构简式,可知分子式为C H NO ,故A错误;
5 9 4
B.谷氨酸分子( )中有1个手性碳原子(用*标出),故B错误;
C.谷氨酸单钠属于钠盐,能溶于水,故C正确;
D.X有(不含立体异构) 、 、
、 、 、
、 、 ,共8种,故D正
确;
选CD。
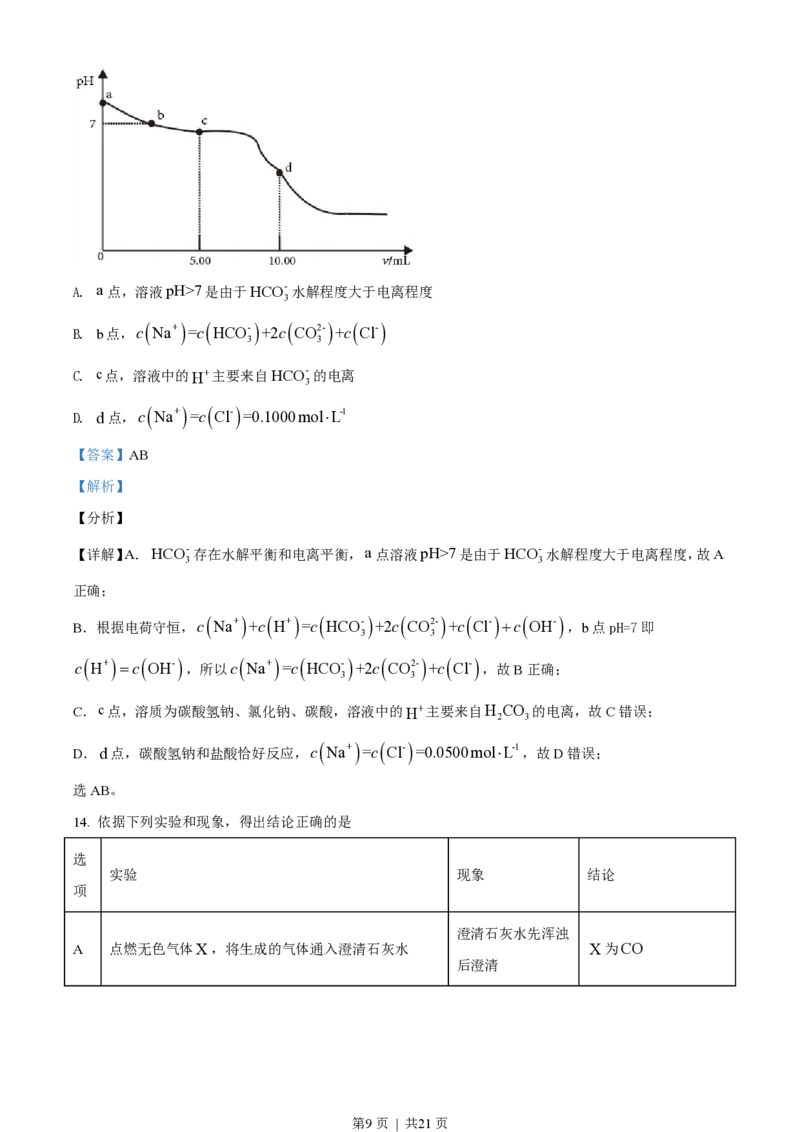
13. 25℃时,向10.00mL0.1000mol×L-1的NaHCO 溶液中滴加0.1000mol×L-1的盐酸,溶液的pH随加
3
入的盐酸的体积V 变化如图所示。下列有关说法正确的是
第8页 | 共21页A. a点,溶液pH>7是由于HCO- 水解程度大于电离程度
3
B. b点,c
Na+
=c
HCO-
+2c
CO2-
+c
Cl-
3 3
C. c点,溶液中的H+主要来自HCO- 的电离
3
D. d点,c Na+ =c Cl- =0.1000mol×L-1
【答案】AB
【解析】
【分析】
【详解】A.HCO- 存在水解平衡和电离平衡,a点溶液pH>7是由于HCO- 水解程度大于电离程度,故A
3 3
正确;
B.根据电荷守恒,c
Na+
+c
H+
=c
HCO-
+2c
CO2-
+c
Cl-
+c
OH-
,b点pH=7即
3 3
c
H+
=c
OH-
,所以c
Na+
=c
HCO-
+2c
CO2-
+c
Cl-
,故B正确;
3 3
C.c点,溶质为碳酸氢钠、氯化钠、碳酸,溶液中的H+主要来自H CO 的电离,故C错误;
2 3
D.d点,碳酸氢钠和盐酸恰好反应,c Na+ =c Cl- =0.0500mol×L-1,故D错误;
选AB。
14. 依据下列实验和现象,得出结论正确的是
选
实验 现象 结论
项
澄清石灰水先浑浊
A 点燃无色气体X,将生成的气体通入澄清石灰水 X为CO
后澄清
第9页 | 共21页B 25℃时,向无色的Y溶液中滴加1~2滴酚酞试液 溶液仍为无色 Y溶液的pH<7
在淀粉和I 的混合溶液中滴加KSCN溶液。[已知:
2
C SCN 、SCN-分别与卤素单质、卤素离子性质相 溶液仍为蓝色 氧化性: SCN 2