高三化学考前速记高频考点合集五
六、有关元素化合物的易错易混点
(一)易错易混再练
1.因为海水中氯的含量高,所以氯被称为“海洋元素” 。 ( )
2.SO2可漂白纸浆,不可用于杀菌、消毒。( )
3.常温下,可用铁质容器或铝制容器储存、运输浓硝酸和浓硫酸。( )
4.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业。( )
5.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的。( )
6.Na2O2粉末投入含酚酞的水中,水中先变红后褪色说明Na2O2具有漂白性。( )
7.氯气通入品红溶液中,溶液褪色,则氯气具有漂白性。( )
8.面包师用小苏打作发泡剂烘焙面包是因为Na2CO3可与酸反应。( )
9. 钾能置换出NaCl溶液中的钠。( )
10.为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化。( )
11.锌与硫酸反应时,硫酸的浓度越大,产生H2的速率越快。( )
12.少量液溴通常保存在无色玻璃试剂瓶中,并在液溴上加少量水液封。( )
13.长时间盛放石灰水的烧杯应先加入适量的稀H2SO4进行洗涤。( )
14.实验室中可利用二氧化锰或高锰酸钾与浓盐酸反应制取氯气,两制备方法中氯气的发生装置完全相同。( )
15.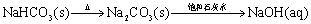 物质间转化均能一步实现。( )
物质间转化均能一步实现。( )
16. 铁在高温下与 H₂O(g) 发生置换反应生成 Fe₃O₄。( )
17. 用洁净的铂丝对某溶液进行焰色试验,火焰呈黄色,则溶液中一定含有 Na⁺,不含 K⁺。( )
18. 制作面点时加入食用纯碱,利用 NaHCO₃ 中和发酵过程产生的酸。 ( )
19. 向盛有 FeSO₄ 溶液的试管中滴加几滴 KSCN 溶液,振荡,再滴加几滴新制氯水,根据溶液颜色变化,可判断 Fe²⁺ 是否具有还原性。( )
20. 金属钠着火时,用细沙覆盖灭火。( )
21. 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象,可知稀硝酸的氧化性比浓硝酸强。( )
22. 探究 Cu 和浓 HNO₃ 反应后溶液呈绿色的原因,将 NO₂ 通入下列溶液至饱和:①浓 HNO₃、②Cu(NO₃)₂ 和 HNO₃ 混合溶液,①无色变黄色,②蓝色变绿色,则 Cu 和浓 HNO₃ 反应后溶液呈绿色的主要原因是溶有 NO₂。( )
23. 为了使火腿肠颜色更鲜红,可多加入些亚硝酸钠。( )
24. Na₂CO₃·10H₂O 的风化是化学变化。( )
25.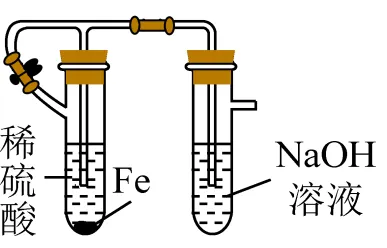 制备并观察氢氧化亚铁的生成。( )
制备并观察氢氧化亚铁的生成。( )
26. 做焰色试验前,铂丝用稀盐酸清洗并灼烧至火焰呈无色。( )
27. 将金属钠在燃烧匙中点燃,迅速伸入集满 CO₂ 的集气瓶中,瓶中产生大量白烟,有黑色颗粒产生,可得出 CO₂ 具有氧化性。( )
28. 过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂。( )
29. 向 Na[Al(OH)₄] 溶液中滴加 NaHCO₃ 溶液,有沉淀和气体生成。( )
30. 将蘸有浓氨水的玻璃棒靠近某试剂瓶瓶口,试剂瓶瓶口有白烟生成,则试剂瓶中盛装的一定是浓盐酸。( )
31. Al₂O₃ 的熔点高,可作耐高温材料,实验室可用氧化铝坩埚熔化 NaOH、Na₂CO₃ 固体等( )
32. 明矾可作净水剂,起到杀菌消毒的作用。( )
33. AlO₂⁻ 与 NH₄⁺ 在水溶液中因发生相互促进水解反应不能大量共存。( )
34. 合金材料中不可能含有非金属元素。( )
35. 合金的硬度一般大于成分金属,而熔点一般低于成分金属。( )
36. 火烧孔雀石炼铜是采用的焦炭法来冶炼金属。( )
37. 电解 AlCl₃、FeCl₃、CuCl₂ 的混合溶液时,阴极上依次析出 Cu、Fe、Al。( )
38. 标准状况下,11.2 L Cl₂ 与水充分反应转移电子数为 0.5NA。( )
39. 1 mol 氯气分别与铁和铝完全反应时转移的电子数均为 3NA。( )
40. “84”消毒液的消毒原理与 H₂O₂ 的相同,都是利用强氧化性。( )
41. 过量 SO₂ 通入 NaClO 溶液中:SO₂ + ClO⁻ + H₂O === HClO + HSO₃⁻。( )
42. 含 4 mol HCl 的浓盐酸与足量 MnO₂ 反应,可制备 22.4 L Cl₂。( )
43. 用 MnO₂ 和浓盐酸制取 Cl₂ 的反应中,氧化剂与还原剂物质的量之比为 1∶4。( )
44. Cl₂、F₂ 与 H₂O 反应的原理相同,不属于置换反应。( )
45. 只用 AgNO₃ 溶液可鉴别 Na₂CO₃、NaCl 和 KBr。( )
46. 为验证Br₂的氧化性强于I₂,将少量溴水加入KI溶液中,再加入CCl₄,振荡,静置,可观察到下层液体呈紫红色。( )
47. 硫黄易溶于CS₂,所以可用CS₂溶解试管内壁的硫。( )
48. SO₂、漂白粉、Na₂O₂都能使鲜花褪色,其原理相同。( )
49. SO₂和Cl₂等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好。( )
50. 浓硫酸具有强氧化性,所以浓硫酸不可用于干燥H₂和CO。( )
⚠️ 易错易混提醒
1. 焰色反应与物理变化
Na及其化合物发生焰色反应时火焰颜色均为黄色,且该变化为物理变化。鉴别Na、K利用焰色反应,二者混合时鉴别K元素要隔着蓝色钴玻璃。
2. 钠与氧气反应电子转移
无论Na与O₂反应生成Na₂O还是Na₂O₂,只要参与反应的Na的质量相等,则转移电子的物质的量一定相等。
3. Na₂O₂电子式与离子比
Na₂O₂的电子式为Na⁺[:Ö:Ö:]²⁻Na⁺,阴阳离子个数比为1:2。
4. Na₂O₂与水/CO₂反应电子转移
1 mol Na₂O₂与足量水或二氧化碳的反应中转移的电子数为Nₐ。
5. Na₂O₂漂白性原理
Na₂O₂具有强氧化性,能氧化破坏有机色素的分子结构,具有漂白性。
6. Na₂O₂与SO₂反应方程式
Na₂O₂与SO₂反应的化学方程式为Na₂O₂ + SO₂ = Na₂SO₄。
7. 高炉炼铁还原剂
热还原法中使用的还原剂为碳、一氧化碳和氢气,在高炉炼铁中,加入的还原剂是焦炭,但真正作还原剂的是CO。
8. 电解法冶炼活泼金属使用的是熔融的金属盐或金属氧化物,不是盐溶液。钠、镁、铝的冶炼是电解熔融的 NaCl、MgCl₂、Al₂O₃;不用氧化镁是因为其 ______ 高,不用氯化铝是因为 AlCl₃ 是共价化合物,熔融态不导电。
9. 在金属活动性顺序表中,虽然前面的金属能够将后面的金属从其化合物中置换出来,但不一定是从其盐溶液中置换,例如 Na 由于活泼性太强,不能从 CuCl₂ 溶液中置换出 Cu,但是可以在熔融状态下置换出铜。
10. 将空气液化,然后逐渐升温,先制得氮气,余下氧气。
11. 碱金属(如:Na、K)与酸反应,有时要考虑其与水的反应。也就是说不管酸足量与否,碱金属一定会完全反应。生成 H₂ 的量取决于碱金属的量。
12. 能与冷水反应放出气体单质的物质不一定是活泼的金属单质或活泼的非金属单质,还可以是 2Na₂O₂ + 2H₂O = O₂↑ + 4NaOH。
14. 镁和溴水反应,研究表明水起催化剂的作用。
15. 加热 Mg(HCO₃)₂ 溶液生成的是 Mg(OH)₂ 沉淀,而不是 MgCO₃ 沉淀,因为 Mg(OH)₂ 比 MgCO₃ 更难溶于水。反应方程式为 Mg(HCO₃)₂ △ MgCO₃↓ + CO₂↑ + H₂O MgCO₃ + H₂O △ Mg(OH)₂ + CO₂↑。
16. 要逐一溶解 Al(OH)₃ 和 AgCl 时,要先加 NaOH 再加氨水,以防止先加氨水生成银氨溶液溶解 Al(OH)₃。
17. 少量 SO₂ 气体通入 NaClO 溶液中: SO₂ + H₂O + 3ClO⁻ = SO₄²⁻ + Cl⁻ + 2HClO,切记不是生成 H⁺,因为 NaClO 过量。
18. 虽然自然界含钾的物质均易溶于水,自然界钾元素含量不低,但以复杂硅酸盐形式存在难溶于水,故需施钾肥来满足植物生长需要。
19. Fe 与 Cl₂ 反应只能生成 FeCl₃,与 I₂ 反应生成 FeI₂,与反应物的用量无关。
20. Fe 与水蒸气在高温下反应生成 H₂ 和 ______,而不是 Fe₂O₃。
21. 过量的 Fe 与硝酸作用,或在 Fe 和 Fe₂O₃ 的混合物中加入盐酸,均生成 Fe²⁺。要注意产生的 Fe³⁺ 还可以氧化单质 Fe 这一隐含反应:Fe + 2Fe³⁺ = 3Fe²⁺。
22. NO₃⁻ 与 Fe²⁺ 在酸性条件下不能共存。
33. Fe₂O₃、Fe(OH)₃ 与氢碘酸反应时,涉及 Fe³⁺ 与 I⁻ 的氧化还原反应,产物为 Fe²⁺、I₂ 和 H₂O。
34. FeCl₃ 溶液加热浓缩时,因 Fe³⁺ 水解和 HCl 的挥发,得到的固体为 Fe(OH)₃,灼烧后得到红棕色 Fe₂O₃ 固体;而 Fe₂(SO₄)₃ 溶液蒸干时,因硫酸是难挥发性的酸,将得不到 Fe(OH)₃ 固体,最后得到的固体仍为 Fe₂(SO₄)₃。
35. 注意亚铁盐及 Fe(OH)₂ 易被空气中氧气氧化成三价铁的化合物。如某溶液中加入碱溶液后,最终得到红褐色沉淀,并不能断定该溶液中一定含有 Fe³⁺,也可能含有 Fe²⁺。
36. FeCl₂ 可以由化合反应制得,但不可由单质间通过化合而制得。
37. 在分析浓盐酸和二氧化锰,浓硫酸和铜等反应问题时,要看清楚是提供 nmol 酸还是有 nmol 酸参加反应,这里要注意酸由浓变稀所带来的问题;要看清楚是有 nmol 酸参加反应,还是有 nmol 酸被氧化(或被还原)。
38. Cu 和一定量的浓 HNO₃ 反应,产生的是 NO₂ 和 NO 的混合气体,当 Cu 有剩余,再加入稀 H₂SO₄,Cu 继续溶解。
39. 常见的铜矿有黄铜矿(主要成分为 CuFeS₂)、孔雀石[主要成分为 CuCO₃·Cu(OH)₂]等。此外铁在自然界中还以游离态的形式存在于陨铁中。自然界中也存在少量的单质铜。
40. 与 AlO₂⁻ 不能大量共存的离子有 H⁺、Al³⁺、Fe³⁺、HCO₃⁻ 等。要注意 AlO₂⁻ 与 HCO₃⁻ 的反应并非相互促进水解,而是因为酸性 HCO₃⁻ > Al(OH)₃。
41. 氟气与氢氧化钠溶液可发生反应: 2NaOH + 2F₂ = 2NaF + OF₂ + H₂O。
42. CaH₂ 与 Na₂O₂、CaC₂、FeS₂ 化合物类型相同,但化学键类型不完全相同,CaH₂ 只有离子键。
43. 工业上制备粗硅,是用过量的 C 和 SiO₂ 高温下反应,由于 C 过量,生成的是 CO 而不是 CO₂。
44. SiO₂不导电,是制作光导纤维的材料;Si是半导体,是制作光电池的材料。
45. SiO₂是酸性氧化物,酸性氧化物一般能与水反应生成酸,但SiO₂不溶于水;酸性氧化物一般不与酸作用,但SiO₂能与HF反应,不过SiO₂不属于两性氧化物,因为该反应生成的不是盐和水。
46. 硅酸盐大多难溶于水,但硅酸钠水溶液称为花玻碱或水玻璃,却是盐溶液且属一种矿物胶。NaOH溶液或纯碱溶液能用玻璃试剂瓶(内壁光滑),但不能用玻璃塞,因玻璃塞中裸露的二氧化硅与碱性溶液反应生成硅酸钠将瓶塞与瓶口粘在一起。
47. 1molCl₂参加反应,转移电子数不一定为2NA。如反应Cl₂+2NaOH===NaCl+NaClO+H₂O,1mol Cl₂参加反应,转移电子数目为NA。
48. 实验室制Cl₂,除了用MnO₂和浓盐酸反应外,还可以用KMnO₄、KClO₃、NaClO与浓盐酸反应且都不需要加热,因此酸性KMnO₄溶液用的是H₂SO₄酸化而不是盐酸。
49. ClO⁻不论在酸性环境中还是在碱性环境中均能体现强氧化性,如ClO⁻与SO₃²⁻、I⁻、Fe²⁺均不能大量共存;向Ca(ClO)₂溶液中通入SO₂气体生成CaSO₄而不是CaSO₃,其离子方程式为Ca²⁺+3ClO⁻+SO₂+H₂O=CaSO₄↓+Cl⁻+2HClO(少量SO₂);Ca²⁺+2ClO⁻+2SO₂+2H₂O=CaSO₄↓+2Cl⁻+SO₄²⁻+4H⁺(过量SO₂)。
50. 利用加压液化法分离NH₃,这与氢键有关(氨气的沸点比较高)。
51.NH₄(NH₄H)是离子晶体,溶于水溶液显碱性:NH₃+H₂O=NH₃·H₂O+H₂
52. .SO₂通入石灰水中的现象与CO₂类似,但比起CO₂现象产生得快。主要原因有:SO₂比CO₂溶解度大,且对应H₂SO₃酸性比H₂CO₃强。
53. 工业保存氯气的方法:将氯气干燥后加压液化贮存于钢瓶中。
54. AgCl能溶于足量的氨水,生成银氨络离子;
银氨溶液中加足量的盐酸又能生成AgCl沉淀。[Ag(NH₃)₂]⁺+OH⁻+Cl⁻+3H⁺=AgCl↓+2NH₄⁺+H₂O 要警惕类似反应出现在推断题中。
55. 大气中大量二氧化硫来源于煤和石油的燃烧以及金属矿石的冶炼。
56. 活性炭、二氧化硫、氯水等都能使品红褪色,但反应本质有所不同,活性炭是吸附品红,为物理变化,SO₂是生成不稳定的化合物且可逆,氯水是发生氧化还原反应且不可逆。
57. 在次氯酸钠溶液中通入少量二氧化硫得到的不是亚硫酸钠与次氯酸,而是得到NaCl和H₂SO₄,因为次氯酸可以氧化亚硫酸钠。
58. 浓硝酸、浓硫酸在常温下能与铝、铁等发生钝化反应,反应很快停止,不是不反应;但在常温下浓硫酸与铜不反应,浓硝酸与铜能反应。
59. SO₂和Cl₂等体积混合通入溶液中,氯气的漂白性不但不增强,反而消失。
60. 把SO₂气体通入BaCl₂溶液中,没有沉淀生成,但若通入NH₃或加入NaOH溶液,或把BaCl₂改成Ba(NO₃)₂均有白色沉淀生成,前两者生成BaSO₃沉淀,后者生成BaSO₄沉淀。
61. 浓盐酸和MnO₂(足量)、浓H₂SO₄和Cu(足量,加热)、浓HNO₃和Cu(足量)反应时,随反应进行,产物会发生变化或反应停止。
62. 足量Zn和浓H₂SO₄反应,开始生成SO₂,随着硫酸变稀,还会生成氢气。
63. NO只能用排水法或气囊法收集,NO₂不能用排水法,可用排苯法收集。
64. 工业上制备的盐酸显黄色是因为溶有Fe³⁺,而浓HNO₃显黄色是因为溶有NO₂。
65. NO₂能被NaOH溶液吸收,NO单独不能被强碱溶液吸收,NO与NO₂混合能被NaOH溶液吸收。
66. NO₂或NO与O₂通入水的计算中常用到4NO+3O₂+2H₂O=4HNO₃、4NO₂+O₂+2H₂O=4HNO₃两个方程式,也可以利用n(元素化合价的变化),根据电子守恒进行计算。
67. 强氧化性酸(如HNO₃、浓H₂SO₄)与金属反应不生成H₂;金属和浓HNO₃反应一般生成NO₂,而金属和稀HNO₃反应一般生成NO。
68. 实验室制备NH₃,除了用Ca(OH)₂和NH₄Cl反应外,还可用浓氨水的分解(加NaOH固体或CaO)制取,而检验NH₄⁺用浓NaOH溶液并加热,用湿润的红色石蕊试纸检验生成的气体,以确定NH₄⁺的存在。
69. 收集NH₃时,把一团干燥的棉花放在试管口,以防止与空气对流;收集完毕,尾气处理时,应放
70. 浓盐酸和浓氨水反应有白烟生成,常用于HCl和NH₃的相互检验。
71. 忽视NO₃⁻在酸性条件下的强氧化性。在酸性条件下NO₃⁻不能与Fe²⁺、I⁻、SO₃²⁻、S²⁻等还原性较强的离子大量共存。
72. 在书写离子方程式时,忽视HNO₃的强氧化性,将氧化还原反应简单地写成复分解反应。
 夜雨聆风
夜雨聆风




