寻找锁与钥匙:从经典到AI,分子对接工具全图鉴
在药物研发的漫长征途中,分子对接(Molecular Docking)始终扮演着“红娘”的角色。它试图在数以亿计的小分子中,为蛋白质受体寻找那个最契合的“灵魂伴侣”。
从基于物理势场的传统算法,到如今深度学习下的“共折叠”革命,分子对接技术正经历着前所未有的范式演进。本文将带你一览当前主流的分子对接方法,解析它们的“独门绝技”与适用场景。
一、经典派:工业界的稳健基石
经典对接方法核心在于“搜索算法+打分函数”,它们通常将蛋白视为刚性或半刚性,在预设的口袋中寻找能量最低点。
1. Glide:学术与工业的“金标准”
作为Schrödinger 旗下的王牌,Glide 凭借基于网格(Grid)的算法和极高的预测精度,稳坐工业界头把交椅。
- 核心:提供 HTVS(高通量)、SP(标准)、XP(特高精度)三种模式。
- 优缺点:打分函数极其精细,能敏锐捕捉氢键和疏水作用;缺点是商业授权昂贵,对蛋白柔性处理有限。
- 适用场景:先导化合物的深度精修与商业级虚拟筛选。
2. AutoDock Vina:科研人员的“国民工具”
- 核心:迭代局部搜索与经验打分。
- 优缺点:免费开源、速度极快,是目前引用率最高的方法之一。但其打分函数相对简化,在处理复杂金属离子或共价结合时略显吃力。
- 适用场景:大规模分子库的初步过滤及基础学术研究。
3. FlexS:柔性分子的“手术刀”
- 核心:采用“碎片增量构建”法,将配体拆分再重新组装。
- 适用场景:专门应对那些拥有极多旋转键、构象极度复杂的长链分子。
二、 AI 进化派:打破传统束缚
当深度学习介入,对接不再仅仅是物理模拟,而变成了概率分布的推理。
1. DiffDock:盲对接的“导航仪”
- 核心:基于扩散模型(Diffusion Model)的生成式 AI。
- 优缺点:它最大的突破是不再需要预设“口袋”,能全蛋白搜索。但在局部物理结构的合理性(如原子重叠)上,有时不及经典方法。
- 适用场景:靶点结构未知或结合位点不明确的创新药研发。
2. Gnina:AI 赋能的“质检员”
- 核心:在经典 Vina 采样基础上,引入 CNN(卷积神经网络)进行重新打分。
- 优缺点:结合了物理采样的严谨和深度学习对复杂特征的识别。
- 适用场景:需要高精度打分,希望在 Vina 基础上进一步降低假阳性率。
三、共折叠派:下一代终极范式
这一派系彻底模糊了“对接”的界限,将蛋白和配体作为一个整体进行结构预测。
1. AlphaFold 3 (AF3):跨界的统治力
- 核心:全原子扩散预测模型。
- 亮点:解决了困扰药化家几十年的“诱导契合(Induced Fit)”难题。它能预测蛋白在结合配体后的形变,真正实现了动态响应。
- 场景:复杂复合物建模(蛋白–核酸–配体)及高难度靶点验证。
2. Boltz-2:开源界的新星
- 核心:类 AF3 架构,强调结构预测与亲和力评估的同步。
- 亮点:宣称能以极速完成接近物理金标准的亲和力预测,为开源社区提供了强力支持。
总结:如何选择你的“药学罗盘”?
为了方便大家决策,我们整理了以下对比表:
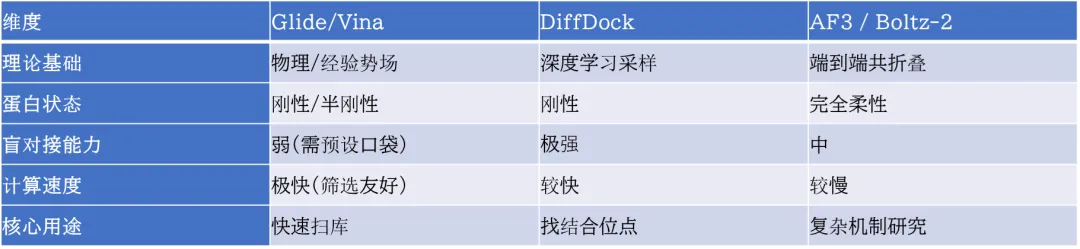
结语: > 没有任何一种算法是完美的。在实际研发中,往往采用“Vina初筛 -> Glide复筛 -> AF3验证”的阶梯式策略。随着算力与算法的迭代,我们离“精准预测药物活性”的梦想正越来越近。
 夜雨聆风
夜雨聆风




