【2026版高考总复习红与勾讲与练化学电子版第九章第43讲酸碱中和滴定及应用

1.了解酸碱中和滴定的原理和滴定终点的判断方法,知道指示剂选择的方法。2.掌握酸碱中和滴定的操作、数据处理及误差分析的方法。3.掌握滴定法在定量测定中的应用。
考点一 酸碱中和滴定原理及操作

1.滴定原理
(1)用已知浓度的酸(或碱)滴定未知浓度的碱(或酸),根据中和反应的等量关系来测定碱(或酸)的浓度。
(2)酸碱指示剂发生颜色突变,表明反应已经完全,指示滴定终点。
|
指示剂 |
变色范围的pH |
||
|
石蕊 |
<5.0红色 |
5.0~8.0紫色 |
>8.0蓝色 |
|
甲基橙 |
<3.1红色 |
3.1~4.4橙色 |
>4.4黄色 |
|
酚酞 |
<8.2无色 |
8.2~10.0浅红色 |
>10.0红色 |
2.实验用品
(1)仪器:酸式滴定管(如图A)、碱式滴定管(如图B)、滴定管夹、铁架台、锥形瓶、烧杯、烧瓶。
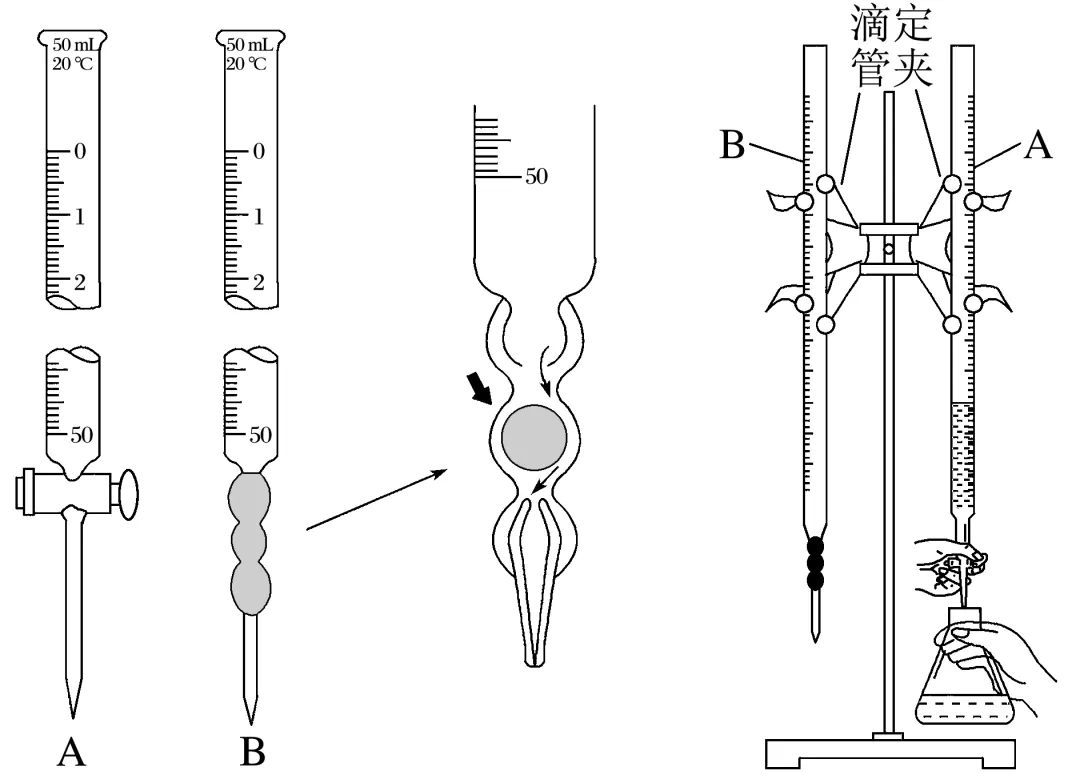
(2)试剂:标准液、待测液、指示剂、蒸馏水。
3.实验操作(以标准盐酸滴定待测NaOH溶液为例)
(1)滴定前的准备

(2)滴定
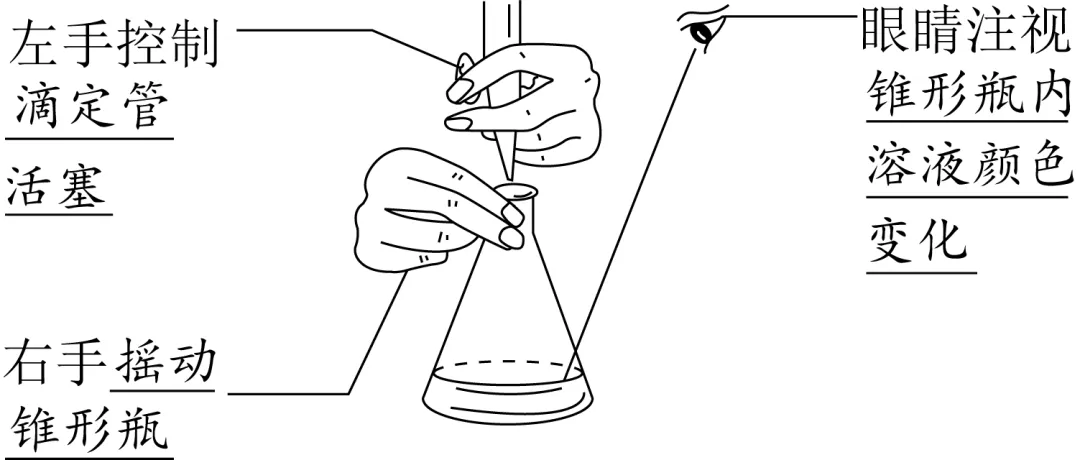
(3)终点判断
等到滴入最后半滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,视为滴定终点并记录标准液的体积。
4.数据处理
按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据c(NaOH)=c(HCl)·V(HCl)V(NaOH)计算。
5.滴定曲线
在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。当滴定接近终点(pH=7)时,很少量的碱(或酸)就会引起溶液pH的突变(如图为NaOH滴定盐酸的滴定曲线)。
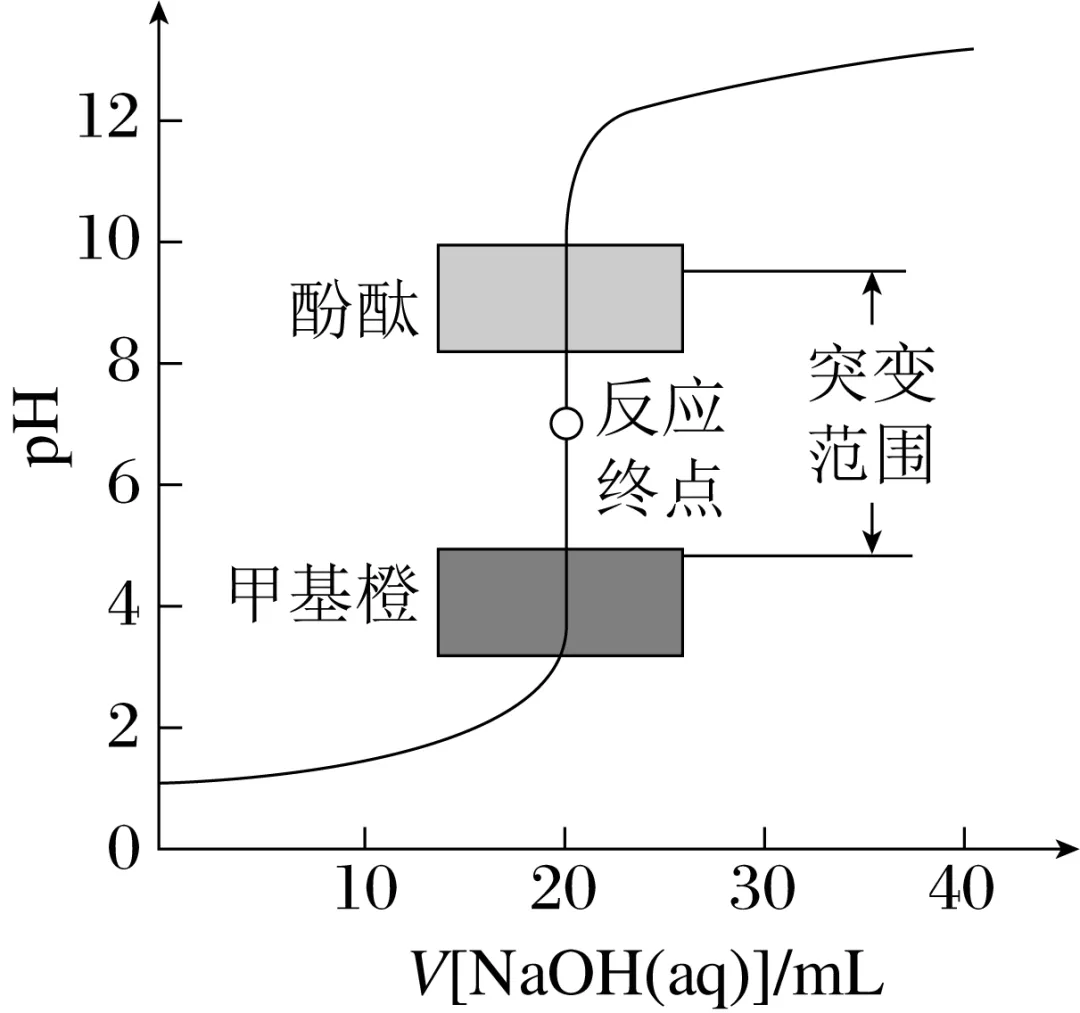
6.误差分析
分析依据:cB=cA·VAVB(VB表示准确量取的待测液的体积,cA表示标准溶液的浓度)。
若VA偏大,则cB偏大;若VA偏小,则cB偏小。

正确的打“√”,错误的打“×”。
(1)滴定管和锥形瓶在滴定前都应该用待装溶液润洗。(×)
(2)滴定终点就是酸碱恰好中和的点。(×)
(3)酸碱指示剂越多变色越明显,指示剂至少加入2~3 mL。(×)
(4)酸碱中和滴定进行中,眼睛要时刻观察滴定管内溶液液面的变化。(×)
(5)滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁。(√)

题组一 中和滴定的操作
1.下列实验操作中正确的是( B )
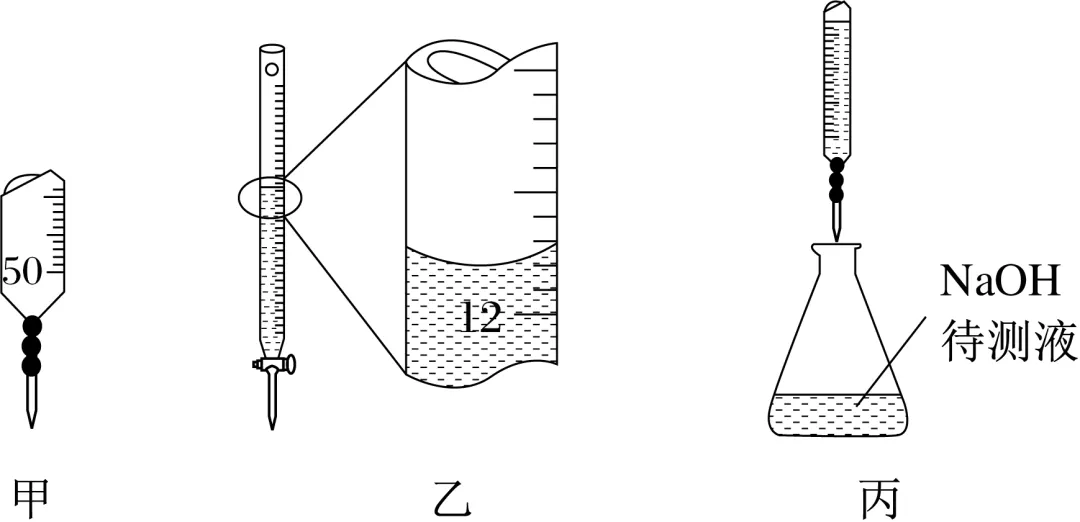
A.选用如图甲所示的仪器,准确量取一定体积的K2Cr2O7标准溶液
B.中和滴定时,滴定管用所盛装的反应液润洗2~3次
C.如图乙所示,记录滴定终点读数为12.20 mL
D.按如图丙所示进行中和滴定实验
解析:K2Cr2O7具有强氧化性,所以不能用碱式滴定管量取,而应该选用酸式滴定管,A错误;中和滴定时,滴定管用所盛装的反应液润洗2~3次,以保证标准液浓度的准确性,B正确;酸式滴定管的示数从上到下依次增大,且可读到小数点后两位,根据题图所示数据,其终点读数为11.80 mL,C错误;滴定氢氧化钠待测液时,需用酸液,即标准液需装在酸式滴定管中,而不是题图所示的碱式滴定管,D错误。

通过网盘分享的文件:2026红对勾讲与练高三政治等9个文件
链接: https://pan.baidu.com/s/1PV9jm4aYOjX-uWLS9hJnUw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风





