【2026版三维高考设计高中化学人教版培优讲义word电子版第4讲氧化还原反应方程式的配平与计算
课标要求
能利用得失电子守恒法进行氧化还原反应方程式的配平和计算。

考点一氧化还原反应方程式的配平

1.氧化还原反应方程式配平的三大原则
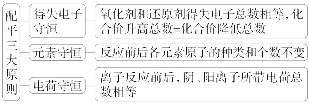
2.氧化还原反应方程式配平的一般步骤
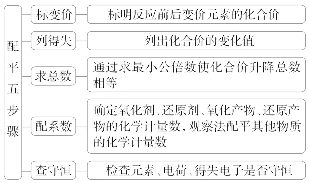
【配平示例】 配平化学方程式:
K2Cr2O7+H2C2O4+H2SO4 Cr2(SO4)3+K2SO4+CO2↑+H2O
Cr2(SO4)3+K2SO4+CO2↑+H2O

|
一 |
正向配平 |
1.(1)H2S+KMnO4+H2SO4 K2SO4+MnSO4+S↓+H2O
K2SO4+MnSO4+S↓+H2O
(2)KI+KIO3+H2SO4 I2+K2SO4+H2O
I2+K2SO4+H2O
(3)Mn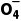 +H++Cl-
+H++Cl- Mn2++Cl2↑+H2O
Mn2++Cl2↑+H2O
|
二 |
逆向配平 |
2.(1)KClO KCl+KClO3
KCl+KClO3
(2)I2+NaOH NaI+NaIO3+H2O
NaI+NaIO3+H2O
(3)P4+KOH+H2O K3PO4+PH3↑
K3PO4+PH3↑
(4)NH4NO3 N2↑+O2↑+H2O
N2↑+O2↑+H2O
|
三 |
含未知数的配平 |
3.(1)CO+NOx CO2+N2
CO2+N2
(2)FexS+HCl S+FeCl2+H2S
S+FeCl2+H2S
(3)Na2Sx+NaClO+NaOH Na2SO4+NaCl+H2O
Na2SO4+NaCl+H2O
|
四 |
缺项配平 |
4.(1)Fe3++SO2+ Fe2++S
Fe2++S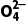 +
+
(2)ClO-+Fe(OH)3+ Cl-+Fe
Cl-+Fe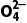 +H2O
+H2O
(3)Mn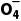 +H2O2+
+H2O2+ Mn2++O2↑+H2O
Mn2++O2↑+H2O
(4)将NaBiO3固体(黄色,微溶)加入MnSO4和H2SO4的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该反应的离子方程式:
NaBiO3+Mn2++ Na++Bi3+++
Na++Bi3+++

(1)缺项方程式是指某些反应物或生成物在方程式中没有写出来,它们一般为水、酸(H+)或碱(OH-),其配平方法:先用“化合价升降法”配平含有变价元素的物质的化学计量数,然后由原子守恒和电荷守恒确定未知物,最后根据原子守恒和电荷守恒进行配平。
(2)补项原则
|
条件 |
补项原则 |
|
酸性条件下 |
缺H或多O补H+,少O补H2O |
|
碱性条件下 |
缺H或多O补H2O,少O补OH- |
考点二电子守恒思想在氧化还原反应计算中的应用

1.电子守恒法计算的原理
氧化剂得电子总数=还原剂失电子总数
2.电子守恒法计算的流程


|
一 |
确定元素的价态或物质的组成 |
1.在酸性条件下,可发生如下反应:Cl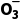 +2M3++4H2O
+2M3++4H2O M2
M2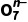 +Cl-+8H+,M2
+Cl-+8H+,M2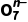 中M的化合价是()
中M的化合价是()
A.+4 B.+5C.+6 D.+7
2.某强氧化剂[XO(OH)2]+可被Na2SO3还原,氧化产物为S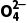 。如果还原1.2×10-3 mol[XO(OH)2]+需用30 mL 0.1 mol·L-1 Na2SO3溶液,那么X元素被还原后的物质可能是()
。如果还原1.2×10-3 mol[XO(OH)2]+需用30 mL 0.1 mol·L-1 Na2SO3溶液,那么X元素被还原后的物质可能是()
A.XO B.X2O3C.X2O D.X
|
二 |
电子守恒在氧化还原滴定中的应用 |
3.某工业废水中含有Cr2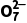 2
2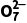 :取20 mL废水,加入适量稀硫酸,再加入过量的V1 mL c1 mol·L-1(NH4)2Fe(SO4)2溶液,充分反应(还原产物为Cr3+)。用c2 mol·L-1 KMnO4溶液滴定过量的Fe2+至终点,消耗KMnO4溶液V2 mL。则原废水中c(Cr2
:取20 mL废水,加入适量稀硫酸,再加入过量的V1 mL c1 mol·L-1(NH4)2Fe(SO4)2溶液,充分反应(还原产物为Cr3+)。用c2 mol·L-1 KMnO4溶液滴定过量的Fe2+至终点,消耗KMnO4溶液V2 mL。则原废水中c(Cr2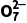 )为。
)为。
考点三新情境下氧化还原反应方程式的书写

新情境下氧化还原反应方程式的书写流程
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价的变化配平化学方程式,具体书写流程如下:

【书写示例】 KMnO4能与热的硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式是
。

|
一 |
依据陈述信息书写方程式 |
1.(1)已知在酸性条件下,FeSO4能将+6价铬还原为+3铬,写出K2Cr2O7与FeSO4溶液在酸性介质中反应的离子方程式:。
(2)在酸性条件下,NaClO2可发生反应生成NaCl,并释放出ClO2,该反应的离子方程式为;
将生成的ClO2通入KI和H2SO4的混合溶液中,发生反应的离子方程式为。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




