【2026版三维高考设计高中化学人教版培优讲义word电子版第47讲沉淀溶解平衡
课标要求
1.认识难溶电解质在水溶液中存在沉淀溶解平衡,了解沉淀的生成、溶解与转化。
2.能综合运用离子反应、化学平衡原理,分析和解决生产、生活中有关难溶电解质的实际问题。

考点一难溶电解质的沉淀溶解平衡及其应用

(一)沉淀溶解平衡
1.概念
在一定温度下的水溶液中,当沉淀和溶解的速率相等时,即建立了沉淀溶解平衡状态。
2.影响因素
(1)内因:难溶电解质本身的性质,这是决定因素。
(2)外因
以AgCl(s)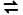 Ag+(aq)+Cl-(aq) ΔH>0为例,说明外因对沉淀溶解平衡的影响。
Ag+(aq)+Cl-(aq) ΔH>0为例,说明外因对沉淀溶解平衡的影响。
|
条件 |
移动方向 |
平衡后c(Ag+) |
平衡后c(Cl-) |
|
加入AgNO3 |
增大 |
减小 |
|
|
加H2O |
正向 |
不变 |
|
|
升温 |
增大 |
||
|
通入HCl |
逆向 |
增大 |
|
|
加入K2S |
减小 |
增大 |
归纳总结
(1)浓度:加水稀释,平衡向沉淀溶解的方向移动,Ksp不变。
(2)温度:绝大多数难溶电解质的溶解是吸热的,升温,平衡向沉淀溶解的方向移动,Ksp增大。
(3)同离子效应:加入与难溶电解质构成微粒相同离子组成的物质,平衡向生成沉淀的方向移动,Ksp不变。
(二)沉淀溶解平衡的应用
1.沉淀的生成
(1)调节pH法:如除去NH4Cl溶液中的FeCl3杂质,可加入氨水调节pH,使Fe3+生成Fe(OH)3沉淀而除去,离子方程式为。
(2)沉淀剂法:以H2S、Na2S等沉淀污水中的Hg2+、Cu2+等重金属离子。写出用H2S除去Cu2+的离子方程式:。
2.沉淀的溶解
如要使Mg(OH)2沉淀溶解,可加入盐酸、NH4Cl溶液等。
3.沉淀的转化
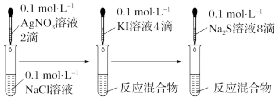
(1)实验探究AgCl、AgI、Ag2S的转化
|
实验 操作 |
|
||
|
实验现象 |
有白色沉淀析出 |
白色沉淀转化为色沉淀 |
黄色沉淀转化为色沉淀 |
|
化学方程式 |
NaCl+AgNO3 |
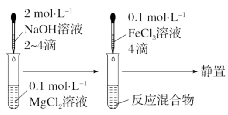
(2)实验探究Mg(OH)2与Fe(OH)3的转化
|
实验 操作 |
|
|
|
实验 现象 |
产生白色沉淀 |
白色沉淀转化为色沉淀 |
|
化学 方程式 |
MgCl2+2NaOH |
实验结论:Mg(OH)2沉淀转化为Fe(OH)3沉淀,说明溶解度:。
(3)沉淀转化的应用
锅炉除垢,将CaSO4转化为CaCO3的离子方程式为;
ZnS沉淀中滴加CuSO4溶液得到CuS沉淀的离子方程式为。

判断正误(正确的打“√”,错误的打“×”)。
(1)沉淀达到沉淀溶解平衡时,溶液中溶质离子浓度一定相等,且保持不变。()
(2)BaSO4 Ba2++S
Ba2++S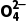 和BaSO4(s)
和BaSO4(s)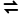 Ba2+(aq)+S
Ba2+(aq)+S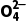 (aq),两式所表示的意义相同。()
(aq),两式所表示的意义相同。()
(3)在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小。()
(4)在含有Mg(OH)2沉淀的饱和溶液中加入固体NH4Cl,沉淀量不变。()
(5)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度。()
(6)溶解度较小的沉淀不可以转化成溶解度较大的沉淀。()

|
一 |
沉淀溶解平衡移动及影响因素 |
1.某兴趣小组对氢氧化镁的溶解进行如图探究实验。下列说法错误的是()
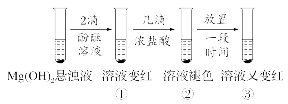
A.c(OH-):①=③
B.③中存在:2c(Mg2+)>c(Cl-)
C.③中溶液又变红的原因:沉淀溶解平衡正向移动
D.①中存在沉淀溶解平衡:Mg(OH)2(s)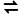 Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
2.已知溶液中存在平衡:Ca(OH)2(s)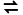 Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法不正确的是(填序号)。
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法不正确的是(填序号)。
①升高温度,平衡逆向移动 ②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度 ③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液 ④恒温下,向溶液中加入CaO,溶液的pH升高 ⑤给溶液加热,溶液的pH升高 ⑥向溶液中加入Na2CO3溶液,其中固体质量增加 ⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
|
二 |
沉淀溶解平衡的应用 |
3.(2024·福建福州模拟)为研究沉淀的生成及其转化,某小组进行如下实验。关于该实验的分析不正确的是()
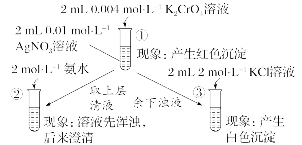
A.①中浊液中存在平衡:Ag2CrO4(s)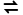 2Ag+(aq)+Cr
2Ag+(aq)+Cr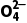 (aq)
(aq)
B.②中溶液变澄清的原因:AgOH+2NH3·H2O [Ag(NH3)2]OH+2H2O
[Ag(NH3)2]OH+2H2O
C.③中颜色变化说明有AgCl生成
D.该实验可以证明Ag2CrO4沉淀可以转化为AgCl沉淀

沉淀先后顺序的判断
向溶液中加入沉淀剂,当可能有多种沉淀生成时,哪种沉淀的溶解度最小(当各种沉淀的Ksp表达式相同时,Ksp越小,沉淀的溶解度越小),则最先生成该沉淀。如:
(1)向含等浓度Cl-、Br-、I-的混合液中加入AgNO3溶液,最先生成的沉淀是AgI。
(2)向含等浓度C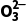 、OH-、S2-的混合液中加入CuSO4溶液,最先生成的沉淀是CuS。
、OH-、S2-的混合液中加入CuSO4溶液,最先生成的沉淀是CuS。
(3)向Mg(HCO3)2溶液中加入适量NaOH溶液,生成的沉淀是Mg(OH)2而不是MgCO3[原因是Mg(OH)2的溶解度比MgCO3的小]。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风