Adv. Mater.:可部署3D打印血管支架及其表面催化内源性一氧化氮生成
研究背景
动脉粥样硬化是导致心脏病和中风的主要全球健康挑战。目前最常见的临床治疗是血管成形术和支架植入,但现有技术存在显著局限性。基于导管的球囊扩张和传统支架植入可导致血管壁损伤、炎症和支架内再狭窄。尽管支架技术从裸金属支架、药物洗脱支架发展到生物可吸收支架,它们仍面临永久性植入导致晚期再狭窄,或聚合物涂层药物耗尽、支架降解产生酸性副产物及炎症等问题。因此,迫切需要一种能够长期稳定发挥功能、减少炎症并有效预防再狭窄的新型先进支架系统。
研究内容
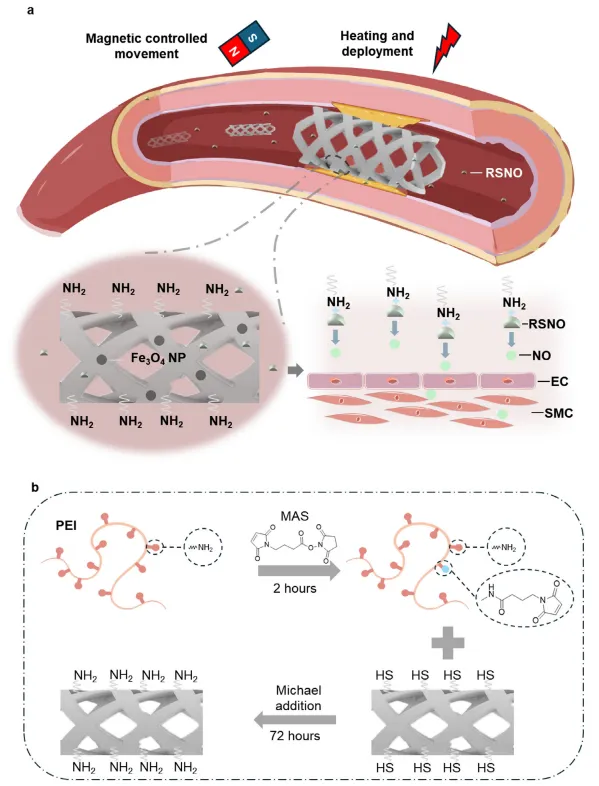
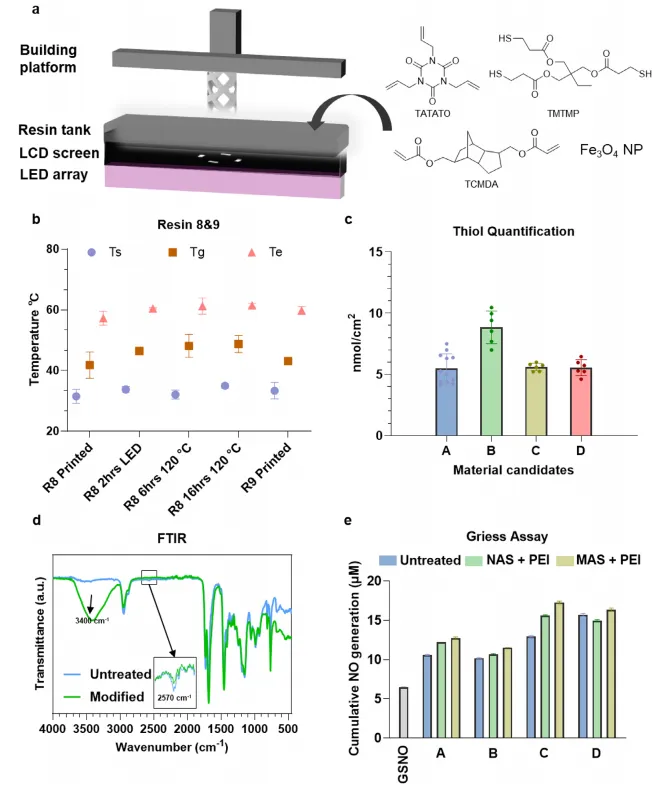
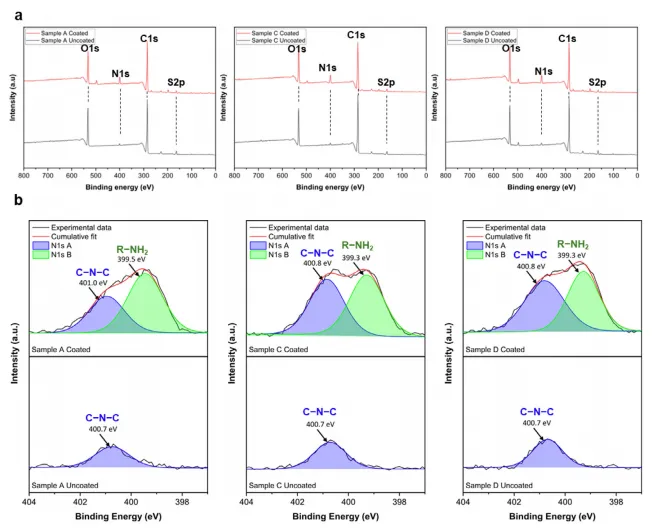
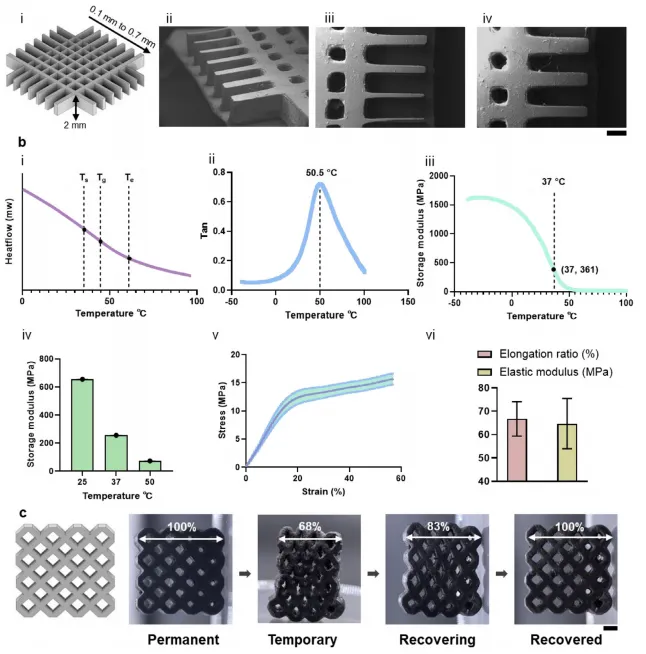
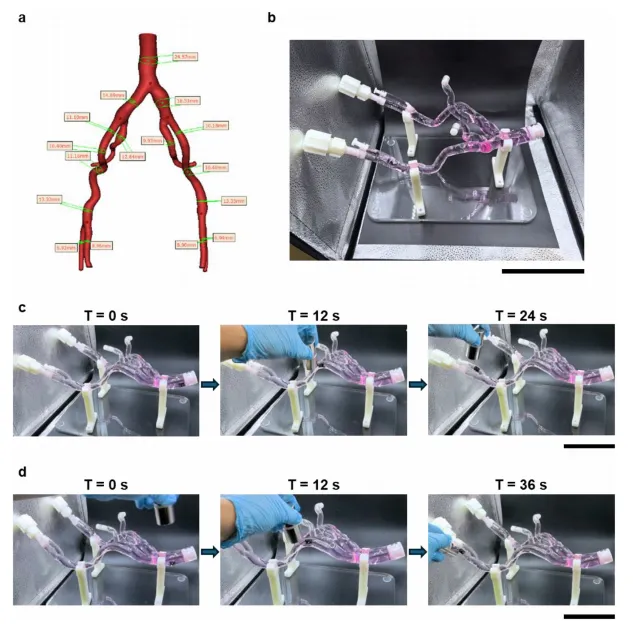
澳大利亚新南威尔士大学Cyrille Boyer、Rona Chandrawati团队报道了一种名为DSENO的可部署3D打印血管支架,它将形状记忆功能与表面催化产生内源性一氧化氮相结合。该支架采用高分辨率LCD 3D打印技术,通过优化含有Fe3O4纳米颗粒和多种交联剂的打印树脂,制备出一种具有可控玻璃化转变温度的复合材料。支架表面通过迈克尔加成反应修饰了聚乙烯亚胺,其胺基能够催化内源性S-亚硝基硫醇分解,持续产生一氧化氮。研究对材料的热机械性能、表面修饰、催化产生一氧化氮的能力、生物相容性、血液相容性、打印分辨率、形状记忆功能、磁控导航与近红外光热部署等进行了全面的表征与验证,并在体外血管模型中展示了其磁控导航、远程部署和支架功能。该工作以“Deployable 3D-Printed Vascular Stent with Surface-Catalysed Endogenous Nitric Oxide Generation”为题,发表在Advanced Materials期刊上。
文章亮点
-
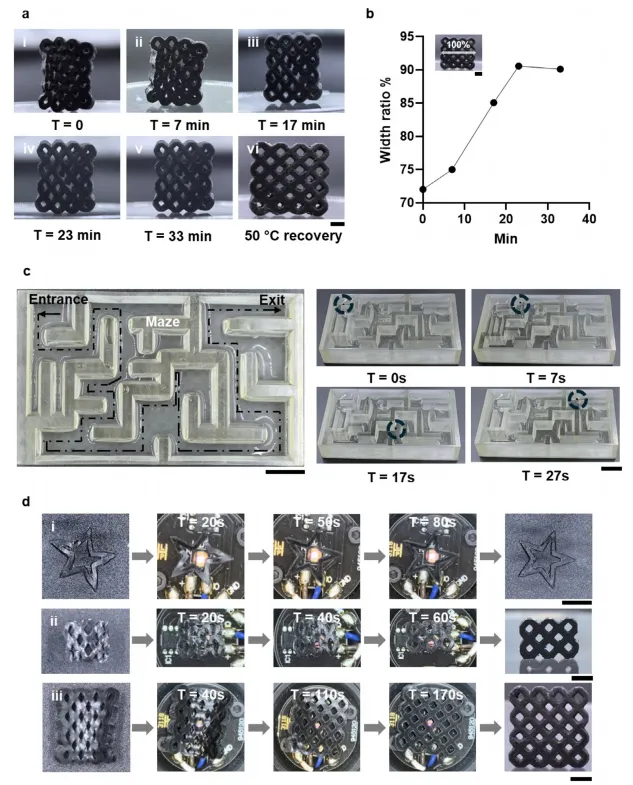
无导管远程部署:利用磁性Fe₃O₄和形状记忆聚合物,实现支架的磁控导航和NIR光热触发展开,避免球囊扩张带来的组织损伤。
-
内源性NO持续生成:表面PEI涂层催化血液中RSNO分解,实现NO的持续原位释放,克服药物洗脱支架药量有限的局限。
-
个性化3D打印设计:采用高分辨率LCD 3D打印,可定制支架结构,适应不同患者血管解剖结构,提升贴合度和临床适应性。
-
多材料协同优化:系统筛选树脂中TMTMP、TCMDA、TATATO和Fe₃O₄的比例,优化热力学性能、表面修饰效率和NO催化能力。
-
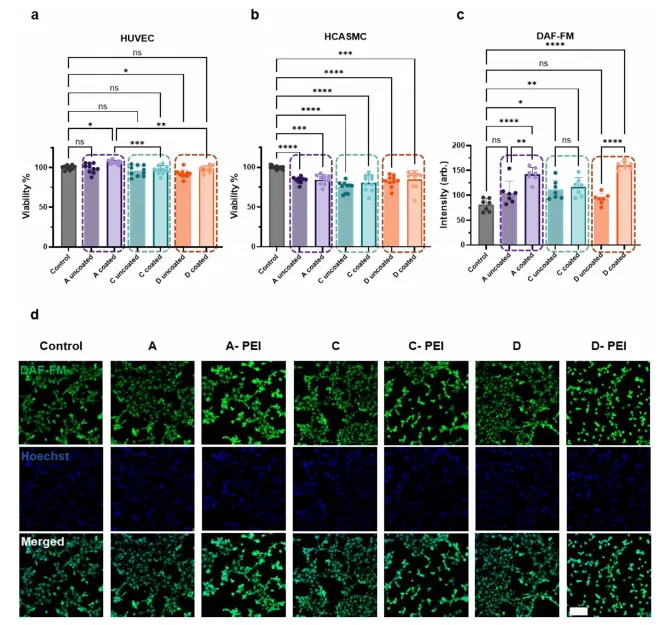
多维度功能验证:在细胞水平验证了其对内皮细胞的良好相容性和对平滑肌细胞的抑制作用;在体外血管模型中验证了磁控导航和光热展开的可行性。

K. Zhou, Z. Han, K. Lin, et. al., Deployable 3D-Printed Vascular Stent with Surface-Catalysed Endogenous Nitric Oxide Generation, Advanced Materials, 2026; 0:e20199. https://doi.org/10.1002/adma.202520199
 夜雨聆风
夜雨聆风




