【2026年南方台江苏专用教辅电子版化学培优word讲义高考特训16电解质溶液中粒子浓度大小比较

高考特训16 电解质溶液中粒子浓度大小比较
1. (2024·苏锡常镇二模)实验室用如下方案测定Na2CO3和NaHCO3混合物的组成:称取一定质量样品溶解于锥形瓶中,加入2滴指示剂M,用标准盐酸滴定至终点时消耗盐酸V1 mL;向锥形瓶中再加入2滴指示剂N,继续用标准盐酸滴定至终点,又消耗盐酸V2 mL。下列说法正确的是(D)
A.指示剂M、N可依次选用甲基橙、酚酞
B. 样品溶解后的溶液中:2c(Na+)=3c(CO2-3)+3c(HCO-3)+3c(H2CO3)
C. 滴定至第一次终点时的溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO-3)+2c(CO2-3)
D. 样品中Na2CO3和NaHCO3物质的量之比为V1V2-V1
【解析】 在滴定过程中,第一次到达滴定终点时,Na2CO3转化为NaHCO3,第二次达到滴定终点时NaHCO3转化为NaCl、H2O、CO2,故选择的指示剂M为酚酞、N为甲基橙,A错误;当Na2CO3和NaHCO3等物质的量混合时,根据元素守恒得2c(Na+)=3c(CO2-3)+3c(HCO-3)+3c(H2CO3),B错误;第一次到达滴定终点时,溶液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HCO-3)+2c(CO2-3)+c(Cl-),C错误;根据关系式:Na2CO3~HCl~NaHCO3,V1mL盐酸全部用于与Na2CO3反应,V2 mL 盐酸用于与所有 NaHCO3反应,故样品中Na2CO3和NaHCO3物质的量之比为V1V2-V1,D正确。
2. (2024·海安中学)室温下,向FeSO4溶液中加入足量氨水-NH4HCO3混合溶液,生成FeCO3沉淀。已知:Kb\rc\)(\a\vs4\al\co1(NH3·H2O)=1.8×10-5,Ka1\rc\)(\a\vs4\al\co1(H2CO3)=4.0×10-7,Ka2\rc\)(\a\vs4\al\co1(H2CO3)=5.0×10-11。下列说法正确的是(B)
A. 生成FeCO3的离子方程式:
Fe2++2HCO-3===FeCO3↓+CO2↑+H2O
B. 0.1 mol/L NH4HCO3溶液中:(pH=7.8):c\a\vs4\al\co1(NH\o\al(+4))>c\a\vs4\al\co1(HCO\o\al(-3))>c\rc\)(\a\vs4\al\co1(H2CO3)>c\rc\)(\a\vs4\al\co1(NH3·H2O)
C. 0.2 mol/L氨水和0.2 mol/L NH4HCO3溶液等体积混合:c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(NH3·H2O)=c\rc\)(\a\vs4\al\co1(H2CO3)+c\a\vs4\al\co1(HCO\o\al(-3))+c\a\vs4\al\co1(CO\o\al(2-3))
D. 生成FeCO3沉淀后的滤液中:c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(H+)=c\rc\)(\a\vs4\al\co1(OH-)+c\a\vs4\al\co1(HCO\o\al(-3))+2c\a\vs4\al\co1(CO\o\al(2-3))
【解析】 向FeSO4溶液中加入足量氨水-NH4HCO3混合溶液,生成FeCO3的离子方程式为Fe2++NH3·H2O+HCO-3===FeCO3↓+NH+4+H2O,A错误;0.1 mol/L NH4HCO3溶液的pH=7.8,说明HCO-3的水解程度大于NH+4的水解程度,故c\a\vs4\al\co1(NH\o\al(+4))>c\a\vs4\al\co1(HCO\o\al(-3))>c\rc\)(\a\vs4\al\co1(H2CO3)>c\rc\)(\a\vs4\al\co1(NH3·H2O),B正确;0.2 mol/L氨水和0.2 mol/L NH4HCO3溶液等体积混合,二者恰好发生反应,此时溶质为(NH4)2CO3,由元素守恒可得,c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(NH3·H2O)=2c\rc\)(\a\vs4\al\co1(H2CO3)+2c\a\vs4\al\co1(HCO\o\al(-3))+2c\a\vs4\al\co1(CO\o\al(2-3)),C错误;生成FeCO3沉淀后的滤液中还有SO2-4,存在电荷守恒:c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(H+)=c\rc\)(\a\vs4\al\co1(OH-)+c\a\vs4\al\co1(HCO\o\al(-3))+2c\a\vs4\al\co1(CO\o\al(2-3))+2c\a\vs4\al\co1(SO\o\al(2-4)),D错误。
3. (2023·海门中学)缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液里存在H2CO3-HCO-3缓冲体系,可使血液的pH稳定在7.4左右。当血液pH低于7.2或高于7.6时,会发生酸中毒或碱中毒。H2CO3-HCO-3缓冲体系的缓冲作用可用下列平衡表示:H+(aq)+HCO-3(aq)H2CO3(aq)CO2(g)+H2O(l)。实验室配制37 ℃时不同比例的NaHCO3-H2CO3缓冲溶液(已知:该温度下,H2CO3:pKa1≈6.1、pKa2≈10.3,101.3≈20)。
下列说法正确的是(C)
A. 人体发生碱中毒时注射NaHCO3溶液可以缓解症状
B. pH=7的缓冲体系中:
c(H2CO3)<c(HCO-3)<c(CO2-3)
C. pH=7.4的缓冲体系中:
c(HCO-3)∶c(H2CO3)≈20∶1
D. c(HCO-3)∶c(H2CO3)=1的缓冲体系中:
c(OH-)+2c(H2CO3)+2c(CO2-3)=c(Na+)+c(H+)
【解析】 NaHCO3溶液呈碱性,人体发生碱中毒时,可以注射酸性溶液缓解症状,A错误;c(H2CO3)<c(HCO-3)<c(CO2-3)的溶液不可能呈中性,B错误;pH=7.4的缓冲体系中,-3cH2CO3=-3cH2CO3×1cH+=Ka1cH+=10-6.110-7.4=101.3≈20,C正确;c(HCO-3)∶c(H2CO3)=1的缓冲体系中,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HCO-3)+2c(CO2-3)=c(OH-)+c(H2CO3)+2c(CO2-3),D错误。
4. (2024·无锡锡东高中)室温下,由二氧化锰与硫化锰矿(含Fe、Mg等杂质)制备MnSO4的流程如图所示。已知:Kb\rc\)(\a\vs4\al\co1(NH3·H2O)=1.80×10-5,Kal\rc\)(\a\vs4\al\co1(H2CO3)=4.30×10-7,Ka2\rc\)(\a\vs4\al\co1(H2CO3)=5.60×10-11,Ksp\rc\)(\a\vs4\al\co1(MnCO3)=2.24×10-11。下列说法不正确的是(D)
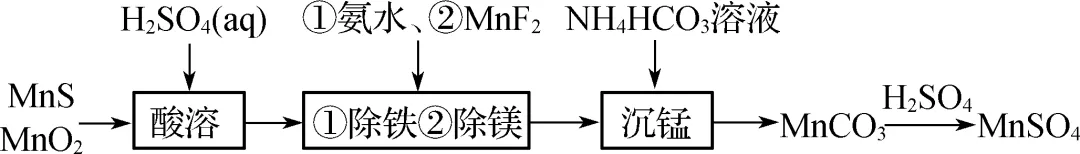
A. “酸溶”时的主要离子方程式:4MnO2+MnS+8H+===5Mn2++SO2-4+4H2O
B. 氨水中离子浓度:c\rc\)(\a\vs4\al\co1(OH-)=c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(H+)
C. “沉锰”后上层清液存在:
\rc\)(\a\vs4\al\co1(H+)\rc\\rc\)(\a\vs4\al\co1(Mn2+)=2.5
D. NH4HCO3溶液中:
c\a\vs4\al\co1(NH\o\al(+4))<2c\a\vs4\al\co1(CO\o\al(2-3))+c\a\vs4\al\co1(HCO\o\al(-3))
【解析】“酸溶”时离子方程式:4MnO2+MnS+8H+===5Mn2++SO2-4+4H2O,A正确;根据电荷守恒,氨水中存在:c\rc\)(\a\vs4\al\co1(OH-)=c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(H+),B正确;“沉锰”后上层清液中:\rc\)(\a\vs4\al\co1(H+)\rc\\rc\)(\a\vs4\al\co1(Mn2+)=\rc\)(\a\vs4\al\co1(H+))·c\b\lc\(\rc\3))\rc\\rc\)(\a\vs4\al\co1(Mn2+))·c\b\lc\(\rc\3))=\rc\)(\a\vs4\al\co1(H2CO3))Ksp\b\lc\(\rc\)(\a\vs4\al\co1(MnCO3))=2.5,C正确;NH4HCO3溶液中存在电荷守恒:c\a\vs4\al\co1(NH\o\al(+4))+c\rc\)(\a\vs4\al\co1(H+)=2c\a\vs4\al\co1(CO\o\al(2-3))+c\a\vs4\al\co1(HCO\o\al(-3))+c\rc\)(\a\vs4\al\co1(OH-),Kb\rc\)(\a\vs4\al\co1(NH3·H2O)>Kal\rc\)(\a\vs4\al\co1(H2CO3),NH+4水解程度小于HCO-3水解程度,溶液呈碱性,c\rc\)(\a\vs4\al\co1(H+)<c\rc\)(\a\vs4\al\co1(OH-),故c\a\vs4\al\co1(NH\o\al(+4))>2c\a\vs4\al\co1(CO\o\al(2-3))+c\a\vs4\al\co1(HCO\o\al(-3)),D错误。
5. (2024·扬州)硫代硫酸钠(Na2S2O3)的制备和应用相关流程如图所示。已知:25 ℃时,H2SO3的Ka1=1.4×10-2,Ka2=6.0×10-8;H2CO3的Ka1=4.5×10-7,Ka2=5.0×10-11。
下列说法正确的是(A)
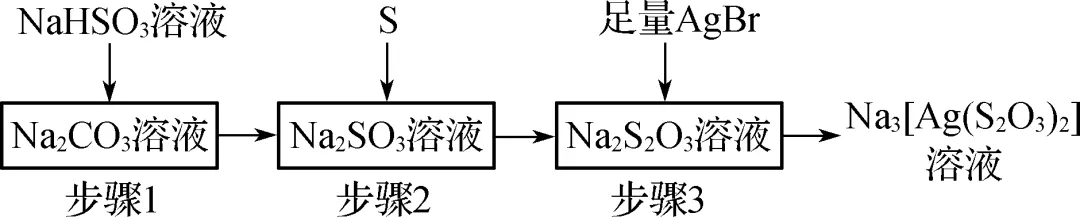
A. 步骤1过程中pH=8时,c\a\vs4\al\co1(SO\o\al(2-3))·c(CO2-3)=0.03c\a\vs4\al\co1(HSO\o\al(-3))·c\a\vs4\al\co1(HCO\o\al(-3))
B. 步骤1所得的溶液中:c\rc\)(\a\vs4\al\co1(Na+)=2[c(H2SO3)+c(HSO-3)+c(SO2-3)]
C. 步骤3所得的清液中:
c\rc\)(\a\vs4\al\co1(Ag+)·c\rc\)(\a\vs4\al\co1(Br-)>Ksp\rc\)(\a\vs4\al\co1(AgBr)
D. 步骤3的离子方程式为
Ag++2S2O2-3===\a\vs4\al\co1(Ag\b\lc\(\rc\)(\a\vs4\al\co1(S2O3))2)3-
【解析】Ka2(H2SO3)·Ka2(H2CO3)=2-2-3--3=3×10-18,pH=8,c(H+)=10-8,故c(SO2-3)·c(CO2-3)=3×10-1810-16·c(HSO-3)·c(HCO-3)=0.03c(HSO-3)·c(HCO-3),A正确;步骤1中,Na2CO3溶液与NaHSO3溶液反应生成亚硫酸钠和碳酸氢钠,根据元素守恒,钠离子的浓度应大于2倍的含硫微粒浓度之和,B错误;步骤3所得是清液中,c\rc\)(\a\vs4\al\co1(Ag+)·c\rc\)(\a\vs4\al\co1(Br-)≤Ksp(AgBr),C错误;步骤3的离子方程式为AgBr+2S2O2-3===\a\vs4\al\co1(Ag\b\lc\(\rc\)(\a\vs4\al\co1(S2O3))2)3-+Br-,D错误。
6. (2024·南通市联考)H2C2O4为二元弱酸。20 ℃时,配制一组c(H2C2O4)+c(HC2O-4)+c(C2O2-4)=0.100 mol/L的H2C2O4和NaOH混合溶液,溶液中部分粒子的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中粒子的物质的量浓度关系一定正确的是(B)
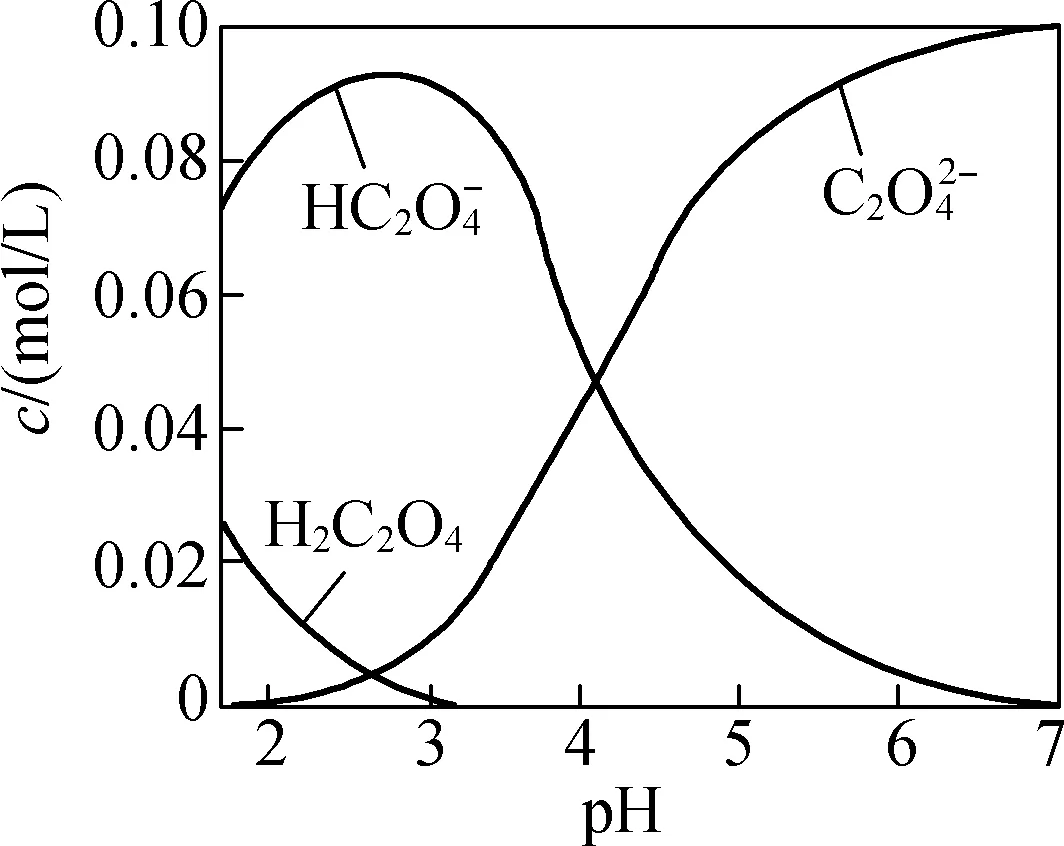
A. pH=2.5的溶液中:
c(H2C2O4)+c(C2O2-4)>c(HC2O-4)
B. c(Na+)=0.100 mol/L的溶液中:
c(H+)+c(H2C2O4)=c(OH-)+c(C2O2-4)
C. c(HC2O-4)=c(C2O2-4)的溶液中:
c(Na+)>0.100 mol/L+c(HC2O-4)
D. pH=7的溶液中:c(Na+)< 2c(C2O2-4)
【解析】由图可知,pH=2.5的溶液中c(H2C2O4)和c(C2O2-4)浓度之和小于c(HC2O-4),则c(H2C2O4)+c(C2O2-4)<c(HC2O-4),A错误;c(Na+)=0.100 mol/L溶液为NaHC2O4溶液,溶液中存在质子守恒:c(H+)+c(H2C2O4)=c(OH-)+c(C2O2-4),B正确;c(HC2O-4)=c(C2O2-4)的溶液中,pH约为4,溶液存在电荷守恒:
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




