【2026年南方台江苏专用教辅电子版化学培优word讲义第26讲化学工艺流程(选择题)

第26讲 化学工艺流程(选择题)
1. (2023·常熟中学一调)以含钴废渣(主要成分为CoO和Co2O3,含少量Al2O3和ZnO)为原料制备CoCO3的工艺流程如图所示。下列说法正确的是(C)
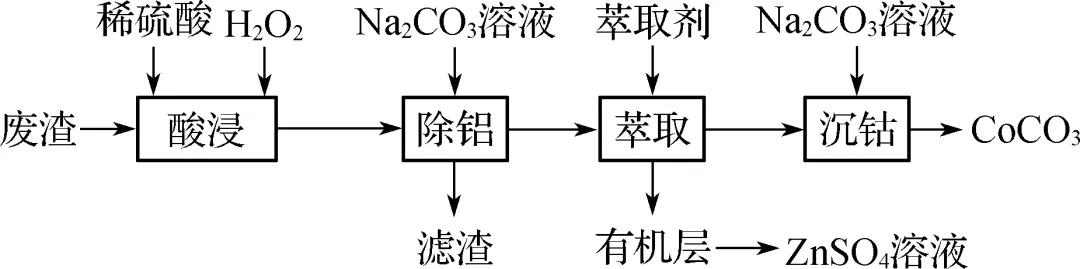
A.酸浸时可采用高温提高酸浸速率
B. 除铝时加入Na2CO3溶液过滤后所得滤渣是Al2(CO3)3
C. 萃取时萃取剂总量一定,分多次加入萃取比一次加入萃取效果更好
D. 沉钴时将含Co2+的溶液缓慢滴加到Na2CO3溶液中,可提高CoCO3的产率
【解析】 温度过高,H2O2分解,不利于提高酸浸速率,A错误;除铝时加入Na2CO3溶液过滤后所得滤渣是Al(OH)3,B错误;萃取过程中,多次萃取能使萃取效率提高,C正确;将含Co2+的溶液缓慢滴加到Na2CO3溶液中,可能生成Co(OH)2沉淀,降低CoCO3的产率,D错误。
2. (2023·泰州、宿迁、宜兴中学)某研究小组利用BaS的还原性提纯HBr并制取MgBr2的方案如图所示。下列说法错误的是(B)
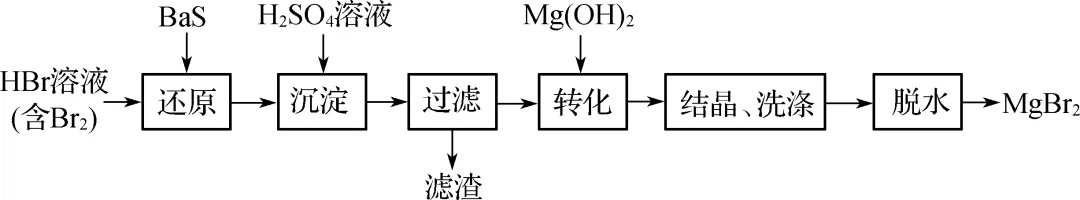
A.“沉淀”步骤中不可使用Na2SO4溶液代替硫酸
B. 滤渣中只有BaSO4
C. “转化”步骤中发生反应的离子方程式为Mg(OH)2+2H+===Mg2++2H2O
D. 将MgBr2·6H2O晶体在溴化氢气氛中加热得到MgBr2固体
【解析】“沉淀”步骤中若使用Na2SO4溶液代替硫酸,则得到的滤液中主要成分为NaBr,NaBr与Mg(OH)2不反应,A正确;滤渣的主要成分是BaSO4和S,B错误;“转化”步骤的离子方程式为Mg(OH)2+2H+===Mg2++2H2O,C正确; MgBr2水解生成的HBr挥发,加热促进水解,将MgBr2·6H2O直接加热得不到MgBr2固体,需要在HBr的气流中加热脱水才能得到MgBr2固体,D正确。
3. (2024·如皋中学二检)黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe2O3)生产硝酸铜溶液的流程如图所示。下列说法错误的是(C)
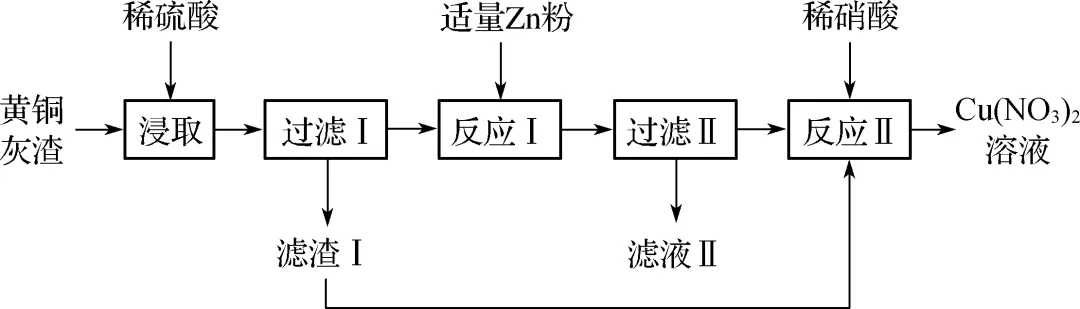
A.“浸取”时适当提高硫酸浓度可加快反应速率,但不宜过量太多
B. 若反应中所加Zn过量,所得Cu(NO3)2溶液中含Zn(NO3)2
C. 滤液Ⅱ含Zn2+、Fe2+、Fe3+、SO2-4等离子
D. 反应Ⅱ会产生NO污染环境,可将滤渣灼烧后再加稀硝酸
【解析】 反应Ⅰ处加入Zn粉,若前面加入的H2SO4过量,则会消耗更多的Zn,A正确;若Zn过量,滤渣中有Cu和Zn,加入稀硝酸,Cu和Zn均可以被溶解,生成Cu(NO3)2和Zn(NO3)2,B正确;Fe3+的氧化性强于Cu2+,Zn与Cu2+反应前,必然将Fe3+还原为Fe2+,所以滤液Ⅱ中不存在Fe3+,C错误;稀硝酸与金属产生NO,滤渣为Cu,先灼烧生成CuO,再溶于稀硝酸,不会产生NO,D正确。
4. (2023·东台中学)工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰\rc\)(\a\vs4\al\co1(MnCO3),其工业流程如图。下列说法错误的是(D)
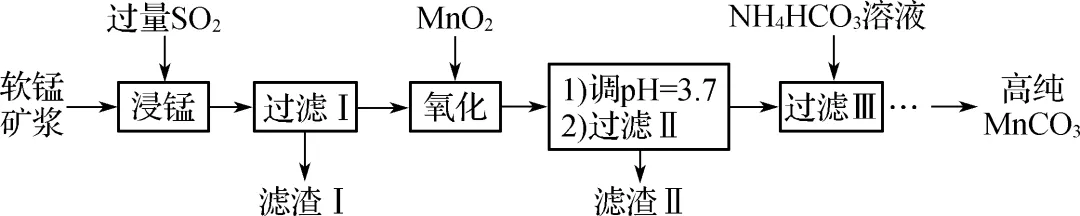
A.“浸锰”过程中Fe2O3与SO2反应的离子方程式为Fe2O3+SO2+2H+===2Fe2++SO2-4+H2O
B. “过滤Ⅰ”所得滤液中主要存在的金属阳离子为Mn2+和Fe2+
C. “滤渣Ⅱ”的主要成分含有Fe(OH)3
D. 向“过滤Ⅱ”所得的滤液中加入NH4HCO3溶液发生反应的主要离子方程式为Mn2++ CO2-3===MnCO3↓
【解析】“浸锰”过程通入过量SO2,将Mn(Ⅳ)和Fe(Ⅲ)还原成Mn2+和Fe2+,Fe2O3与SO2反应离子方程式为Fe2O3+SO2+2H+===2Fe2++SO2-4+H2O,A、B正确;调节pH=3.7,MnO2将Fe2+氧化为Fe(OH)3,C正确;滤液为MnSO4溶液,加入NH4HCO3溶液反应的离子方程式为Mn2++2HCO-3===MnCO3↓+CO2↑+H2O,D错误。
5. (2023·高邮调研)工业上采取合理的方法可以将SO2转化为硫酸钾等有用的物质,其一种转化路线如图所示。下列说法正确的是(C)
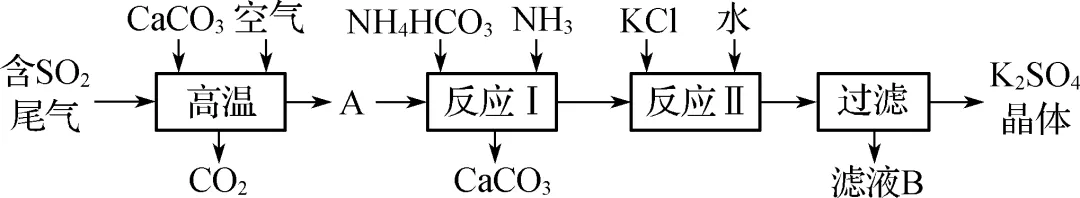
A.通入空气的主要目的是搅拌
B. 过程中发生的都是非氧化还原反应
C. “反应Ⅱ”的化学方程式为\rc\)(\a\vs4\al\co1(NH4)2SO4+2KCl===K2SO4↓+2NH4Cl
D. 滤液B中含有的主要离子是NH+4、K+、SO2-4
【解析】 通入空气的主要目的是将SO2氧化为SO2-4,A错误;CaCO3、SO2和空气高温焙烧生成CaSO4和CO2,该过程是氧化还原反应,B错误;反应Ⅱ中\rc\)(\a\vs4\al\co1(NH4)2SO4和KCl反应生成K2SO4沉淀和NH4Cl,C正确;滤液B主要含有NH+4、Cl-,D错误。
6. (2023·海安中学)高氯酸铵(NH4ClO4)受热或撞击可分解成N2、Cl2、O2和H2O,可用作火箭推进剂。一种以工业NaClO3(含少量的Na2Cr2O7和Na2CrO4)溶液制取高氯酸铵的流程如下,电解时使用惰性电极,电解后溶液中有NaClO4生成。
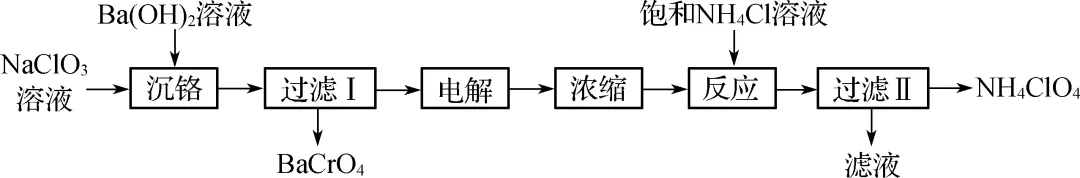
关于制取高氯酸铵的反应,下列说法正确的是(C)
A.沉铬时加入Ba\rc\)(\a\vs4\al\co1(OH)2有利于CrO2-4转化为Cr2O2-7
B. 电解时阴极电极反应式为
ClO-3+2e-+2OH-===ClO-4+H2O
C. 加入饱和NH4Cl溶液反应时可能有NH3生成
D. NaClO4、NH4Cl、NH4ClO4三种物质中,NH4ClO4溶解度最大
【解析】 Cr2O2-7+H2O2CrO2-4+2H+,沉铬时加入Ba\rc\)(\a\vs4\al\co1(OH)2有利于Cr2O2-7转化为CrO2-4,CrO2-4和Ba2+结合生成BaCrO4沉淀,A错误;电解时ClO-3在阳极发生失电子的氧化反应生成ClO-4,B错误;电解生成氢氧化钠,加入饱和NH4Cl溶液会生成氨气,C正确;NaClO4、NH4Cl、NH4ClO4三种物质中,NH4ClO4溶解度最小,D错误。
7. (2023·海门期末)锑(Sb)可用作阻燃剂、电极材料、催化剂等物质的原材料。一种以辉锑矿(主要成分为Sb2S3,还有Fe2O3、Al2O3、MgO等)为原料提取锑的工艺如下:
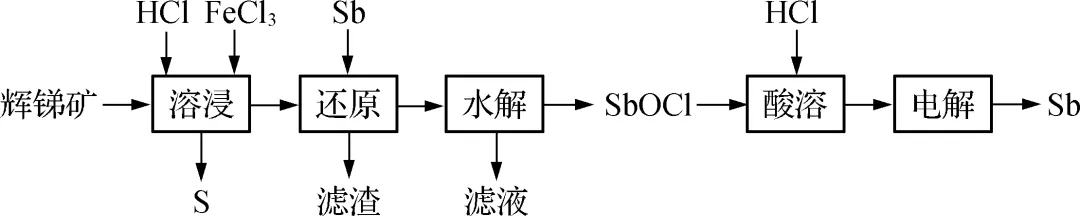
下列说法不正确的是(D)
A. “水解”时可加入Na2CO3粉末以促进水解
B. “还原”的目的是防止Fe3+在后续水解生成Fe(OH)3,影响产品纯度
C. “滤液”中含有的主要金属阳离子有:
Fe2+、Al3+、Mg2+
D. “溶浸”时Sb2S3转化为SbCl3,离子方程式为Sb2S3+Fe3++6Cl-===2SbCl3+Fe2++3S
【解析】 Sb3+发生水解的离子方程式为Sb3++Cl-+H2OSbOCl+2H+,可加入Na2CO3粉末促进Sb3+水解,A正确;辉锑矿中加入盐酸、FeCl3溶液“溶浸”,加入Sb,Sb将Fe3+还原为Fe2+,目的是防止Fe3+在后续水解生成Fe(OH) 3,B正确;“滤液”中含有的主要金属阳离子有Fe2+、Al3+、Mg2+,C正确;“溶浸”时,Sb3+需要进入溶液中,说明SbCl3可溶于水,书写离子方程式时,SbCl3需要拆分为离子形式,D错误。
8. (2023·南菁中学期初)工业上以硫酸泥(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)为原料提取硒,流程如图所示。下列说法错误的是(C)
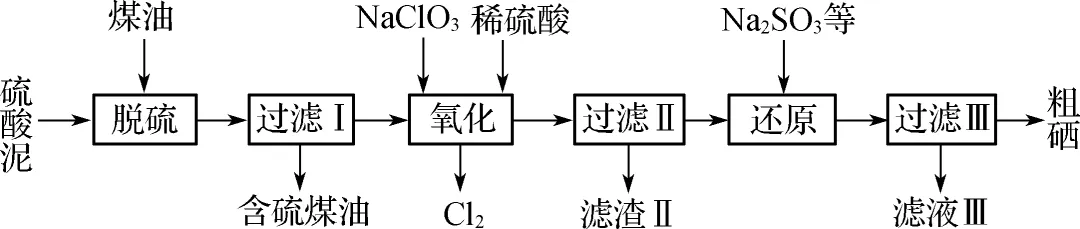
A.脱硫过程中,利用了相似相溶原理
B. 氧化过程中,Se转化为H2SeO3的反应中氧化剂和还原剂的物质的量之比为4∶5
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




