【2026版高考总复习红与勾讲与练化学电子版第四章 第16讲铜及其化合物金属材料及金属的冶炼

1.了解铜单质及其重要化合物的性质、用途、制备原理及过程。2.了解合金的概念及金属材料的重要应用。3.能根据金属的活动性顺序选择合适的冶炼方法。
考点一 铜及其化合物

1.熟记铜及其常见化合物的颜色
|
物质 |
颜色 |
物质 |
颜色 |
|
Cu |
紫红色 |
CuSO4 |
白色 |
|
CuO |
黑色 |
CuSO4·5H2O |
蓝色 |
|
Cu2O |
砖红色 |
Cu2(OH)2CO3 |
绿色 |
|
Cu2S |
黑色 |
Cu(OH)2 |
蓝色 |
2.铜及其重要化合物的性质及应用
(1)铜在潮湿的空气中生成铜锈[Cu2(OH)2CO3]:2Cu+O2+CO2+H2O===Cu2(OH)2CO3(填化学方程式)。
(2)常用灼热的铜粉除去N2中的O2,用灼热的CuO除去CO2中的CO。
(3)新制的Cu(OH)2常用来检验醛基。
(4)无水CuSO4遇水蒸气变为蓝色晶体(CuSO4·5H2O),可用于检验H2O。
(5)过量的Cu和浓硝酸反应,得到NO2和NO的混合气体,再加入稀硫酸,Cu继续溶解。
(6)Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2O,此反应中当Cu过量时,H2SO4也不能完全反应。此反应不适用于制备CuSO4,因为会产生污染性气体SO2且H2SO4的利用率低。
(7)Cu+的性质
①+1价铜有较强的还原性,易被氧化剂氧化为+2价。
②+1价铜在酸性条件下,易发生歧化反应生成Cu和Cu2+,如Cu2O加入稀硫酸的离子方程式:Cu2O+2H+===Cu+Cu2++H2O。
 “√”,错误的打“×”。
“√”,错误的打“×”。
(1)将铜片置于干燥的空气中,不易被腐蚀。(√ )
(2)CuO是金属氧化物,与水反应生成Cu(OH)2。(× )
(3)CuSO4·5H2O失去结晶水属于物理变化。(× )
(4)铜锈是铜被空气中的氧气缓慢氧化生成的氧化物。(× )
(5)过量的铜与浓硝酸反应一定没有一氧化氮生成。(× )

题组一 铜及其化合物的性质和应用
1.某研究小组通过实验探究Cu及其重要化合物的性质,下列操作正确且能达到目的的是( D )
A.将铜丝插入浓硫酸中加热,反应完后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿的铜器放入稀盐酸中浸泡,除去铜绿
解析:A项,应将反应后的液体倒入盛水的烧杯中,并不断搅拌,不符合题意;B项,应将铜丝在空气中加热到红热后伸入盛满氯气的集气瓶中,不符合题意;C项,CuCl2水解生成的盐酸易挥发,加热蒸干CuCl2溶液得不到无水CuCl2固体,不符合题意。
2.(2024·江西赣州二十三校高三期中联考)铜元素的“价—类”二维图如图,下列有关说法正确的是( C )
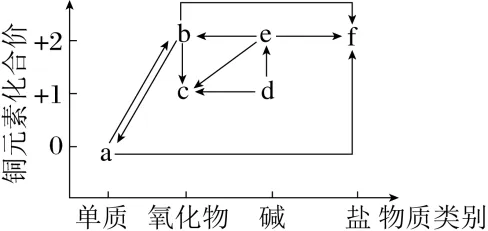
A.a可直接转化为e
B.b转化为c一定需要另加还原剂
C.新制的e可用于检验葡萄糖中的醛基
D.直接加热f溶液一定可得到f固体
解析:由题图元素化合价和物质类别可推出:a为Cu,b为CuO,c为Cu2O,d为CuOH,e为Cu(OH)2,f为可溶性铜盐。Cu不可一步转化成Cu(OH)2,A错误;CuO加热条件下自身可分解为Cu2O,B错误;新制的Cu(OH)2可用于检验葡萄糖中的醛基,C正确;Cu2+会发生水解反应,加热CuCl2溶液时得不到CuCl2固体,D错误。
题组二 铜的重要化合物的制备
3.用CuCl2·2H2O制取无水CuCl2的实验装置如图所示。下列说法错误的是( D )
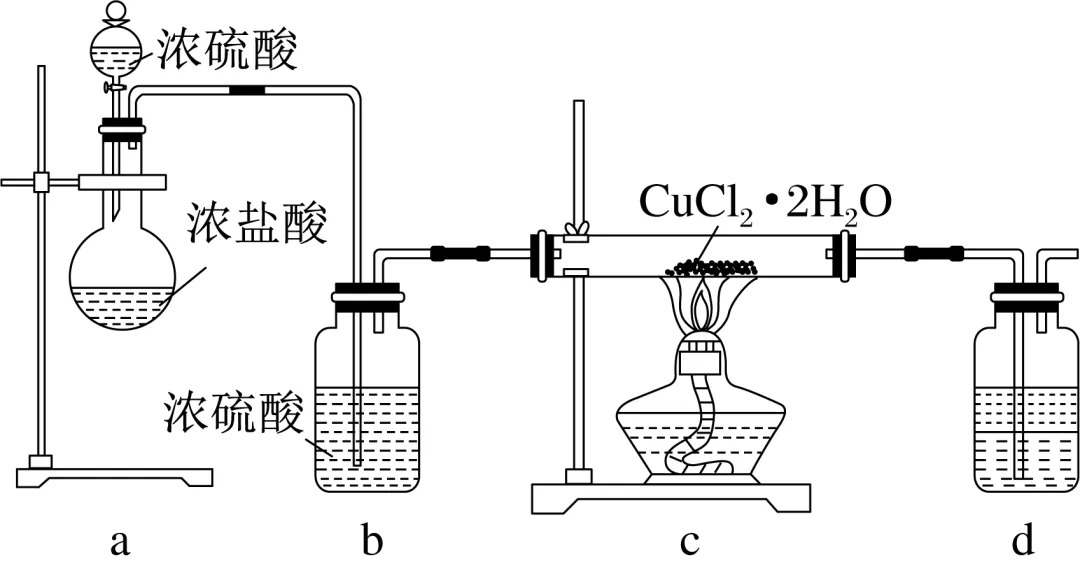
A.通入HCl可以抑制CuCl2的水解
B.先滴入浓硫酸,再点燃c处酒精灯
C.硬质玻璃管内部右侧会出现白雾
D.装置d中上层为苯,下层为NaOH溶液
解析:氯化铜水解反应为CuCl2+2H2O⥫⥬Cu(OH)2+2HCl,生成的HCl易挥发,通入HCl可以抑制CuCl2的水解,A正确;CuCl2·2H2O加热失去结晶水必须在HCl的气流中进行,所以先滴入浓硫酸产生HCl气体,使硬质玻璃管中充满HCl气体后再点燃c处酒精灯,B正确;硬质玻璃管内部右侧有生成的水蒸气和通入的HCl,由于HCl极易溶于水,会产生白雾,C正确;HCl极易溶于水,为了防止倒吸,d中下层应为有机溶剂,可以是四氯化碳,上层为氢氧化钠溶液,D错误。
4.(2024·安徽池州高三期末)用低品铜矿(主要含CuS、FeS)制备Cu2O的一种工艺流程如下:
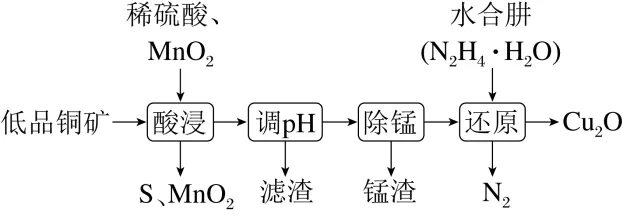
下列说法正确的是( C )
A.“酸浸”过程中FeS发生反应的离子方程式为S2-+4H++MnO2===Mn2++S+2H2O
B.“调pH”的目的是除去溶液中的Fe2+
C.使用Na2CO3溶液“除锰”时,锰渣中可能会含有少量Mn(OH)2
D.“还原”过程中参与反应的氧化剂和还原剂的物质的量之比为2∶1
解析:低品铜矿(主要含CuS、FeS)与稀硫酸、二氧化锰反应生成硫单质、硫酸铜、硫酸锰、硫酸铁等,调节溶液的pH,过滤后,向滤液中加入除锰的物质,再向溶液中加入水合肼得到氧化亚铜。FeS固体难溶于水不能拆成离子形式,2FeS+12H++3MnO2===2Fe3++2S+6H2O+3Mn2+,A项错误;“调pH”的目的是除去溶液中的Fe3+,B项错误;CO2-3和Mn2+相互促进水解,生成少量Mn(OH)2,C项正确;水合肼中氮元素为-2价,最后变为0
通过网盘分享的文件:2026红对勾讲与练高三政治等9个文件
链接: https://pan.baidu.com/s/1PV9jm4aYOjX-uWLS9hJnUw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风





