【2026版高考总复习红与勾讲与练化学电子版第七章第32讲化学反应的热效应

第32讲 化学反应的热效应
1.知道常见的吸热反应和放热反应,能解释化学反应中能量变化的本质。2.能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应。3.了解中和反应反应热测定的原理及操作,了解燃烧热的含义和能源及能源利用的意义。4.了解盖斯定律及其简单应用,能进行反应焓变的简单计算。
考点一 焓变 热化学方程式

1.反应热 焓变
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境吸收的热量。
(2)焓变
①焓(H):焓是与内能有关的物理量。
②焓变(ΔH):生成物的焓与反应物的焓之差。
③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,用符号ΔH表示,常用单位:kJ·mol-1(或kJ/mol)。
2.吸热反应和放热反应
(1)常见的吸热反应和放热反应

(2)理解吸热、放热反应的两个角度
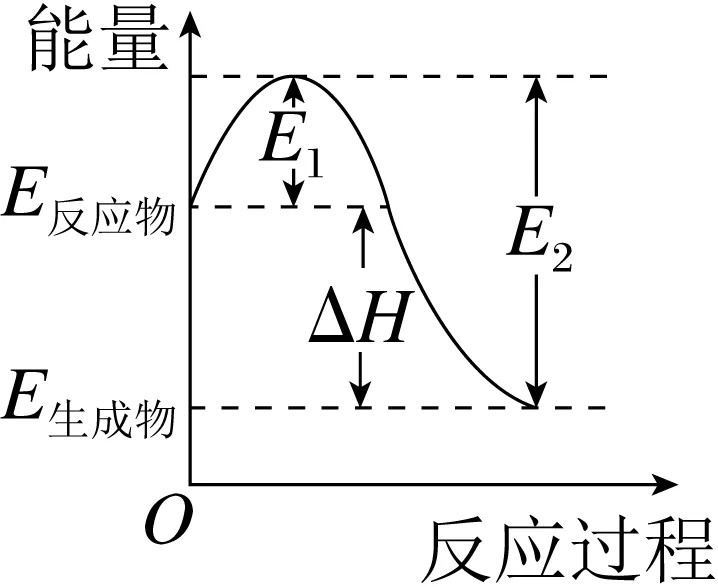
①从反应过程能量图理解
|
项目 |
放热反应(ΔH<0) |
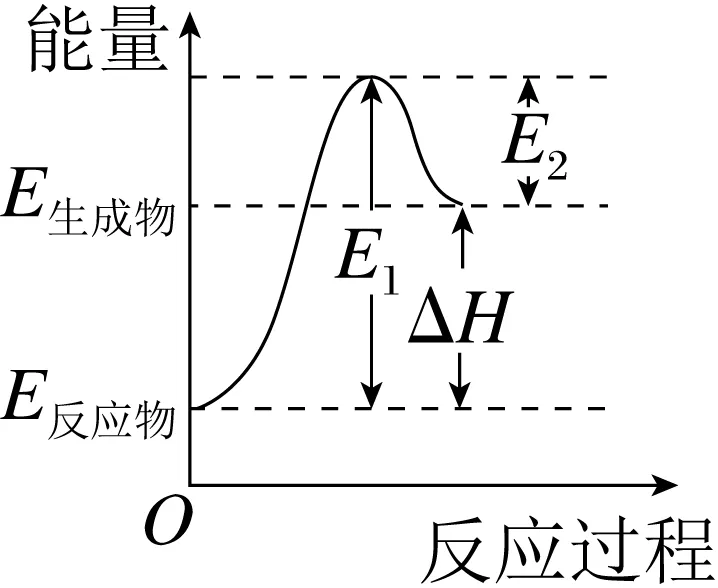
吸热反应(ΔH>0) |
|
图示 |
|
|
|
解释与 说明 |
①E1代表反应物断键吸收的能量,即反应物的键能之和。过渡态理论认为E1为正反应的活化能 ②E2代表形成化学键时释放的能量,即生成物的键能之和。过渡态理论认为E2为逆反应的活化能 ③ΔH为该反应过程的反应热 ΔH=∑E(生成物)-∑E(反应物) ΔH=反应物的总键能-生成物的总键能 ΔH=E(正反应活化能)-E(逆反应活化能) |
②从化学键角度理解
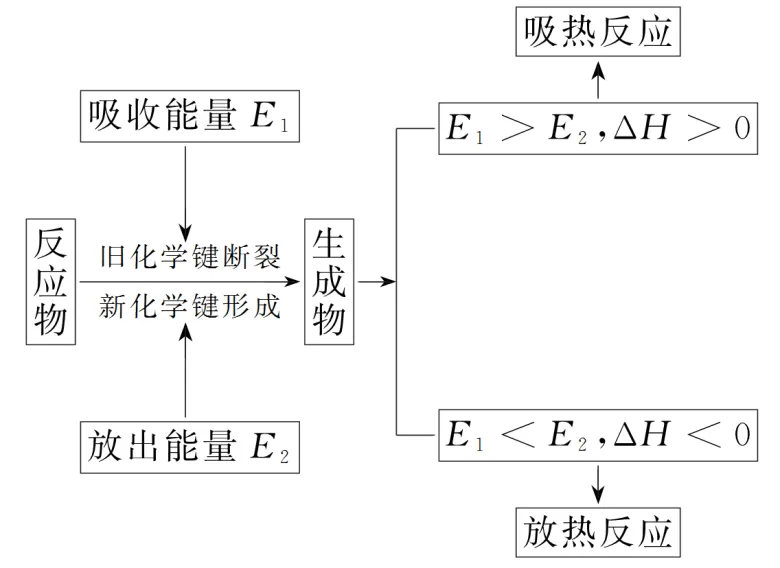
3.热化学方程式
(1)概念:表明反应所释放或吸收的热量的化学方程式。
(2)意义:不仅表明了化学反应中的物质变化,也表明了化学反应中的能量变化。
(3)热化学方程式的书写步骤及要求


正确的打“√”,错误的打“×”。
(1)反应体系的焓就是体系的内能。(×)
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应。(×)
(3)石墨转变为金刚石是吸热反应,则金刚石比石墨更稳定。(×)
(4)吸热反应中,反应物总能量高于生成物总能量。(×)
(5)可逆反应的ΔH表示发生了反应的那部分的热量变化。(×)
(6)活化能越大,表明化学反应吸收的能量越多。(×)

题组一 反应热与能量变化示意图
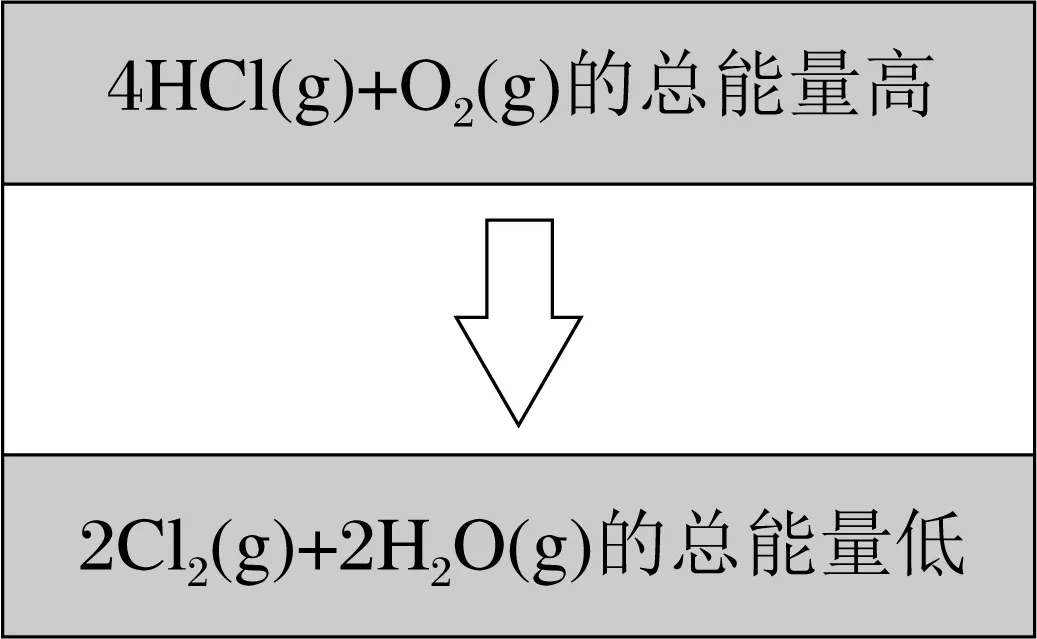
1.(2025·河南三门峡高三月考)1868年狄青和洪特发现了用空气中的氧气来氧化氯化氢气体制取氯气的方法:4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)。化学反应与能量变化如图所示。下列说法正确的是( C )
A.该反应为吸热反应
B.若H2O为液态,则生成物总能量将变大
C.4HCl(g)和O2(g)总能量高于2Cl2(g)+2H2O(g)的总能量,反应时向环境释放能量
D.断开旧化学键吸收的总能量大于形成新化学键所释放的总能量
解析:据题图可知,4HCl(g)+O2(g)的总能量高于2Cl2(g)+2H2O(g)的总能量,反应为放
通过网盘分享的文件:2026红对勾讲与练高三政治等9个文件
链接: https://pan.baidu.com/s/1PV9jm4aYOjX-uWLS9hJnUw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风