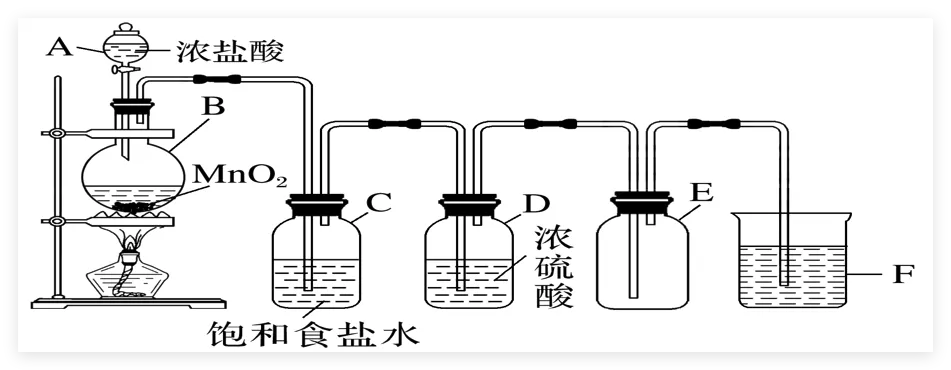

Cl2在水中存在以下两个重要平衡:
(I)Cl2 + H2O = H+ + Cl- + HClO K1(298K)=4.2 ×10-4
(II)Cl2 + Cl- = Cl3- K2(298K)=0.19
反应II对我们来说是陌生的,不过可以类比I2+I- =I3-进行理解。
在氯水中,反应I进行的程度小,生成的Cl-浓度低,导致反应II的发生速率很慢,因此在氯水中,反应I为主要平衡。
而在NaCl溶液中,Cl-浓度较大,会使反应II成为主要平衡。换句话说,Cl-浓度越大,Cl2溶解度越大!事实果真如此吗?让我们来看数据:
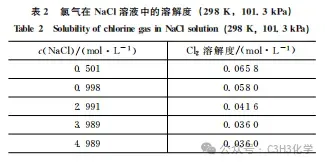
显然,随着c(NaCl)的增大,Cl2的溶解度是减小的。
这是为什么呢?
一种可能的解释是:有另一种“力量”抵消掉了反应II对Cl2溶解度的增大效应!
分别取0.3 mol/L、0.6 mol/L、0.9 mol/L 的Na2SO4溶液和NaCl溶液,通入Cl2对比溶解度,得到如下曲线:
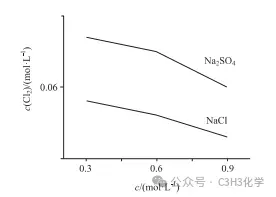
随着两种溶液浓度的增大,Cl2的溶解度都在减小。对于Na2SO4溶液来说,要么是Na+在抑制Cl2的溶解,要么是SO42-在抑制Cl2的溶解。同理,对于NaCl溶液来说,一方面,也能推断出Na+或者Cl-在抑制Cl2的溶解;另一方面,Cl2被Cl-结合而促进溶解的趋势也不能被忽视。
再分析。等浓度的Na2SO4溶液要比NaCl溶液溶解更多Cl2,说明SO42-对Cl2溶解的抑制能力弱于Cl-对Cl2溶解的抑制能力,并在Na2SO4溶液中,Na+对Cl2的溶解有抑制用。
这样,另一种“抵消”Cl2与Cl-发生反应II的溶解效应的“力量”,就找到了。
它是Na+对Cl2溶解的抑制作用!按照高中化学物质结构的理论,可以解释这种“抑制”作用-----盐析效应。Na+结合了水分子,使得水分子变成了囚中之兽,难以用范德华力束缚住Cl2,从而减弱Cl2的溶解性。
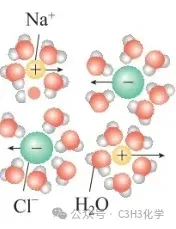
所以,Cl2在饱和食盐水中溶解性较差的原因:Na+对Cl2的盐析效应与Cl-借助反应I逆向移动平衡的“协同作用”。在教学中,没有必要引入Cl2与Cl-生成Cl3-的陌生反应,也没有必要正式给学生介绍何谓“盐析效应”,在适当的教学时机,拓展思考Na+对Cl2与H2O分子间作用力的影响,也能起到发展学生认知的教学效果。
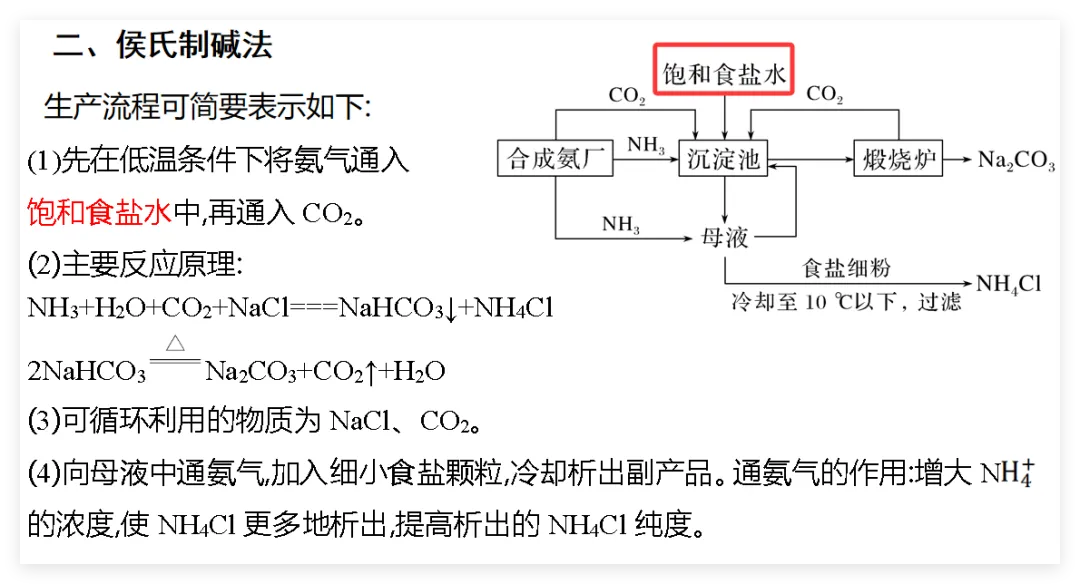

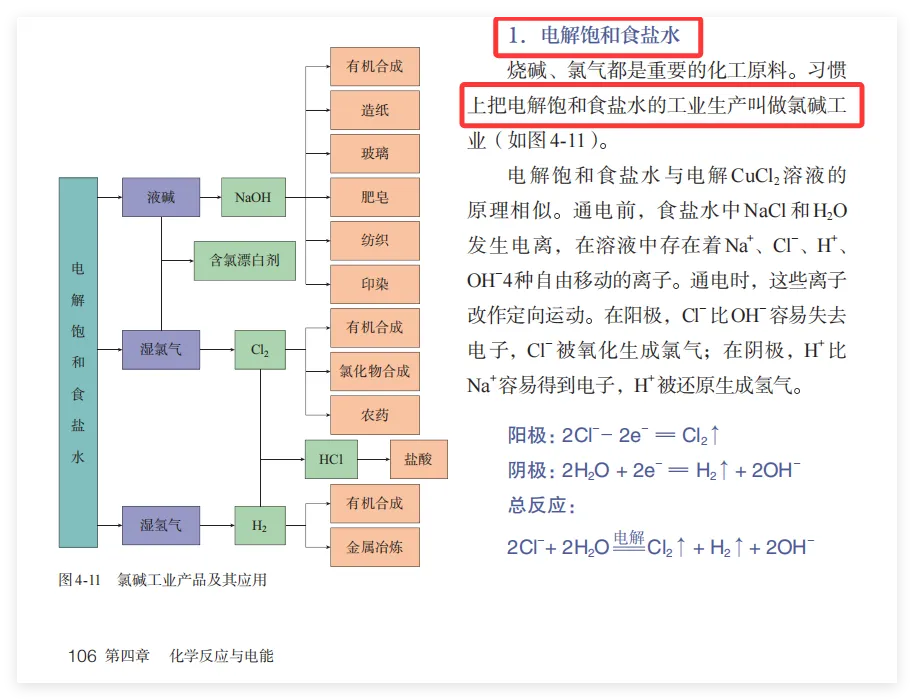
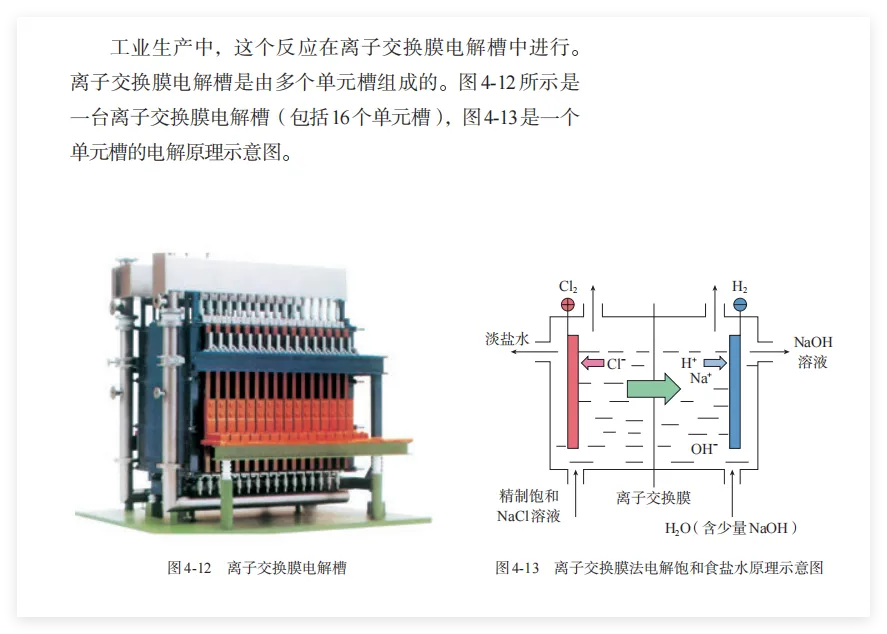
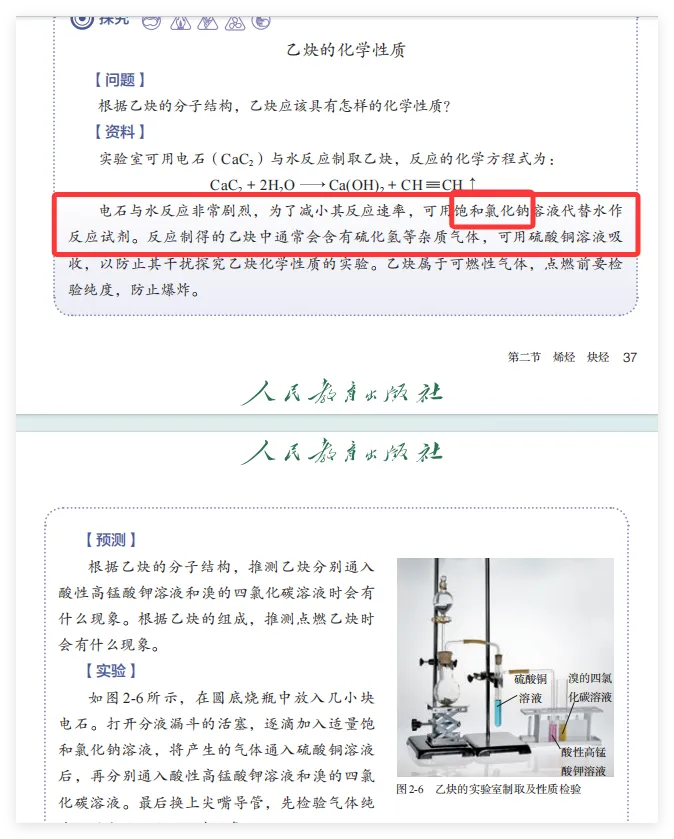

其次,有时候用纯水萃取会产生乳化现象而导致无法分层,而饱和食盐水由于渗透压大,难以产生乳化现象;
最后,由于饱和食盐水的渗透压大,可以将有机相中的一部分水分带走,利于之后的干燥处理。

3.将盛有混合物的蒸发皿冷却。稍待片刻,向混合物中加入20ml 热蒸馏水(用250ml烧杯中的热水即可),再冷却,然后加入25ml饱和食盐水,充分搅拌,观察现象。

我用夸克网盘分享了「饱和食盐水在实验中的不同作用(七大经典实验应用).pdf」,链接:https://pan.quark.cn/s/32f10a223c10用…………………………………………………………
免责声明:所载内容来源于互联网,微信公众号等公开渠道,我们对文中观点持中立态度,本文仅供参考、交流。转载的稿件版权归原作者和机构所有
我用夸克网盘分享了「饱和食盐水在实验中的不同作用(七大经典实验应用).pdf」,链接:https://pan.quark.cn/s/32f10a223c10用…………………………………………………………
免责声明:所载内容来源于互联网,微信公众号等公开渠道,我们对文中观点持中立态度,本文仅供参考、交流。转载的稿件版权归原作者和机构所有
★①扫描以下二维码,关注“高中化学徐老师”微信公众号; ★②点亮文末在看(此项务必完成)
分享是一种美德,随手转发到朋友圈,让更多人受益!
★③在公众号右上角,点“发消息”,可在对话框输入今日关键词:
【饱和食盐水七大应用】
若喜欢本文,敬请转发
免责声明
[1]本订阅号所收集的资料来源于互联网,转载的目的在于传递更多信息用于各位老师教学资源来参考,避免各位重复劳动!并不代表本订阅号赞同其观点和对其真实性负责,也不构成任何其他建议。如果您发现订阅号上有侵犯您的知识产权的作品,请与我们取得联系,我们会及时修改或删除。
[2]订阅号内资料均免费下载,请在有效期内进行下载,下载后的资料仅供您教学自用,不得在网络传播,不得用于商业用途。
- THE END -
分享
收藏
赞
在看四连,为化学人加油!
 夜雨聆风
夜雨聆风


