文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(十七)中和反应
实验深度突破
一、实验原理
中和反应是酸与碱作用生成盐和水的反应,实质是酸中的 H+与碱中的 OH-结合生成
H O(离子方程式:H++OH-=H O)。该反应属于复分解反应,多数情况下无明显现象,需借
2 2
助酸碱指示剂(如酚酞、石蕊)或pH试纸判断反应终点。
二、实验步骤与现象(以NaOH溶液与稀盐酸反应为例)
实验用品
药品:NaOH溶液、稀盐酸、酚酞试液(或石蕊试液)。
仪器:烧杯、胶头滴管、玻璃棒、pH试纸(或pH计)。
操作:
1、指示剂法(酚酞)
步骤:
(1)向盛有5 mL NaOH溶液的烧杯中滴加2~3滴酚酞试液,溶液变红。
(2)用胶头滴管逐滴加入稀盐酸,边滴边用玻璃棒搅拌,直至溶液恰好由红色变为无色
(中和反应终点)。
现象:初始溶液呈红色(碱性),滴加盐酸后红色逐渐变浅,最终变为无色(中性或酸
性)。
2、pH监测法
步骤:
(1)取少量NaOH溶液于试管中,用pH试纸测定初始pH(pH>7)。
(2)逐滴加入稀盐酸并振荡,多次测定pH,直至pH=7。
现象:pH逐渐减小,从碱性(pH>7)变为中性(pH=7),若盐酸过量则pH<7。
三、实验结论
1、酸与碱能发生中和反应,生成盐和水:NaOH+HCl=NaCl+H O。
2
2、中和反应的实质是H+与OH-结合生成H O,反应过程中溶液酸碱性发生变化。
2
3、指示剂或pH监测可判断反应终点:酚酞遇碱变红,中性或酸性时无色;pH=7为中
性。
四、误差分析
若溶液未完全褪色就停止滴加盐酸,可能导致NaOH未完全反应,溶液仍呈碱性。
若盐酸滴加过量,溶液呈酸性,但酚酞仍为无色,需通过pH试纸确认终点。
五、实验注意事项
1、安全操作:
(1)酸和碱具有腐蚀性,避免接触皮肤和眼睛,若不慎接触,立即用大量水冲洗。
(2)稀释浓酸(如浓硫酸)时,需将酸缓慢倒入水中并搅拌,不可颠倒顺序(防止暴沸飞
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
溅)。
2、试剂用量:滴加盐酸时需逐滴缓慢加入,防止过量(若溶液变为无色后继续滴加盐
酸,溶液仍为无色,但此时盐酸过量)。
3、指示剂选择:
(1)强碱与强酸反应时,酚酞和石蕊均适用(酚酞颜色变化更明显);
(2)若为强碱与弱酸(或弱碱与强酸)反应,需选择更合适的指示剂,如石蕊在弱酸性中
呈红色,可能干扰终点判断。
六、实验改进与创新装置
1、微型化实验
目的:减少试剂用量,降低污染,适合分组实验。
操作:用点滴板代替烧杯,在点滴板孔穴中滴加 NaOH溶液和酚酞,再用微型滴管逐滴
加入稀盐酸。
现象:孔穴中溶液由红变无色,清晰直观。
2、数字化实验:用pH传感器实时监测
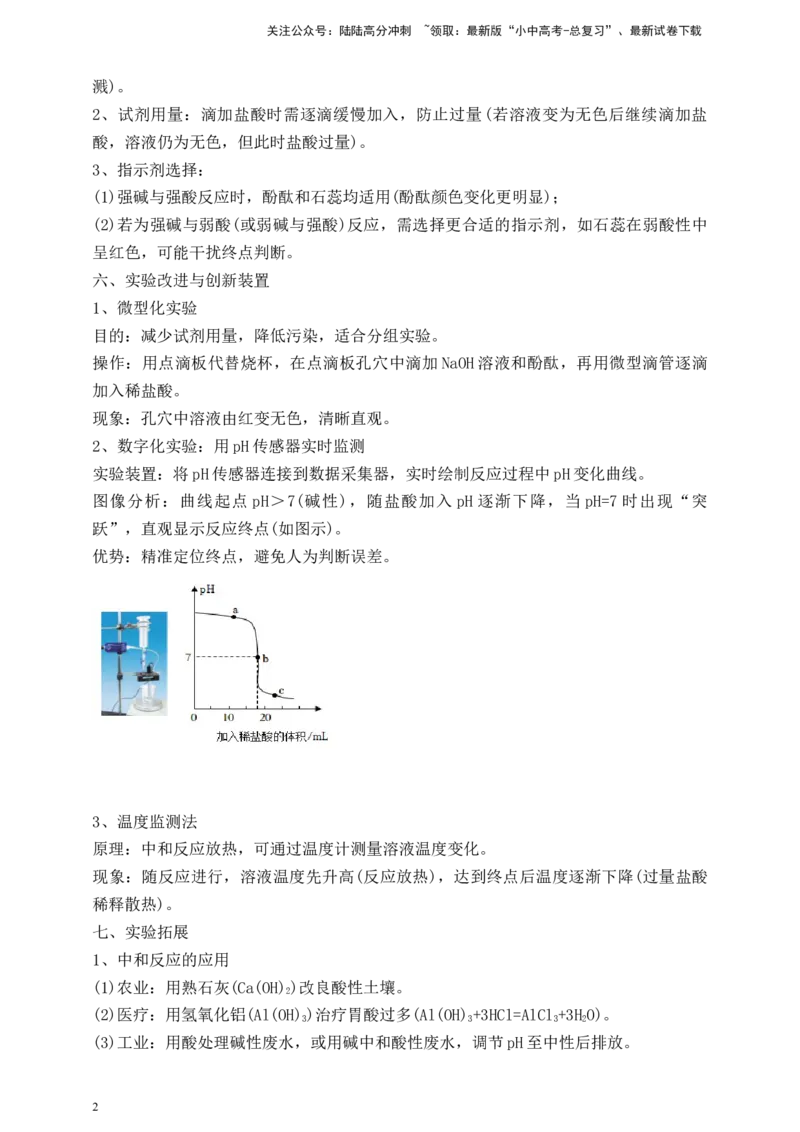
实验装置:将pH传感器连接到数据采集器,实时绘制反应过程中pH变化曲线。
图像分析:曲线起点 pH>7(碱性),随盐酸加入 pH 逐渐下降,当 pH=7 时出现“突
跃”,直观显示反应终点(如图示)。
优势:精准定位终点,避免人为判断误差。
3、温度监测法
原理:中和反应放热,可通过温度计测量溶液温度变化。
现象:随反应进行,溶液温度先升高(反应放热),达到终点后温度逐渐下降(过量盐酸
稀释散热)。
七、实验拓展
1、中和反应的应用
(1)农业:用熟石灰(Ca(OH) )改良酸性土壤。
2
(2)医疗:用氢氧化铝(Al(OH) )治疗胃酸过多(Al(OH) +3HCl=AlCl +3H O)。
3 3 3 2
(3)工业:用酸处理碱性废水,或用碱中和酸性废水,调节pH至中性后排放。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2、拓展实验设计
(1)探究不同酸与碱的中和反应:
用稀硫酸代替盐酸,与NaOH反应,观察现象:2NaOH+H SO =Na SO +2H O。
2 4 2 4 2
(2)验证中和反应放热:
用温度计测量反应前后溶液温度,或用 U型管压强变化装置(反应放热导致空气膨胀,U
型管液面左低右高)。
八、中考常见问题
1、为什么中和反应需要指示剂或pH监测?
答:多数中和反应无明显现象,需借助外物判断酸与碱是否恰好完全反应。
2、能否用石蕊试液代替酚酞?
答:可以。石蕊遇碱变蓝,遇酸变红,但若盐酸过量,溶液由蓝色变为红色,颜色变化
跨度大,适合演示实验,但颜色过渡不如酚酞明显(酚酞从红到无色突变更易观察)。
3、中和反应一定生成中性溶液吗?
答:不一定。若强酸与强碱完全反应,溶液呈中性;若强酸与弱碱(如NH ·H O)反应,
3 2
溶液呈酸性;若弱酸(如CH COOH)与强碱反应,溶液呈碱性(盐类水解导致)。
3
中考命题探秘
一、考情分析
中和反应实验在历年中考化学里都是重点考查内容,是衔接酸碱知识的关键纽带,其出
现频率高,几乎每年各地的中考卷都会涉及。命题方向倾向于将中和反应的原理、操作
与酸碱的性质、溶液酸碱度的变化、化学方程式书写等知识融合,考查学生对知识的综
合运用能力。从对近年来中考真题的统计分析来看,无论是基础题型,像选择题、填空
题,还是区分度较高的实验探究题、计算题,中和反应实验相关内容都频繁出现,着重
考查学生的知识迁移、逻辑推理与实验探究能力。
二、考查形式
1.基本概念与原理:考查中和反应的定义,判断给定反应是否属于中和反应;要求学生
理解中和反应的实质,即氢离子(H+)和氢氧根离子(OH-)结合生成水,并能运用这一
原理分析相关问题。例如,解释酸碱混合后溶液酸碱性变化的原因。
2.实验操作细节:考查实验仪器的选择与使用,如量筒、滴管、烧杯等;试剂的取用,
像胶头滴管的垂直悬空滴加、试剂瓶瓶塞的倒放等;实验步骤的先后顺序,如在中和反
应中,酸滴入碱溶液还是碱滴入酸溶液,以及判断反应终点的方法,如借助指示剂颜色
变化(酚酞从红色变为无色,或石蕊从蓝色变为紫色再变为红色)。
3.实验现象分析:要求学生准确描述中和反应过程中的现象,如溶液颜色变化、温度变
化(酸碱中和反应一般为放热反应,溶液温度升高);分析现象背后的化学反应原理,
例如为什么向滴有酚酞的氢氧化钠溶液中滴加稀盐酸,溶液颜色会逐渐变浅直至无色。
4.实验设计与探究:给定实验目的,如探究中和反应是否发生、反应后溶液中溶质成
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
分,让学生设计完整实验方案。方案需涵盖实验步骤、所需试剂、预期现象和结论;可
能涉及控制变量法的运用,如探究酸和碱反应时,控制酸或碱的浓度、体积等变量,研
究其对反应的影响。
5.数据处理与分析:在实验探究中,若给出溶液pH值变化曲线、温度变化数据等,要
求学生通过分析数据得出中和反应的发生、反应进程(是否恰好完全反应)、溶液酸碱
性变化趋势等结论;利用数据进行简单计算,如根据中和反应的化学方程式,计算酸或
碱的浓度、溶质质量等。
6.实际应用关联:结合生活、生产实际,考查中和反应在改良酸性土壤(用熟石灰中和
土壤酸性)、处理工厂酸性废水(用碱性物质中和)、医药领域(治疗胃酸过多用氢氧
化铝等碱性药物)等方面的应用原理;分析实际应用场景中的化学反应过程,以及可能
出现的问题和解决方法。
三、中考所占分值或比例
中和反应实验在中考化学试卷中的分值占比通常在 5%-15%之间,具体分值一般为5-10
分。在不同地区的试卷中,分值分布有所差异。在一些以基础知识考查为主的地区,选
择题和填空题中涉及中和反应实验的分值可能在 3-5分;而在注重实验探究和综合能力
考查的地区,实验探究题若以中和反应为背景,分值可达 6-8分,再加上其他题型中的
相关考查,总分值可能会更高。
四、中考预测
1.考查形式创新:未来中考可能会引入更多新颖的实验情境和技术手段,如借助数字化
实验设备,像pH传感器、温度传感器、电导率传感器等,实时监测中和反应过程中的
各项数据变化,并据此进行深度分析和探究,考查学生对新技术的理解和应用能力。
2.联系实际紧密化:会更加注重中和反应在实际生活和新兴科技领域的应用考查,如在
环保新材料研发、生物制药中的酸碱调节、新能源电池电解液的酸碱平衡等方面,以实
际问题为导向,考查学生运用化学知识解决复杂问题的能力。
3.学科素养融合化:着重考查学生的化学学科核心素养,如科学探究与创新意识、证据
推理与模型认知、科学态度与社会责任等。在实验设计与探究题中,鼓励学生提出创新
性的实验思路和方法;在实际应用考查中,引导学生关注化学对社会发展和环境保护的
重要意义。
五、备考建议
1.夯实基础知识:深入理解中和反应的概念、原理、实质和化学方程式书写,对比不同
酸碱中和反应的特点,总结规律;结合酸碱的性质,构建完整的知识体系,明确中和反
应在酸碱知识板块中的核心地位。
2.强化实验操作:通过实际操作实验或观看高清实验视频,熟悉中和反应实验的每一个
步骤、仪器使用规范和注意事项;掌握判断反应终点的方法,如指示剂的选择和使用;
观察实验现象时,要全面、细致,并能准确描述和分析。
3.加强题型训练:针对不同考查形式的题目进行专项练习,尤其是实验设计与探究题和
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实际应用题。在练习过程中,掌握解题思路和方法,学会从题目中提取关键信息,运用
所学知识进行分析和解答;总结错题原因,及时查漏补缺。
4.建立知识网络:将中和反应与酸碱盐的性质、化学方程式计算、溶液的酸碱性与 pH
等知识建立紧密联系,形成完整的知识网络;通过思维导图、知识框架图等方式,梳理
知识脉络,便于知识的记忆和提取。
5.关注实际应用:平时多留意中和反应在生活、生产、科研等领域的应用实例,积累素
材;学会从化学视角分析实际问题,将实际问题转化为化学问题,运用所学知识解决,
提高知识迁移和应用能力。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
6