当CRISPR-Cas9凭借精准的基因剪切能力成为生命科学的“明星工具”,研究者们却始终被它的瓶颈所困:多基因组合敲除成本高到难以承受、必需基因敲除后细胞直接死亡无法观测、动物模型的结果难以转化到人类……
如今,虚拟敲除这一AI与单细胞多组学融合的革命性技术,彻底打破了物理实验的边界。它无需触碰真实的DNA链,就能在数字世界中模拟基因失活的全局效应,正在重构药物研发、肿瘤研究和发育生物学的整个工作流。
顶刊都在用的「虚拟敲除」到底是啥?他与传统敲除相比有哪些优势?我们又该如何将其引入到自己的实验当中呢?今天就带大家一起探讨。

联系丸子,解锁更多小分子靶点筛选、蛋白互作技术干货~
一、到底什么是虚拟敲除?
简单来说,虚拟敲除是纯计算驱动的基因功能研究方法:它不通过基因编辑技术物理破坏目标基因,而是依托基因调控网络模型或单细胞基础大模型,在计算机中阻断目标基因的信息流,推演其失活后细胞、组织乃至整个系统的表型变化。
目前主流的技术路线有三条,分别对应不同的研究场景:
把单细胞转录组数据抽象成“基因交通网”,每个基因是网络中的节点,基因间的调控关系是连接节点的道路。
● 先通过野生型细胞数据构建完整的基因调控网络;
● 虚拟敲除时,直接切断目标基因的所有“出度道路”(即阻断它向所有下游基因传递信号);
● 对比敲除前后网络的变化,找出受影响的基因和通路。
代表工具:
scTenifoldKnk(张量分解+流形对齐)、GenKI(变分图自编码器,解决传统方法的计算伪影问题)。
将单细胞转录本视为“生命语言”,用千亿级参数的Transformer模型学习基因间的“语法规则”。
● 预训练阶段:模型学习大量单细胞数据中基因表达的序列规律;
● 虚拟敲除时:像“屏蔽文章中的某个关键词”一样,删除目标基因的词元;
● 模型自动推演“关键词缺失”后,整个“句子(细胞状态)”会发生什么变化。
代表工具:
Geneformer(3000万细胞预训练,秩值编码技术)、scGPT(3300万细胞预训练,零样本预测能力)。
针对微生物代谢和细胞代谢研究,构建全基因组尺度的代谢反应网络。
● 基于“基因-蛋白质-反应”的映射规则,用数学优化方法计算代谢流的分布;
● 虚拟敲除时,将目标酶对应的代谢反应通量强制设为0;
● 重新计算网络达到新稳态时的代谢流变化,找到关键的代谢节点。
代表工具:
COBRA Toolbox、FindTargetsWEB。
二、与传统实验敲除对比有哪些优势?
物理敲除(如CRISPR-Cas9)仍是验证基因功能的“金标准”,但虚拟敲除在通量、成本、安全性和适用范围上,展现出了互补优势:
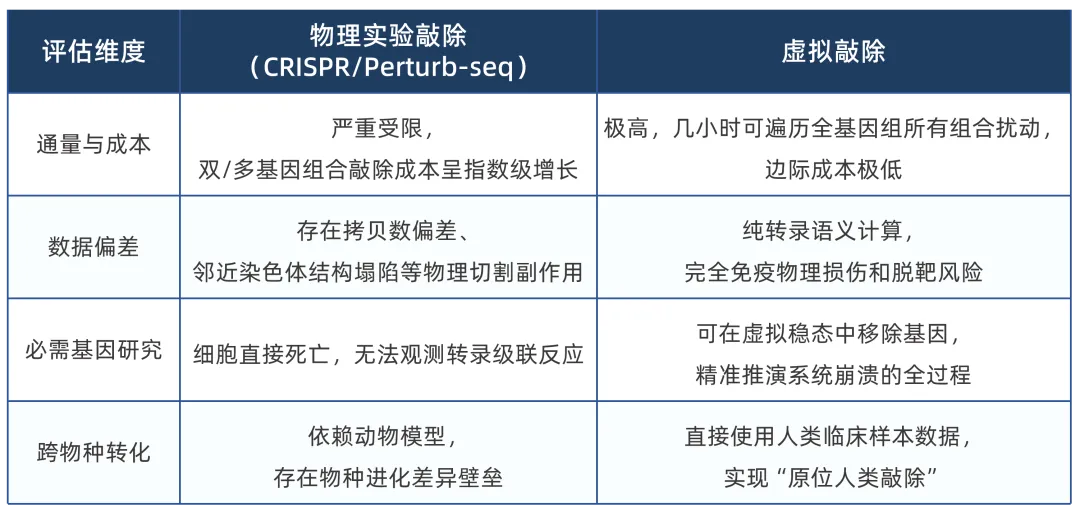
具体来说,这4个优势解决了传统研究的核心痛点:
① 突破组合筛选的通量天花板:
探索合成致死需要筛选大量双基因组合,物理实验构建文库的成本和难度难以承受,而虚拟敲除能轻松覆盖所有未被测试的组合空间。
② 规避CRISPR的“假阳性”陷阱:
CRISPR切割DNA引发的双链断裂,会导致非特异性细胞死亡,常让研究者误判基因为“必需基因”,虚拟敲除则完全没有这个问题。
③ 破解必需基因的“致死悖论”:
维持细胞生存的核心基因一旦被物理敲除,细胞会立即死亡,研究者永远看不到它如何调控系统稳态;虚拟敲除能完整呈现基因缺失后转录网络的崩溃过程。
④ 消除动物模型的转化障碍:
小鼠与人类的基因调控网络存在巨大差异,很多在小鼠中有效的靶点在人体临床试验中失效;虚拟敲除可直接基于人类肿瘤、临床活检样本进行推演。
三、虚拟敲除有哪些应用场景?
这项技术已经从理论走向实战,在多个关键领域取得了突破性成果:
合成致死是抗癌药物开发的核心方向(如BRCA突变与PARP抑制剂)。传统CRISPR筛选效率低且难以评估正常细胞毒性,而虚拟敲除可基于肿瘤细胞系图谱,高通量预测基因互作。
案例:
在肝细胞癌研究中,研究者通过虚拟敲除发现ARID1A与TEAD1存在强合成致死信号,后续物理敲低TEAD1后,ARID1A突变的肝癌细胞出现显著的增殖停滞。
虚拟敲除能精准模拟切断肿瘤与免疫细胞间的通信,预测免疫治疗的响应和耐药机制。
案例:
在泛癌肿瘤微环境研究中,虚拟敲除恶性细胞的TSPAN6基因后,发现PD-L1等免疫抑制配体的表达显著下调,能有效激活耗竭性T细胞;在NRAS突变黑色素瘤研究中,虚拟敲除揭示了STAT3在耐药细胞中的通路重构,指明了联合抑制STAT3与RAS的治疗方案。
无需构建基因敲除动物模型,就能快速解析致病基因的分子机制。
案例:
针对杜氏肌营养不良症的致病基因Dmd,虚拟敲除后筛选出190个显著受影响的下游基因,这些基因高度富集在肌动蛋白收缩、细胞外基质互作通路,与患者肌肉无力的临床表型完全吻合。
针对多重耐药菌,虚拟敲除能快速锁定致命的代谢节点,加速抗生素研发。
案例:
对铜绿假单胞菌的全基因组代谢网络进行单反应级虚拟敲除,筛选出一旦失活就会导致细菌无法合成生物量的绝对必需节点,并直接对接药物数据库评估可成药性。
四、如何把虚拟敲除融入你的实验?
对于传统湿实验研究者,无需精通复杂的算法,按照这5个标准化步骤,就能快速上手虚拟敲除技术:
● 只有单一物种/细胞系的野生型单细胞数据:选scTenifoldKnk或GenKI,挖掘基因共表达模块和调控中枢;
● 有大型异质性细胞图谱,需要零样本推演:选Geneformer或scGPT等单细胞基础大模型;
● 研究细胞代谢或微生物工程:选COBRA Toolbox或FindTargetsWEB,进行通量平衡分析。
原始数据的质量直接决定预测结果的准确性:
● 用Seurat或Scanpy过滤劣质细胞(如线粒体基因比例>10%、文库深度<500的细胞);
● 提取方差最大的2000-5000个高变基因,降低矩阵稀疏度的干扰;
● 按照模型要求转换格式(如Geneformer需要Loom文件,scGPT需要AnnData格式)。
直接使用预训练模型难以精准预测特定研究场景,需要进行微调:
● 以Geneformer为例,保持12层Transformer隐藏层非冻结,用低学习率(5×10-5)训练约10个Epoch;
● 注意防止数据泄露:仅用细胞的宏观状态(如是否激活)作为标签,隐藏已知靶标信息。
图算法工具:
复制野生型网络邻接矩阵,将目标基因所在行的权重全部设为0;
大模型工具:
调用对应的扰动模块,删除目标基因的词元;
代谢模型工具:
将目标反应的通量上下限设为0,重新计算稳态流分布。
● 用余弦相似度、Wilcoxon秩和检验等方法量化扰动前后的表型漂移,通过KEGG/GO富集分析找到关键通路;
● 最重要的一步:将计算得出的高优先级候选靶点,投入CRISPR编辑、免疫荧光、蛋白质印迹等湿实验中验证,形成严谨的数据闭环。
结语
虚拟敲除技术正在打开生命科学研究的“数字维度”,它让我们能以极低的成本、极高的通量,探索物理实验无法触及的基因功能空间。当然,虚拟敲除并非要取代传统湿实验,而是与它们形成强大的互补:AI负责在数字世界中快速筛选海量假说,湿实验负责验证核心结论,而定量蛋白质组学则是连接两者的关键桥梁。
未来,随着多模态虚拟细胞技术的发展,我们终将实现对生命系统的精准模拟与重构,为攻克癌症、罕见病等疑难疾病带来全新的希望。
从干实验到湿实验:蛋白质组学为虚拟敲除画上完美句号
虚拟敲除主要基于转录组数据进行推演,而蛋白质才是生命功能的直接执行者。转录水平的变化是否能转化为蛋白水平的效应、是否存在翻译后修饰的调控,这些都需要定量蛋白质组学来验证和补充。

联系丸子,了解更多~

联系丸子,了解更多~
推荐
谱度众合:细胞/动物模型定量蛋白质组学解决方案
为了帮助研究者完成从“虚拟预测”到“功能验证”的完整闭环,谱度众合推出细胞/动物模型定量蛋白质组学解决方案,完美承接虚拟敲除的研究成果:
✔ 全流程服务:从细胞沉淀/动物组织样品的蛋白提取、酶解,到高分辨液质联用检测,再到全套生物信息学分析,一站式交付;
✔ 多维度深度分析:提供差异蛋白筛选、GO/KEGG/Hallmark富集分析、GSEA分析、蛋白质互作网络构建,综合差异显著性、功能相关性和网络重要性,筛选最多20个关键蛋白和20条关键通路;
✔ 个性化定制:可根据你虚拟敲除的靶基因、施加的药物/病毒刺激,进行针对性的数据库挖掘和关联分析;
✔ 论文级交付:提供符合SCI发表标准的结果图表,以及方法学和结果的中英文描述文案,直接助力论文撰写。
参考文献
1. Heirendt L, Arreckx S, Pfau T, et al. Creation and analysis of biochemical constraint-based models using the COBRA Toolbox v.3.0. Nat Protoc. 2019;14(3):639-702.
2. Osorio D, Zhong Y, Li G, et al. scTenifoldKnk: an efficient virtual knockout tool for gene function predictions via single-cell gene regulatory network perturbation. Patterns (N Y). 2022;3(3):100434.
3. Srivatsa S, Montazeri H, Bianco G, et al. Discovery of synthetic lethal interactions from large-scale pan-cancer perturbation screens. Nat Commun. 2022;13(1):7346.
4. Yang Y, Li G, Zhong Y, et al. Gene knockout inference with variational graph autoencoder learning single-cell gene regulatory networks. Nucleic Acids Res. 2023;51(13):6578-6592.
5. Fang L, Pan H, Zhu Y. Integrating computational engines to identify TSPAN6 as a migrasome-associated target for immunotherapy sensitization. Front Immunol. 2026;17:1782717.

 夜雨聆风
夜雨聆风