
很多医械同仁在后台留言,希望能看到医用电气设备风险管理报告的标准模板拆解与实操解读。
本期医械加油站就针对这份适配GB9706.1与YY/T 0316双标准的合规模板,逐项拆解核心框架、审评要点与实操要求,用通俗专业的方式带大家快速吃透,助力医用电气设备企业高效完成风险管理报告编制,顺利通过检测核查与审评验收。
一、报告核心编制依据
GB9706.1-2020 检测专用风险管理报告,是医用电气设备合规检测的核心支撑文件,必须严格对标多重标准与产品资料编制,核心依据如下:
风险管理通用标准:YY/T 0316-2016《医疗器械风险管理对医疗器械的应用》
电气安全强制标准:GB9706.1-2020《医用电气设备 第 1 部分:基本安全和基本性能的通用要求》;
配套并列标准:YY 9706.102-2021(电磁兼容专用要求)、GB/T 16886系列(生物学评价);
产品专属资料:产品技术要求、使用说明书、设计开发文档、检测报告等。
二、报告整体框架:7 大核心章节全覆盖
本模板采用全生命周期风险管理逻辑搭建框架,共7 大核心章节,覆盖从产品基础信息到最终评审的全流程,是检测审评的完整合规证据链:
第一章 综述:产品基础信息 + 风险管理组织 + 计划 + 流程; 第二章 风险分析:评估方法 + 可接受准则 + 双重安全特征分析; 第三章 风险评价与控制:控制前后风险评估 + 风险矩阵对比; 第四章 综合剩余风险评价:剩余风险汇总 + 公开告知 + 评审结论; 第五章 风险 / 收益分析:控制措施合理性 + 受益风险对比; 第六章 生产和生产后信息:风险信息收集 + 闭环更新机制; 第七章 风险管理评审:评审输入 + 计划核查 + 最终结论。
三、核心章节深度拆解
第一章 综述:筑牢报告基础信息
综述是报告的总览页,核心解决“产品是什么、谁来管、怎么管”三大问题,是审评第一眼核查的核心内容:
产品简介:需完整列明结构组成、工作原理、电气安全特征、适用范围 / 禁忌、使用环境、预期使用寿命,为风险识别提供基础依据;
风险管理职责:明确总经理、研发、质量、管理者代表的权限,组建跨部门风险管理小组,确保责任到人;
风险管理计划:界定全生命周期管控范围,明确评审、验证要求,确定风险可接受准则;
风险管理过程:明确风险分析→评价→控制→生产后信息的全流程,配套流程图更直观。
第二章 风险分析:报告核心计算与识别环节
本章是报告的技术核心,直接决定风险管控的科学性与合规性,重点拆解两大核心内容:
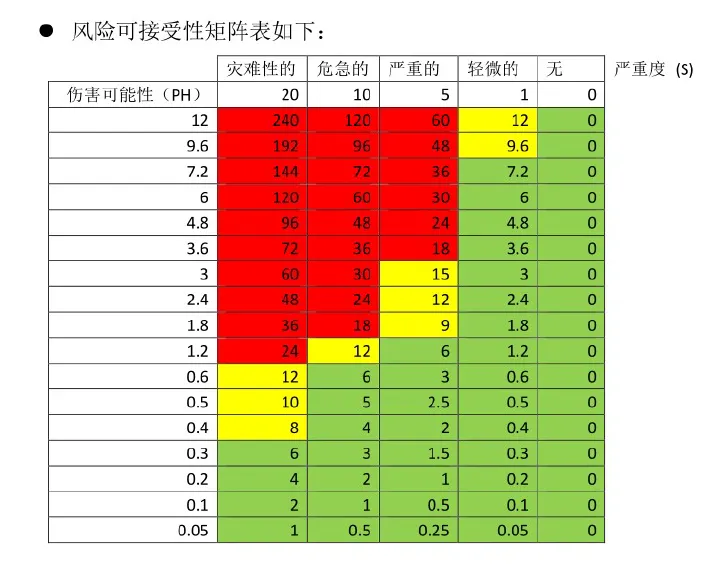
风险评估计算方法(固定不可修改)
采用RPN 风险系数法,计算公式严格统一:
风险系数:RPN=S×PH 伤害可能性:PH=PHS×PLH 严重度(S)分级:灾难性 20、危急 10、严重 5、轻微 1、无 0; 风险可接受准则: RPN>15:不可接受,必须采取风险控制措施; 7.5≤RPN≤15:需控制,无措施时需做风险 / 受益分析; RPN<7.5:可接受,鼓励优化但不强制。
双重安全特征分析(审评必查) YY/T 0316-2016 安全特征分析:依据标准附录 C 清单,识别操作、生物、能量、化学等全维度危害; GB9706.1-2020 风险特征分析:覆盖 56 项标准核查问题,重点识别电气、机械、软件、电磁兼容等医用电气设备专属风险。
第三章 风险评价与控制:风险闭环管控核心
本章核心是“先评估、再控制、后复评”,形成风险管控闭环:
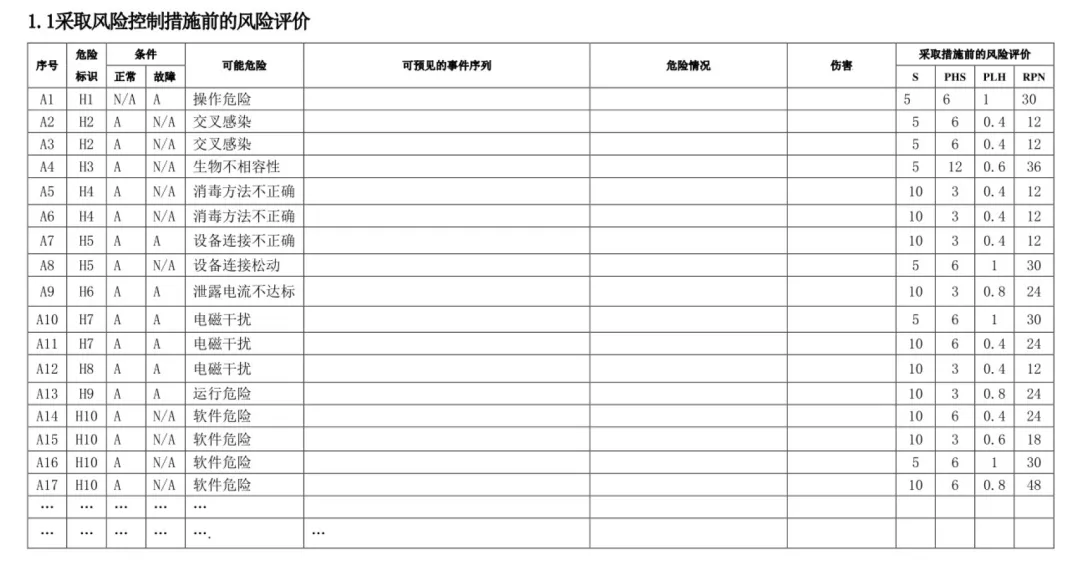
控制前风险评价:对识别的所有危害,计算 RPN 值,判定风险等级;
风险控制措施:针对不可接受风险,采取设计优化、说明书警示、安全装置等措施;
控制后风险评价:重新计算 RPN 值,验证措施有效性;
风险矩阵对比:形成控制前后两张矩阵表,直观展示风险降低效果,是审评重点核查内容。
第四章 综合剩余风险评价:最终风险判定
所有风险控制完成后,需开展综合剩余风险评审,核心结论要求:
无不可接受、ALARP 等级风险项;
剩余风险均在说明书中以警告、禁忌、操作要求明确告知使用者;
公开需告知的剩余风险(如未经培训禁止操作、使用时需监护设备状态);
最终结论:产品临床受益远大于剩余风险,综合剩余风险可接受。
第五章 风险 / 收益分析:管控合理性验证
本章核心验证风险控制措施的合理性:
风险控制措施未新增原材料、新工艺,未产生新危害;
产品临床受益远大于剩余风险,风险控制措施科学有效。
第六章 生产和生产后信息:全生命周期闭环
按医疗器械 GMP 要求,建立生产后风险信息闭环机制:
建立用户反馈、不良事件、投诉信息收集处理程序;
跟踪同类产品标准更新、公开信息,及时复盘更新风险;
出现新风险时,重新启动风险管理流程,确保全周期风险可控。
第七章 风险管理评审:最终合规结论
评审小组对全报告进行终审,核心输出 3 大结论:
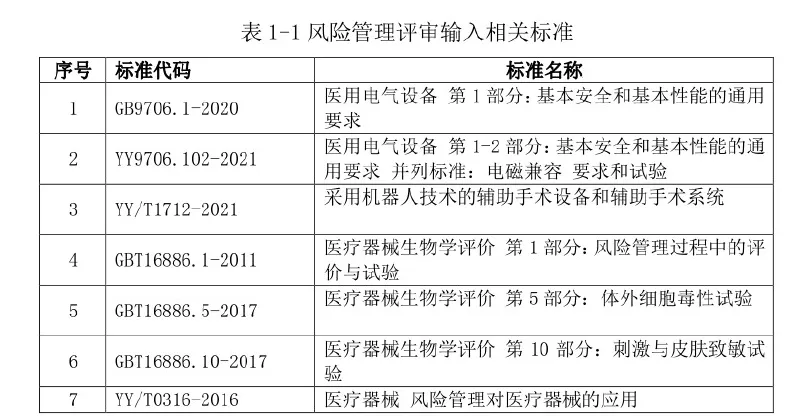
风险管理计划已全面落实实施;
综合剩余风险可接受;
已建立生产后信息收集机制,产品受益超过风险。
四、实操合规核心要点
风险计算必须精准,RPN 公式、分级、可接受准则不可随意修改;
YY/T 0316 与 GB9706.1 双重特征分析必须完整,无遗漏风险点;
剩余风险必须公开告知,并在说明书中体现;
全流程记录可追溯,风险控制措施需有验证证据支撑。
为方便大家快速落地 GB9706.1 检测相关风险管理工作,我们已为大家整理好GB9706.1 检测专用风险管理报告空白模板,在公众号后台回复关键词 9706,即可一键领取完整资料包。
后续医械加油站还会持续更新更多医械注册、检测、体系、申报相关的实用模板与干货内容,持续关注,干货不错过~


 夜雨聆风
夜雨聆风