
RNA-DNA 杂交体是细胞内最普遍、几乎无处不在的内源性核酸结构之一,可在所有生物体中引发基因组不稳定性。尽管其对基因组完整性的危害已有大量报道,但 RNA-DNA 杂交体在 DNA 合成起始和转录过程中 mRNA 的生成中同样不可或缺。此外,在亚优条件下,它们还参与 DNA 修复并调控基因表达。
当 RNA-DNA 杂交体不能被及时解离时,会成为从细菌到人类多种生物中基因组不稳定性的驱动因素,并与癌症及神经系统疾病的发生密切相关。RNA 中 2′-羟基的化学特性使其能够切割邻近 DNA 的磷酸二酯键,从而诱发 DNA 链断裂。持续存在的杂交体还会阻碍 DNA 复制,引起复制叉停滞、激活 DNA 损伤应答,并导致高频重组和染色体重排,严重威胁细胞存活与基因组稳定性。
大量研究表明,从细菌到真核生物的复制性 DNA 聚合酶都会错误地将核糖核苷酸(rNMPs)掺入 DNA 中。这种“糖基错误”是基因组中 RNA-DNA 杂交体的重要来源:在每一轮复制中,细菌可掺入数千个 rNMPs,而哺乳动物细胞甚至超过百万个。
若这些 rNMPs 残留在模板链中,会显著减缓或阻滞复制性 DNA 聚合酶的延伸,包括细菌 Pol III 和真核生物 Pol δ。除单个 rNMP 外,连续多个 rNMPs 也可能被掺入基因组,例如由跨损伤 DNA 聚合酶产生的 R 片段,或由转录过程中形成的 R 环整合而成的 RNA 片段。这些 RNA 片段对 DNA 复制构成严重障碍。
如果这些嵌入的 RNA 不能被及时修复,细胞可能需要依赖逆转录酶,以 RNA 为模板合成 DNA,否则复制叉将停滞并最终崩溃,激活 DNA 损伤应答并引发突变,危及基因组完整性。
A 家族 DNA 聚合酶广泛存在于细菌、病毒和真核生物中,其经典代表是大肠杆菌 DNA 聚合酶 I(Pol I)。该酶除 DNA 合成活性外,还具有 5′→3′ 核酸外切酶和 3′→5′ 校对外切酶活性,从而实现高保真 DNA 合成。
值得注意的是,缺失 3′→5′ 校对活性的 Pol I Klenow 片段可表现出逆转录酶活性。类似地,真核生物 Pol θ 作为另一种 A 家族聚合酶,其校对结构域失活,具有高度易错性,并能催化以 RNA 为模板的 DNA 修复。这些发现提示:校对功能失活的 A 家族 DNA 聚合酶可能普遍具备内在的逆转录酶活性。
长期以来,大肠杆菌 Pol I 一直被视为细菌 Pol I 的模型。然而,与革兰氏阴性菌不同,许多革兰氏阳性菌进化出缺乏 3′→5′ 校对活性的 Pol I,这是由于阻碍 Mg²⁺ 配位的突变所致。这种“残留但失活”的校对结构域与真核 Pol θ 的特征高度相似。
基于此,发表于bioRxiv的一篇论文(原文标题:DNA polymerase I is an efficient reverse transcriptase that mediates RNA-templated DNA repair synthesis),文章提出假设:革兰氏阳性菌的 Pol I 可能具备内在的逆转录酶活性,从而在基因组中存在嵌入 RNA 时,催化以 RNA 为模板的 DNA 修复。
核心发现
该研究系统分析了含核糖核苷酸模板对枯草芽孢杆菌 A 家族与 C 家族 DNA 聚合酶的影响。结果显示:
模板中 RNA 的存在会迅速阻滞复制性 C 家族聚合酶 PolC 和 DnaE 的合成;
相比之下,枯草芽孢杆菌 Pol I(BsPol I)表现出强大的逆转录酶活性,能够以 RNA 为模板高效合成 DNA;
Pol I 能跨越连续核糖核苷酸片段,提示其在复制性聚合酶受阻时可接管合成任务;
多种细菌 Pol I 同源物同样具有不同程度的逆转录酶活性;
在缺乏 Pol I 的情况下,DNA 中 rNMP 的掺入会显著加剧基因组不稳定性。
BsPol I 缺失使细胞对核糖核苷酸掺入高度敏感
为验证 Pol I 在体内应对 RNA-DNA 杂交体的作用,作者使用羟基脲(HU)诱导核糖核苷酸还原酶抑制,从而增加 rNMP 和 R 片段的形成(图 1A)。结果显示:
ΔpolA 菌株在 10 mM HU 下生长明显受抑(图 1B);
缺失 RNase HIII(ΔrnhC)的菌株表现出更严重的 HU 敏感性;
同时缺失 Pol I 和 RNase HIII 的菌株对复制应激最为敏感。
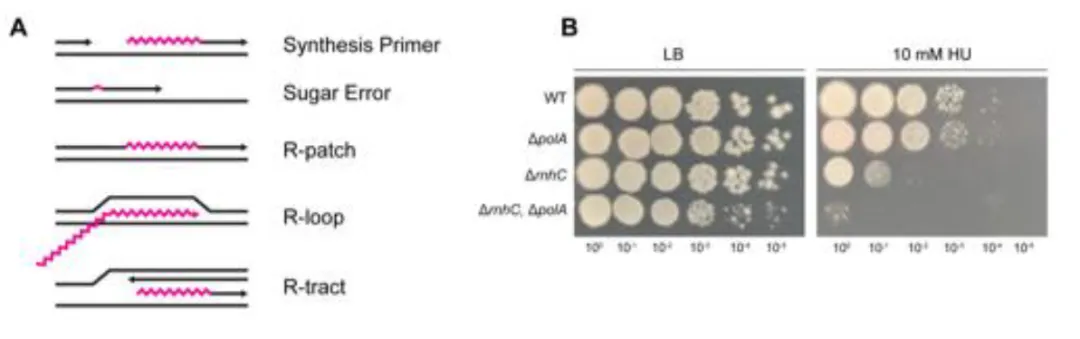
Figure 1. The absence of BsPol I sensitizes cells to ribonucleotide incorporation.
这些结果表明,Pol I 在体内应对 RNA-DNA 杂交体、维持复制稳定性中发挥关键作用。
枯草芽孢杆菌 Pol I 是高效逆转录酶
在体外生化实验中,作者比较了 Pol I、PolC、DnaE 与经典逆转录酶 M-MuLV RT 的活性。结果显示:
三种聚合酶在 DNA 模板上均能高效延伸(图 2A、2B);
当模板完全由 RNA 构成时,只有 Pol I 能在不同缓冲条件下完全跨越 RNA 模板,生成与 RT 对照相同的产物(图 2C–F);
PolC 仅产生中间产物,DnaE 则几乎完全受阻。
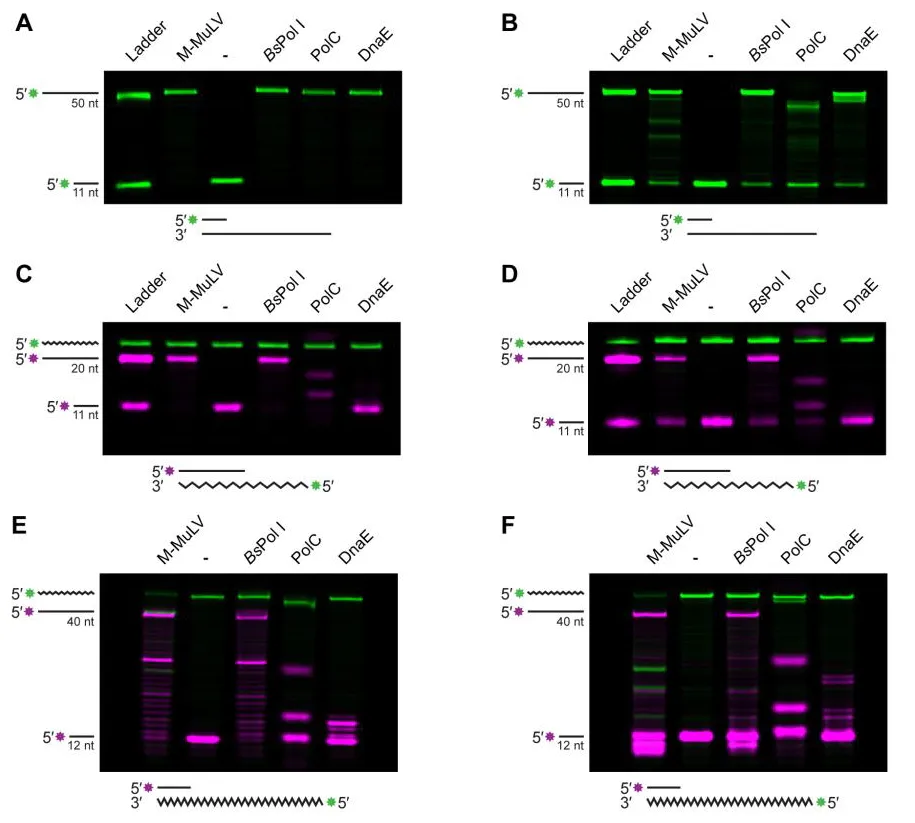
Figure 2. BsPol I can use RNA as a synthesis template.
这些结果明确表明,BsPol I 具有稳定而本征的逆转录酶活性。
Pol I 的逆转录功能在细菌中高度保守
作者进一步分析了多种细菌 Pol I,发现具有 RT 活性的 Pol I 多数缺乏完整的 DEDD 校对基序。在来自大肠杆菌、金黄色葡萄球菌、李斯特菌和分枝杆菌的 Pol I 中:
所有蛋白在 DNA 模板上均具备聚合酶活性(图 3A、3B);
在 RNA 模板上,其 RT 活性存在差异,但在优化的 RT 缓冲液中均可生成全长产物(图 3C–F);
BsPol I 和 SaPol I 表现最为高效,而 EcPol I 活性相对较弱(图 3C、3D)。
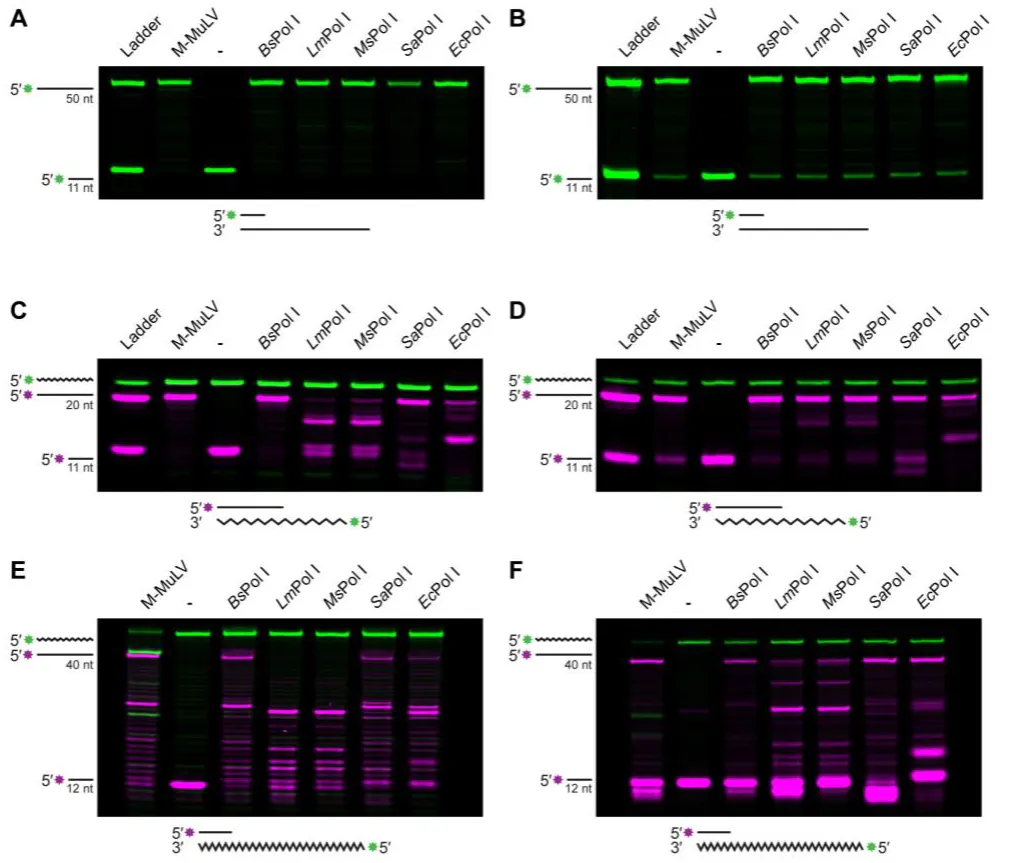
Figure 3. RNA-templated DNA repair is conserved in bacterial Pol I enzymes.
Pol I 可跨越嵌入的核糖核苷酸片段
在模拟体内复制障碍的实验中,作者构建了含不同长度 rNMP 片段的模板(图 4A)。结果显示:
BsPol I 和 EcPol I 能跨越多达 15 个连续 rNMPs,生成全长产物(图 4B);
随着 rNMP 数量增加,中间产物增多,提示效率下降;
其他 Pol I 同源物跨越能力较弱,但仍可耐受短 rNMP 片段(图 4C);
复制性聚合酶 PolC 在超过 1 个 rNMP 时几乎完全停滞(图 4D、4E);
DnaE 可跨越 1–5 个 rNMP,但更长片段同样导致合成阻断(图 4D)。
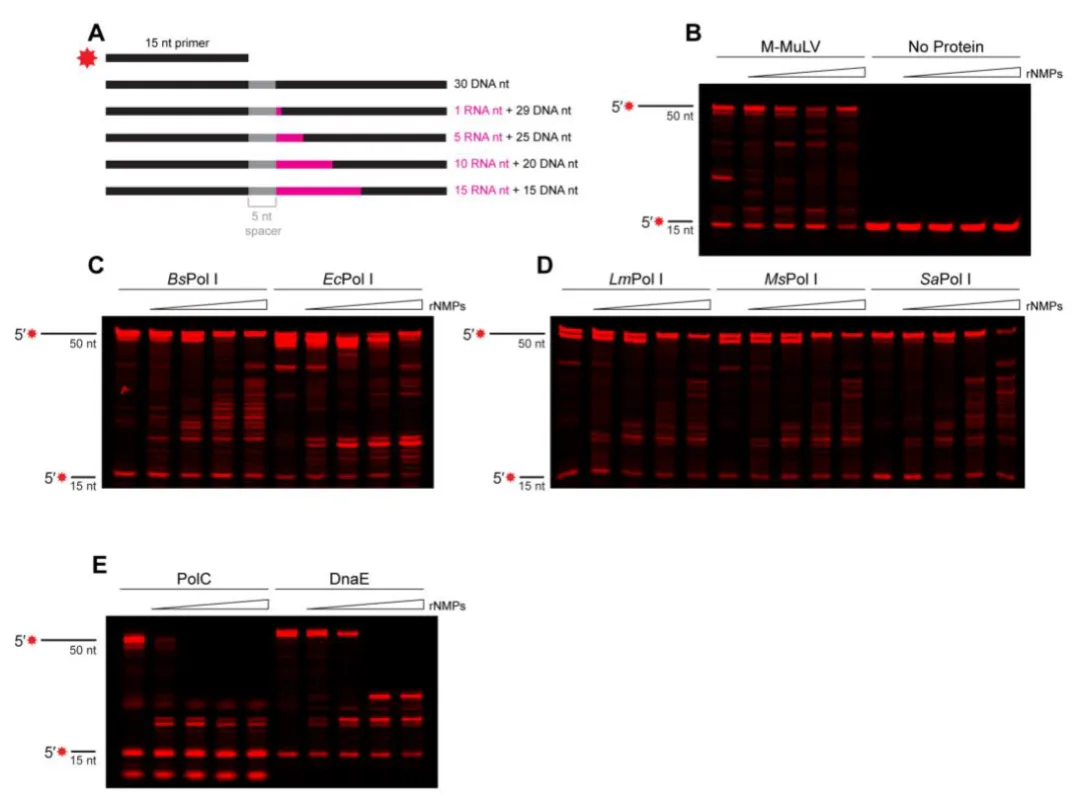
Figure 4. Pol I can traverse embedded ribonucleotides.
2025
总结


本研究系统证明:细菌 Pol I 是一种被长期低估的逆转录酶。当基因组 DNA 中嵌入核糖核苷酸或 RNA 片段、复制性聚合酶受阻时,Pol I 能以 RNA 为模板完成 DNA 合成,帮助复制叉继续前进。这一机制在多种细菌中高度保守,对维持基因组稳定性至关重要。
由于篇幅所限,本文仅摘录部分内容进行介绍。如需了解更多详情,欢迎点击下方链接阅读原文。
原文阅读:https://doi.org/10.64898/2025.12.22.696026
免责声明:本文内容仅供参考,不构成任何医疗或科研建议。小编水平有限,如有错误欢迎在评论区中指出。

关于图维
图维生物拥有自主知识产权的新模式药物智能合成平台nMECA,专注于高通量、优性价比的长链RNA和ssDNA、CRISPR基因编辑试剂,以及抗体-核酸偶联(AOC)的研发与生产。


邮箱|order@pixelbiosciences.com
官网|https://www.pixelbiosciences.com
 夜雨聆风
夜雨聆风