文档内容
第 73 讲 以物质含量或组成测定为主的综合实验
[复习目标] 1.掌握物质含量或组成测定的一般方法。2.掌握定量测定实验的思维模型。
类型一 物质含量的测定
1.重量分析法
(1)在重量分析中,一般首先采用适当的方法,使被测组分以单质或化合物的形式从试样中
与其他组分分离。
(2)重量分析法不需要指示剂,实验的关键是准确判断反应是否完全,以及反应前后固体(或
液体)质量的变化。
(3)重量分析法包括分离和称量两个过程。根据分离的方法不同,重量分析法又可分为沉淀
法、挥发法、萃取法等。
(4)计算方法
采用重量分析法进行定量计算时,可根据实验中发生反应的化学方程式或原子守恒确定相关
物质之间的定量关系,再结合实验数据列出关系式,并进行相关计算。
2.滴定分析法
(1)滴定分析法是将已知准确浓度的标准溶液,滴加到待测溶液中(或者将待测溶液滴加到标
准溶液中),直到所加的标准溶液与待测溶液按化学计量关系定量反应完全为止,然后测量
标准溶液消耗的体积,根据标准溶液的浓度和所消耗的体积,计算出待测物质的含量。
(2)实验的关键是准确量取待测溶液,根据指示剂的颜色变化确定滴定终点。
(3)根据标准溶液和待测溶液间反应类型的不同,可将滴定分析法分为四大类:中和滴定、
氧化还原滴定、络合滴定和沉淀滴定。
3.气体体积法
(1)通过测量反应生成气体的体积进行定量分析的方法,实验的关键是准确测量生成气体的
体积。
(2)测气体体积的方法分为直接测量法和间接测量法
将气体通入带有刻度的容器中,直接读取气体的体积。根据所用测量仪
直接测量法
器的不同,直接测量法可分为倒置量筒法和滴定管法两种
利用气体将液体(通常为水)排出,通过测量所排出液体的体积从而得到
间接测量法 气体体积。常用的测量装置为用导管连接的装满液体的广口瓶和空量
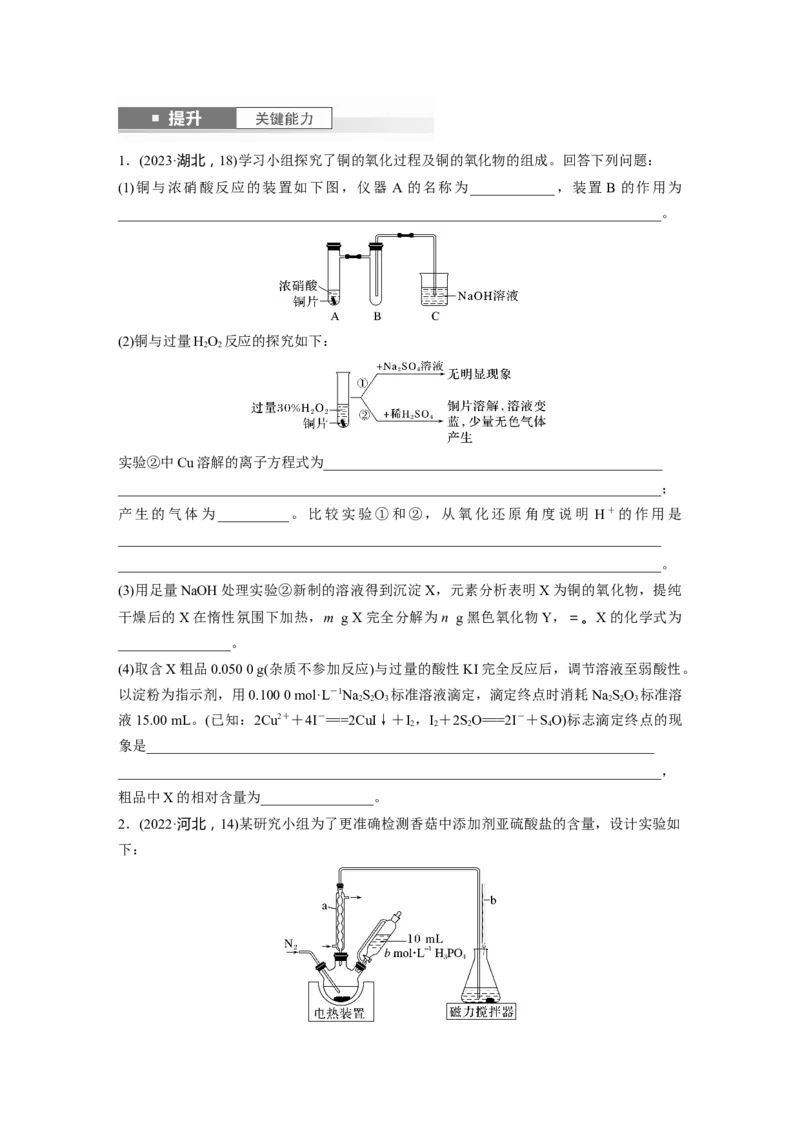
筒。排水法收集气体时,要保证“短进长出”1.(2023·湖北,18)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器 A 的名称为____________,装置 B 的作用为
_____________________________________________________________________________。
(2)铜与过量HO 反应的探究如下:
2 2
实验②中Cu溶解的离子方程式为________________________________________________
_____________________________________________________________________________;
产生的气体为__________。比较实验①和②,从氧化还原角度说明 H+的作用是
_____________________________________________________________________________
_____________________________________________________________________________。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯
干燥后的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,=。X的化学式为
________________。
(4)取含X粗品0.050 0 g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。
以淀粉为指示剂,用0.100 0 mol·L-1NaSO 标准溶液滴定,滴定终点时消耗NaSO 标准溶
2 2 3 2 2 3
液15.00 mL。(已知:2Cu2++4I-===2CuI↓+I ,I +2SO===2I-+SO)标志滴定终点的现
2 2 2 4
象是________________________________________________________________________
_____________________________________________________________________________,
粗品中X的相对含量为________________。
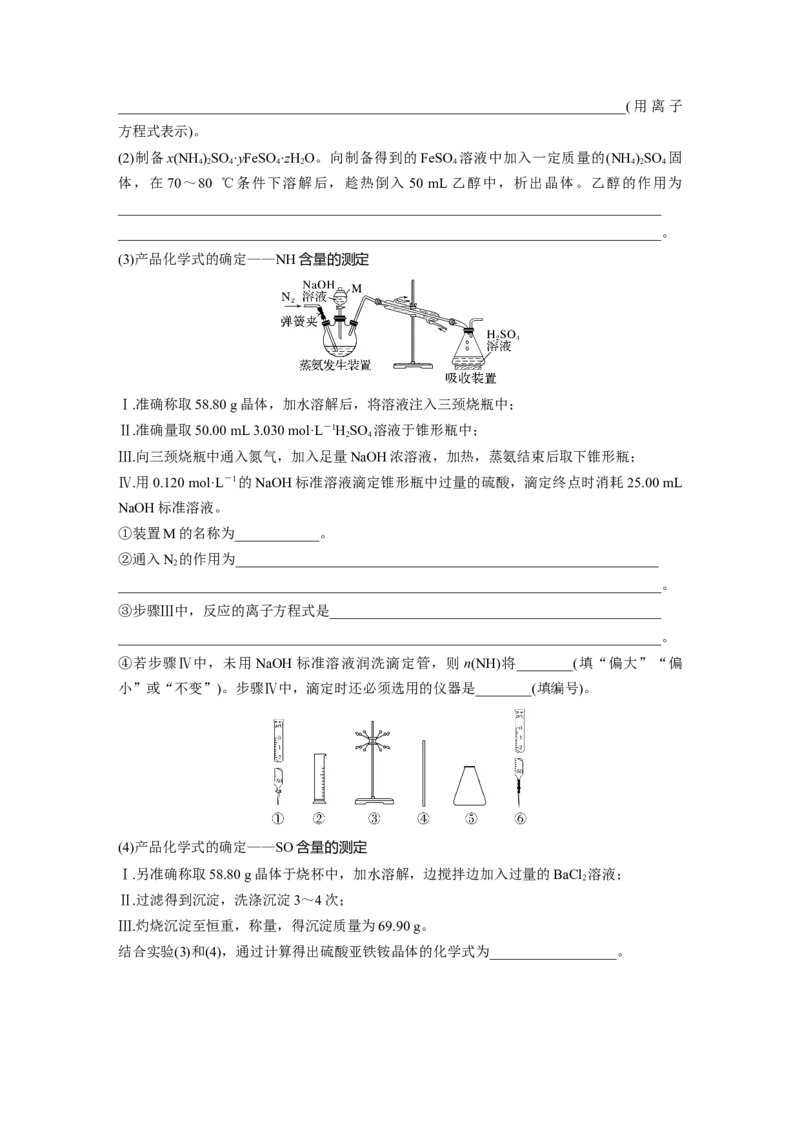
2.(2022·河北,14)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如
下:①三颈烧瓶中加入10.00 g香菇样品和400 mL水;锥形瓶中加入125 mL水、1 mL淀粉溶液,
并预加0.30 mL 0.010 00 mol·L-1的碘标准溶液,搅拌。
②以0.2 L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,
至终点时滴定消耗了1.00 mL碘标准溶液。
③做空白实验,消耗了0.10 mL碘标准溶液。
④用适量NaSO 替代香菇样品,重复上述步骤,测得SO 的平均回收率为95%。
2 3 2
已知:K (H PO )=7.1×10-3,K (H SO )=1.3×10-2
a1 3 4 a1 2 3
回答下列问题:
(1)装置图中仪器a、b的名称分别为______________________________________________、
___________________。
(2)三颈烧瓶适宜的规格为________(填标号)。
A.250 mL B.500 mL C.1 000 mL
(3)解释加入HPO ,能够生成SO 的原因:_______________________________________。
3 4 2
(4)滴定管在使用前需要______、洗涤、润洗;滴定终点时溶液的颜色为__________;滴定
反应的离子方程式为_____________________________________________________________。
(5)若先加磷酸再通氮气,会使测定结果______(填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为________ mg·kg-1(以SO 计,结果保留三位有效数字)。
2
类型二 物质组成的测定
确定物质组成的注意事项
(1)测定实验中要有消除干扰气体的意识
如用惰性气体将干扰气体排出,或用溶液吸收干扰气体等。
(2)测定实验中要有被测量气体全部被测量的意识
如可采取反应结束后继续向装置中通入惰性气体以使被测量气体全部被吸收剂吸收的方法。
(3)测定实验中要有“数据”的采集处理意识
①称量固体质量时,中学一般用托盘天平,可估读到0.1 g,精确度要求高的实验中可以用
分析天平或电子天平。
②测量液体体积时,一般实验中选用适当规格的量筒,可估读到0.1 mL,准确度要求高的
定量实验如中和滴定中选用滴定管,可估读到0.01 mL。
③气体除了量取外,还可以称量。称气体的质量时一般有两种方法:一种方法是称反应装置
在放出气体前后的质量减小值;另一种方法是称吸收装置前后的质量增大值。
④用pH试纸(测得整数值)或pH计(精确到0.01)直接测出溶液的pH,经过计算可以得到溶液
中H+或OH-的物质的量浓度。1. (2023·湖州、衢州、丽水三地市模拟)某研究小组利用转炉铜渣(主要成分是Cu、Cu O、
2
FeO等)制备胆矾,流程如下:
请回答:
(1)制备胆矾时,除反应釜、量筒、酒精灯、玻璃棒、漏斗外,以下的实验仪器还必须使用
的有________(填字母)。
A.烧杯 B.容量瓶
C.蒸发皿 D.移液管
(2)步骤 Ⅰ 中,反应温度在80 ℃时相同时间内铜的浸出率达到最高,继续升温会导致浸出
率下降,其原因是_______________________________________________________________
______________________________________________________________________________。
(3)下列有关说法不正确的是______(填字母)。
A.步骤 Ⅰ 中,温度升至临近实验温度可关闭加热电源,利用反应放热维持体系温度
B.步骤 Ⅱ 中,过滤前需煮沸10 min,主要目的是破坏胶体结构,便于过滤
C.步骤 Ⅱ 中,控制pH在3.5~4,是为了除铁,并抑制硫酸铜的水解
D.步骤 Ⅲ 后,测定结晶水时加热脱水后的坩埚应放在实验台陶土网上冷却后再称量
(4)从滤液中分离提纯得到胆矾样品并测定其中结晶水个数,可按以下步骤进行,请从下列
选项中选择合理的操作,补全如下步骤(填字母)。
________→过滤→乙醇洗涤→________→称量干燥坩埚的质量为m g→______→______→
1
冷却后称量得到总质量为m g→重复上述两步操作,最终总质量恒定为m g
3 4
a.加热蒸发、冷却结晶
b.加热、蒸发结晶
c.将坩埚加热至胆矾全部变为白色
d.称量样品质量为m g
2
e.将样品干燥
f.称量样品和坩埚总质量为m g
2
(5)该样品中结晶水的个数为______________[用(4)中字母写出表达式]。
2.(2023·山西怀仁模拟)硫酸亚铁铵晶体[x(NH )SO ·yFeSO ·zHO][M=(132x+152y+18z)
4 2 4 4 2
g·mol-1]是常见的补血剂。
已知:①硫酸亚铁铵晶体在空气中不易被氧化。
②FeSO 溶液与(NH )SO 反应可得到硫酸亚铁铵。
4 4 2 4
(1)FeSO 溶液的制备。将铁粉、一定量HSO 溶液反应制得FeSO 溶液,其中加入的铁粉需
4 2 4 4
过量,除铁粉不纯外,主要原因是_________________________________________________________________________________________________________________________(用离子
方程式表示)。
(2)制备x(NH )SO ·yFeSO ·zHO。向制备得到的FeSO 溶液中加入一定质量的(NH )SO 固
4 2 4 4 2 4 4 2 4
体,在 70~80 ℃条件下溶解后,趁热倒入 50 mL 乙醇中,析出晶体。乙醇的作用为
_____________________________________________________________________________
_____________________________________________________________________________。
(3)产品化学式的确定——NH含量的测定
Ⅰ.准确称取58.80 g晶体,加水溶解后,将溶液注入三颈烧瓶中;
Ⅱ.准确量取50.00 mL 3.030 mol·L-1HSO 溶液于锥形瓶中;
2 4
Ⅲ.向三颈烧瓶中通入氮气,加入足量NaOH浓溶液,加热,蒸氨结束后取下锥形瓶;
Ⅳ.用0.120 mol·L-1的NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗25.00 mL
NaOH标准溶液。
①装置M的名称为____________。
②通入N 的作用为____________________________________________________________
2
_____________________________________________________________________________。
③步骤Ⅲ中,反应的离子方程式是_______________________________________________
_____________________________________________________________________________。
④若步骤Ⅳ中,未用NaOH标准溶液润洗滴定管,则n(NH)将________(填“偏大”“偏
小”或“不变”)。步骤Ⅳ中,滴定时还必须选用的仪器是________(填编号)。
(4)产品化学式的确定——SO含量的测定
Ⅰ.另准确称取58.80 g晶体于烧杯中,加水溶解,边搅拌边加入过量的BaCl 溶液;
2
Ⅱ.过滤得到沉淀,洗涤沉淀3~4次;
Ⅲ.灼烧沉淀至恒重,称量,得沉淀质量为69.90 g。
结合实验(3)和(4),通过计算得出硫酸亚铁铵晶体的化学式为__________________。