
北京时间2026年4月17日,美国斯坦福大学Alex Gao课题组在Science上发表题为“Protein-templated synthesis of dinucleotide repeat DNA by an anti-phage reverse transcriptase”的研究论文。
该研究首次发现并阐明了一种细菌逆转录酶Drt3b,它无需核酸模板,而是利用自身氨基酸侧链作为“模具”,精确合成特定序列的DNA。这一发现,是自1970年诺奖得主David Baltimore等人发现逆转录酶以来,对生命信息传递基本规则的又一次标志性突破,不仅填补了生物信息传递的关键拼图,也为我们理解生命的编码规则开辟了新的维度。
生命的蓝图如何代代相传?中心法则为我们描绘了遗传信息从DNA到RNA再到蛋白质的经典路径。随后,逆转录酶(RT)和RNA依赖的RNA聚合酶(RdRp)的发现,打破了信息单向流动的传统认知。然而,在这些已知的生命过程中,一个共同的‘规则’似乎从未被打破:所有序列特异性的聚合酶,都必须依赖一条核酸(DNA或RNA)作为合成的模板。那么,一个更大胆的问题随之而来:生命世界中是否存在“例外”?有没有一种聚合酶,可以完全摆脱对核酸模板的依赖,直接以蛋白质为模板来合成DNA? 换言之,蛋白质蕴含的化学信息,能否直接被‘翻译’回DNA的遗传密码中?这需要一种前所未见、真正意义上的“蛋白质依赖的DNA聚合酶”。
该研究始于一个独特的细菌防御系统——DRT3(Defense-associated Reverse Transcriptase 3)。它由两个来自不同分支的逆转录酶——Drt3a和Drt3b,以及一个非编码RNA(ncRNA)构成。研究团队证实,当DRT3在细菌(如E. coli)中表达时,能够高效抵御多种噬菌体的入侵。通过对表达DRT3的细菌进行non-stranded 双链DNA(dsDNA)测序分析,他们发现细胞内会自主产生大量由poly(GT/AC)交替重复序列组成的dsDNA,且这一过程无需噬菌体感染即可发生(图1)。体外生化实验进一步证实,纯化的DRT3复合物确实能够合成这种特异的dsDNA。其中,Drt3a负责产生单链poly(GT) DNA,而Drt3b则负责合成互补的poly(AC)单链,并共价连接到自身蛋白上(图1)。
为了揭示这一精妙的合成机制,研究团队利用冷冻电镜技术,成功解析了DRT3复合物在“静息(Resting)”和“延伸(Elongating)”两种状态下的高分辨率(2.6 Å)结构。结构显示,DRT3形成了一个具有D3对称性的6:6:6复合物,即由6个Drt3a、6个Drt3b和6个ncRNA分子组成。整个结构形似一个由两个三聚体“背靠背”组成的六聚体核心(图1)。
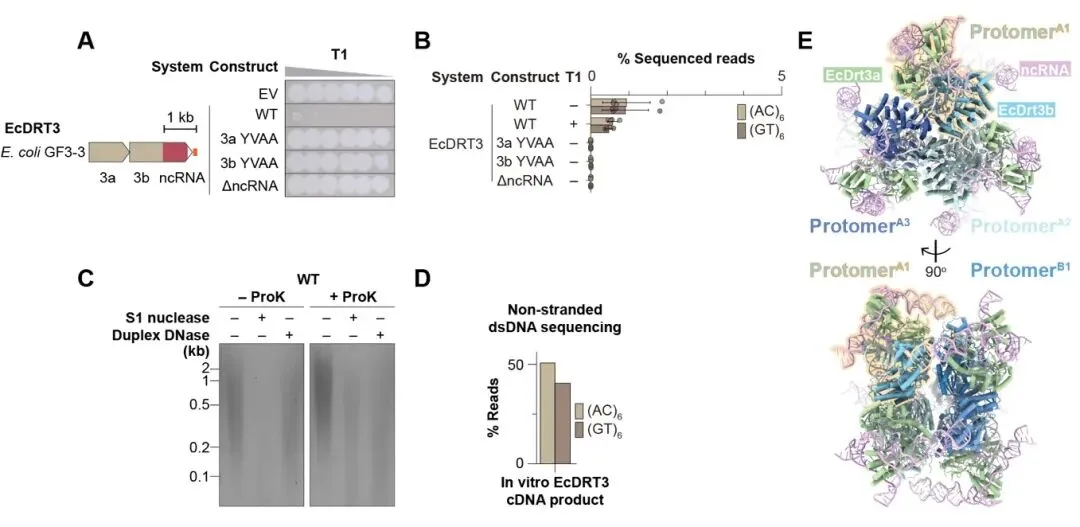
图1. DRT3系统能自主合成poly(GT/AC)双链DNA. 图注: (A) DRT3系统抗噬菌体活性测试。(B-D) 体内及体外合成的poly(GT/AC) dsDNA产物的测序与凝胶分析。(E) DRT3六聚体复合物的冷冻电镜结构。
精细的结构分析清晰地揭示了两个RT协同工作的分子基础。Drt3a的机制相对“传统”,它像端粒酶一样,以ncRNA上一段保守的ACACAC序列为模板,指导poly(GT) DNA链的合成(图2)。与之相比,Drt3b的机制则截然不同。结构清晰地显示,在Drt3b的活性中心,虽然有一条正在合成的poly(AC) DNA链,但完全不存在任何核酸模板,其模板结合通道也被自身结构物理性地阻塞。那么,Drt3b是如何在无模板的情况下精确合成poly(AC)序列的呢?答案在于其活性位点的氨基酸残基直接构成了“蛋白质模板”。
研究团队通过结构解析发现,Glu26和Arg253这两个关键残基,通过一套协同的、交替的识别机制,保证了AC序列的精确合成(图2)。具体而言,Glu26通过与dATP (dA18) 形成特异性氢键,负责在掺入位点选择dATP。同时,Arg253通过阳离子-π相互作用进一步增强了对dATP的亲和力。与此同时,Arg253与Glu26协同,通过与前一个已掺入的dC17碱基形成稳固的氢键,并结合空间位阻效应,确保了AC序列中C位置的保真度。
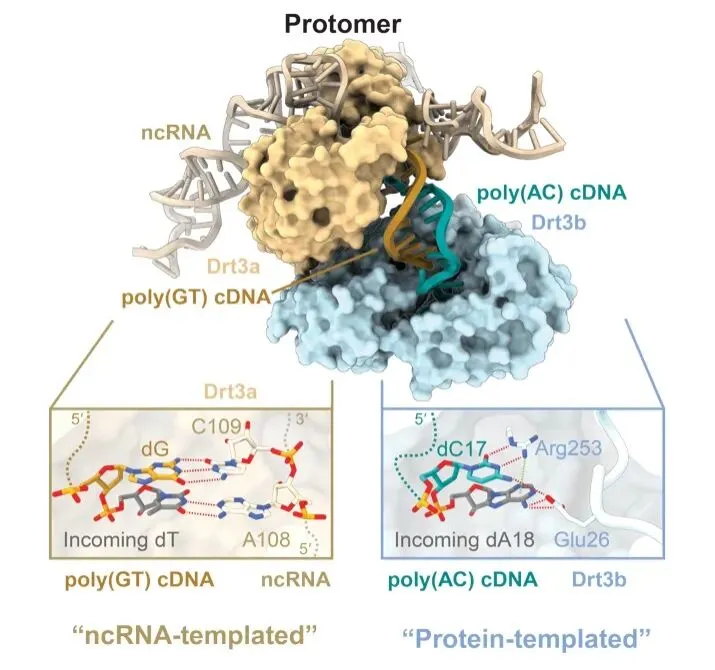
图2. DRT3复合物的DNA合成机制:经典的ncRNA模板与颠覆性的蛋白质模板。
这两个保守的氨基酸残基通过一系列精妙的氢键识别和空间位阻,共同构筑了一个蛋白质“模具”。通过定点突变实验(如E26A),研究团队也证实了这些残基对于维持合成效率和序列保真度的决定性作用。
这是首次从结构上完整阐明长链、序列特异性DNA的蛋白质模板合成机制。 它有力地表明,蛋白质的功能远不止于催化和构成结构: 其自身的氨基酸序列和三维构象,本身就蕴含着可被解读的潜在“遗传信息”,并将其写入DNA。此外,研究还发现,DRT3系统通过识别噬菌体编码的ST61蛋白来激活其抗病毒防御反应(图3)。
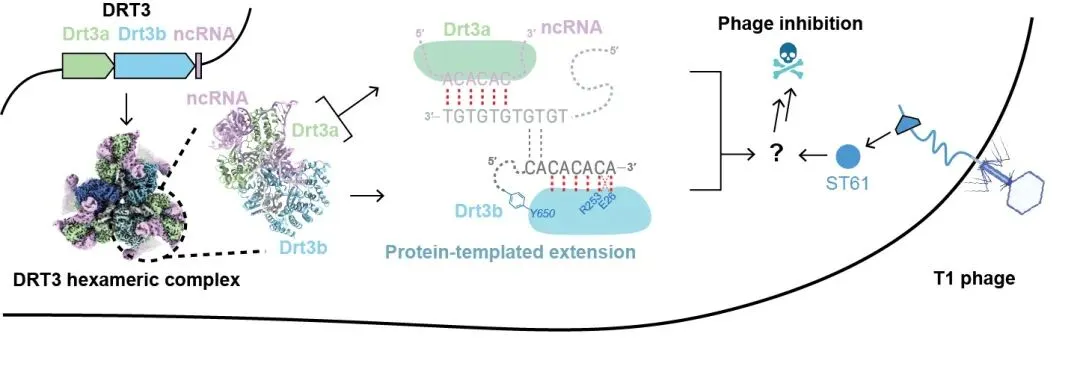
图3. DRT3系统的抗噬菌体分子机制模型。
本研究揭示了DRT3作为一个精密细菌防御武器的内在机制。其内部包含两个分工明确的逆转录酶:Drt3a遵循以RNA为模板的传统路径,而Drt3b则开创了以蛋白质为模板的新模式。二者协同合成dsDNA,共同实现抗噬菌体功能。
Drt3b的发现,是分子生物学研究中的一项重要突破,极大地拓展了该领域的认知边界。它与此前已知的、仅限于极短产物的蛋白质模板合成(如tRNA的CCA尾添加或Rev1聚合酶添加单个C碱基)有本质不同:Drt3b能够合成数千碱基长的、序列高度特异的DNA。即使与功能上相似的RDE-3相比,Drt3b在机制上也更为独特,它利用RT的结构框架,却完全以蛋白质侧链实现了核酸模板的功能。
这一发现不仅极大地拓展了我们对核酸聚合酶功能多样性的认知,也为“蛋白质→DNA”这一全新的生物信息传递路径提供了结构和生化证据。这项工作为理解生命的演化、探索全新的基因编辑和信息存储工具开辟了无限的想象空间。
斯坦福大学生物化学系Alex Gao助理教授为本文通讯作者。博士后邓谱涓、Hyunbin Lee与博士生Carlo Armijo为该研究的共同第一作者。斯坦福大学Sarafan ChEM-H Cryo-EM助理主任王淏清博士也对该研究做出了重要贡献。
相关论文信息:
https://www.science.org/doi/10.1126/science.aed1656
相关新闻:
https://www.science.org/content/article/scientists-stunned-fundamentally-new-way-life-produces-dna
*封面图片由AI生成
编辑 | 余 荷
欲知更多内容,敬请围观小柯机器人频道:

 夜雨聆风
夜雨聆风