 这篇文章发表于2026年5月28日,由芝加哥大学普利兹克分子工程学院研究团队主导完成。研究者围绕一个核心问题展开:如何在整个小鼠个体尺度上,同时解析不同器官和细胞的空间分布与基因表达情况。为此,他们构建了一套覆盖全身的空间转录组技术与计算分析框架,将整只小鼠切片后进行高通量测序,并结合超过5900万单细胞数据进行整合分析,从而在全身范围内精确定位数百种细胞类型及其分布特征。
这篇文章发表于2026年5月28日,由芝加哥大学普利兹克分子工程学院研究团队主导完成。研究者围绕一个核心问题展开:如何在整个小鼠个体尺度上,同时解析不同器官和细胞的空间分布与基因表达情况。为此,他们构建了一套覆盖全身的空间转录组技术与计算分析框架,将整只小鼠切片后进行高通量测序,并结合超过5900万单细胞数据进行整合分析,从而在全身范围内精确定位数百种细胞类型及其分布特征。
同时,研究还开发了一个名为LABEL的人工智能模型,可以直接通过常规病理切片图像自动识别器官、组织甚至细胞类型。进一步地,作者利用该体系研究全身炎症反应,发现不同组织间存在协同变化的基因表达模式。整体来看,这项工作首次实现了“全身尺度”的分子与细胞图谱构建,为系统性理解疾病机制提供了重要工具。
研究目的
数 据
本研究整合和产生的数据规模非常大,主要包括:
- 全身空间转录组数据
:对约6周龄小鼠进行整体切片,每张切片约覆盖58万–61万个空间点位(spot) - 单细胞参考数据
:整合466个单细胞研究,共约5900万细胞 - 细胞类型注释
:最终识别并映射约379种细胞类型(从495种细胞类型中筛选) - 组织覆盖范围
:包含16个主要器官系统(如脑、肝、肾、肠等) - 空间分辨表达数据
:平均每个spot检测约600多个基因、1200多个UMI - 疾病模型数据
:构建LPS诱导全身炎症模型,检测到约5000多个差异基因 - 图像数据
:对应的H&E全身切片图像,用于训练AI模型
模型构建
1. 全身空间转录组构建(Array-seq)
作者首先开发了一套适用于整只小鼠的组织切片方法,并结合Array-seq空间转录组技术,实现了对整只小鼠切片的基因表达检测。这一步的关键在于既要保证组织结构完整,又要保持RNA质量,从而能够在单个切片中同时获得多个器官的空间表达信息,构建真正意义上的“全身空间表达图谱”。
2. 单细胞参考整合与细胞类型推断
为了在空间数据中识别细胞类型,作者整合了来自大量公开研究的单细胞RNA-seq数据,构建了一个覆盖全身各组织的参考数据库。然后基于这些参考数据,为每一个空间点位推断其细胞组成,实现从“空间表达”到“空间细胞类型”的转化,从而在全身尺度上精确定位不同细胞类型的分布。
3. 空间细胞类型映射算法
在具体计算层面,作者开发了一套细胞类型分配方法,通过将空间转录组数据与参考基因集进行匹配,推断每个spot中最可能的细胞类型。这种方法可以在复杂组织环境中区分不同细胞,并在多个器官中保持较高一致性,同时与已有方法(如RCTD、cell2location)进行了对比验证,证明其可靠性。
4. LABEL人工智能模型(病理图像自动注释)
作者进一步开发了一个名为LABEL的AI模型,将空间转录组数据与病理切片图像(H&E)进行结合。该模型利用预训练图像模型提取特征,并结合空间信息进行分类,从而实现仅通过普通病理图像即可预测器官、组织甚至细胞类型。这一方法的意义在于大幅降低测序成本,使空间信息的获取更加高效。
5. 全身炎症模型分析(LPS模型)
为了验证该平台的应用价值,作者构建了LPS诱导的全身炎症模型,并对全身空间表达进行分析。通过比较处理组与对照组,系统识别不同组织中的差异基因、炎症信号以及细胞状态变化,揭示炎症反应不仅局限于单一器官,而是呈现出全身协同调控的特征。
6. 配体-受体通讯分析(跨器官信号网络)
在更深入的机制层面,作者分析了不同细胞之间的配体-受体相互作用,构建跨器官的信号通讯网络。结果发现,在炎症状态下,多种信号通路(如趋化因子、细胞因子等)在多个器官中同时增强,说明疾病过程具有明显的系统性特征,而不仅仅是局部变化。
结果解读
Fig1 全身空间转录组成功构建
作者通过优化整只小鼠切片与Array-seq技术,获得了覆盖多个器官的空间转录组数据,并且在单张切片中保持了良好的组织结构和RNA质量。结果显示,不同器官在空间上的表达模式清晰可辨,且能准确对应组织学结构,同时还能细分到器官内部的功能区域,如脑区分层、小肠不同结构层以及肝脏的代谢分区,说明该方法在空间分辨率和生物学准确性上都具备较高可靠性。
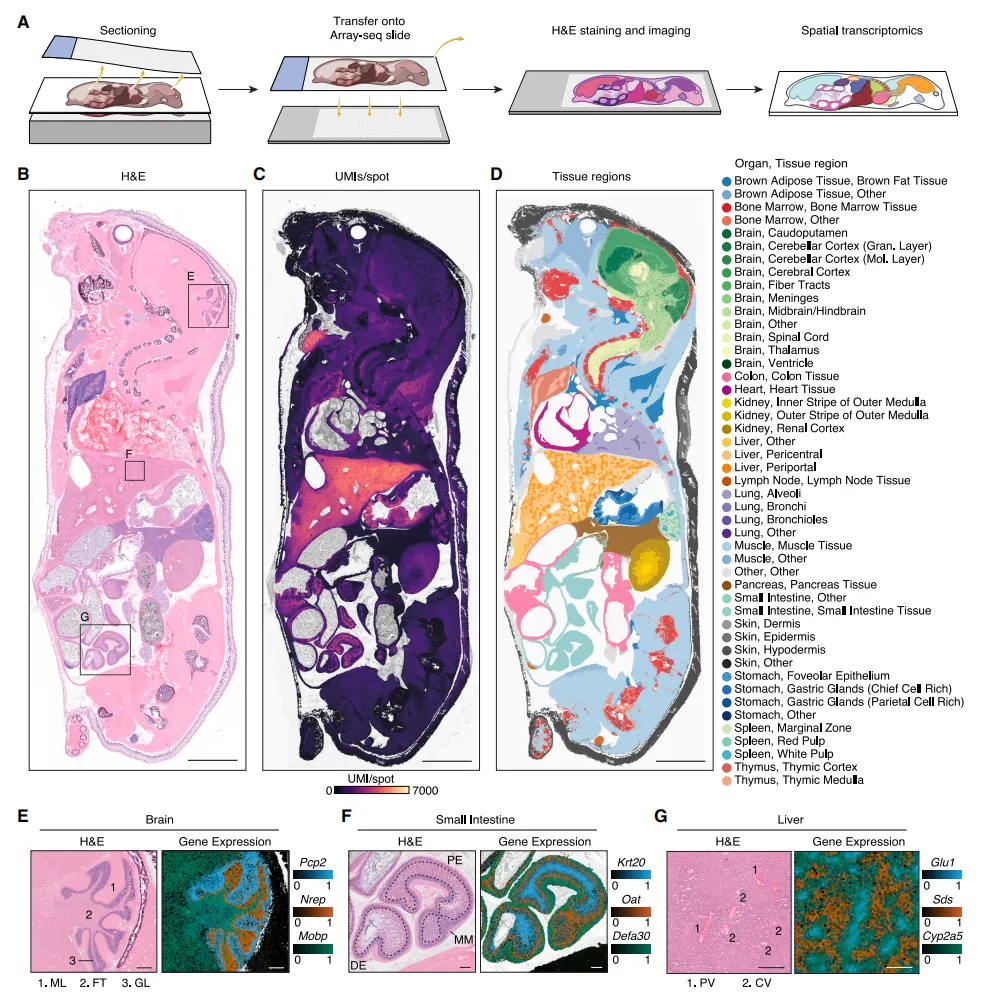
Fig2 全身细胞类型空间分布图谱
通过整合大规模单细胞数据,作者在全身尺度上对细胞类型进行了系统注释,并成功将数百种细胞类型映射到空间位置。结果表明,不同细胞类型在各器官中的分布符合生物学规律,例如肌肉细胞在肌肉组织中占主导,免疫细胞集中于免疫器官,同时也能在非免疫组织中检测到一定比例。此外,该方法还能识别精细结构中的细胞分布,如脑和胸腺中的特定细胞亚群,体现了较高的分辨能力。
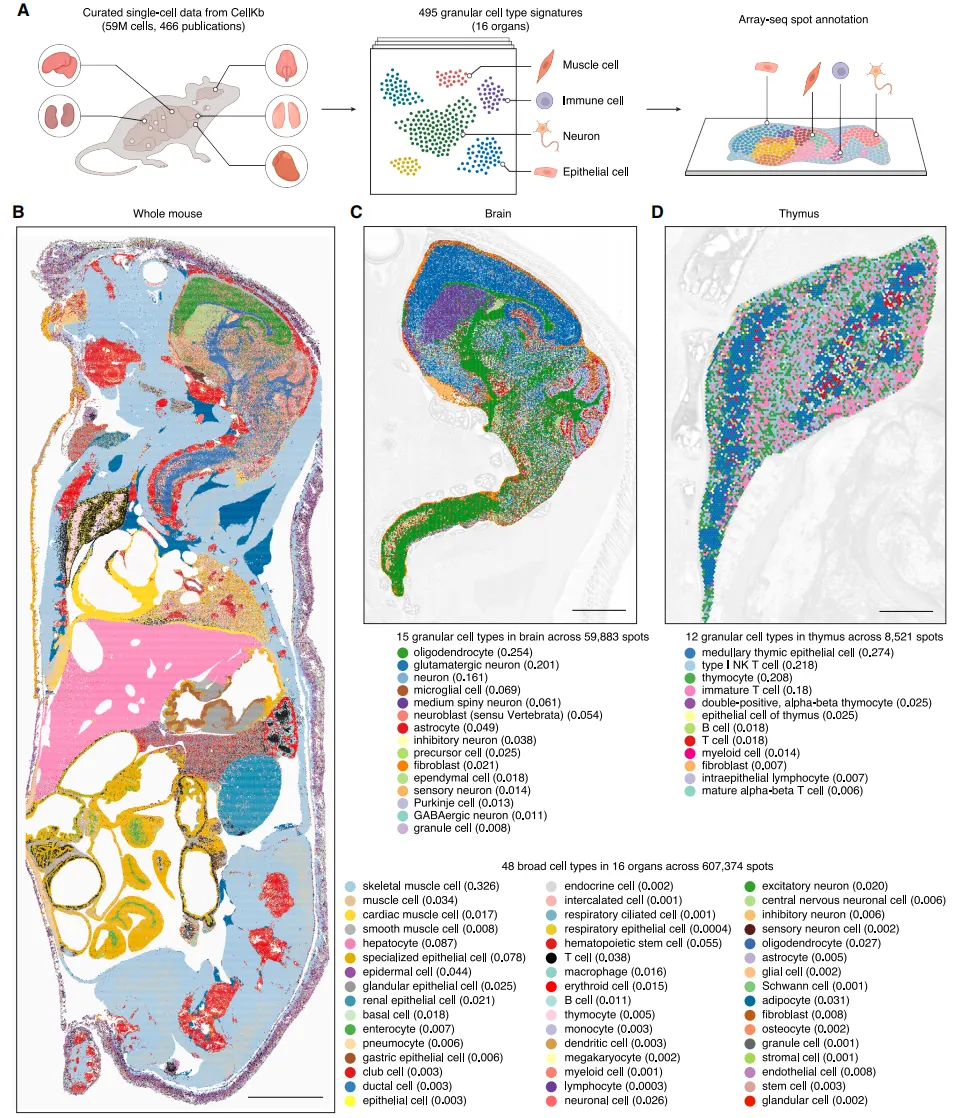
Fig3 AI模型实现病理图像自动注释
作者构建了LABEL模型,将空间转录组信息与病理图像结合,实现了无需测序即可对H&E切片进行器官、组织及细胞类型的自动识别。结果显示,该模型在大多数器官层面具有较高准确率,并且在部分组织结构和细胞类型上也表现良好,尽管在少数结构相似或样本较少的组织中存在误判,但整体证明了利用AI从图像中推断分子信息的可行性。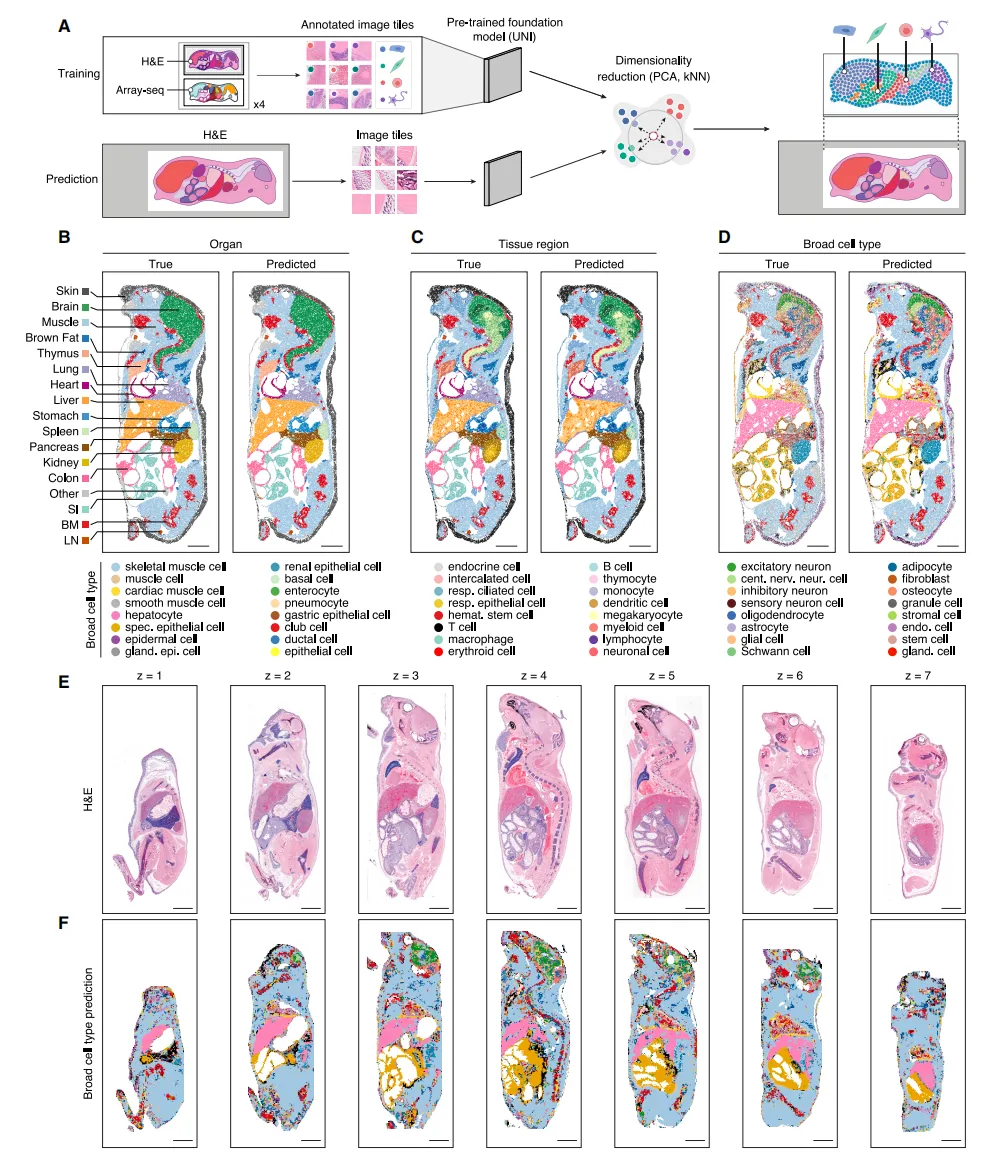
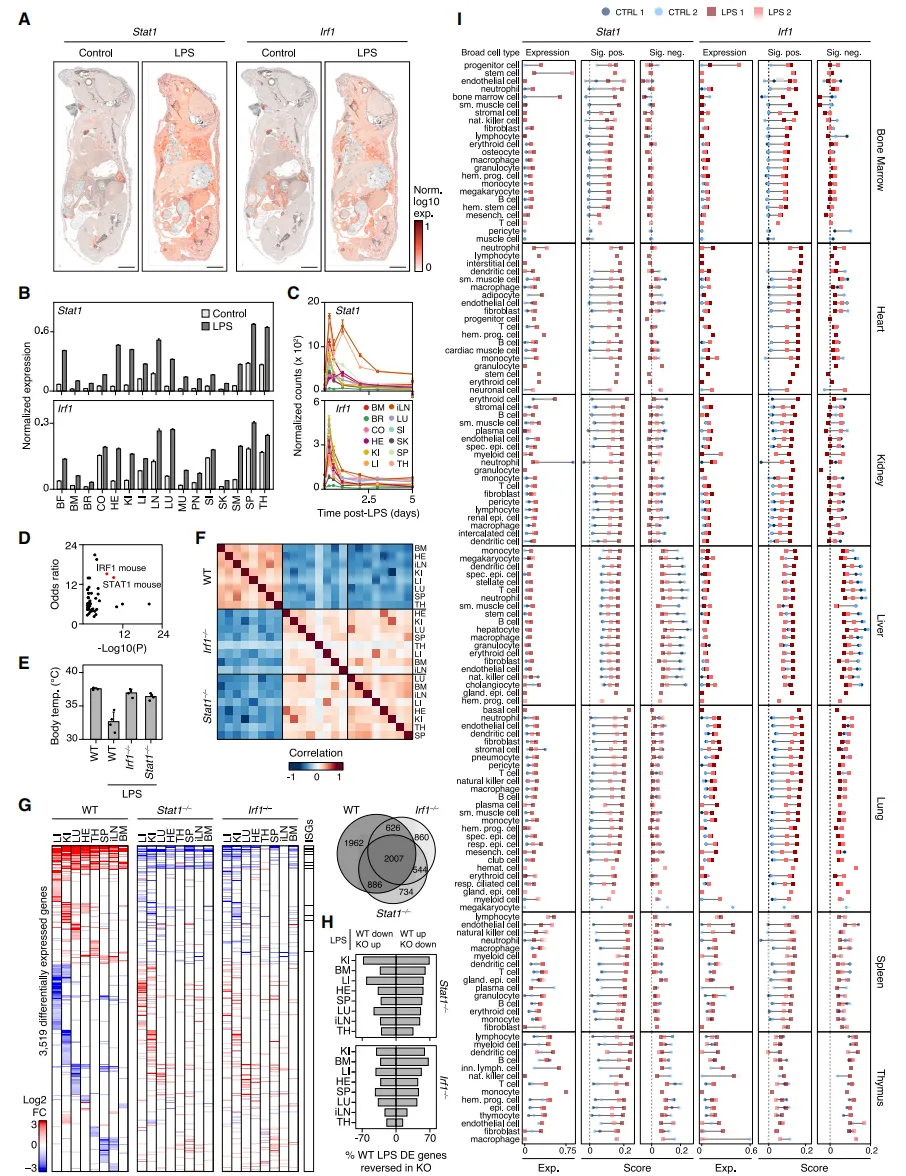
Fig4 全身炎症反应的空间重构
在LPS诱导的炎症模型中,作者发现不同器官中存在广泛且协调的基因表达变化,涉及数千个差异基因。炎症相关基因如急性期蛋白、趋化因子和干扰素刺激基因在多个组织中呈现特异或广泛上调,表明炎症反应具有明显的全身性特征,而不仅仅局限于单一器官。
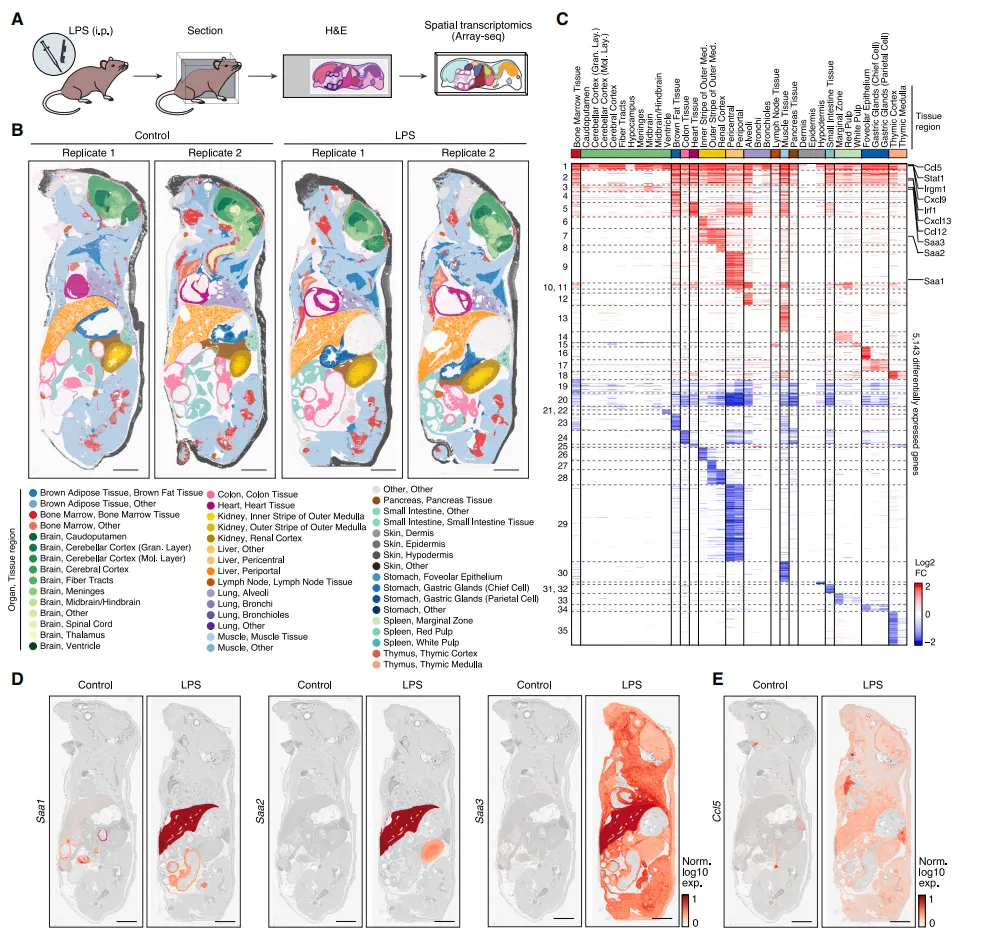
Fig5 炎症相关信号分子空间分布特征
进一步分析显示,不同炎症相关分子在各组织中的表达具有明显空间特异性。例如某些急性期蛋白主要集中在肝脏,而部分趋化因子则在免疫器官或特定组织中更为显著,这种差异化分布反映了不同器官在炎症中的分工与协同作用。
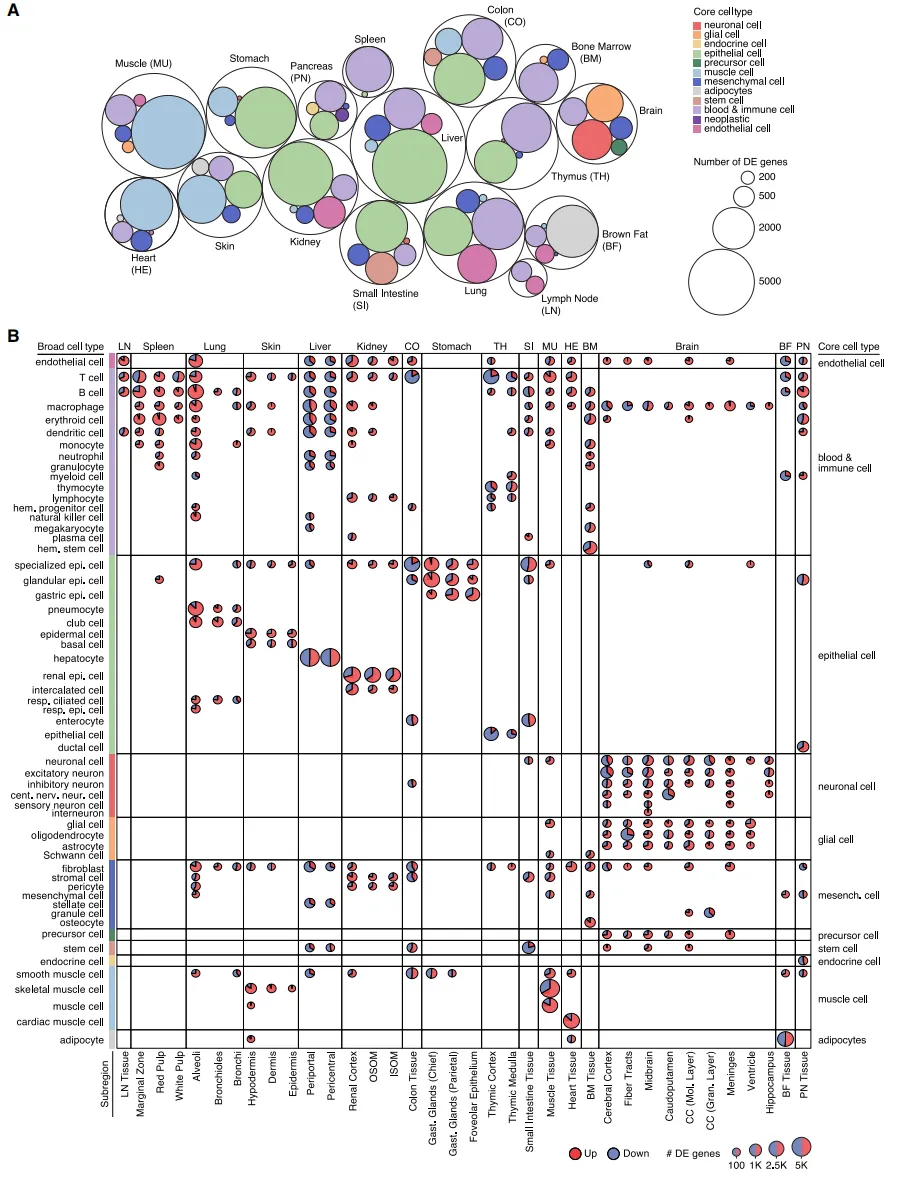
Fig6 全身细胞通讯网络重塑
通过配体-受体分析,作者揭示炎症状态下全身范围内细胞间通讯显著增强,尤其是炎症相关信号通路在多个器官中同步激活。同时也观察到部分抗炎信号的上调,提示机体在炎症过程中不仅存在激活反应,也伴随着调控和平衡机制。
总 结
Fig1 全身尺度技术的意义
研究首次实现了在整只小鼠层面同时获取空间与分子信息,突破了传统只能局部研究的限制,为系统性理解生命过程提供了全新技术基础。这种方法为未来构建“全身图谱”奠定了关键基础。
Fig2 细胞类型空间组织的新认知
通过在全身范围内精确定位细胞类型,研究揭示了不同细胞在器官之间的分布规律及其组织结构关系,有助于重新理解细胞在不同生理环境中的功能差异及其协同作用。
Fig3 AI与空间组学的融合前景
LABEL模型展示了将空间转录组与人工智能结合的潜力,未来有望仅通过常规病理图像实现分子层面的预测,这对于临床应用具有重要价值,可以显著降低成本并提高分析效率。
Fig4–5 疾病的全身系统性特征
炎症模型结果表明,疾病往往不是局部事件,而是涉及多个器官和细胞类型的系统性变化,不同组织在炎症过程中承担不同角色,这为理解复杂疾病提供了新的视角。
Fig6 跨器官通讯调控机制
研究进一步强调了细胞通讯在全身调控中的核心作用,炎症状态下多种信号通路在不同器官中协同变化,提示未来可以从“跨器官网络”的角度研究疾病机制和干预策略。
文章代码

论文链接:https://doi.org/10.1016/j.cell.2026.03.006
 夜雨聆风
夜雨聆风