
今天在Int.J.Mol.Sci(IF=4.9)发现一个好东西:AI增强版单细胞分析!
单细胞转录组分析咱们都知道,没有特别要求一般都是有固定的R包和标准化流程,但是这篇文章竟然借助AI搞了一个AI加强版的单细胞,这具体是怎么回事?让我们一起来拆解一下吧!

AI加强的单细胞分析主要体现在这些方面:
1.AI辅助细胞类型注释:在传统SingleR算法基础上,引入GPTCelltype(基于大语言模型的AI工具)对内皮细胞亚群进行精准注释,通过整合基因表达特征和背景知识库,解决了传统注释对稀有/过渡细胞亚群识别不足的问题,明确了心肌内皮细胞的异质性;
2.AI驱动的基因网络构建:用hdWGCNA结合AI的网络分析算法,对内皮细胞的基因表达数据构建共表达网络,快速筛选出核心模块(M1/M2)和枢纽基因(如S100A8),替代了传统人工筛选差异基因的低效方式;
简单来说,AI增强的单细胞分析就是让AI成为“单细胞数据的智能分析师”,从海量数据中自动、精准地找到研究的核心靶点(如本研究的S100A8),而非人工逐一验证,大幅提升了靶点发现的效率和准确性。
除了利用AI对单细胞分析进行增强,该研究还应用了前沿的虚拟敲除和虚拟筛选,形成了一套新的虚拟细胞范式:
1.AI驱动的蛋白分子互作模拟:通过AlphaFold3模拟S100A8与CD14的3D结合结构,预测二者的相互作用位点和结合稳定性,为分子机制研究提供结构基础。
2.基因的虚拟敲除验证:用scTenifoldKnk工具构建虚拟心肌内皮细胞模型,模拟敲除S100A8基因后,细胞内心肌收缩、能量代谢相关基因的表达变化,提前验证S100A8作为核心靶点的功能,明确其在MI/R损伤中的关键作用。
这篇文章可以说把AI和生信巧妙结合,碰撞出了新的火花。这篇文章新技术占比很高,有想做虚拟细胞的朋友可以好好参考下,如果需要相关技术的支持欢迎随时来滴滴智博哦!



生信铲屎官
定制生信分析
生信云服务器
研究设计
1)首先获取小鼠MI/R模型的单细胞RNA-seq数据,完成数据质控、批次效应校正与细胞类型注释,通过hdWGCNA构建内皮细胞基因共表达网络,结合差异基因筛选与交集分析,锁定内皮细胞炎症调控核心基因;
2)对核心基因进行GO/KEGG富集分析,明确其主要参与的信号通路,借助STRING构建PPI网络,结合AlphaFold3预测核心蛋白的互作结构与结合位点;
3)利用scTenifoldKnk开展S100A8虚拟敲除实验,模拟其功能缺失后的基因表达变化,通过AutoDock进行分子对接虚拟筛选,筛选出与S100A8稳定结合的候选药物AG;
4)构建CMECs的H/R体外损伤模型,检测不同浓度AG对细胞活力、通路关键分子及炎症因子的影响,验证AG对S100A8/IL-17通路的调控作用;
5)建立小鼠MI/R体内损伤模型,通过多维度检测验证AG的体内治疗效果,完成核心靶点与候选药物的体内外闭环验证。
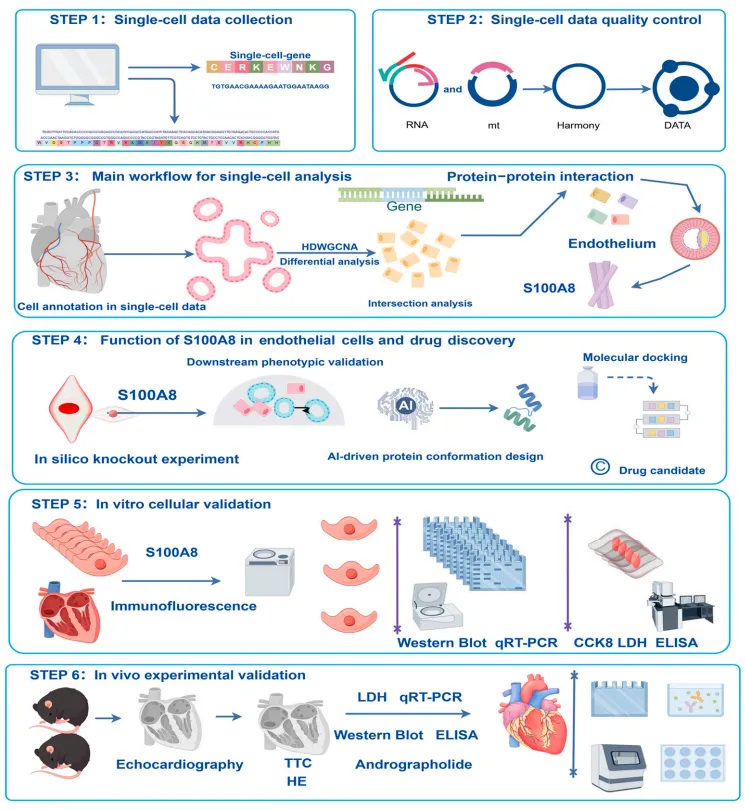
主要结果
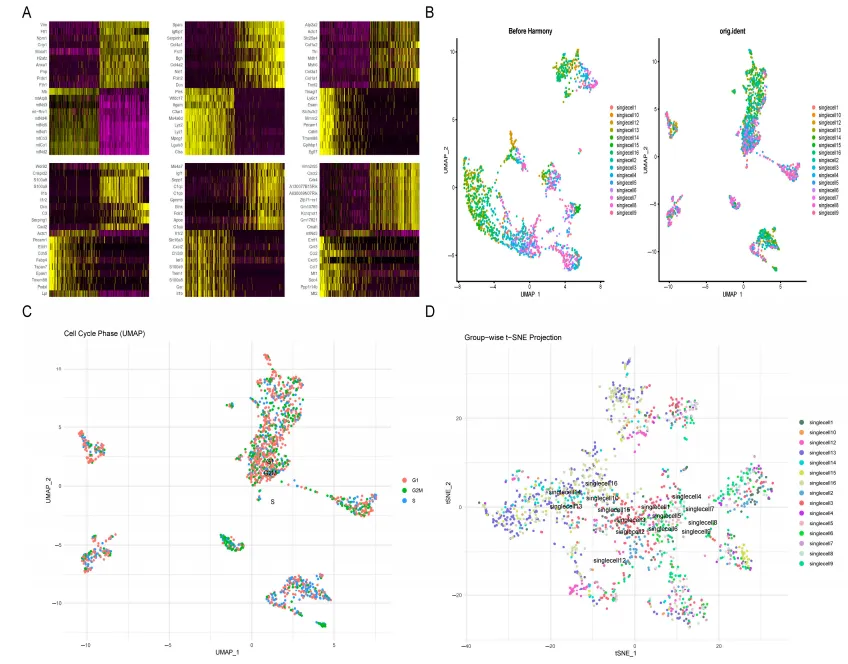
1.单细胞RNA-seq数据整合与质控
通过PCA、UMAP和t-SNE等方法分析测序数据,发现细胞周期不影响细胞聚类,批次效应校正效果良好,低维表征可保留大部分生物学信息,为后续分析奠定基础。
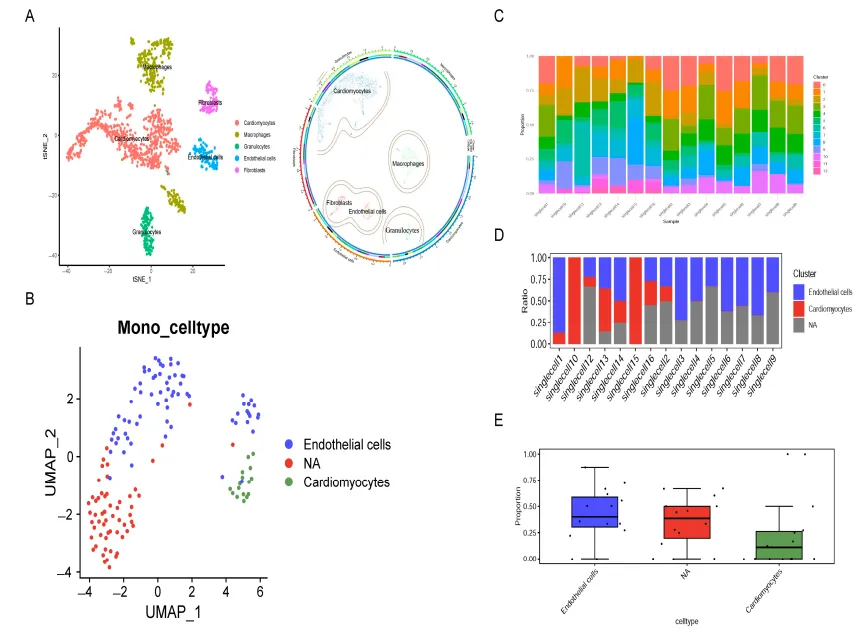
2.心肌组织细胞注释结果
通过SingleR和GPTCelltype完成细胞注释,发现小鼠心肌组织可分为5类核心细胞,内皮细胞存在异质性亚群,各样本的细胞组成及亚群比例均存在显著的动态差异。
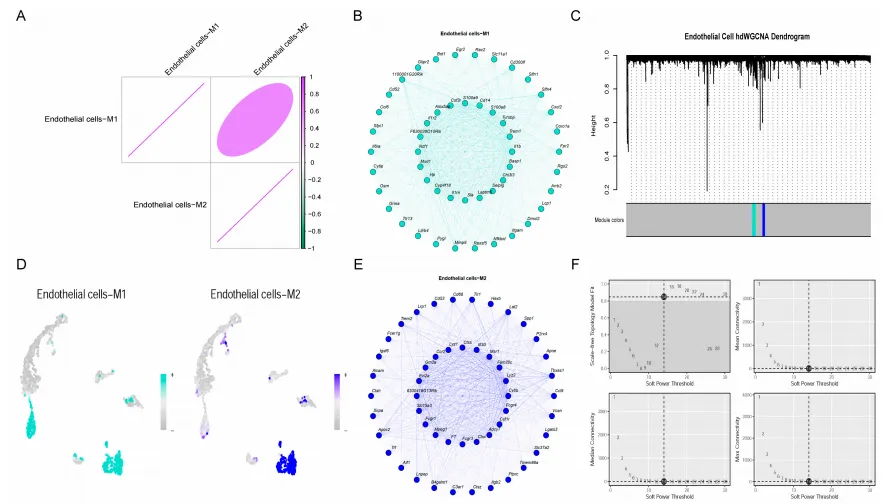
3.内皮细胞基因共表达网络分析
通过hdWGCNA构建内皮细胞基因共表达网络,发现内皮细胞可分为M1、M2两个核心模块,S100A8为M1炎症模块的核心基因,拥有较高的模块关联性。
4.内皮细胞核心基因与通路富集分析
通过差异基因与共表达基因的交集分析及GO/KEGG富集分析,发现S100A8是内皮细胞高表达核心基因,核心基因主要富集于IL-17炎症信号通路。
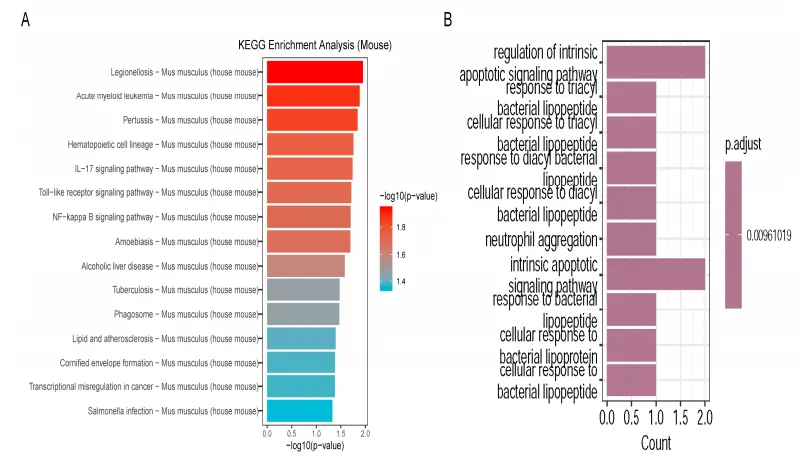
5.核心基因蛋白互作与结构预测
通过STRING构建PPI网络并结合AlphaFold3预测蛋白结构,发现CD14是PPI网络中心枢纽蛋白,S100A8与CD14存在潜在结合位点,构成炎症调控关键轴。
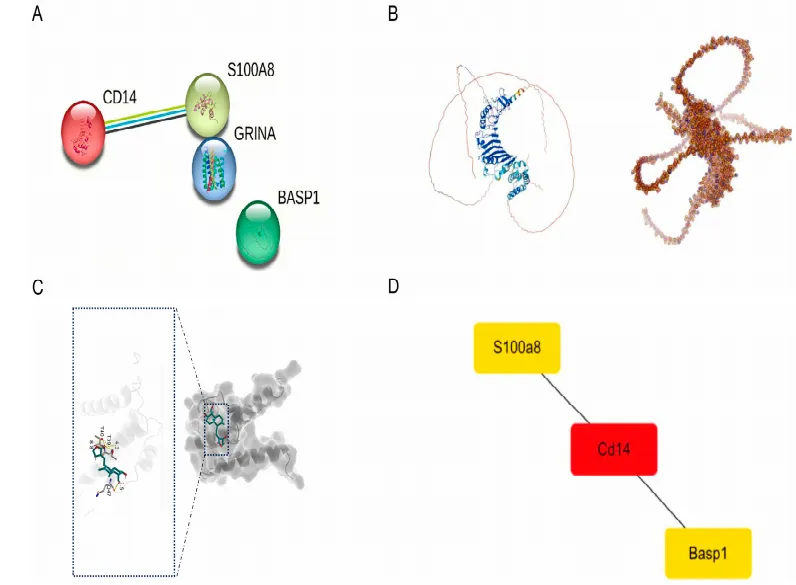
6.S100A8虚拟敲除与药物分子对接
通过scTenifoldKnk开展S100A8虚拟敲除,结合AutoDock进行分子对接,发现敲除S100A8显著影响心肌收缩和能量代谢基因,AG与S100A8可稳定结合。
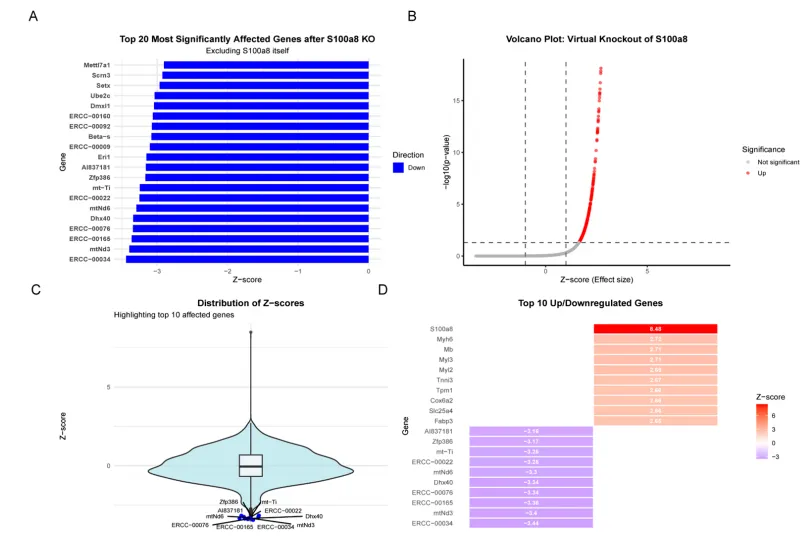
智博有话说
总得来说,这套框架跳出了传统单细胞分析的固定流程,充分发挥了AI的智能挖掘的优势和虚拟细胞的预实验价值,不管是心血管疾病还是其他方向的研究,都能参考复现,真正实现生信研究的降本增效!不想苦哈哈养细胞,想让你的研究搭上AI+虚拟细胞的技术快车,摆脱传统实验的低效试错?欢迎您随时滴滴智博,咱们的专业技术团队可为您打造专属方案,从设计到落地一站式搞定!

方案设计
生信分析
 夜雨聆风
夜雨聆风