一、元素周期律、元素周期系和元素周期表
1.元素周期律
(1)定义:元素的性质随原子的原子序数递增发生周期性递变,这一规律叫做元素周期律
(2)实质:元素性质的周期性变化是元素原子的核外电子排布周期性变化的必然结果。
2.元素周期系
(1)定义:元素按其原子核电荷数递增排列的序列称为元素周期系。这个序列中的元素性质随着核电荷数的递增发生周期性的重复。
(2)特点:元素周期系周期性发展就像螺壳上的螺旋。
(3)形成:
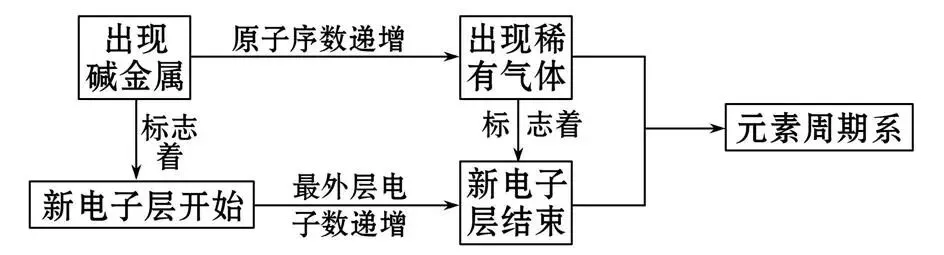
(4)原因:元素周期系的形成是由于元素的原子核外电子的排布发生周期性的重复。
3.元素周期表
(1)含义:元素周期表是呈现元素周期系的表格。
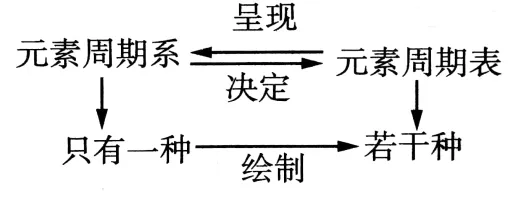
(2)元素周期系与元素周期表的关系:
(1)门捷列夫提出的原子序数是按相对原子质量从小到大的顺序对元素进行编号
(2)原子序数是按照元素核电荷数由小到大的顺序给元素编号而得到的序数。
(3)原子序数=核电荷数=质子数=核外电子数
(3)元素周期系只有一个,元素周期表多种多样。
二、元素周期表的结构
1.周期(七横七周期,三短四长)
从上到下 | 类别 | 各周期原子的电子层数 | 各周期最多容纳的元素种类数 | 同周期内原子序数变化规律 |
第一周期 | 短周期 | 1 | 2 |
|
第二周期 | 2 | 8 | ||
第三周期 | 3 | 8 | ||
第四周期 | 长周期 | 4 | 18 | |
第五周期 | 5 | 18 | ||
第六周期 | 6 | 32(含镧系15种元素) | ||
第七周期 | 7 | 32(含锕系15种元素) |
2.族(十八纵行十六族,七主八副一0)
列数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
类别 | 主族 | 副族 | 第VIII族 | 副族 | 主族 | 0族 | ||||||||||||
名称 | IA | IIA | IIIB | IVB | VB | VIB | VIIB | 第VIII族 | IB | IIB | IIIA | IVA | VA | VIA | VIIA | 0族 |
周期序数=电子层数;主族元素族序数=原子最外层电子数。
三、构造原理与元素周期表
1.根据构造原理得出的核外电子排布与周期中元素种类数的关系
(1)各周期总是从ns能级开始、以np结束(第一周期除外,第一周期从1s1开始,以1s2结束),中间按照构造原理依次排满各能级。而从ns能级开始以np结束递增的核电荷数(或电子数)就等于每个周期里的元素数,具体数据如下:

(2)能级组:能量相近的能级合并成一组,共七个能级组,也就形成了7个周期,特点:能级组之间能量相差较大,能级组之内能量相差很小。
2.原子核外电子排布与族的关系
族 | 按族分类 | 价层电子排布式 | 价层电子数 | 特点 |
I A | 主族 | ns1 | 1 | 族序数=最外层电子数 =价层电子数 |
ⅡA | ns2 | 2 | ||
ⅢA | ns2np1 | 3 | ||
IVA | ns2np2 | 4 | ||
VA | ns2np3 | 5 | ||
ⅥA | ns2np4 | 6 | ||
ⅦA | ns2np5 | 7 | ||
ⅢB | 副族(镧系、锕系除外) | (n-1)d1-10ns1-2 | 3 | 价层电子数=族序数 |
ⅣB | 4 | |||
VB | 5 | |||
VIB | 6 | |||
VIIB | 7 | |||
I B | 11 | (n-1)d轨道为全充满状态, 族序数=最外层ns轨道 上的电子数 | ||
ⅡB | 12 | |||
Ⅷ | Ⅷ族 | (n-1)d6-10ns0-2 | 8 | Ⅷ族第1列元素的价电子数 =族序数 Ⅷ族第2列元素的价电 子数为9 Ⅷ族第3列元素的价 电子数为10 |
9 | ||||
10 | ||||
0 | 0族 | 1s2或ns2np6(n>1) | 2或8 | 为原子轨道全充满的 稳定结构 |
(1)对于主族和0族元素而言,价层电子数=ns能级上的电子数或ns+np能级上的电子总数;
(2)对于副族(镧系和锕系除外)和第VIII族而言,价层电子数=(n-1)d+ns能级上的电子总数。
(4)第1行s区右边的小格移到最右端作为第18列;
(5)将第2、3行p区的6个格平移到最右端作为第13~18列;
(6)第4、5行不变;
(7)将第6、7行f区的14个格放到一个格中。
四、元素周期表的分区
1.按电子排布分区
(1)按核外电子排布式中最后填入电子的能级符号可将元素周期表(第IB族、第ⅡB族除外)分为s、p、d、f 4个区,而第IB族、第ⅡB族的元素原子的核外电子因先填满了(n-1)d能级而后填充ns能级而得名ds区。这5个区的位置关系如图所示。
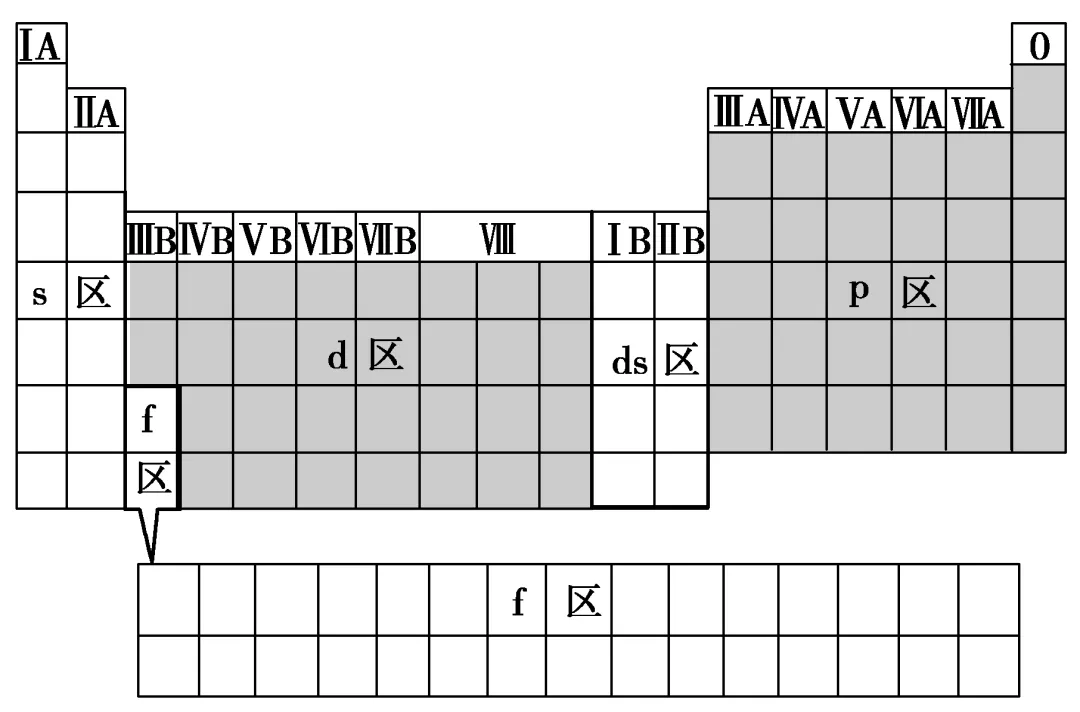
(2)各区元素原子的价层电子排布、元素的位置及类别
分区 | 元素位置 | 价层电子排布式 | 元素种类及性质特点 |
|---|---|---|---|
s区 | IA族、ⅡA族 | ns1-2 | 原子的核外电子最后排布在ns能级上, 属于活泼金属元素(H除外),为碱 金属元素和碱土金属元素 |
p区 | ⅢA~ⅦA族及0族 | ns2np1-6(He除外) | 原子的核外电子最后排布在np能级 (He为s能级)上,为非金属元素和 少数金属元素 |
d区 | ⅢB~ⅦB族(镧系、锕系除外) 以及Ⅷ族 | (n-1)d1-9ns1-2(Pd除外) | 为过渡金属元素,原子的核外电子最 后排布在(n-1)d能级上,d轨道可以不 同程度地参与化学键的形成 |
ds区 | IB族、ⅡB族 | (n-1)d10ns1-2 | 为过渡金属元素,核外电子先填满(n-1)d 能级而后再填充ns能级,由于d轨道已填 满电子,因此d轨道一般不参与化学键 的形成 |
f区 | 镧系和锕系 | (n-2)f0-14(n-1)d0-2ns2 | 镧系元素化学性质相似;锕 系元素化学性质相似 |
2.按金属元素与非金属元素分区
(1)金属元素、非金属元素在元素周期表中的位置
沿着周期表中硼、硅、砷、碲、砹、与铝、锗、锑、钋、之间画一条线,线的左边是金属元素(氢除外),线的右边是非金属元素。非金属元素要集中在元素周期表右上角的三角区内(如图)。
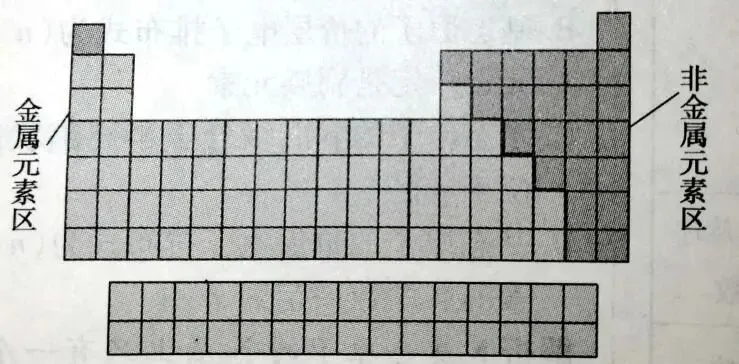
(2)金属与非金属交界处元素的性质特点:在元素周期表中位于金属和非金属分界线上的元素兼有金属和非金属的性质,位于此处的元素(如硼、硅、锗、砷、锑等)常被称为半金属或类金属(一般可用作半导体材料) 。
再探元素周期表
(1)现行元素周期表含118种元素,共有七个周期,每个周期包含的元素数目如下:
周期 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
数目 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
第一周期结尾元素(He)原子核外只有2个电子,根据构造原理,其电子排布式为1s2。与该元素同族的其他周期元素Ne、Ar、Kr、Xe、Rn等,原子核外电子数依次增加了8、8、18、18、32,根据构造原理,它们的最外层电子排布通式为ns2np6。所以,第一周期结尾元素的电子排布跟同族的其他周期元素的不同。
(2)元素周期表共有18个列。从左向右,第1一12列中,除第3列中的镧系和锕系以外,其他的价层电子数都等于列数;第13~18列中,除第18列中的氦以外,其他的价层电子数都等于列数减10。除了镧系、锕系和氨以外,同列元素价层电子数相等。元素周期表所划分的族及族序数,从左向右排列如下:
IA族、ⅡA族;ⅢB族→IB族;Ⅷ族;IB族、ⅡB族;ⅢA族→IA族;0族。
(3)从原子结构方面来说,元素周期表中右上角三角区的元素,大多数的价层电子排布为ns2np1~6(He除外),价层电子数较多,得电子相对容易,失电子相对困难。从元素周期表中元素性质递变规律来说,同周期元素从左到右非金属性逐渐增强(不包括0族元素),同主族元素从下向上非金属性逐渐增强。综上可知,在元素周期表中非金属主要集中在右上角三角区内。
再探元素周期表
(1)从原子核外电子排布来看,随着原子序数的递增,第IA族和第ⅡA族元素的最后一个电子填充在了最外电子层的s能级,第ⅢA族~第ⅦA族元素的最后一个电子填充在了最外电子层的p能级,而副族元素的最后一个电子填充在了次外电子层的d能级或倒数第三个电子层的f能级。从元素性质来看,第IA族(除氢
外)和第ⅡA族元素大多数是活泼金属元素:第ⅢA族~第ⅦA族元素大多数是非金属元素,有些还是活泼的非金属元素。综合上述可知,处在第ⅡA族与第ⅢA族之间的副族元素(这里未包括第Ⅷ族元素,下同),应称之为过渡元素。过渡元素价层电子跟它们的族序数的关系是第ⅢB族~第ⅦB族,价层电子数等于族序数:第IB族和第ⅡB族,价层电子数等于族序数加10。过渡元素的价层电子排布通式:第ⅢB族~第IB族,除镧系和锕系以外,其余都是(n-1)d1~5ns1~2;第IB族和第ⅡB族是(n-1)d10ns1~2。
(2)s区有2个纵列,d区有8个纵列,p区有6个纵列。 s区元素的价层电子排布通式为nsl-2,d区元素的价层电子排布通式为(n-1)d1-9ns1-2,ds区元素的价层电子排布通式为(n-1)d10ns1-2,它们的最外层电子数均不超过2,化学反应中容易失去电子,所以s区(除氢元素外)、d区和ds区的元素都是金属元素。
(3)由于元素的金属性和非金属性之间并没有严格的界限,处于非金属与金属分界线上的元素,基态原子的最外层电子数范围是3~7(只有At是7),总体上比金属元素基态原子最外层电子数多,比非金属元素基态原子最外层电子数少,既能表现出一定的金属性,又能表现出一定的非金属性,所以它们常被称为半金属或类金属。
(4)Cr:3d54s(非3d44s2):Cu:3d104s1(非3d94s2)它们的电子排布不符合构造原理(它们的3d轨道达到半充满或全充满结构,是一种能量较低的稳定结构),不符合构造原理的还有Ag(4d105s1)、Au(5d106s1)等。
(5)119号元素应位于第八周期第IA族,故基态原子最外层电子排布为8s1;周期分别为一、二、三四、五、六、七,元素种数分别为2×12、2×22、2×22、2×32、2×32、2×42、2×42,以此预测第八周期元素种数为2×52=50(种)。
五、对角线规则
1.对角线规则:在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的(如锂和镁在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物),这种相似性被称为对角线规则,如图所示。
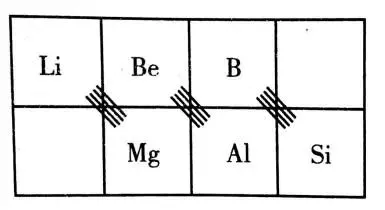
2.锂和镁的相似性
(1)锂与镁的沸点较为接近:
元素 | Li | Na | Be | Mg |
|---|---|---|---|---|
沸点/℃ | 1341 | 881.4 | 2467 | 1100 |
(2)在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物,并且Li2O和MgO与水反应都十分缓慢。
4Li+O2点燃2Li2O、2Mg+O2点燃2MgO
(3)能直接与氮气反应:生成相应的氮化物Li3N和Mg3N2。
(4)锂和镁的氢氧化物加热分解:分别生成Li2O、H2O和MgO、H2O。
(5)在碱金属的氟化物、碳酸盐和磷酸盐中:只有锂盐是难溶于水的,相应的镁盐也难溶于水。
3.铍和铝的相似性
(1)二者的氧化物Al2O3和BeO的熔点和硬度都很高;
(2)都可与酸、碱反应放出氢气;
(3)铍在浓硝酸中也发生钝化;
(4)氧化物和氢氧化物都具有两性,既能溶于强酸又能溶于强碱溶液:Be(OH)2+2HCl=BeCl2+2H2O,
Be(OH)2+2NaOH=Na2BeO2+2H2O;
(5)BeCl2和AlCl3都是共价化合物,易升华。
4.硼和硅的相似性
(1)自然界中B与Si均以化合物的形式存在。
(2)B与Si的单质都易与强碱反应,且不与稀酸反应:Si+2KOH+H2O= K2SiO3+2H2↑,2B+2KOH+2H2O = 2KBO2+3H2↑。
对角线规则的应用
(1)首先,这种对角线规则是有一定理论支撑的。如Li和Mg,以Na为参照,根据元素金属性递变规律,金属性LiNa,Mg <Na,则Li和Mg金属性相似。其次,这种对角线规则是一种经验规则,也就是说从理论上来说它并不是很严谨,所以它在实用方面有一定的局限性,应慎重使用。< span>
(2)Li、Mg的电负性分别为1.0、1.2;Be、A1的电负性分别为1.5、1.5;B、Si的电负性分别为2.0、1.8。它们的电负性接近,说明它们对键合电子的吸引力相当,它们表现出的性质相似,如Li、Mg在空气中燃烧的产物分别为Li2O和MgO;Be(OH)2、Al(OH)3均属于难溶的两性氢氧化物;B、Si的含氧酸都是弱酸等。
注意:对角线规则是从相关元素及其化合物的许多性质中总结出来的经验规则,不是定理。
 夜雨聆风
夜雨聆风
